Влияние инкубации в гипертонических растворах хлорида натрия на повреждаемость ДНК лимфоцитов периферической крови человека Y-излучением и перекисью водорода
Автор: Воробьева Н.Ю., Архангельская Е.Ю., Бушманов А.Ю., Осипов А.Н.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Генетика
Статья в выпуске: 4 т.10, 2014 года.
Бесплатный доступ
Цель: изучить влияние инкубации в гипертонических растворах NaCI на относительный количественный выход однонитевых разрывов (ОР) и щелочно-лабильных сайтов (ЩС) ДНК, индуцированных у-излучением и перекисью водорода в лимфоцитах периферической крови человека in vitro. Материал и методы. Для исследований использовали лимфоциты, выделенные из периферической крови физически здоровых женщин-доноров в возрасте 21-26 лет. Облучение клеток в дозах 1, 2, 3 и 5 Гр проводили на установке «АГАТ-Р1» (Россия, источник у-излучения 60Со, мощность дозы 1 Гр/мин) при 4°С. С перекисью водорода (25, 50 и 100 мкмоль/л) клетки инкубировали 15 мин при 4°С. Анализ ОР и ЩС ДНК проводили с помощью метода ДНК-комет в щелочных условиях. Результаты. Инкубация клеток в 0,35 моль/л растворе NaCI (диссоциация негистоновых белков) приводит к увеличению выхода ОР и ЩС ДНК, индуцируемых у-излучением и перекисью водорода, приблизительно в 1,3 раза. Увеличение концентрации NaCI до 0,6 моль/л (диссоциация линкерного гистона Н1) приводит почти к двойному увеличению выхода повреждений ДНК (~ в 1,7-1,8 раза). Дальнейшее повышение концентрации NaCI, ведущее к нарушению структуры нуклеосом (1,2 моль/л) и почти полной депротеинизации хроматина (2 моль/л), увеличивает выход повреждений ДНК не столь выраженно, как предполагалось (~ в 2,2 раза при концентрации 2 моль/л). Заключение. Результаты исследований показали, что инкубация в гипертонических растворах NaCI значительно увеличивает чувствительность ДНК лимфоцитов к повреждающему действию свободных радикалов.
Гипертонические растворы хлорида натрия, гистоны, лимфоциты, метод днк-комет, однонитевые разрывы днк, перекись водорода, у-излучение, хроматин
Короткий адрес: https://sciup.org/14918043
IDR: 14918043
Effect of incubation in sodium chloride hypertonic solutions on Y-radiation and hydrogen peroxide induced DNA damage in human peripheral blood lymphocytes
Aim: to study the effect incubation in NaCI hypertonic solutions on the yield of DNA single-strand breaks (SSB) and alkali-labile sites (ALS) induced by y-radiation and hydrogen peroxide in human peripheral blood lymphocytes in vitro. Material and methods. The lymphocytes isolated from the peripheral blood of healthy women donors aged 21-26 years were used for the study. Cell irradiation at doses of 1, 2, 3 and 5 Gy was performed using the "AGAT P1" unit (Russia, y-radiation source — 60Co, a dose rate of 1 Gy/min) at 4°C. In case of hydrogen peroxide exposure (25, 50 and 100 uM) the cells were incubated for 15 minutes at 4°C. Analysis of the DNA SSB and ALS was performed using the alkaline DNA comet assay. Results. Incubation of cells in 0.35 M NaCI solution (non-histone proteins dissociation) increases the yield of DNA SSB and ALS induced by v-radiation and hydrogen peroxide at ~ 1.3 times. Increasing the NaCI concentration to 0.6 M (linker histone H1 dissociation) leading to almost double increase in the DNA damage yield (~ 1.7-1.8 times). Further increasing the NaCI concentration leading to disruption of the structure of nucleosomes (1.2 M) and almost complete chromatin deproteinization (2 M) increased the yield of DNA damage not such pronounced as expected (~ 2.2-fold at 2 M concentration). Conclusion. The results showed that incubation in NaCI hypertonic solutions significantly increases the sensitivity of lymphocytes to DNA damaging action of free radicals.
Текст научной статьи Влияние инкубации в гипертонических растворах хлорида натрия на повреждаемость ДНК лимфоцитов периферической крови человека Y-излучением и перекисью водорода
1 Введение. Согласно современным радиобиологическим представлениям радиочувствительность клеточных популяций обусловлена способностями клеточных систем: 1) предотвращать возникновение повреждений ДНК; 2) репарировать индуцированные радиацией повреждения ДНК; 3) эффективно элиминировать клетки, в которых репарация повреждений ДНК невозможна. Как правило, при рассмотрении первого «эшелона» клеточной защиты от ионизирующего излучения основное внимание обращают на механизмы нейтрализации / детоксикации свободных радикалов, в которые вовлечены ферменты (супероксиддисмутаза, каталаза, глутатионпероксидаза и др.), хелаторы редокс-активных металлов, низкомолекулярные антиоксиданты (витамины Е и С, каротин, глутатион и др.), белки с высоким содержанием SH-групп (например, металлотионеины) и т.д.. Однако еще на заре развития радиационной биологии было известно, что чувствительность клеток к воздействию ионизирующего излучения, как правило, зависит от степени дифференцировки, длительности клеточного цикла и пролиферативной активности клеток (закон Ж. Бергонье и Л. Трибондо, сформулированный авторами в 1906 г.). Позднее показано, что перечисленные процессы так или иначе связаны с изменениями конформационной структуры и соотношением активных и неактивных участков хроматина. Так, активный хроматин (эухроматин) в большей степени повреждается свободными радикалами, образующимися при радиолизе воды, чем неактивный (гетерохроматин) [1]. Предполагается, что это обусловлено тем, что активно транскрибируемые последовательности не защищены от атак свободных радикалов структурными белками хроматина. При репликации ДНК наблюдается аналогичная ситуация (снижение «конформационной» защиты хроматина). В результате выход радиационно-индуцированных повреждений ДНК максимален именно в фазе синтеза ДНК (S-фаза клеточного цикла) [2].
Известно, что изменение ионной силы, например, с помощью гипертонических растворов NaCl приводит к нарушению этих взаимодействий и депротеинизации хроматина [3]. Использование растворов NaCl c постепенно повышающейся тоничностью позволяет проводить своеобразное, ступенчатое «раздевание» хроматина: при концентрации NaCl 0,35 моль/л происходит диссоциация негистоновых белков; 0,5–0,6 моль/л — негистоновых белков и линкерного гистона; 1,2 моль/л — негистоновых белков, линкерного гистона и коровых гистонов H2A-Н2B; 2 моль/л — полная депротеинизация хроматина [4]. Использование этого подхода позволяет изучать роль структурных белков хроматина в его организации и конформационном изменении доступа свободных радикалов к ДНК.
Цель: изучение влияния гипертонических растворов NaCl, вызывающих ступенчатую депротеинизацию хроматина, на выход однонитевых разрывов
(ОР) и щелочно-лабильных сайтов (ЩС) ДНК, индуцированных γ-излучением и перекисью водорода в лимфоцитах периферической крови человека in vitro.
Материал и методы. Для исследований использовалась кровь пяти физически здоровых женщин-доноров в возрасте 21–26 лет. Забор периферической крови проводили в вакутейнеры с литий-гепарином в качестве антикоагулянта (Vacuette). У всех доноров получено согласие на проведение данного исследования. Выделение лимфоцитов из гепаринизированной крови человека проводили путем центрифугирования в градиенте плотности фиколл-верографин (Histopaque-1077, Sigma-Aldrich) в соответствии с прилагаемой инструкцией. После выделения лимфоциты отмывали и ресуспензировали в фосфатносолевом буфере (рН 7,4) до конечной концентрации 1x106 клеток/мл.
500 мкл суспензии клеток смешивали с 500 мкл 1 % раствора легкоплавкой агарозы (тип IV) в фосфатно-солевом буфере (рН 7,4) при температуре 37,5ºС. 75 мкл полученной смеси наносили на предварительно покрытые слоем 1 % нормоплавкой агарозы предметные стекла, накрывали покровными стеклами и оставляли на 10 мин при 4ºC до образования плотного геля.
Полученные агарозные слайды с иммобилизированными в них клетками (далее — агарозные слайды) инкубировали 1 час при 4°С в 20 ммоль/л Тris-HCl буфере, рН 7,4, содержащем NaCl в разных концентрациях (0,14; 0,35; 0,6; 1,2; 2,0 моль/л).
Облучение агарозных слайдов в среде инкубации проводили на установке «АГАТ-Р1» (Россия, источник гамма-излучения 60Co) при мощности дозы 1 Гр/ мин и температуре 4˚C.
Для обработки агарозных слайдов Н2О2 добавляли Н2О2 до конечной концентрации 25, 50 или 100 ммоль/л и инкубировали 15 мин при 4°С. Анализ однонитевых разрывов ДНК и щелочно-лабильных сайтов проводили с помощью метода ДНК-комет в щелочных условиях [5]. Сразу после облучения или инкубации с Н2О2 агарозные слайды переносили в холодный (4˚C) лизирующий буфер (2.5 моль/л NaCl, 100 ммоль/л Na2EDTA, 20 ммоль/л Tris-HCl, pH 10.0, 1% Triton X-100 и 10% DMSO) и выдерживали в течение 1 ч в темноте при 4˚C. После лизиса клеток слайды переносили в холодный (4˚C) щелочной раствор (300 ммоль/л NaOH, 1 ммоль/л EDTA, рН>13) и выдерживали 20 мин для расплетания (щелочной денатурации) нитей ДНК. Электрофорез проводили в щелочном буфере при напряжении 0,75 В/см при комнатной температуре в течение 10 мин. После электрофореза проводили нейтрализацию для рена-турации (восстановления нативности) ДНК (3-кратная промывка в 0,4 моль/л Трис-НСl буфере, рН 7,4). После этого слайды слегка подсушивали и фиксировали в 70%-ном этаноле в течение 10 мин. Для окраски ДНК использовали акридиновый оранжевый (2 мкг/мл в фосфатно-солевом буфере, рН 7,4). Визуализацию ДНК-комет проводили с помощью люминесцентного микроскопа Axioscop-40 FL (Carl Zeiss) и видеосистемы на основе цифровой камеры MRс 5
(Carl Zeiss) с программой AxioVision 4.8 (Carl Zeiss). На каждом слайде регистрировали по 100 комет. Обрабатывали по 3 слайда от каждого донора на экспериментальную точку. Для анализа и обработки микрофотоизображений ДНК-комет использовали программу СASP 1.2.2 (СASPlab).
Статистическая обработка результатов проводилась с использованием пакета статистических программ Statistica 8.0 (StatSoft). Результаты исследований представлены как среднее арифметическое результатов серии независимых экспериментов и стандартной ошибки.
Результаты. На предварительном этапе работы исследованы зависимости изменений относительного количества ОР и ЩС в выделенных лимфоцитах периферической крови здоровых доноров от дозы γ-излучения и концентрации перекиси водорода при воздействии in vitro.
Хорошо известно, что при проведении электрофореза ДНК в геле агарозы доля (%) ДНК, мигрирующей в область «хвоста», зависит от степени ее фрагменти-рованности. При щелочном значении рН (рН~12), когда происходит денатурация / расплетание двунитевых молекул ДНК до однонитевых нитей, этот показатель будет зависеть преимущественно от количества ОР ДНК, как доминирующего по сравнению с двунитевы-ми разрывами типа повреждений ДНК. Повышение рН (>13) приводит к дополнительному образованию ОР по щелочно-лабильным участкам ДНК, представляющим собой апуриновые и апиримидиновые сайты [6]. В работе использовалась наиболее часто применяемая в генотоксикологических исследованиях модификация ДНК-комет при рН>13, позволяющая оценивать преимущественно сумму ОР и ЩС.
На рис. 1 представлены результаты исследований изменения уровня ОР и ЩС в лимфоцитах периферической крови человека при их облучении in vitro в дозах 1, 2, 3 и 5 Гр c мощностью дозы 1 Гр/мин при 4°С. Каждая точка, представленная на рисунке, представляет собой среднее из пяти независимых экспериментов. Было показано, что в области доз до 5 Гр кривая «доза — эффект» образования ОР и ЩС в лимфоцитах периферической крови человека при воздействии γ-излучения апроксимируется линейной функцией у =2,14+6, 91x ( R 2=0.99), где у — % ДНК в хвосте ДНК-комет; х — доза облучения в Гр.
Используемые в экспериментах условия, а именно относительно короткое время облучения (до 5 мин) и низкая (4°С) температура, значительно снижающая эффективность работы клеточных систем репарации повреждений ДНК, позволяют предположить, что наблюдаемые нами изменения % ДНК в хвосте комет зависят преимущественно от количества первичных ОР и ЩС, индуцированных γ-излучением. Линейный характер зависимостей образования первичных ОР и ЩС ДНК от дозы облучении при остром, кратковременном воздействии является характерным для живых клеток [7]. Считается, что при воздействии на клетки млекопитающих γ-излучения в дозе 1 Гр в среднем в одной клетке образуется примерно 1000 ОР ДНК [6]. Анализ дозовой кривой, представленной на рис. 1, позволят заключить, что при использованных нами экспериментальных условиях каждые 1000 ОР и ЩС ДНК увеличивают долю ДНК, мигрирующей во время электрофореза в область хвоста ДНК-комет, примерно на 7%.
Ионизирующее излучение повреждает ДНК как при прямом попадании кванта или частицы в молекулу ДНК (непосредственная передача энергии молекуле ДНК и молекулам воды, вплотную прилегающим к ДНК), так и косвенно, индуцируя свободные радикалы (преимущественно HO• радикал), повреждающие ДНК. Хорошо известно, что около 70% повреждений ДНК можно предотвратить добавлением низкомолекулярных антиоксидантов, нейтрализующих HO• радикал, что свидетельствует о существенной роли свободных радикалов в индукции повреждений ДНК в живых клетках при воздействии редкоионизирую-щего излучения. Поэтому представлялось интересным сравнить эффекты, вызванные воздействием ионизирующего излучения, с ДНК-повреждающим действием агентов, индуцирующих свободные радикалы, но не вызывающих прямых повреждений ДНК. В качестве такого агента была выбрана перекись водорода. В живых клетках перекись водорода в реакциях с ионами металлов переменной валентности и супероксиданион радикалом (реакции Фентона и Габер-Вейса) приводит к образованию повреждающего ДНК HO• радикала. Для того чтобы снизить эффективность работы ферментов, разлагающих перекись водорода (каталаза, глютанионпероксидазы), а также ферментов репарации ДНК, инкубацию клеток проводили при 4°С. Усредненные результаты пяти независимых экспериментов представлены на рис. 2.
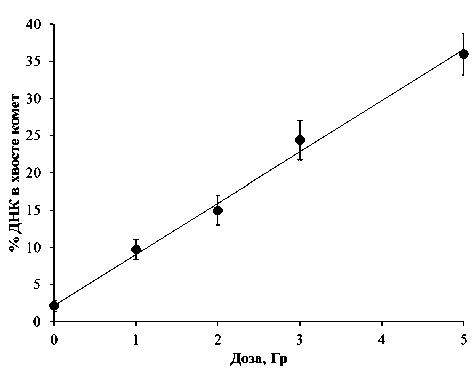
Рис. 1. Зависимость изменений уровня однонитевых разрывов и щелочно-лабильных сайтов ДНК (% ДНК в хвосте комет) в лимфоцитах периферической крови человека от дозы γ-излучения при облучении in vitro
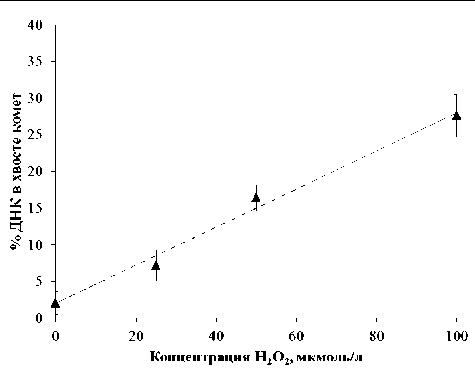
Рис. 2. Зависимость изменений уровня однонитевых разрывов и щелочно-лабильных сайтов ДНК (% ДНК в хвосте комет) в лимфоцитах периферической крови человека от концентрации перекиси водорода при инкубации клеток in vitro
Как видно из рис. 2, кривая «доза — эффект» образования ОР и ЩС в лимфоцитах периферической крови человека при воздействии перекиси водорода в концентрациях 25, 50 и 100 мкмоль/л апроксимиру-ется линейной функцией у =2,03+0,26 x ( R 2=0,99), где у — % ДНК в хвосте ДНК-комет, х — концентрация перекиси водорода в мкмоль/л.
Сравнительный анализ дозовых кривых, полученных при воздействии на клетки γ-излучения и перекиси водорода (см. рис. 1 и 2 соответственно), показывает, что при использованных нами экспериментальных условиях количество ОР и ЩС индуцированных в лимфоцитах γ-излучением в дозе 1 Гр соответствует эффекту действия перекиси водорода в концентрации ~25 мкмоль/л.
Для исследований роли структуры хроматина в клеточной радиочувствительности, с учетом результатов исследований дозовых зависимостей индукции ОР и ЩС ДНК, выбрана доза 2 Гр. При облучении в этой дозе лимфоцитов крови, находящихся в изотоническом растворе NaCl, наблюдалось ~5 кратное увеличение доли ДНК в хвосте комет.
Усредненные результаты трех независимых экспериментов, представленные на рис. 3, свидетельствуют о том, что депротеинизация хроматина в растворах со ступенчато увеличиваемой тоничностью (от 0,14 до 2,0М), увеличивает чувствительность ДНК к повреждающему действию свободных радикалов, индуцируемых ионизирующим излучением с ростом тоничности среды. Из рис. 3 видно, что кривая фактически делится на 2 участка с разными линейными угловыми коэффициентами 13,5 — до и 4,4 — после 0,6 моль/л NaCl. Именно при этой концентрации происходит полная диссоциация линкерного гистона H1, играющего ключевую роль в компактной укладке нуклеосом в тонкую фибриллу хроматина.
Подобная зависимость получена и при воздействии перекиси водорода на лимфоциты крови, инкубированные в растворах NaCl разной тоничности (рис. 4). Диссоциация негистоновых белков (0,35 моль/л NaCl) приводит к увеличению выхода ОР и ЩС ДНК ~в 1,3 раза. Увеличение тоничности среды до концентрации 0,6 моль/л, вызывающей диссоциацию линкерного гистона Н1, приводит почти к двойному увеличению выхода повреждений ДНК (~в 1,7–1,8 раза). Дальнейшее повышение концентрации NaCl, ведущее к нарушению структуры нуклеосом (1,2 моль/л) и почти полной депротеинизации хроматина (2 моль/л), увеличивает выход повреждений ДНК не столь выраженно, как предполагалось (~ в 2,2 раза при концентрации 2 моль/л).
Обсуждение. Основой процесса самоорганизации хроматина являются слабые взаимодействия его базовых структурных компонентов — ДНК и белков. Белки хроматина обеспечивают его сложную конформационную структуру, лимитируя тем самым доступ свободных радикалов к ДНК. Это существенно снижает количество индуцируемых свободными радикалами повреждений ДНК. Гипертонические растворы вызывают диссоциацию белков хроматина и тем самым увеличивают выход повреждений ДНК, индуцированных ионизирующим излучением и перекисью водорода. При этом ключевым белком, обеспечивающим корректную сборку нуклеосом в компактные архиструктуры хроматина, по всей видимости, является линкерный гистон Н1. Удаление этого белка приводит к серьезным нарушениям структуры хроматина, снижению компактности, образованию глыбчатой структуры и резкому увеличению
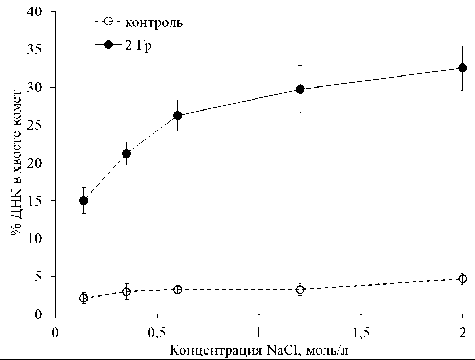
Рис. 3. Влияние изменения конформации хроматина лимфоцитов крови человека с помощью гипертонических растворов NaCl на уровень однонитевых разрывов ДНК щелочнолабильных сайтов ДНК при воздействии γ-излучения в дозе 2 Гр
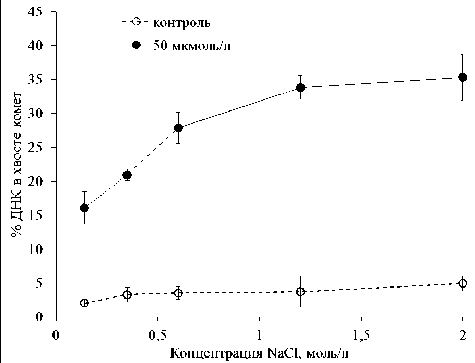
Рис. 4. Влияние изменения конформации хроматина лимфоцитов крови человека с помощью гипертонических растворов NaCl на уровень однонитевых разрывов ДНК щелочнолабильных сайтов ДНК при воздействии перекиси водорода в концентрации 50 мкмоль/л доступа свободных радикалов к ДНК. Показано, что инкубация клеток линии СНО-1 в среде, содержащей 0,5 моль/л NaCl и вызывающей диссоциацию гистона Н1, увеличивает выход повреждений ДНК, индуцированных γ-излучением, примерно в два раза [8], что близко к значениям, полученных в результате наших экспериментов. Инкубация лимфоцитов периферической крови человека в 0,5 моль/л растворе NaCl приводит к статистически достоверному увеличению спонтанных повреждений и увеличению повреждаемости ДНК 365 нм УФ-излучением, индуцирующим оксидативный стресс [9]. Интересно, что радиорези-стентные потомки облученных фибробластов джунгарского хомячка линии DH-TK характеризуются более компактной структурой хроматина по сравнению с материнскими клетками [10].
Заключение. В результате проведённых исследований показано, что степень компактизации хроматина является одним из ведущих факторов, определяющих клеточную чувствительность к оксидативному стрессу. При этом критическим белком, обеспечивающим корректную сборку нуклеосом в компактные архиструктуры хроматина и тем самым ограничивающим доступ свободных радикалов к ДНК, является линкерный гистон Н1. Увеличение тоничности среды до концентрации, вызывающей диссоциацию линкерного гистона Н1, приводит почти к двойному увеличению выхода повреждений ДНК.
Список литературы Влияние инкубации в гипертонических растворах хлорида натрия на повреждаемость ДНК лимфоцитов периферической крови человека Y-излучением и перекисью водорода
- Folle GA. Nuclear architecture, chromosome domains and genetic damage. Mutat Res 2008; 658 (3): 172-183
- McArt DG, McKerr G, Saetzler K, et al. Comet sensitivity in assessing DNA damage and repair in different cell cycle stages. Mutagenesis2010; 25 (3): 299-303
- Dmitrieva Nl, Burg MB. High NaCI promotes cellular senescence. Cell Cycle 2007; 6 (24): 3108-3113
- Elia MC, Bradley MO. Influence of chromatin structure on the induction of DNA double strand breaks by ionizing radiation. Cancer Res 1992; 52 (6): 1580-1586
- Osipov A, Arkhangelskaya E, Vinokurov A, et al. DNA comet Giemsa staining for conventional bright-field microscopy. Int J Mol Sci 2014; 15 (4): 6086-6095
- Osipov AN, Smetanina NM, Pustovalova MV, et al. The formation of DNA single-strand breaks and alkali-labile sites in human blood lymphocytes exposed to 365-nm UVA radiation. Free Radic Biol Med 2014; 73: 34-40 DOI: 10.1016/j.freeradbiomed.2014.04.027 PubMed: 24816295
- Osipov AN, Klokov DY, Elakov AL, et al. Comparison in vivo Study of Genotoxic Action of High-Versus Very Low Dose-Rate gamma-Irradiation. Nonlinearity Biol Toxicol Med 2004; 2 (3): 223-232
- Roos WP, Binder A, Bohm L. The influence of chromatin structure on initial DNA damage and radiosensitivity in CHO-K1 andxrsl cells at low doses of irradiation 1-10 Gy. Radiat Environ Biophys2002; 41 (3): 199-206
- Сметанина H.M., Пустовалова M.B., Осипов A.H. Влияние инкубации в гипертонических растворах хлорида натрия на повреждаемость ДНК лимфоцитов крови человека длинноволновым УФ-излучением. Радиационная биология. Радиоэкология 2013; 53 (6): 620-624)
- Алипов Е.Д., Тырсина Е.Г., Саримов P.M. и др. Приобретенная радиорезистентность потомков облученных клеток сопровождается перестройками в организации хроматина. Радиационная биология. Радиоэкология 2004; 44 (2): 188-197).


