Влияние электрохимических процессов на электроды и формирование осадков
Автор: Ташполотов Ы., Сатыбалдыев А.Б., Ибраимов Т.К.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Естественные науки
Статья в выпуске: 3 т.12, 2026 года.
Бесплатный доступ
Исследовано влияние электрохимических процессов в питьевой воде на перенос микрочастиц и образование осадков при воздействии постоянного электрического поля, создаваемого двумя медными электродами. Эксперименты проводились в электролитической ячейке объёмом 1 л: напряжение изменяли в диапазоне 0–29 В, а межэлектродное расстояние — от 5 до 50 мм. Наблюдались выделение газов на обоих электродах (электролиз воды), формирование вокруг анода рыхлой медной «шубы» и сравнительно слабое загрязнение катода. Установлено, что масса осадка в ряде режимов превышает измеренную потерю массы анода, что указывает на вовлечение компонентов воды в состав продуктов. Для учёта исходной минерализации выполнен рентгенофлуоресцентный анализ растворённых примесей. Предложена физико-химическая интерпретация эффекта: анодное растворение меди (Cu → Cu2+ + 2e−) сопровождается катодным восстановлением воды с образованием OH− и H2, что формирует pH-градиенты в приэлектродных зонах; миграция Cu2+ и перенос OH− приводят к осаждению Cu(OH)2 и последующей трансформации в CuO. Экспериментальные зависимости массы осадка от межэлектродного расстояния и напряжённости поля представлены графически и аппроксимированы простыми аналитическими выражениями, включая обобщённую модель m(d,E), пригодную для оптимизации режимов электроосаждения и оценки параметров процессов очистки водных сред. Отмечено, что аналогичный дисбаланс масс наблюдается и для серебряных электродов, что подтверждает универсальность механизма. Результаты могут быть использованы при проектировании компактных электрофизических установок для селективного извлечения металлов и контроля вторичного загрязнения воды в реальных условиях.
Электролиз воды, медные электроды, перенос частиц, осаждение металлов, увеличение массы осадка
Короткий адрес: https://sciup.org/14134685
IDR: 14134685 | УДК: 541.124: 621.316: 669.295 | DOI: 10.33619/2414-2948/124/03
Influence of Electrochemical Processes on Electrodes and Precipitate Formation
This paper investigates the influence of electrochemical processes in drinking water on the transport of microparticles and the formation of precipitates under a DC electric field generated by two copper electrodes. Experiments were performed in a 1 L electrolytic cell: the applied voltage was varied from 0 to 29 V, and the interelectrode distance from 5 to 50 mm. Gas evolution was observed at both electrodes (water electrolysis), along with the formation of a loose copper “coat” around the anode and comparatively weak fouling of the cathode. It was found that, under a number of operating regimes, the deposit mass exceeds the measured anode mass loss, indicating the incorporation of water components into the solid products. To account for the initial mineralization, X-ray fluorescence analysis of dissolved impurities was carried out. A physicochemical interpretation of the effect is proposed: anodic copper dissolution (Cu → Cu2+ + 2e−) occurs simultaneously with cathodic water reduction producing OH− and H2, which generates pH gradients in the near-electrode regions; migration of Cu2+ and transport of OH− lead to precipitation of Cu(OH)2 followed by transformation to CuO. The experimental dependences of deposit mass on the interelectrode distance and electric-field strength are presented graphically and approximated by simple analytical expressions, including a generalized model m(d,E), suitable for optimizing electroprecipitation regimes and estimating parameters of water-treatment processes. It is noted that a similar mass imbalance is also observed for silver electrodes, supporting the universality of the mechanism. The results can be applied to the design of compact electrophysical units for selective metal extraction and for controlling secondary water contamination under real operating conditions.
Текст научной статьи Влияние электрохимических процессов на электроды и формирование осадков
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 541.124: 621.316: 669.295
Исследование поведения дисперсных систем в электрических полях является актуальной задачей физики и электрохимии, имеющей практическое значение в процессах очистки воды, разделения веществ и электросинтеза [1, 2].
В данной работе рассматривается образование осадок микрочастиц, присутствующих в питьевой воде, под действием относительно слабого постоянного электрического поля, создаваемого медными электродами. Особое внимание уделяется анализу электрохимических процессов, сопровождающих перенос частиц, и их влиянию на формирование осадков на электродах, включая ранее наблюдаемые эффекты образования медной «шубы» вокруг анода и увеличения массы осадка по сравнению с потерей массы электрода [2, 3].
Движение заряженных частиц, диспергированных в жидкой среде, в условиях воздействия приложенного электрического поля, представляет собой процесс электрофореза. В основе явления лежит электростатическое взаимодействие: частицы, несущие электрический заряд, получают определённый импульс, направленный в сторону противоположно заряженного электрода. Действующая при этом сила (F e ) непосредственно пропорциональна величине заряда частицы (q) и напряженности приложенного поля (E), выражаясь фундаментальным соотношением F e =qE. Однако направленное движение частиц не ускоряется бесконечно. Со временем возникает гидродинамическое сопротивление (F d ), порождаемое вязкими силами в жидкости. Эта противодействующая сила значительно зависит от геометрических параметров самих частиц и вязкостных характеристик среды. Таким образом, достигается устойчивое равновесное состояние, в котором частицы движутся с постоянной электрофоретической скоростью.
Установившаяся скорость электрофореза (ϑ) определяется соотношением, связывающим её с электрическим зарядом частицы и интенсивностью электрического поля, с одной стороны, и параметрами жидкости и самой частицы — с другой. Более конкретно, электрофоретическая скорость прямо пропорциональна заряду и напряженности поля, при этом обратно зависима от вязкости среды и характерных линейных размеров частиц, что находит подтверждение в ряде экспериментальных исследований [4, 5].
Однако в реальных системах, особенно при наличии электродов, погруженных в водный раствор, необходимо учитывать сопутствующие электрохимические процессы, которые могут существенно влиять на pH среды, состав раствора и состояние поверхности электродов, что, в свою очередь, отражается на переносе частиц и процессах осаждения [5].
Для проведения более глубокого анализа проблемы, рассмотрим существующие знания в области физики, электрохимии и коллоидной химии:
Уравнения электродных реакций: на медном аноде . В кислой или нейтральной среде основной реакцией является окисление меди с образованием ионов меди(II) [5, 6]:
Cu(т) → Cu²⁺(водн) + 2e(1)
Однако, в зависимости от pH раствора и наличия других анионов, могут протекать и другие реакции. Например, при наличии хлорид-ионов может образовываться хлоридный комплекс меди:
Cu(т) + 2Cl⁻(водн) → [CuCl₂]⁻(водн) + e⁻(2)
или
Cu(т) + 4Cl⁻(водн) → [CuCl₄]²⁻(водн) + 2e⁻ .(3)
В щелочной среде окисление меди может привести к образованию оксидов или гидроксидов меди:
Cu(т) + 2OH⁻(водн) → Cu(OH)₂(т) + 2e⁻.(4)
или
2Cu(т) + 2OH⁻(водн) → Cu₂O(т) + H₂O(ж) + 2e⁻(5)
Учитывая, что в контексте очистки питьевой воды pH может варьироваться, но обычно находится в диапазоне слабокислого до слабощелочного, наиболее вероятной реакцией на аноде является образование ионов Cu²⁺.
На медном катоде (где происходит восстановление): Реакции восстановления на катоде зависят от pH раствора и наличия восстанавливающихся ионов.
В кислой среде (pH < 7) основной реакцией является восстановление ионов водорода с образованием газообразного водорода:
2H⁺(водн) + 2e⁻ → H₂(г).(6)
В нейтральной или щелочной среде (pH ≥ 7) основной реакцией является восстановление воды с образованием газообразного водорода и гидроксид-ионов:
2H₂O(ж) + 2e⁻ → H₂(г) + 2OH⁻(водн).(7)
Также, если в растворе присутствуют ионы меди(II), они могут восстанавливаться на катоде до металлической меди:
Cu²⁺(водн) + 2e⁻ → Cu(т).(8)
Эти электродные реакции оказывают значительное влияние на всю систему:
Изменение концентрации ионов меди: окисление меди на аноде увеличивает концентрацию ионов Cu²⁺ в растворе вблизи анода.
Изменение pH: восстановление воды на катоде приводит к образованию гидроксидионов, повышая pH вблизи катода. Это может влиять на заряд частиц и их стабильность [7-9].
Образование газообразного водорода: выделение водорода на катоде может создавать перемешивание раствора вблизи электрода и влиять на транспорт частиц.
Возможное осаждение гидроксида меди: в области повышенного pH вблизи катода и при наличии ионов Cu²⁺, мигрирующих от анода, может происходить осаждение гидроксида меди:
Cu²⁺(водн) + 2OH⁻(водн) → Cu(OH)₂(т) . (9)
Это может быть одним из компонентов осадка, образующегося на электродах.
Понимание этих основных электрохимических реакций является критически важным для анализа поведения дисперсных систем в электрических полях. Они напрямую влияют на химический состав раствора вблизи электродов, pH и концентрацию ионов, что, в свою очередь, определяет заряд и стабильность микрочастиц, а также процессы их осаждения на электродах [5, 6].
В частности, кинетика электродных реакций описывается уравнениями Батлера-Фольмера, которые зависят от перенапряжения на электроде [11] .
Уравнения массопереноса учитывают диффузию, миграцию и конвекцию ионов в растворе, влияя на концентрацию реагентов у электродов и, следовательно, на скорость реакций [10] .
Для описания массопереноса ионов в электрическом поле могут быть использованы уравнения Нернста-Планка [7] .
Модели изменения pH могут учитывать производство и потребление ионов H⁺ и OH⁻ в результате электрохимических реакций и их диффузию в растворе . Такой подход может быть использован для оптимизации параметров процесса (например, напряжение, время воздействия, геометрия электродов) для достижения максимальной эффективности очистки или разделения.
Материалы и методы
Пробу питьевой воды объемом 1 л поместили в электролитическую ячейку и погрузили в нее медные электроды. Перед погружением в воду электроды промыли дистиллированной водой, а остатки воды с электродов удалили фильтровальной бумагой.
В экспериментах с медными электродами, погружёнными в питьевую воду и подключёнными к источнику постоянного напряжения (0-29 В), при изменении расстояния между электродами от 5 мм до 50 мм наблюдались следующие явления [11-19].
Образование газовых пузырьков на обоих электродах, что свидетельствует об электролизе воды. На катоде преимущественно выделялся водород, а на аноде — кислород.
Анодный медный (а также серебряный) электрод постепенно и заметно растворялся, высвобождая в воду ионы меди, отдавая электроны источнику тока. В результате происходил перенос материала анодного электрода, формируя вокруг анода рыхлый осадок, названный нами «шубой».
Отсутствие заметных изменений на катоде, который оставался относительно чистым.
Увеличение массы образовавшегося осадка меди по сравнению с измеренной потерей массы анода. Аналогичный эффект наблюдался при использовании серебряных электродов, где увеличение массы осадка было еще более значительным (в 2-3 и более раза).
Эти наблюдения указывают на то, что процессы, происходящие на аноде, являются более сложными, чем просто электрохимическое растворение меди.
Результаты и обсуждение
Роль электрохимических процессов в формировании осадков. По-видимому в этих экспериментах ключевую роль в наблюдаемых явлениях играет электролиз воды, который приводит к значительным изменениям pH в приэлектродных областях [6].
Процессы на катоде: на катоде происходит восстановление воды с образованием водорода и гидроксид-ионов, формируя щелочную среду. Это приводит к тому, что высокий pH вблизи катода может препятствовать осаждению меди, даже при наличии мигрирующих к катоду под действием электрического поля ионов (Cu²⁺). Кроме того , восстановление ионов меди до металлического состояния может быть затруднено из-за преобладающего восстановления воды на катоде [20].
В связи с необходимостью определения влияния состава воды в реакторе на электрохимические процессы в начальном этапе эксперимента, был проведён анализ питьевой воды рентгенофлуоресцентным методом, результаты которого приведены в Таблице 1.
Таблица 1
ХИМИЧЕСКИЙ СОСТАВ ПИТЬЕВОЙ ВОДЫ
|
Концентрация химических элементов, присутствующих в питьевой воде |
Массовая концентрация, мг/дм3 |
ПДК |
|
Марганец |
0,045 |
0,1(0,5) |
|
Молибден |
0,007 |
0,25 |
|
Кобальт |
0,0011 |
0,1 |
|
Натрий |
112 |
20 |
|
Калий |
10 |
0,25 |
|
Ванадий |
0,0031 |
0,1 |
|
Никель |
0,02 |
0,01 |
|
Хром |
0,05 |
0,5 |
Учитывая предоставленный анализ воды (Таблица 1) и информацию о том, что частицы этих элементов менее 1 мкм, что указывает на их нахождение в коллоидном или растворенном состоянии, процесс переноса под действием электрического поля будет существенно отличаться от переноса более крупных твердых частиц:
Состояние элементов: поскольку частицы имеют размер менее 1 мкм, а вода прозрачна, большинство указанных элементов, вероятно, присутствуют в ионной форме или в виде очень мелких коллоидных частиц. Это означает, что перенос будет определяться преимущественно движением ионов и наночастиц.
Заряд ионов: зависит от pH и окислительно-восстановительного потенциала воды. Например:
Марганец может присутствовать в виде Mn²⁺, Mn³⁺ или MnO₄⁻, в зависимости от условий.
Молибден в нейтральной и щелочной среде обычно присутствует в виде анионов молибдатов (MoO₄²⁻).
Кобальт может находиться в форме ионов Co²⁺ или Co³⁺.
Натрий и калий присутствуют как катионы Na⁺ и K⁺ соответственно.
Ванадий образует различные ионы (VO₂⁺, VO₄³⁻ и др.) в зависимости от pH и окислительно-восстановительного потенциала.
Никель обычно присутствует в виде катиона Ni²⁺.
Хром (Cr) может существовать как катионов Cr3+(в кислой среде) или анионов CrO 4 2-, Cr2O 7 2- (в щелочной среде), в зависимости от pH и окислительно-восстановительного потенциала.
Электромиграция (Ионная миграция): основным механизмом переноса для ионов является их движение под действием электрического поля. Катионы будут перемещаться к катоду, а анионы – к аноду.
Электрофорез (для коллоидных частиц): если некоторые элементы присутствуют в виде наноразмерных коллоидных частиц, они также будут перемещаться в электрическом поле, если обладают поверхностным зарядом, зависящим от материала частиц и свойств воды.
Влияние концентрации: концентрации определяемых элементов, за исключением натрия и калия, относительно низкие. Это означает, что эффекты высокой ионной силы могут быть менее значительными, но не исключены. Натрий и калий, как основные ионы, будут активно участвовать в переносе заряда. Низкая концентрация других металлов может привести к их меньшему вкладу в общий перенос заряда, но их накопление на электродах может быть значимым.
Электролиз воды: при напряжении 15 В электролиз воды неизбежен, особенно вблизи электродов, что приведет к образованию водорода и кислорода и изменению pH в приэлектродных областях. Изменение pH может существенно повлиять на форму существования и заряд ионов металлов, а также на заряд коллоидных частиц.
Диффузия и конвекция: помимо движения под действием электрического поля, ионы и коллоидные частицы будут перемещаться за счет диффузии (из-за градиента концентрации) и конвекции (вызванной электроосмосом, тепловыми эффектами или гравитацией).
Оценка переноса для конкретных элементов. Катионы (Na⁺, K⁺, Co²⁺, Ni²⁺, Mn²⁺ (вероятно)): будут двигаться к катоду. Скорость зависит от заряда, размера и степени гидратации иона. Щелочные металлы (Na⁺, K⁺) обладают высокой подвижностью. Анионы (MoO₄²⁻, CrO₄²⁻, Cr2O 7 2- (вероятно), MnO₄⁻ (вероятно): будут двигаться к аноду. Ванадий и марганец: форма существования сильно зависит от pH и окислительно-восстановительного потенциала, которые могут изменяться в процессе электролиза, что делает направление их движения неопределенным. Они могут накапливаться в определенных областях реактора.
Влияние концентрации. Натрий (112 мг/дм3) и калий (10 мг/дм3): эти ионы будут основными переносчиками заряда в растворе из-за их относительно высокой концентрации. Они будут активно участвовать в процессе электромиграции. Остальные металлы (Mn, Mo, Co, V, Ni, Cr): их концентрации значительно ниже. Они будут перемещаться под действием электрического поля, но их вклад в общий перенос заряда может быть менее значительным. Однако их накопление на электродах может представлять интерес с точки зрения извлечения или осаждения.
На аноде происходит окисление воды, приводящее к образованию кислорода и ионов водорода, что создает кислую среду вблизи электрода. Эта кислая среда способствует растворению медного анода по реакции (1). Однако значительное увеличение массы осадка указывает на то, что осадок состоит не только из металлической меди. Вероятным объяснением является химическое взаимодействие ионов меди с компонентами воды и продуктами электролиза. В кислой среде ионы меди могут образовывать различные соединения, включая оксиды и гидроксиды, которые могут осаждаться на поверхности анода [22]. Например, образование оксида меди может происходить по реакции:
2Cu2+ + O_2 + 2H_2O → 2CuO + 4H+. (10)
Образование гидроксида меди возможно при локальном повышении pH вблизи анода за счет диффузии гидроксид-ионов, образующихся на катоде:
Cu2+ + 2OH- → Cu(OH)_ 2 (11)
Включение кислорода и водорода из воды в состав этих соединений объясняет увеличение массы осадка по сравнению с потерянной массой меди. Экспериментальные результаты зависимости напряженности электрического поля от расстояния между электродами, представлены в Таблице 2.
Таблица 2
ЗАВИСИМОСТЬ МАССЫ МЕДНОГО ОСАДКА ОТ РАССТОЯНИЯ МЕЖДУ ЭЛЕКТРОДАМИ И НАПРЯЖЕННОСТИ ЭЛЕКТРИЧЕСКОГО ПОЛЯ МЕЖДУ НИМИ
|
Масса медной осадки, г |
Расстояние, см |
Напряженность электрического поля Е, В/см |
|
0,88 |
2,0 |
11.76 |
|
0,66 |
4,0 |
6,13 |
|
0,48 |
6.0 |
4,25 |
|
0,39 |
8.0 |
3,31 |
|
0,32 |
9,0 |
3,06 |
Из Таблицы 1 видно, что с увеличением напряжения масса медного осадка уменьшается. Это указывает на обратную зависимость между этими двумя параметрами. Аналогично, с уменьшением напряженности электрического поля масса медного осадка также уменьшается. Это означает, что чем меньше напряженность электрического поля, тем меньше меди оседает. С увеличением расстояния между электродами масса медного осадка уменьшается. Для полного анализа построим график зависимости массы медного осадка от расстояния между электродами (Рисунок 1) и напряженности электрического поля между ними (Рисунок 2).
Анализируя данные, представленные на Рисунке 1, можно отметить, что масса образующегося осадка m (в г) и расстояние между электродами d (в см) демонстрируют практически линейную взаимосвязь. Это наблюдение подтверждается линией тренда, обозначенной в качестве линейной аппроксимации. Вместе с тем на графике отчётливо заметны незначительные отклонения экспериментальных точек от проведённой линии. Подобные расхождения могут быть вызваны случайными погрешностями при выполнении измерений, неточностями приборов либо наличием некоторых нелинейных факторов, которые не были отражены в рамках простейшей линейной модели.
Исходя из вышеизложенного, можно заключить, что с увеличением межэлектродного расстояния наблюдается тенденция к снижению массы осадка. Вероятно, подобный эффект обусловлен ослаблением напряжённости электрического поля, что, в свою очередь, снижает его эффективность в процессе осаждения вещества на электродах. Полученная зависимость в математическом виде может быть описана следующим уравнением:
m=1.20 - 0.1d (12)
Это указывает на то, что чем больше расстояние между электродами тем меньше меди оседает в ячейке.
Графическое представление результатов (Рисунок 2) отчётливо иллюстрирует сложный нелинейный характер связи, проявляющейся между массой образующегося осадка (m, г) и приложенной напряжённостью электрического поля (E, В/см).
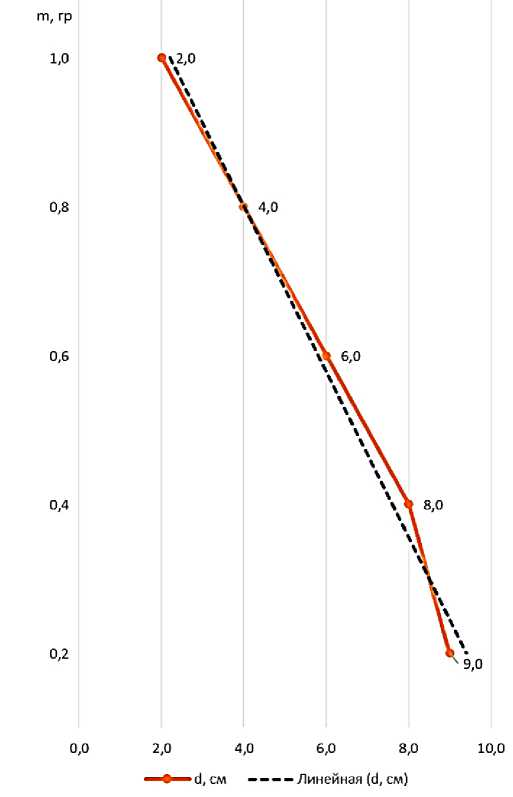
Рисунок 1. Зависимость массы медного осадка от расстояния между электродами
В начальной области графика, соответствующей относительно низким уровням электрического поля, наблюдается ярко выраженная тенденция быстрого возрастания массы осадка: каждое незначительное повышение напряжённости поля сопровождается заметным увеличением количества выпадающего вещества. Однако эта закономерность постепенно претерпевает изменения, и при достижении определённого порогового значения напряжённости дальнейший рост массы осадка существенно замедляется. Таким образом, характер кривой приобретает всё более плавный вид, что свидетельствует о снижении эффективности процесса при высоких значениях напряжённости и подчёркивает выраженную нелинейность изучаемой зависимости. Увеличение напряженности электрического поля, вероятно, приводит к усилению электростатических сил, действующих на заряженные частицы осаждаемого вещества. Это может способствовать более эффективному притяжению частиц к электродам и, следовательно, увеличению массы осадка. Замедление роста массы осадка при высоких значениях напряженности поля может свидетельствовать о насыщении какого-либо процесса, лимитирующего дальнейшее увеличение осаждения. Например, может достигаться предел скорости доставки частиц к электродам или возникать конкурирующие процессы (например, обратное распыление осадка при очень высоких полях). Нелинейный характер зависимости указывает на то, что механизм осаждения является более сложным, чем простое линейное взаимодействие с электрическим полем. Могут играть роль и другие факторы, такие как поляризация частиц, диэлектрофорез, влияние поля на среду и т.д.
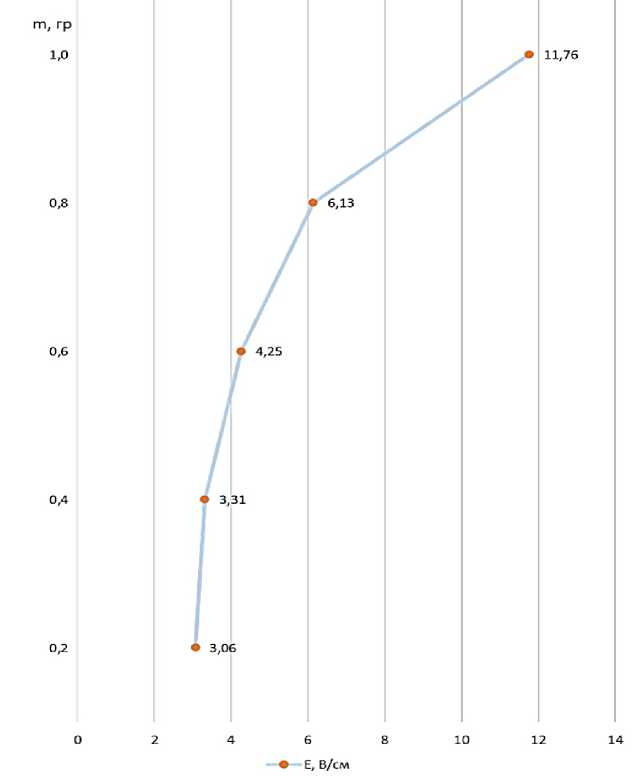
Рисунок 2. Зависимость массы медного осадка от напряженности электрического поля между электродами
График зависимости представленный на рисунке 2 можно аппросимировать в виде формулы:
m=0.07 + 0.12E - 0.05E2 (13)
Полученные результаты свидетельствуют о том, что количество образующегося медного осадка непосредственно определяется целым рядом взаимосвязанных факторов, среди которых наиболее значимыми являются напряжённость приложенного электрического поля, а также пространственное расстояние между электродами, используемыми в экспериментальной установке.
Ссылаясь на ранее приведённые формулы (12) и (13), справедливые для исследуемой системы, обладающей аддитивными свойствами, представляется возможным вывести обобщённое аналитическое выражение, позволяющее описать функциональную зависимость массы медного осадка одновременно от электрического поля и межэлектродного промежутка:
m = 0.035 - 0.05d + 0.06E - 0.025E2. (14)
Электрохимическое осаждение меди представляет собой сложный процесс, результативность которого определяется совокупностью электрических параметров и конфигурацией электролитической ячейки. При изменении пространственного расположения электродов, а именно при увеличении расстояния между ними, наблюдается заметное снижение эффективности процесса осаждения. Однако компенсация такой потери эффективности за счёт повышения приложенного напряжения является неоднозначным решением: хотя увеличение напряжения отчасти восполняет уменьшение эффективности, оно одновременно влечёт за собой дополнительные негативные эффекты, снова снижая конечную результативность осаждения меди. В связи с этим очевидна необходимость комплексного подхода, при котором учитывается влияние всех перечисленных факторов. Только такой системный анализ позволит подобрать оптимальные условия, способствующие достижению максимальной эффективности электроосаждения меди. Аналогичные процессы могут происходить и с серебряными электродами, приводя к образованию оксидов или других соединений серебра.
Вывод
Перенос частиц в питьевой воде под действием электрического поля сопровождается активными электрохимическими процессами на электродах, которые оказывают существенное влияние на формирование осадков. Образование медной «шубы» вокруг анода и увеличение массы осадка по сравнению с потерянной массой электрода объясняются химическим растворением металла анода в кислой среде, созданной электролизом воды, и последующим осаждением соединений металла (оксидов, гидроксидов) с включением компонентов воды. Дальнейшие исследования, включающие моделирование и детальный анализ состава осадков, необходимы для полного понимания механизмов, лежащих в основе наблюдаемых явлений.


