Влияние эндокардиальной процедуры “лабиринт” у пациентов с фибрилляцией предсердий на динамику показателей системы протеолиза внеклеточного матрикса и факторов роста
Автор: Баталов Роман Ефимович, Хлынин Михаил Сергеевич, Усенков Станислав Юрьевич, Гусакова Анна Михайловна, Суслова Татьяна Евгеньевна, Попов Сергей Валентинович
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 3 т.30, 2015 года.
Бесплатный доступ
Цель: определить влияние интервенционного вмешательства по поводу фибрилляции предсердий (ФП) на динамику протеолиза внеклеточного матрикса. Материал и методы. В исследование вошли 50 пациентов с персистирующей - 27 (18 мужчин), средний возраст 62,1±9,4 лет и длительно-персистирующей - 23 (14 мужчин), средний возраст 64±11 лет формами ФП, с наличием показаний для проведения интервенционного лечения аритмии. Выполнена радиочастотная антральная изоляция легочных вен, задней стенки левого предсердия (ЛП), левого истмуса сердца с использованием системы CARTO (Biosense Webster, США). Определяли динамику показателей системы протеолиза внеклеточного матрикса и факторов роста в сыворотке крови - матриксных металлопротеиназ (ММП) -1, -3, -9, тканевого фактора роста-β1 (TGF-β1), тканевого ингибитора матриксных металлопротеиназ (ТИМП-1), фактора роста фибробластов (FGF), до процедуры “Лабиринт”, непосредственно после нее, через одни сутки, через 3 и 6 мес. Результаты. Концентрация всех матриксных металлопротеиназ непосредственно после процедуры резко снижалась, что, скорее всего, связано со значительным и объемным термическим поражением ЛП. Через сутки концентрация ММП-1 имела тенденцию к восстановлению, в то время как ММП-3 сохранялась на предыдущем уровне, а ММП-9 резко возрастала до уровня, превышающего таковой до вмешательства. По истечению 3 мес. наблюдения концентрация ММП-1 и -3 практически возвращалась к исходной, а ММП-9 резко снижалась до уровня, имеющегося непосредственно после процедуры. Через полгода наблюдения концентрация ММП-1 имела тенденцию к снижению, и была ниже исходного уровня, уровень ММП-3 также не достиг исходного, в то время как концентрация ММП-9 вернулась к исходной точке. Концентрация тканевого фактора роста-β1 также резко снижалась непосредственно сразу после процедуры, с медленным восстановлением к 6-му мес. наблюдения, чего нельзя сказать о факторе роста фибробластов. Так, сразу после процедуры его концентрация снижалась, что можно объяснить массовой гибелью клеток в миокарде предсердий. Через сутки концентрация увеличивалась и достигала исходных значений. Через 3 и 6 мес. концентрация снижалась. Заключение. Снижение активности металлопротеиназ и факторов роста при отсутствии аритмии после РЧА - результат прекращения структурного ремоделирования и, возможно, его регресса.
Фибрилляция предсердий, радиочастотная аблация, фиброз, внеклеточный матрикс, структурное ремоделирование предсердий
Короткий адрес: https://sciup.org/14920039
IDR: 14920039 | УДК: 616.12-008.313.2
Effects of endocardial MAZE procedure on dynamics of extracellular matrix proteolysis and growth factor concentrations in patients with atrial fibrillation
Aim. The aim of the study was to determine the effects of interventional treatment for atrial fibrillation (AF) on the dynamic changes in the system of extracellular matrix proteolysis. Material and methods. A total of 50 patients were included in the study: 27 patients (18 males) had persistent AF (mean age of 62.1±9.4 years); 23 patients (14 males) had long-lasting persistent AF (mean age of 64±11 years). All patients received radiofrequency antral pulmonary veins isolation and linear lesions on the back wall of the left atrium and the mitral isthmus with CARTO system (Biosense Webster, USA). Blood serum changes in the parameters of extracellular matrix proteolysis and concentrations of growth factors including matrix metalloproteinase (MMP)-1, MMP-3, MMP-9, tissue growth factor β1 (TGF-β1), tissue inhibitor of matrix metalloproteinases 1 (TIMP-1), and fibroblast growth factor (FGF) were determined before the Maze procedure, immediately after the procedure, after 1 day, 3 months, and 6 months. Results. The concentrations of all MMPs immediately after the Maze procedure dramatically decreased most likely due to significant thermal damage of the left atrium. On the next day after the procedure, the MMP-1 concentration restored to the initial level, the MMP-3 concentration remained at the same level, whereas the MMP-9 concentration drastically increased to the level exceeding the initial value. After 3 months, the concentrations of MMP-1 and MMP-3 were near the initial levels, whereas MMP-9 concentration dropped to the level recorded immediately after the procedure. After 6 months of observation, the MMP-1 concentration demonstrated downward trend and was lower than the initial value; the MMP-1 level also did not reach the initial level; and the MMP-9 concentration returned to the initial level. The TGF-β1 concentration also dramatically dropped right after the procedure and slowly recovered during 6 months of follow-up. The decrease in the TGF-β1 concentration immediately after the procedure can be explained by massive cell death in the atrial myocardium. One day after the procedure, the TGF-β1 concentration increased and reached the initial level, but it decreased after 3 and 6 months. Conclusion. The reductions in the concentrations of MMPs and growth factors in the absence of AF after the Maze procedure resulted from the arrest and perhaps the reversal of the structural remodeling.
Текст научной статьи Влияние эндокардиальной процедуры “лабиринт” у пациентов с фибрилляцией предсердий на динамику показателей системы протеолиза внеклеточного матрикса и факторов роста
Фундаментальные механизмы, лежащие в основе ФП, являются предметом интенсивных исследований. Важный синергический вклад в субстрат ФП вносит электрическое, сократительное и структурное ремоделирование. В настоящее время считается, что три условия должны быть выполнены для того, чтобы развилась ФП: а) миокард должен предусматривать возможность инициации и поддержания эпизода; другими словами, он должен обеспечить электрофизиологический субстрат, который подходит для инициации и поддержания ФП; б) вегетативная нервная система должна находиться в дисбалансе; в) должен присутствовать триггер или преципитирующее событие, способные инициировать эпизод. Представляется, что кардиальный фиброз (формирование рубцовой ткани в ответ на повреждение) является важным элементом в развитии “ФП содружественного” субстрата [2].
Выявленные структурные изменения являются важной особенностью субстрата ФП, вызывая фиброз, который изменяет состав предсердной ткани и ее функции.
Фиброз является отличительной чертой аритмоген-ного структурного ремоделирования. Фиброз ткани является результатом накопления фрагментов фибриллярного коллагена, которое происходит чаще всего вследствие процесса репаративного замещения дегенеративной миокардиальной паренхимы с сопутствующим реактивным фиброзом, который способствует интерстициальному растяжению. Экспериментальные модели животных показывают региональные различия в фиброзном ремоделировании с большей чувствительностью предсердий, чем желудочков [9]. Предсердный фиброз представляет собой исход патологических конечных точек, таких как старение, сердечная дисфункция, поражение митрального клапана и, возможно, ишемия миокарда.
Предсердный фиброз – многофакторный процесс, возникающий в результате сложных взаимодействий нейрогормональных и клеточных медиаторов [4]. Структурные изменения в предсердиях пациентов с ФП были выявлены на уровне кардиомиоцитов (КМЦ) и внеклеточного матрикса (ВКМ), что наблюдалось и в клинических, и в экспериментальных парадигмах ФП. ВКМ в основном включает в себя коллаген типа I и III, фибронектин, ламинин, энтактин и фибромодулин. Ремоделирование ВКМ представляет собой неадекватный ответ на изменения в кардиальной структуре и функции в процессе прогрес- сирования сердечно-сосудистых заболеваний (ССЗ). Деградация и изменения ВКМ представляют собой процесс жесткой и динамической регуляции с хрупким балансом между матриксными металлопротеиназами (ММП) и тканевым ингибитором матричной металлопротеиназы (ТИМП) [1].
Точные механизмы и сигнальные пути, участвующие в развитии фиброза предсердий, неизвестны, но многие исследования уже показали сложные взаимодействия между нейрогуморальными и клеточными медиаторами. Триггеры для предсердного фиброза включают в себя активацию ренин-ангиотензин-альдостероновой системы (РААС), воспаление и окислительный стресс [19]. Множественные фибропролиферативные сигнальные пути способствуют переходу из профибротических молекул и медиаторов в предсердный фиброз. Ангиотензин II, известная профибротическая молекула, играет центральную роль в выработке коллагена. Трансформирующий фактор роста- β 1 (TGF- β 1), соединительнотканный фактор роста и тромбоцитарный фактор роста также являются важными посредниками в фибропролиферативных процессах. РААС участвует в структурном ремоделировании и развитии фиброза миокарда.
Трансформирующий фактор роста бета-1 (TGF- β 1) секретируется как КМЦ, так и фибробластами и служит основным медиатором регуляторных сигналов ангиотензина II для аутокринного (воздействие на саму клетку, продуцирующую ангиотензин II/TGF- β 1) и паракринного (воздействие на соседние клетки) механизмов регуляции [17]. Ангиотензин II стимулирует синтез TGF- β 1, который является мощным стимулятором активности фибробластов. И, наоборот, TGF- β 1 реципрокным образом усиливает выработку ангиотензина II и дополнительных профиброгенных факторов; таким образом, формируется цикл положительной обратной связи [3]. TGF- β 1 реализует свое действие преимущественно с помощью белка SMAD и белка SMA; этот сигнальный путь запускает активацию фибробластов и отложение коллагена [8].
Гиперэкспрессия постоянно активного TGF-β1 в миокарде приводит к избирательному фиброзу предсердий, гетерогенности проводимости возбуждения по предсердиям и тем самым способствует развитию ФП [16]. Предсердный фиброгенез у больных с ФП сопровождается двухфазным ответом: отмечается раннее увеличение, а затем потеря способности реагировать на TGF-β1. Похоже, что фиброз прогрессирует, несмотря на компенсатор- ные изменения в TGF-β1-сигнальных путях. Высокие концентрации в плазме крови TGF-β1 и ТИМП-1 являются потенциальными неинвазивными предикторами элект-роанатомического ремоделирования ЛП при неклапанной ФП [7].
Другой важный фактор, способствующий ВКМ ремоделированию сердца, – это ТИМП. ММП относятся к семейству цинкзависимых эндопептидаз, которые ответственны за деградацию всех матричных компонентов между клетками [6]. Аномальное увеличение ММП приводит к деградации матричных белков и ВКМ ремоделированию, в то время как ТИМП имеет прямое ингибирование протеолитической активности активной ММП за счет формирования сильной нековалентной связи 1:1 стехиометрических комплексов с ними. Кардиальная ММП экспрессия и активность возрастают в ряде патологических состояний, таких как сердечная недостаточность (СН) и инфаркт миокарда (ИМ). Большое количество клинических исследований и исследований на животных были направлены на определение изменений ММП и ТИМП при ФП [15]. Уровень белка ММП-9 был выше, чем уровень белка ТИМП-1 в моделях собак с ФП по сравнению с контрольной группой. Активность MMП-9 также выборочно и значимо увеличивалась на 50%, а уровень комплексного белка ТИМП-4 был значительно снижен на 50% в образцах у собак после тахисти-мулированной предсердной недостаточности. В другой модели сердца собак ММП ингибирование снижало предсердное ремоделирование и восприимчивость к ФП. Сверхрегуляция MMП-9, ТИМП-1 и ТИМП-3 была зарегистрирована в моделях свиней после быстрой предсердной стимуляции, вызванной ФП, а также изменений в синтезе коллагена и других белках ВКМ, таких как фибриллин или фибронектин. В модели ФП у собак ВКМ-свя-занная транскрипция в предсердии после желудочковой тахииндуцированной застойной сердечной недостаточности (ЗСН) согласовывалась с фиброзной патофизиологией. У пациентов с ФП увеличение экспрессии MMП-1, -3, -7, -9 и TИМП-1, -2, -3, -4 в ткани предсердий, как сообщалось, способствовало предсердному структурному ремоделированию и дилатации предсердий [14]. Предсердное ВКМ ремоделирование проявляется в селективном снижении регуляции ТИМП-2, а также сверхрегуляции ММП-2 и объеме фракции коллагена в предсердии, что было связано с развитием устойчивой ФП у пациентов с кардиомиопатией (КМП) и СН.
Усиление MMП-9 активности наряду с селективным снижением регуляции экспрессии TИМП-1 при ФП способствовало процессу предсердного структурного ремоделирования. Снижение ингиби-
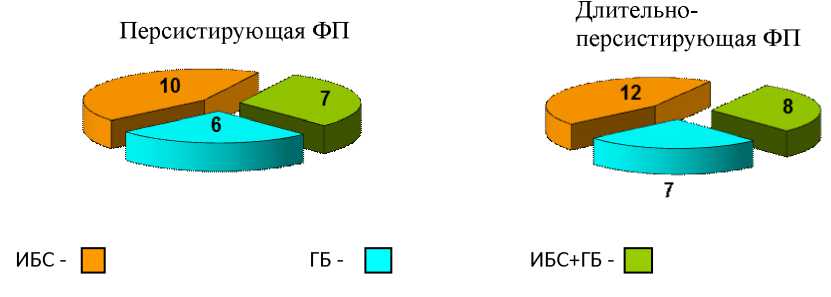
Рис. 1. Клиническая характеристика пациентов
рования активатора плазминогена (ингибитора мощного активатора многих ММП) и экспрессии тканевой металлопротеиназы может способствовать повышению активности металлопротеиназ с увеличением продолжительности ФП у человека. Содержание коллагена, кажется, больше в миокарде предсердий, чем в миокарде желудочков у больных с ФП и СН. Наличие ФП у этих больных может модулировать ММП и TИМП уровни и ВКМ состав в миокарде предсердий [5]. Цель исследования: определить влияние интервенционного вмешательства по поводу ФП на динамику протеолиза внеклеточного матрикса.
Материал и методы
В исследование вошли 50 пациентов с персистирующей – 27 (18 мужчин), средний возраст 62,1±9,4 лет и длительно-персистирующей – 23 (14 мужчин), средний возраст 64±11 лет формами ФП. Клиническая характеристика представлена на рисунке 1.
Критериями включения в исследование были:
-
1) персистирующая или длительно-персистирующая ФП;
-
2) неэффективность как минимум одного антиаритми-ческого препарата для поддержания синусового ритма;
-
3) отсутствие противопоказаний для процедуры “Лабиринт”;
-
4) отсутствие пароксизмов ФП при последующем наблюдении.
Для определения влияния процедуры “Лабиринт” на динамику показателей системы протеолиза внеклеточного матрикса и факторов определялась концентрация в сыворотке крови ММП-1, -3, -9, тканевого фактора рос-та- β 1 (TGF- β 1), тканевого ингибитора матриксных металлопротеиназ (ТИМП-1), фактора роста фибробластов (FGF). Образцы крови забирались до процедуры “Лабиринт”, непосредственно после нее, через одни сутки, через 3 и 6 мес. После взятия крови из вены ее центрифугировали, плазму замораживали и хранили при –70 °С до проведения окончательного анализа.
Всем пациентам проводилось интервенционное лечение ФП. Выполнена радиочастотная антральная изоляция легочных вен, задней стенки ЛП, левого истмуса сердца с использованием системы CARTO (Biosense
Таблица
Динамика концентраций ММП, ТИМП и факторов роста, Me(Q1–Q3)
|
Изучаемые показатели |
I II |
III |
IV |
V |
Kruskal–Wallis test |
||||
|
до |
после |
сутки |
3 мес. |
6 мес. |
PI–II |
р I–III |
р I–IV |
PI–V |
|
|
ММП-1, нг/мл |
4,419 (3,472–5,939) |
2,092 (1,091–4,149) |
3,017 (2,107–4,038) |
3,868 (2,666—5,32) |
3,163 (2,056–6,014) |
0,001 |
0,007 |
0,01 |
0,07 |
|
ММП-3, нг/мл |
9,5115 (8,176–10,027) |
7,628 (4,299–8,778) |
7,750 (4,862–9,198) |
9,168 (5,378–9,768) |
9,739 (6,779–9,972) |
0,001 |
0,01 |
0,7 |
0,9 |
|
ММП-9, нг/мл |
4,438 (2,575–5,388) |
2,421 (1,204–3,875) |
4,669 (4,021–6,869) |
2,944 (1,161–4,423) |
3,342 (2,018–5,041) |
0,01 |
0,02 |
0,001 |
0,6 |
|
ТИМП, нг/мл |
443,8 (418,3–462,0) |
201,97 (155,97–296,4) |
382,1 (316,4–407,3) |
411,6 (396–443,6) |
435,0 (374,2–444,5) |
0,001 |
0,09 |
0,8 |
0,6 |
|
TGF- β 1, нг/мл |
9,714 (6,402–11,978) |
2,3784 (1,512–6,058) |
3,348 (1,853–7,124) |
7,332 (4,59–9,74) |
8,006 (6,641–8,404) |
0,0001 |
0,001 |
0,03 |
0,4 |
|
FGF, пг/мл |
12,651 (8,317–16,26) |
10,052 (5,607–12,275 |
11,746 (7,315–13,284) |
10,469 (7,033–15,827) |
8,008 (7,196–11,325) |
0,01 |
0,4 |
0,95 |
0,72 |
|
ММП-1/TIMP-1/1000 |
0,996 (0,795–1,127) |
1,036 (0,897–1,238) |
0,79 (0,689–0,945) |
0,94 (0,875–1,023) |
0,727 (0,701–0,865) |
0,6 |
0,05 |
0,87 |
0,08 |
|
ММП-3/TIMP-1/1000 |
2,143 (1,652–2,873) |
3,777 (2,974–4,231) |
2,028 (1,789–2,647) |
2,227 (1,712–2,965) |
2,239 (1,624–3,012) |
0,04 |
0,3 |
0,86 |
0,21 |
|
ММП-9/TIMP-1/1000 |
1,0 (0,895–1,234) |
1,199 (0,897–1,956) |
1,222 (1,014–1,567) |
0,715 (0,541–0,951) |
0,768 (0,533–0,984) |
0,06 |
0,1 |
0,05 |
0,05 |
Примечание: p – уровень статистической значимости.
Webster, США). Контроль изолированности вен проводился циркулярным электродом Lasso (Biosense Webster, США). Синусовый ритм в случае необходимости был восстановлен электрической кардиоверсией. После операции в течение 3 мес. все пациенты принимали амиодарон или соталол, варфарин и сопутствующие препараты. В последующем все пациенты были свободны от приема антиаритмиков, но продолжали принимать анитико-агулянты и сопутствующие препараты.
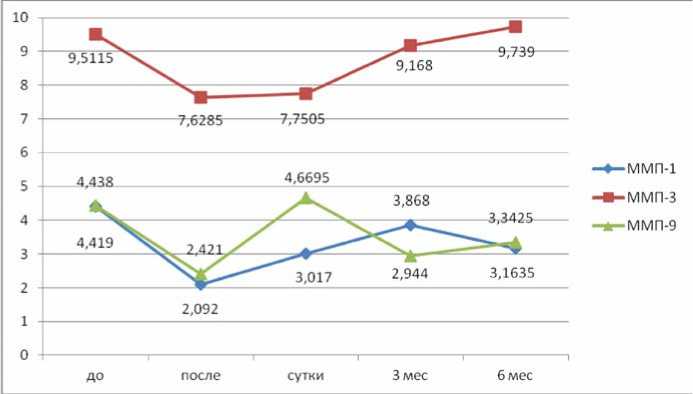
Рис. 2. Динамика концентраций МПП-1, -3, -9 у пациентов после РЧА ФП
Результаты
Все пациенты после прове денного вмешательства и весь срок наблюдения не имели пароксизмов аритмии. Динамика концентрации показателей системы протеолиза представлена в таблице.
Анализируя полученные данные, было выявлено, что концентрация всех ММП непосредственно после процедуры резко снижалась, что, скорее всего, связано со значительным и объемным термическим поражением ЛП. Дальнейшая динамика ММП отличалась. Так, через сутки концентрация ММП-1 имела тенденцию к восстановлению, в то время как ММП-3 сохранялась на предыдущем уровне, а ММП-9 резко возрастала до уровня, превышающего таковой до вмешательства. По истечении 3 мес. наблюдения концентрация ММП-1 и -3 практически возвращалась к исходной, а ММП-9 резко снижалась до уровня, отмечаемого непосредственно после процедуры. Через полгода наблюдения концентрация ММП-1 имела тенденцию к снижению и была ниже исходного уровня, уровень ММП-3 также не достиг исходного, в то время как концентрация ММП-9 вернулась к исходной точке (рис. 2).
Концентрация ТИМП-1 имела более предсказуемый характер, с резким снижением сразу после вмешательства и с медленным восстановлением к 6-му мес. наблюдения (рис. 3).
Более интересным является отношение концентрации ММП к тканевому ингибитору, что, по данным разных авторов, может быть отражением активности ферментов деградации экстрацеллюлярного матрикса. Так, по нашим данным, активность ММП-3 в отношении к тканевому ингибитору резко возрастает сразу после процедуры, что, скорее всего, связано со значительным повреждением тканей и появлением в них большого количества белко-
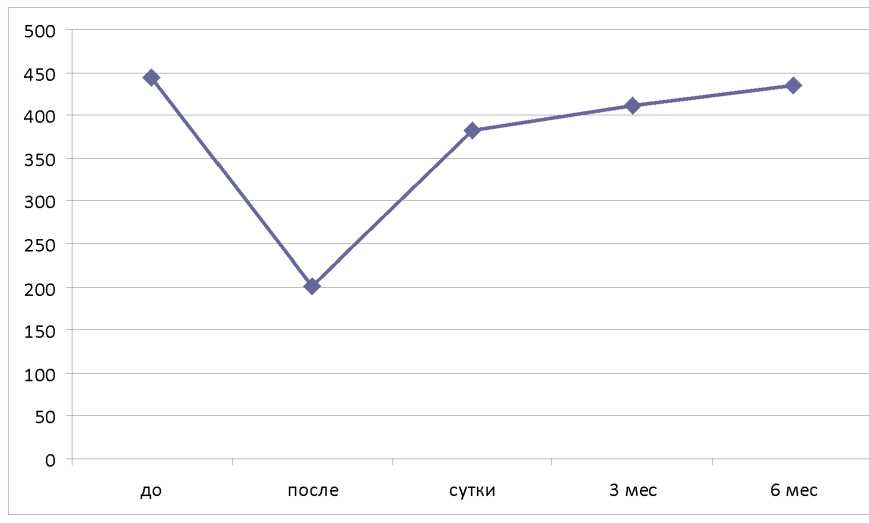
Рис. 3. Динамика концентрации ТИМП-1 у пациентов после РЧА ФП
мо отметить, что через 6 мес. происходит стабилизация процесса в отношении ММП-3, ее концентрация и отношение к ТИМП-1 возвращаются к исходным значениям. Что касается ММП-1 и -9 и отношения к ТИМП-1, то их концентрация в отсутствии эпизодов ФП становится меньше, что, по всей видимости, свидетельствует об изменении фибротических процессов в тканях – их уменьшении, что, возможно, останавливает процесс ремоделирования или даже приводит к его регрессу.
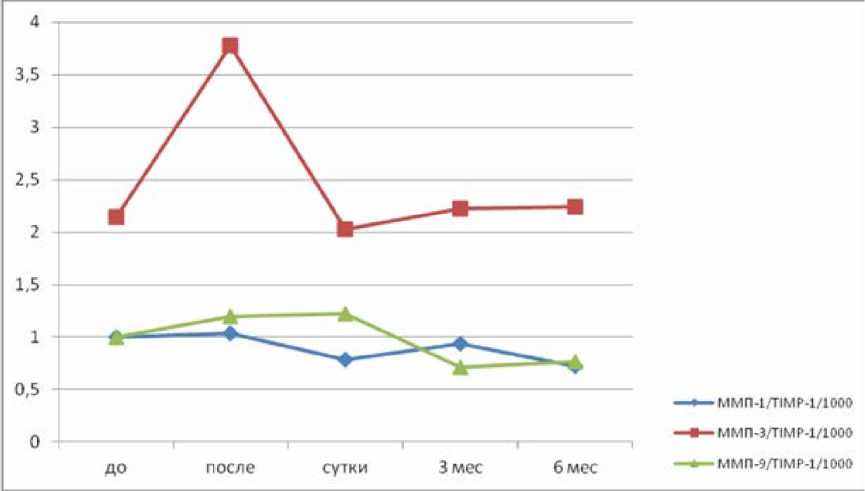
Рис. 4. Отношение концентрации ММП-1, -3, -9 к тканевому ингибитору -1
Динамика концентрации тканевого фактора роста- β 1 также имела резкое снижение непосредственно сразу после процедуры, с медленным восстановлением к 6-му мес. наблюдения, чего нельзя сказать о факторе роста фибробластов (рис. 5). Так, сразу после процедуры его концентрация снижалась, что можно объяснить массовой гибелью клеток в миокарде предсердий. Через сутки концентрация увеличивалась и достигала исходных значений, что свидетельствует о начале процессов восстановления в миокарде предсердий. Через 3 и 6 мес. концентрация снижалась, что можно объяснить только снижением активности фибробластов в отношении синтеза коллагена, уменьшением профиб-ротической составляющей процессов ремоделирования, что напрямую соотносится с активностью ММП и может являться еще одним доказательством замедления или остановки процессов ремоделирования.
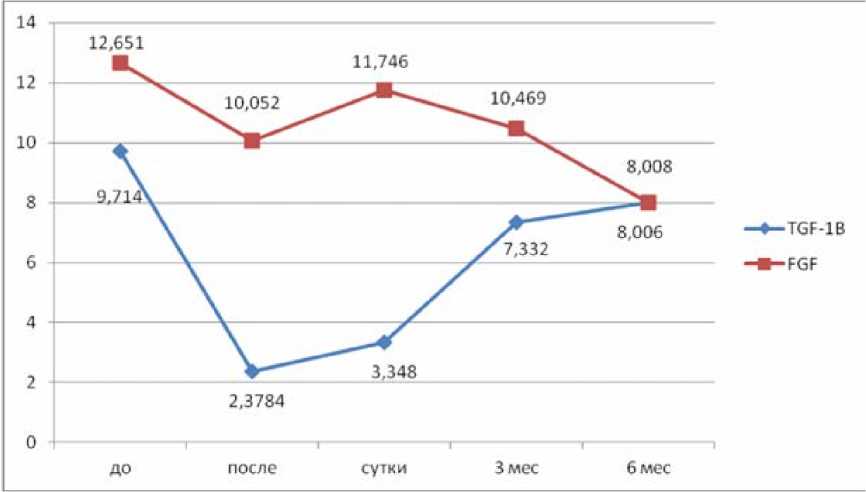
Рис. 5. Динамика тканевого фактора роста- β 1 (TGF- β 1) и фактора роста фибробластов (FGF) у пациентов после РЧА ФП
Заключение
Таким образом, полученные результаты указывают на прямое влияние процедуры “Лабиринт” на концентрацию ММП и факторов роста. Изменение отношения металлопротеиназа/тканевой игибитор является одним из ключевых моментов ремоделирования предсердий, проявляющегося в виде избыточного коллагенооб-разования и, соответственно, приводящего к фиброзу. Снижение активности металлопротеиназ и факторов роста при отсутствии аритмии после РЧА – результат прекращения структурного ремоделирования и, возможно, его регресса. Уменьшение фиброзных изменений – прямой результат исчезновения ФП и, как следствие, электрического ремоделирования, вых фрагментов, остатков коллагена и эластина (рис. 4).
Последующие изменения характеризуют процессы репарации, происходящие в миокарде, восстановление экстрацеллюлярного матрикса. В то же время необходи- что в итоге, возможно, приводит к длительному сохранению синусового ритма. Однако, скорее всего, достигнутое равновесие нестабильно в течение первого полугода наблюдения, учитывая то, что в течение этого времени продолжаются изменения в динамике факторов роста и ММП. Небольшое изменение в электрическом состоянии миокарда предсердий (восстановление проведения из легочных вен с появлением экстрасистолии, появление новых триггеров, тахикардия) могут вновь продолжить процессы электрического ремоделирования и, как следствие, структурного ремоделирования, а это значит, что продолжится избыточный синтез коллагена и замещение КМЦ фиброзной тканью. Поэтому, как показывают полученные данные, в течение первого полугодия после процедуры требуется обращать внимание на возникновение аритмий, проводить их профилактику, что может оказывать прямое влияние на отдаленную эффективность процедуры.
Работа выполнена при финансовой поддержке и на оборудовании Томского регионального центра коллективного пользования, приобретенного при поддержке Минобрнауки России по Соглашению №14.594.21.0001, а также в рамках программы повышения конкурентоспособности Национального исследовательского Томского государственного университета.
Список литературы Влияние эндокардиальной процедуры “лабиринт” у пациентов с фибрилляцией предсердий на динамику показателей системы протеолиза внеклеточного матрикса и факторов роста
- Anyukhovsky E., Sosunov E., Plotnikov A. et al. Cellular electrophysiologic properties of old canine atria provide a substrate for arrhythmogenesis//Cardiovasc. Res. -2002. -Vol. 54. -P. 462-469.
- Bajpai A., Savelieva I., Camm J. Treatment of atrial fibrillation//Br. Med. Bull. -2008. -Vol. 88. -P. 75-94.
- Burstein B., Nattel S. Atrial fibrosis: mechanisms and clinical relevance in atrial fibrillation//J. Am. Coll. Cardiol. -2008. -Vol. 51. -P. 802-809.
- Hanna N., Cardin S., Nattel S. Differences in atrial versus ventricular remodeling in dogs with ventricular tachypacing-induced congestive heart failure//Cardiovasc. Res. -2004. -Vol. 63. -P. 236-244.
- Hinescu M., Gherghiceanu M., Mandache E. Interstitial Cajal-like cells (ICLC) in atrial myocardium: ultrastructural and immunohistochemical characterization//J. Cell. Mol. Med. -2006. -Vol. 10. -P. 243-257.
- Choi E.K., Chang P.C., Lee Y.S. et al. Triggered firing and atrial fibrillation in transgenic mice with selective atrial fibrosis induced by overexpression of TGF-β1//Circ. J. -2012. -Vol. 76 -P. 1354-1362.
- Lee A.A., Dillmann W.H., McCulloch A.D. et al. Angiotensin II stimulates the autocrine production of transforming growth factor-beta 1 in adult rat cardiac fibroblasts//J. Mol. Cell. Cardiol. -1995. -Vol. 27. -P. 2347-2357.
- Purnomo Y., Piccart Y., Coenen T. et al. Oxidative stress and transforming growth factor-β1-induced cardiac fibrosis//Cardiovasc. Hematol. Disord. Drug Targets. -2013. -Vol. 13. -P. 165-172.
- Nattel S., Shiroshita-Takeshita A., Brundel B. Mechanisms of atrial fibrillation: lessons from animal models//Prog. Cardiovasc. Dis. -2005. -Vol. 48. -P. 9-28.
- Ponten A., Folestad E., Pietras K. Platelet4derived growth factor D induces cardiac fibrosis and proliferation of vascular smooth muscle cells in heart-specific transgenic mice//Circ. Res. -2005. -Vol. 97. -P. 1036-1045.
- Ponten A., Li X., Thoren P. et al. Transgenic overexpression of platelet-derived growth factor4C in the mouse heart induces cardiac fibrosis, hypertrophy, and dilated cardiomyopathy//Am. J. Pathol. -2003. -Vol. 163. -P. 673-682.
- Schultz J., Witt S., Glascock B. et al. TGF-beta1 mediates the hypertrophic cardiomyocyte growth induced by angiotensin II//J. Clin. Invest. -2002. -Vol. 109. -P. 787-796.
- Lopez B., Gonzalez A., Ravassa S.J. et al. Circulating Biomarkers of Myocardial Fibrosis: The Need for a Reappraisal//Am. Coll. Cardiol. -2015. -Vol. 65. -P. 2449-2456.
- Rahmutula D., Marcus G.M., Wilson E.E. et al. Molecular basis of selective atrial fibrosis due to overexpression of transforming growth factor-β1//Cardiovasc. Res. -2013. -Vol. 4. -P. 769-779.
- De Jong S., van Veen T.A., de Bakker J.M. et al. Biomarkers of myocardial fibrosis//J. Cardiovasc. Pharmacol. -2011. -Vol. 57. -P. 522-535.


