Влияние конструкции протеза на гемодинамику при транскатетерной имплантации аортального клапана
Автор: Селезнев М.А., Селиванов Г.Д., Пиль Н.Е., Кучумов А.Г.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 1 т.30, 2026 года.
Бесплатный доступ
Транскатетерная имплантация аортального клапана (ТИАК) является малоинвазивным подходом при лечении аортального стеноза у пациентов, которым противопоказано открытое хирургическое вмешательство. Несмотря на активно растущее количество данных миниинвазивных операций, существует ряд осложнений, вызванный ограниченным выбором типов и видов имплантов, не учитывающих индивидуальные особенности пациента, что приводит к вопросу о кастомизации протезов ТИАК. Разработка персонализированных конструкций протезов позволила бы снизить количество постоперационных осложнений, таких как параклапанная регургитация или повреждение фиброзного кольца, повышая качество жизни пациентов на основе оценки гемодинамических показателей. Таким образом, целью данного исследования является численное моделирование гемодинамических характеристик в аорте после ТИАК для оценки влияния конструктивных особенностей протеза на его эффективность. В работе рассматривается восемь параметризованных геометрий протезов, две из которых являются моделями коммерческих клапанов (Evolut R PRO и SAPIEN 3), а остальные шесть – разработанными авторами данной статьи. Решалась связанная задача с учетом взаимодействия жидкости и твердого тела. На входе в аорту задавалась функция скорости, соответствующая данным эхокардиографии, а на выходе – давление, определяемое двухэлементной моделью Франка. Комплексный анализ интегральных показателей позволил выделить три геометрии, демонстрирующие оптимальные площади открытия (EOA>1,5 см2), умеренные градиентами давления (в пределах 7–12 мм рт. ст.), и скорости ниже 2 м/с в пике систолы, а также низкие значения OSI (OSI < 0,25). Данные значения минимизирует риски тромбообразования и преждевременного износа створчатого аппарата. Полученные результаты служат основой для дизайна, проектирования и производства персонализированных протезов ТИАК с учетом анатомических и физиологических особенностей конкретного пациента.
Транскатетерная имплантация аортального клапана, протез аортального клапана, численное моделирование, двусторонний подход ЭйлераЛагранжа, гемодинамические характеристики, параметризованные геометрии
Короткий адрес: https://sciup.org/146283286
IDR: 146283286 | УДК: 531/534: [57+61] | DOI: 10.15593/RZhBiomeh/2026.1.15
Influence of prosthesis design on hemodynamics in transcatheter aortic valve implantation
Transcatheter aortic valve implantation (TAVI) is a minimally invasive approach for the treat-ment of aortic stenosis in patients with a high risk of postoperative complications who are not can-didates for open surgery operation. Despite the rapidly growing number of such operations, they have a number of complications with limited choice of parameters and types of implants that do not take into account the individual characteristics of the patient. This leads to the question of customization of TAVI implants. The development of personalized prosthetic designs can reduce the incidence of postoperative complications, such as paravavular regurgitation or damage to the annulus fibrosus, thereby improving patients’ quality of life by optimizing hemodynamic indicators. Thus, the purpose of this study is to numerically simulate the hemodynamic characteristics in the aorta after TAVI to assess the impact of the prosthesis design on its effectiveness. This paper presents eight parametrized prosthesis geometries: two represent models of commercial valves (Evolut R PRO and SAPIEN 3), and the remaining six were developed by the authors. A coupled problem involving fluid-structure interaction was solved. A velocity profile based on echocardiog-raphy data was prescribed as the inlet boundary condition at the aorta, while a pressure determined by a two-element Windkessel model was prescribed at the outlet. Based on a comprehensive anal-ysis of the integral parameters, three geometries were selected. These geometries demonstrate optimal hemodynamic performance: effective orifice areas exceeding 1.5 cm², moderate pressure gradients (7–12 mmHg), and peak systolic velocities below 2 m/s. Additionally, they exhibit low OSI values (OSI < 0. 25), which is indicative of a reduced risk of thrombosis and premature leaflet fatigue. The obtained results provide a basis for the design, engineering, and manufacture of personalized TAVI prostheses that take into account the specific anatomical and physiological features of each patient.
Текст научной статьи Влияние конструкции протеза на гемодинамику при транскатетерной имплантации аортального клапана
RUSSIAN JOURNAL OF BIOMECHANICS
Долгие годы основным лечением аортального стеноза оставалось открытое хирургическое вмешатель- ство, однако у большей части пациентов, особенно пожилого возраста, имеющих сопутствующие заболевания различного характера, риск проведения такой тяжелой операции является крайне высоким [1].


Эта статья доступна в соответствии с условиями лицензии Creative Commons Attribution-NonCommercial 4.0 International
License (CC BY-NC 4.0)
This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License (CC BY-NC 4.0)
Это послужило стимулом для развития малоинвазивных технологий, способных снизить нагрузку на организм человека [2], во время проведения операции. Ключевое место среди таких операций занимает транскатетерная имплантация аортального клапана (ТИАК) [3]. Малоинвазивный подход позволяет заменить поврежденный клапан, не прибегая к рассечению грудной клетки и остановке сердца, подключая пациента к аппарату искусственного кровообращения [4]. В сжатом состоянии протез вводится через бедренную артерию и доставляется до клапана с помощью специально разработанной системы доставки [5]. Далее имплант устанавливается, прижимая створки нативного клапана к стенкам аорты и начиная функционировать вместо него. По месту установки клапаны можно разделить на два вида: интраанулярные и супраанулярные. Первые устанавливаются строго внутри фиброзного кольца таким образом, что створки протеза оказываются на таком же уровне, где раньше располагались створки родного клапана пациента. Супраанулярные импланты [6] устанавливаются так, что створчатый аппарат протеза фиксируется в восходящей части аорты - синусах Вальсальвы, позволяя имплантировать клапаны с большим эффективным отверстием для пациентов, имеющих узкое фиброзное кольцо. Исследования показывают, что глубина установки клапана и его анатомическая совместимость существенно влияют на трансклапанные градиенты, эффективную площадь отверстия и риски параклапанной недостаточности и дисфункции створок [7; 8]. По типу установки клапаны делятся на саморасширяемые, раскрытие которых происходит благодаря свойствам материала с памятью формы [9; 10], из которых выполнен сетчатый каркас импланта, примерами таких протезов могут послужить Medtronic CoreValve, Evolut PRO, Portico и т. д. и баллоннорасширяемые, которые раскрываются благодаря специальному баллону, встроенному в систему установки ( Sapien 3 , Sikelia , Triskele ).
Несмотря на использование существующих протезов на практике, они имеют ряд факторов риска, которые могут оказать существенное влияние на здоровье пациента. Одним из таких рисков может быть параклапанная регургитация, при которой кровь попадает обратно в левый желудочек из-за недостаточно плотного прилегания протеза к стенкам аорты. Еще одной проблемой может стать повреждение фиброзного кольца или стенок аорты [11]. На практике также встречаются случаи, когда из-за постоянного движения створок клапан деформируется, нарушая дальнейшую гемодинамику. Описанные выше проблемы часто возникают из-за некорректно подобранного размера протеза, а это, в свою очередь, происходит по причине узкой линейки выбора. Врачам приходится делать выбор, исходя из имеющихся вариантов, а организм каждого человека - уникален, что подводит к вопросу о создании пациенто-ориентированных моделей, способных устранить существующие проблемы.
Для разработки новых протезов на помощь приходят методы математического моделирования [12-14], позволяющие определить изменение гемодинамических характеристик после установки протеза в аорту. Хотя многочисленные исследования оценивают различные аспекты ТИАК, сохраняется значительный пробел в знаниях относительно оптимизации конструкции клапана и детального взаимодействия между протезом клапана и естественной средой корня аорты, особенно в случае бикуспидальных аортальных клапанов [15]. Кроме того, долгосрочные последствия различных конструкций створок (внутри- и надкольцевых) и их влияние на долговечность клапанов и гемодинамическую эффективность остаются недостаточно изученными [16; 17]. С помощью численного моделирования можно определить поведение импланта внутри аорты, подбирая нужные параметры для конкретного пациента и позволяя создавать новые решения. Использование метода конечных элементов (FEA), вычислительной гемодинамики (CFD) [18] и моделирования взаимодействия жидкости и твердого тела (FSI) [19] позволяет исследователям более точно характеризовать механику развертывания устройства и работу створчатого аппарата клапана при физиологических нагрузках. В совокупности эти взаимодополняющие методы помогают ученым улучшать конструкции клапана, делая их более эффективными и надежными, способствуя безопасности пациента после проведения операции.
Как уже было сказано ранее, для численного моделирования ТИАК используют три основных метода: метод конечных элементов ( FEA ), вычислительную гидродинамику ( CFD ) и моделирование взаимодействия жидкости и конструкции ( FSI) [20-22]. Метод конечных элементов преимущественно используется для структурного анализа и оценки напряжений и деформаций створчатого аппарата и конструкции стента протеза, возникающих в процессе радиального сжатия, имплантации и при циклических нагрузках во время сердечного цикла [23-27]. Такие исследования позволяют выявить зоны, наиболее подверженные механическому износу и потенциальному разрушению. CFD применяется для анализа гемодинамических характеристик потока при моделировании протеза, установленного в аорту. С помощью CFD рассчитываются параметры, связанные с риском тромбообразо-вания: рециркуляция крови, время пребывания частиц вблизи створок и сдвиговые напряжения [28-31]. Наиболее физиологичным, но и наиболее вычислительно затратным подходом является FSI , который объединяет FEA и CFD , позволяя моделировать взаимодействие движущихся створок и потока крови [27; 32-36]. FSI -модели дают наиболее полное представление о внутрисердечной гемодинамике и механике створок.
Ряд исследований уже продемонстрировал потенциал описанных выше методов для изучения механизмов поведения протеза.
Так, работы [28; 33] показали возможность использования гемодинамических параметров, полученных из пациенто-ориентированных CFD - и FSI - моделей.
г
д
е
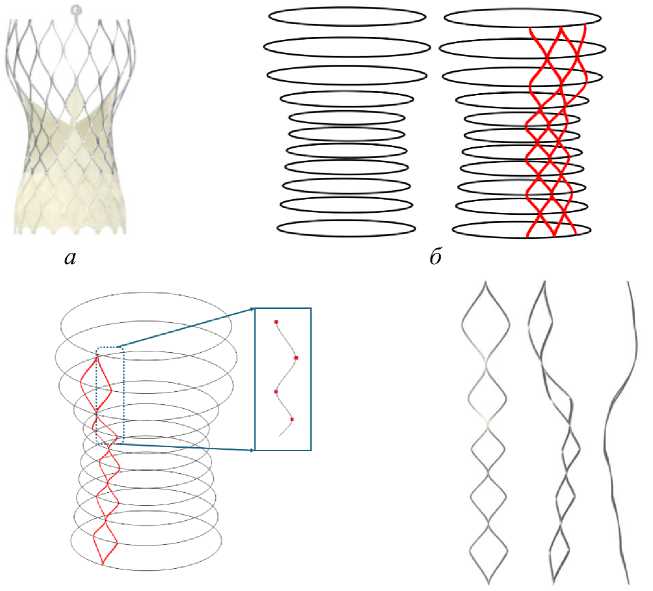
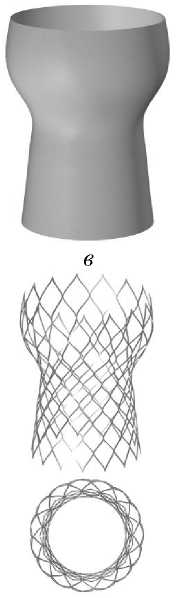
Риc. 1. Алгоритм построения каркаса клапана Evolut R PRO : а – конструкция промышленного клапана, б – построение вспомогательных окружностей, в – готовая поверхность, описывающая форму стента, г – сплайны, построенные по окружностям, д – геометрия одного вертикального сегмента, е – итоговая геометрия
Исследования тромбоза створок выявили влияние анатомии корня аорты [29; 37; 38], особенностей имплантации [27; 36] и даже наличия параклапанной регургитации [39] на параметры кровотока, ассоциированные с риском тромбообразования. Работы [23; 40] детально описали влияние радиального сжатия и асимметричного раскрытия на распределение механических напряжений в створках. В работах [41; 42] применяются методы вычислительной гидродинамики и конечно-элементного анализа для моделирования взаимодействия потока с протезом. В обеих работах используется метод погруженных границ, который является модификацией метода FSI для автоматического расчета контакта между протезом и тканями без введения дополнительных моделей контакта.
В работе [41] представлена валидация пациенто-ори-ентируемой модели транскатетерной замены аортального клапана с использованием метода погруженных границ. Важно также отметить, что в данной работе моделируется полный процесс ТИАК, включающий радиальное сжатие, установку и дальнейшее функционирование. Моделирование саморасширяющегося клапана Evolut R в анатомии конкретного пациента показало хорошее соответствие клиническим данным, представленным в работе [43] (градиент 6,84–9,62 мм рт. ст., EOA 1,32–1,50 см²).
В статье [42] параметрически смоделированы две конфигурации протезов: аналог саморасширяющегося
( THV–A ) и аналог баллоно-расширяемого ( THV–B ). Установлено, что THV–B обеспечивает более высокие скорости кровотока и площадь открытия, но THV–A демонстрирует меньшую регургитацию.
В исследовании [44] численно оценено влияние глубины имплантации саморасширяющегося клапана Medtronic Evolut R на его производительность. Показано, что желудочковая глубина имплантации (2 мм) обеспечивает максимальную площадь контакта (0,59 см²) и силу фиксации (10,26 Н), в то время как промежуточное положение (4 мм) минимизирует риск активации тромбоцитов.
Работа [43] посвящена оценке нормальной функции транскатетерного клапана на основе метода комплексной эхокардиографии. Авторами установлена прямая зависимость эффективной площади отверстия ( EOA ) от анатомии нативного кольца, а также определены нормативные показатели для клапанов семейства SAPIEN и Evolut .
В работе [45] представлена методология оценки напряжения сдвига на стенке сосуда, подчеркивается его роль в прогрессировании атеросклероза и универсальность методов вычислительной гидродинамики для моделирования потоков через транскатетерные клапаны. С более детальным обзором работ, посвященных моделированию ТИАК, можно ознакомиться в исследованиях [46; 47].
д
е
ж
з
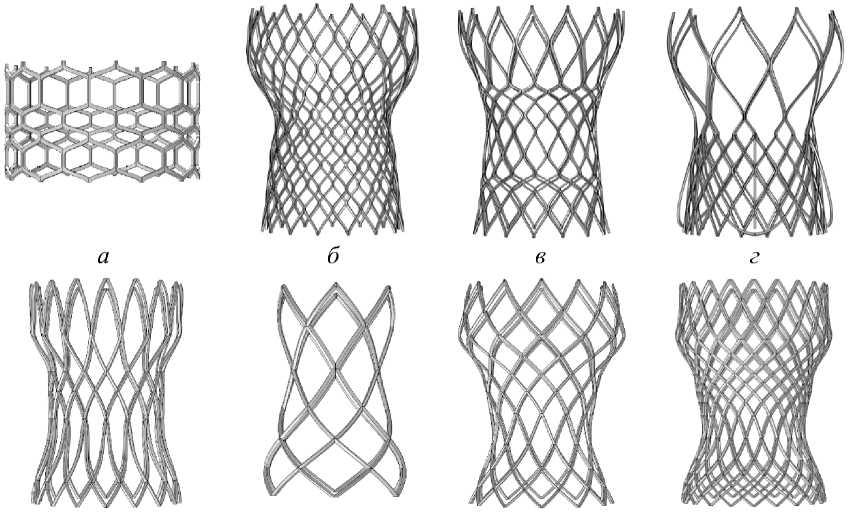
Рис. 2. Проектирование геометрий стентов ТИАК: a – Sapien 3 ; б – Evolut ; в – GAM ; г – RuVal ; д–з – параметризованные геометрии
а
б
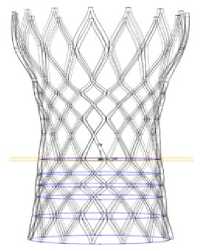
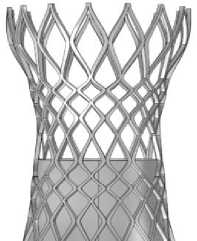
Рис. 3. Построение юбки и створок клапана: а – создание окружностей для лофта; б – окружности, объединенные с помощью инструмента loft
Текущее исследование направлено на устранение недостатков существующих протезов путем разработки и валидации комплексной математической модели, включающей взаимодействие жидкости и твердого тела для моделирования гемодинамических характеристик транскатетерных аортальных клапанов. В частности, будет проведена оценка ключевых гемодинамических параметров, включая скорость кровотока, распределение давления, пристеночные касательные напряжения, индекс колебательных напряжений, эффективную площадь отверстия ( EOA ) и геометрическую площадь отверстия (GOA), а также анализ напряжений створок.
Материалы и методы
Построение геометрий каркасов для ТИАК
В ходе работы были созданы восемь геометрий стентов ТИАК, два из которых являются коммерческими
( SAPIEN и Evolut R Pro ). Для проектирования жестких конструкций использовались различные принципы построения, однако все геометрии имели параметризованную сетчатую структуру, которая позволяет использовать меньшее количество металла, придавая каркасу возможность на основе свойств материала свободно расширяться и сужаться вслед за изменениями аорты. Все геометрии были созданы в коммерческом программном пакете COMSOL Multyphysics .
Основной принцип задания всех геометрий можно разбить на две подзадачи – задание характерной выпуклой формы самой конструкции и придание ей нестандартной ячеистой структуры, которая периодически повторяется на протяжении всей боковой поверхности клапана. Рассмотрим алгоритм построения геометрии на примере построения коммерческого протеза Evolut R PRO (рис. 1). Особенностью формы стента является переменный радиус, который меняется как функция


а
б

в
г
д
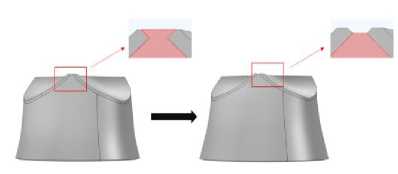
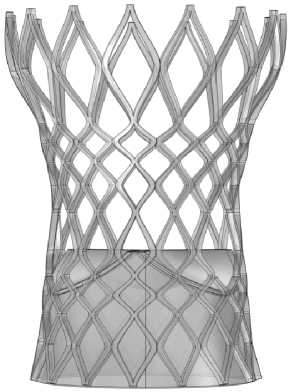
Рис. 4. Компоновка и создание створок, юбки и каркаса: а – создание створок; б – итоговый вид створок в протезе; в – построение юбки; г – сглаживание углов стыка; д – совмещение с каркасом
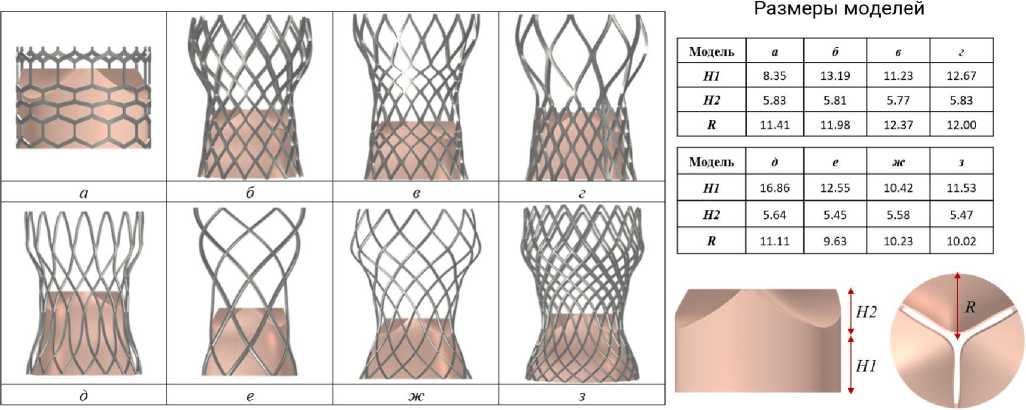
Рис. 5. Итоговые геометрии протезов
высоты. Для получения требуемой геометрии используется интерполяция по замкнутым кривым.
Данные кривые представляют собой окружности с различным радиусом, они образуют собой «скелет», который в итоге помогает построить поверхность стента. Количество и положение этих окружностей зависит от расположения и числа ячеек стента.
Далее для получения гладкой поверхности стента используется интерполяция вспомогательных окружностей при помощи кубических сплайнов Безье, которые обеспечивают плавные переходы между сегментами без нежелательных изломов. В результате выполнения первой подзадачи полученная форма стента выглядит следующим образом (см. рис. 1, в). Следующим этапом становится добавление ячеистой структуры клапана, которую мы будем строить, опираясь на готовую поверхность. Для построения кривых, которые формируют конструкцию стента Evolut R Pro, используется тот же метод, с помощью которого строится его форма, то есть метод интерполяции при помощи рациональных кубических кривых, такие кривые лучше всего подходят для получения форм с плавным изменением кривизны.
Набор кривых образует собой сплайн, фрагмент которого отображен на рис. 1, г .
Каждая кривая охватывает участок между вспомогательными окружностями, тем самым точки, через которые она проходит, определяются радиусом и положением этих окружностей.
Полученная геометрия одного вертикального сегмента ячеистой структуры клапана выглядит следующим образом (см. рис. 1, д ). С его помощью можно получить финальную геометрию стента, используя необходимое число сегментов и расставляя их по кругу (рис. 1, е ).
Таким образом, все геометрии каркасов представлены на рис. 2, более детальное описание построения каждой из геометрий представлено в статье [48].
Построение геометрии створчатого аппарата
Для построения створок совместно с юбкой для каждой из геометрий ( а–з ) были взяты за основу створки, подробный алгоритм построения которых описан в [49]. Для построения нижней части створчатого аппарата (юбки) каждого стента строились окружности, как и при создании самих каркасов, однако у этих окружностей радиусы соответствуют внутренним радиусам каркаса (рис. 3, а ). В качестве примера на рисунках 4, 5 показаны все шаги создания юбки для геометрии под буквой « В ».
Так как каждый клапан имеет разную форму, то и набор окружностей у всех разный, отличительными факторами являются высота, до которой строится юбка и радиусы этих окружностей. Радиусы подбирались так, чтобы юбка касалась геометрии каркаса. Далее из этих окружностей создавалась 3D -геометрия с помощью инструмента loft (см. рис. 3, б) . С помощью полученной геометрии и операций partition objects и delete обрезались лишние части створок (рис. 4, а ) так, чтобы они максимально плотно устанавливались в каркасе (см. рис. 4, б).
Следующим шагом создавалась поверхность, вытянутая из точно таких же окружностей, как и на первом шаге. Для поверхности задавалась толщина равная толщине каркаса: 0,8 мм. В итоге получилась форма стенок для юбки (рис. 4, в). Далее, с помощью операций difference и delete удалялось все лишнее и получалась форма юбки, объеденной со створками. Дополнительно была вырезана часть юбки, которая соединяет створки между собой (рис. 4, г). Это было выполнено с целью улучшения сетки в процессе деформирования створок при численном моделировании. На рис. 4, д представлена итоговая геометрия совместно с каркасом. Итоговый вид всех протезов а-з с указанием размеров, используемых створок, показан на рис. 5.
Построение геометрии аорты
На первом этапе построения геометрии аорты была создана плоскость, в которой была задана кривая с помощью интерполирования точек и дуги (рис. 6, а ). Кривая задает приближенную физиологическую форму синусов аорты. Далее к этой кривой была применена операция вращения относительно оси xw в нижней точке кривой, позволяющая перейти к 3 D форме (рис. 6, б) .
Следующим шагом были добавлены плоскости ( cap faces ) сверху и снизу, чтобы получить закрытую геометрию. После этого к данной фигуре были добавлены верхний и нижний цилиндры разного радиуса (физиологически верно), отвечающие за часть аорты над синусами и под ними соответственно, так, как показано на рис. 6, в . С помощью очередной операции вращения
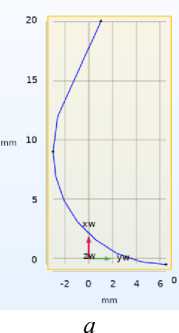

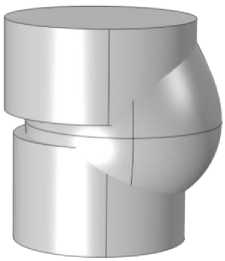
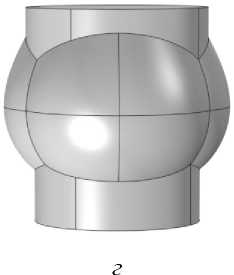
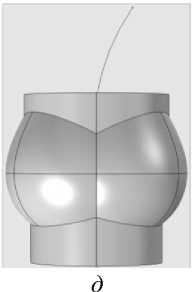

Рис. 6. Алгоритм построение аорты: а - кривая, задающая форму синусов аорты; б - геометрия кривой после вращения; в - часть синуса вместе с цилиндрами, задающими радиусы аорты; г - нижняя часть аорты вместе с синусами; д - форма кривой для верхней части; е - полностью построенная геометрия аорты
получилась геометрия с тремя синусами, применив к ней операцию объединения ( union ), без сохранения внутренних границ, получился следующие результат (рис. 6, г ).
Для построения верхней части была построена линия, повторяющая геометрический изгиб аорты (рис. 6, д ), и к ней применялась операции протяжки ( sweep ) от верхней плоскости. Полностью построенная модель представлена на рис. 6, е . Данную модель удобно регулировать с помощью радиусов цилиндров и форм кривых для синусов и верхней части.
Концептуальная постановка задачи
В рамках данной работы стояла задача оценить гемодинамические характеристики используя 8 геометрий створчатого аппарата, в зависимости от геометрии каркаса, применяя ALE-FSI -подход. В мельчайших кровеносных сосудах кровь нельзя принимать однородной жидкостью из-за сравнимых диаметров эритроцита и капилляра. Однако в сосудах диаметром более 300 мкм кровь может рассматриваться как однородная среда [50]. Поэтому при моделировании кровь принимается несжимаемой ньютоновской жидкостью с постоянными плотностью 1060 кг/м3 и вязкостью 0,0035 Па^с [51]. В крупных сосудах характер течения крови принимается ламинарным [52-54], а профиль скорости имеет равномерное распределение. В качестве упрощения модели, аорта рассматривается как область жидкости, то есть не учитывается материал стенок, а также не учитывается контакт между каркасом протеза и стенкой. Для определения гемодинамических характеристик моделировался один сердечный цикл при патологии. Время такого цикла равно 0,6 с. Все численные расчеты проводились в программной среде COMSOL Multiphysics .
Математическая постановка задачи
Соотношения для описания поведения твердого тела
В данной работе для описания биомеханического поведения створчатого аппарата использовалась анизотропная модифицированная модель Хольцапфеля - Гассера - Огдена [55; 56], включающая в себя в качестве изотропной части модель Муни - Ривлина [57-59]. Данная модель учитывает радиальную и циркулярную ориентацию коллагеновых и эластиновых волокон. Связь между напряжениями и деформации створок можно представить в виде следующей системы:
Таблица 1
Параметры модели Муни – Ривлина
д u
Р —I = v' °,, 51s д W
° s = ^, д е
£ = 1 ( Vus + (Vus )T + (Vus )■ (Vus )T ) ,
Соотношения для описания поведения жидкости
Для описания потока крови записываются уравнения Навье - Стокса [60; 61] с условием несжимаемости:
V-uf = 0, of =- pI + T,
S u f
P —+ pf \vf -uf J-Vp =V-of + b;
где υ – скорость течения крови, u – поле скоростей жидкости, σ – тензор напряжений в жидкости, p f - плотность крови, p - давление, t - девиаторная часть тензора напряжений, I – единичный тензор, b – объемные силы, действующие на жидкость. Кровь считается несжимаемой Ньютоновской жидкостью с постоянной плотностью = 1060 кг/м3 и вязкостью равной 0,0035 Па⸱с. Жидкость моделировалось как ламинарное течение.
Алгоритм взаимодействия твердого тела и жидкости
Для описания поведения жидкости на границе с твердым телом мы использовали двусторонний ALE–FSI подход [62; 63]. Подход можно разделить на два ключевых этапа: на первом этапе численно решается уравнение Навье–Стокса в каждом узле сетки жидкости и определяются поля давлений и скоростей жидкости. На следующем этапе эти условия давлений и скоростей передаются на границу твердого тела, в нашем случае, это створки протеза, и считается сила взаимодействия:
Далее с полученными граничными условиями рассчитываются перемещения створок, используя модель Хольцапфеля – Гассера – Огдена и градиент деформации. После деформации створок, перестраивается и сетка жидкости, затем повторяется снова первый шаг, но уже на новой сетке. Таким образом, происходит весь процесс вычисления. На границах взаимодействия принимается условие совместности:
u s = u f , us = uf , ^ • n s = ff f • n f (15)
где nˆ и nˆ нормали со стороны твердого тела и жидко сти соответственно.
Граничные условия
Граничные условия, используемые в работе представлены на рис. 7, а. Каждый из имплантов устанавливался внутри аорты и имел жесткое закрепление, аорта рассматривалась как область жидкости, то есть без учета деформируемых стенок. На входе в аорту задавалась функция скорости потока крови, график которой представлен на рис. 7, б. Данная функция была получена на основе данных эхокардиографии, предоставленных медицинскими учреждениями. На выходе задавалось давление (рис. 7, в), распределение которого от времени f = n •{-pI + (p (Vuf +(Vuf) T))} (13)
Пересчет силы из–за деформации сетки:
F = f • d U , dV
где F – сила, прикладываемая к границе твердого тела.
Таблица 2
Параметры модели Франка
|
C , мм рт. ст. мл-1 |
R p , |
R c , |
||
|
мм рт. ст. мл-1 |
∙ с |
мм рт. ст. мл-1 |
∙ с |
|
|
3,128 |
0,6652 |
0,0914 |
||
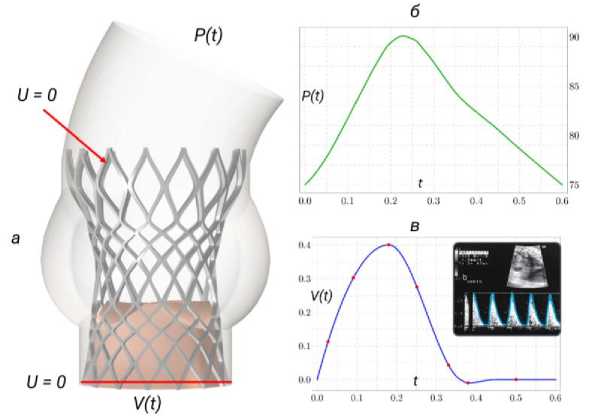
Рис. 7. Граничные условия: а – основные граничные условия; б – давление на выходе; в – скорость на входе
было получено из модели Франка, с параметрами, представленными в табл. 2.
Модель Франка позволяет течение в резервуаре с податливыми стенками через совокупность трех компонентов: упругое сопротивление стенки сосудов, резистивное сопротивление и инерционный компонент, связанный с массой крови. Часто для построения данной модели и упрощения расчетов применяются эквивалентные схемы электрических цепей [64; 65].
Модель Франка описывается следующими соотношениями:
dP ,P ,
C~f + W = Qao ,(16)
dtR
Pao (t )= QaoRc + Pwk ,(17)
Pout = Pao (t),(18)
где P – давление, накопленное в модели Франка (мм рт. ст.), C - коэффициент податливости артерий (мм рт. ст. мл - 1), Rp - сопротивление периферических сосудов (мм рт. ст. мл - 1 ■ c), QAo - объемный расход крови в аорту (мл/с), Pa о( t ) - давление в аорте (мм рт. ст.), Rc - характеристическое сопротивление . (мм рт. ст. мл 1 ■ c).
На стенке аорты было установлено условие прилипания, нижняя часть юбки была закреплена жестко, а створки протеза могли перемещаться свободно.
Расчетная сетка
В исследовании строилась сетка на трех телах: аорта, створчатый аппарат и каркас протеза. Поскольку каждая
А
Б
В
Г
20 мс
100 мс
190 мс
310 мс
380 мс




Скорость, м/с
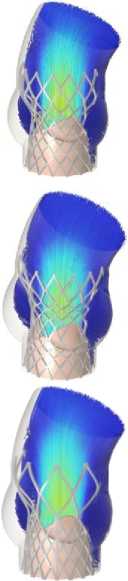
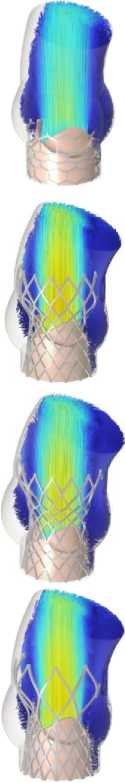
Рис. 8. Распределение поля скоростей в ключевые моменты сердечного цикла для моделей А–Г
геометрия имеет разные размеры, количество элементов у каждой модели свое, в среднем суммарное количество элементов для каждого расчета составляло примерно 240 тысяч тетраэдральных элементов. Дополнительно для аорты были добавлены два пристеночных слоя и 8 слоев было добавлено для внутренней области створчатого аппарата. Важно также отметить, что на створках строилась более мелкая сетка с целью более точного описания их деформации.
Результаты
Расчет гемодинамических характеристик был получен для всех 8 конструкций имплантов, ключевое отличие геометрий заключается в створчатом аппарате, который для каждого протеза имел свою высоту установки и радиус, в зависимости от характерных размеров каркаса. Эти отличия отражаются на полученных результатах.
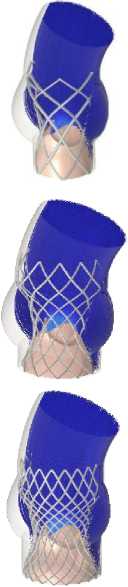
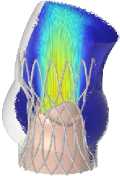
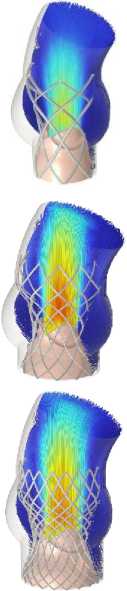
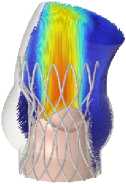
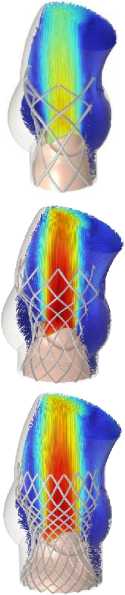
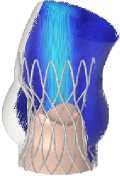
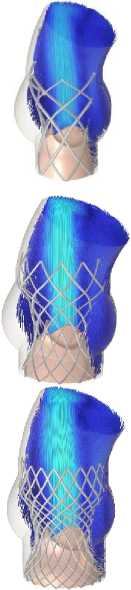
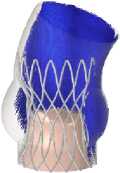
Одной из ключевых характеристик считается скорость поток крови. Были получены распределения скоростей кровяного потока на протяжении одного сердечного цикла. Профиль скорости, который использовался в качестве граничного условия на входе, обеспечил корректную зависимость величины скоростного потока от основных этапов сердечного цикла (систолы и диастолы). Наибольшее значение скорости достигается в момент раскрытия створок протеза, на этапе систолы для всех вариантов имплантов. Это значение варьируется в диапазоне от 1,4 м/с (модель А ) до 2,7 м/c (модель Ж ), что заметно на рис. 8. Тем самым можно утверждать, что данный параметр проявляет сильную зависимость от радиуса створчатого аппарата, который, в свою очередь, ограничен конструкцией каркаса.
В случае модели A , наблюдается обратная ситуация, скорость выходного потока, сильно ниже (~1,4 м/с), по сравнению с остальными клапанами. Створки модели А
Д
Е
Ж
З
20 мс
100 мс
190 мс
310 мс
380 мс




Скорость, м/с
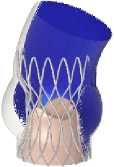
Рис. 9. Распределение поля скоростей в ключевые моменты сердечного цикла для моделей Д–З
а
б
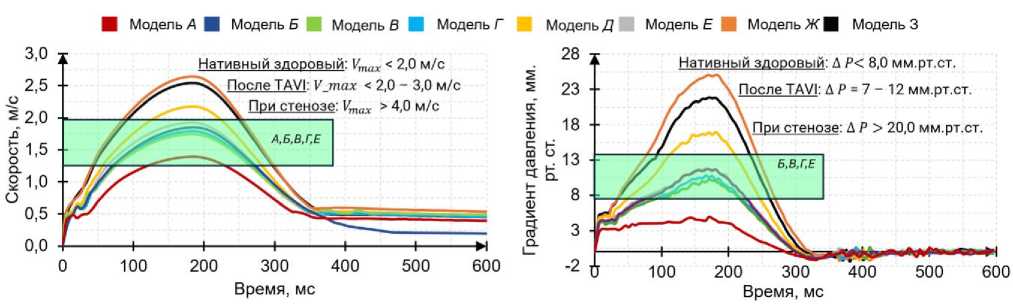
Рис. 10. Интегральные характеристики потока: а – максимальная скорость, б – градиент давления
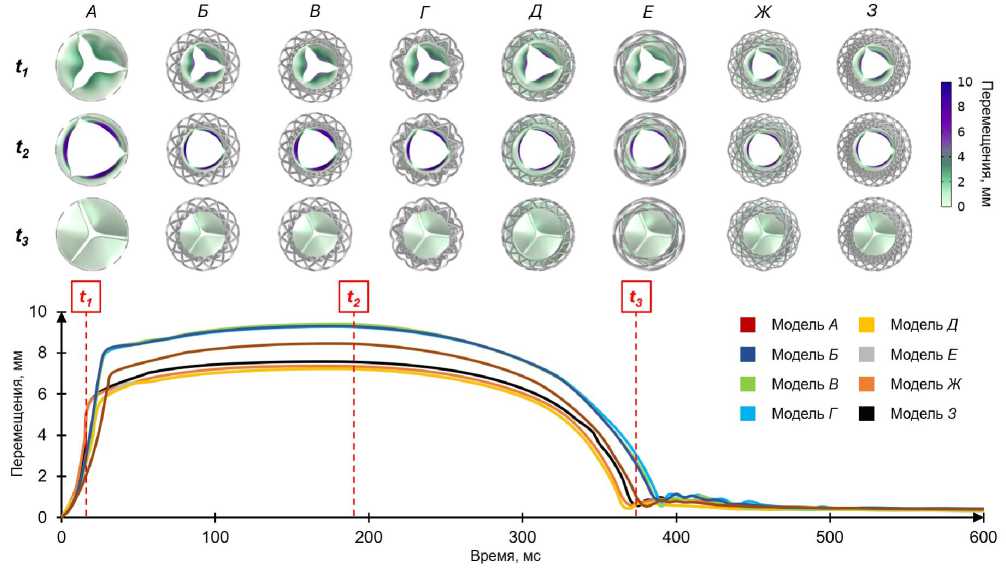
Рис. 11. Распределение перемещений створок аортального клапана в моменты времени t 1 = 20 мс, t 2 = 190 мс, t 3 = 380 мс и максимальные значения перемещений в течение сердечного цикла для моделей А–З
имеют наибольшую площадь, соответственно они могут оказывать высокое сопротивление входному потоку крови и не обеспечивать достаточного градиента давления. Градиент давления (рис. 10, б ) является важной, показательной характеристикой импланта, которая связана со скоростью потока. Чем выше скорость, тем выше градиент давления. Также на рис. 10, б отображен диапазон, отражающий приемлемые значения градиентов. Модели Б , В , Г , Е демонстрируют оптимальные значения, соответствующие эмпирическим данным после установки протеза ТИАК. Модели Ж и З имеют слишком большие градиенты и скорости, которые соответствуют значениям стенозированного нативного клапана. В нативном клапане высокие градиенты связаны с недостаточным раскрытием клапана.
Из-за обозначенных выше геометрических отличий протезов можно проследить характерные отличия профиля потока пиковых скоростей, достигаемых на этапе систолы (рис. 10, а ). Интенсивность потока для нескольких геометрий ( Б, Д, Ж, З ) сохраняется вплоть до изгиба восходящей аорты, при этом концентрация данного потока сохраняется и на переходных этапах (систола – диастола). Данный эффект может спровоцировать сильные завихрения при отражении потока от стенок аорты. В то же время на рис. 10, а видно, что скорости на этапе диастолы в момент закрытия клапана не равны нулю, однако это объясняется тем, что на графике отражена зависимость максимальных скоростей от времени. Градиенты давления после 400 мс начинают колебаться и иногда имеют отрицательное значение, что является физически обосновано, допуская небольшую регургитацию.
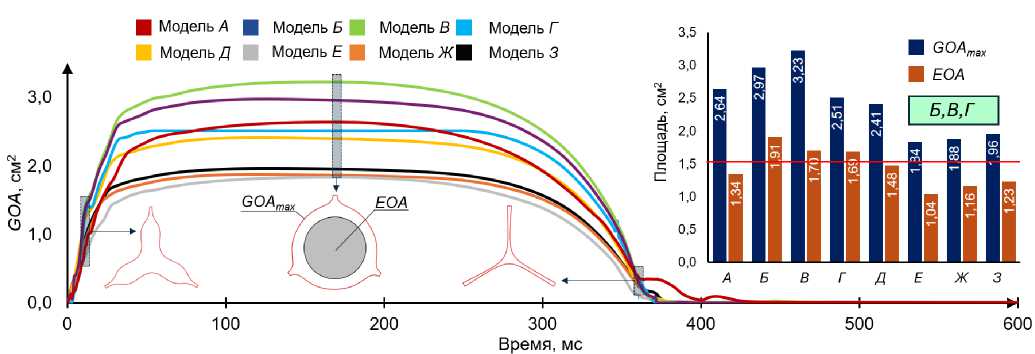
Рис. 12. Изменение геометрической площади клапана ( GOA ) и сравнение ее максимальных значений ( GOA max ) с эффективной площадью просвета ( EOA )
Время, мс
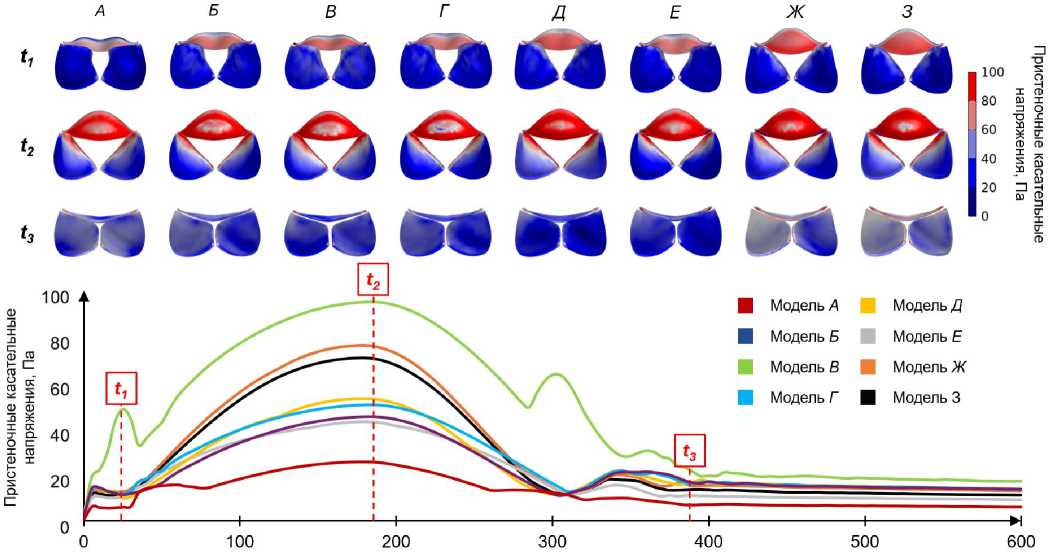
Рис. 13. Распределение пристеночных касательных напряжений и максимальные значения в период сердечного цикла
На рис. 11 показан график максимальных перемещения створок в зависимости от времени для каждой из восьми геометрий. На графике видно, что максимальное открытие створок для каждого имплантата происходит в разные моменты времени. Раньше всех полное открытие створок происходит у геометрии под буквой А , а дольше всех открываются створки клапана Ж . Такие выводы можно сделать, смотря на вид сверху всех геометрий в момент времени t .
В момент времени t модели ( А, Д, Ж, З ) уже закрылись, причем у них прослеживается сначала падение перемещений, а потом небольшой отскок и выход на стационарное значение.
Этот отскок показывает физиологическое колебание створок за счет возникновения инерции. В момент времени 500 мс створки каждого из имплантов можно считать закрытыми. Самым последним закрывается клапан под буквой Г, также данный клапан имеет самые сильные колебания в процессе закрытия.
Максимальные значения перемещений среди всех каркасов составили 9,5 мм у модели В , причем модель достигает своих максимумов одной из самый первых. Наименьшие перемещения оказалась равны 7,3 мм у моделей Д и Е . Таким образом, разница между максимальным и минимальным значениями составила 2,3 мм, что является существенной разницей, демонстрируя влияние вида каркаса на поведение створчатого аппарата.
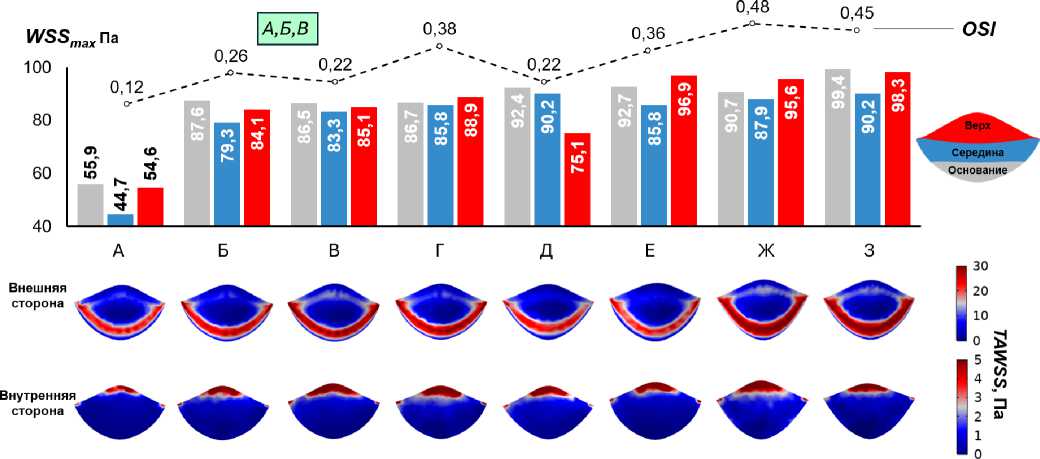
Рис. 14. Максимальные значения пристеночных касательных напряжений в основании, середине и окончании ство-
Еще одними важным показателем является геометрическая ( GOA ) и эффективная ( EOA ) площади открытия клапана. Первая показывает максимальную площадь просвета между створками аортального клапана в период сердечного цикла, а вторая фактическую площадь, через которую проходит жидкость.
По данным характеристикам можно оценить степень тяжести стеноза: чем меньше EOA , тем меньше клапан способен пропускать жидкости, а недостаточный кровоток оказывает негативное влияние на весь организм человека. В случае протеза необходимо обеспечить площадь открытия, максимально приближенную к нативному здоровому клапану.
На рис. 12 представлено изменение площади в процессе открытия створок клапана, наибольшие значения наблюдаются для клапанов моделей А – В . Максимальная площадь открытия составила 3,23 см2 для модели В , а минимальная для модели Е – 1,84 см2. Значения, близкие к 1,5 см2, характерны для стенозированных створок, диапазон нормы варьируется около 3–4 см2, в который попадают модели Б и В . Площадь эффективного открытия клапана соответствует площади потока в самой узкой его части и вычисляется следующим образом:
t2
S inlet ⋅ ∫ u inlet dt
EOA = t t 1 . (19)
и dt max t1
Для средней степени стеноза, при развитом стенозе, при тяжелой степени стеноза, таким образом, чем больше значение данного показателя, тем эффективнее работает клапан. Для рассмотренных моделей наибольшие значения оказались у моделей Б, В и Г, эти модели можно считать приемлемыми по данному критерию, поскольку их площадь может значительно улучшить состояние пациента. Наихудшие показатели у моделей Е, Ж и З близки к 1 см2, что наблюдается при развитой степени стеноза. Такие значения являются недопустимыми для использования на практике.
Следующая рассматриваемая в нашей работе характеристика – это пристеночные касательные напряжения (рис. 13), которые отвечают за долговечность и тромбоген-ность клапанного протеза. Высокие напряжения на створках клапана (В, Ж, З) провоцируют износ поверхности мягких тканей перикарда. Также следует учесть, что поверхность материала, не является идеально гладкой, поэтому наличие различных минеральных примесей в крови в совокупности с высокими пристеночными напряжениями ведет к кальцификации створок имплантата. Из-за повышенных механических напряжений на шероховатой поверхности перикарда начинается рост микроповреждений, в которых происходит осаждение ионов кальция. В то же время слишком малые пристеночные напряжения модели А инициируют процессы тромбообразования, так как являются результатом образования зон замедленного течения и нарушения обмена веществ, адгезии кровяных тел и воспалительного ответа. Интересным замечанием является то, что, несмотря на достаточно высокие пристеночные напряжения, у некоторых моделей (А, Б, Ж, З) на нижней части створок наблюдается рост касательных напряжений и с обратной стороны створчатого аппарата. Данный эффект является следствием сильной завихренности потока (рис. 14), которая, как упоминалось ранее, возникает в результате сохранения интенсивности плотного кровяного потока. Дополнительно на рис. 13 показан еще один параметр – коэффициент осцилляции (колебаний) касательных напряжений, который отражает отклонение касатель- ного напряжения от главного (осевого) направления в течение сердечного цикла. Данный параметр варьируется в диапазоне от 0 до 0,5, что наблюдается из вида соотношения для его вычисления. Чем ниже значение этого индекса, тем лучше для организма человека, поскольку частая смена направления напряжения может влиять на повреждение створчатого аппарата, приводя к повышенной тромбогенности. Модели под буквами А, Б, В, Д показали наилучшие значения, а остальные модели показывают слишком высокие осцилляции, значительно повышая риск образования тромбов после проведения операции. Формула для расчета коэффициента осцилляции использовалась следующая, где т^ - вектор пристеночных касательных напряжений:
OSI = 1
T , )
J T w dt
T
J k w dt l
° j
Обсуждение
В представленном исследовании мы использовали вычислительную модель FSI для оценки гемодинамической эффективности восьми различных конструкций протезов транскатетерных аортальных клапанов, два из которых являются коммерческими аналогами имплантов SAPIEN 3 и Evolut Pro . Основная цель заключалась в выявлении влияния геометрии каркаса и створчатого аппарата на ключевые показатели работы протеза. Полученные результаты демонстрируют значительную вариабельность гемодинамических параметров в зависимости от конструкции, что подтверждает необходимость персонализированного подхода и тщательного выбора параметров протеза для конкретного пациента.
Важно отметить, что результаты моделирования для коммерческих протезов (модели А и Б) находятся в качественном и количественном соответствии с ранее опубликованными данными. Так, модель Б (аналог Evolut Pro) продемонстрировала средний градиент давления, попадающий в диапазон 7–12 мм рт. ст., что согласуется с клиническими показателями, приведенными в работе [43], где для Evolut R, находившегося 30 дней в аорте пациента, указаны значения 7,85 ± 3,08 мм рт. ст. для протеза с входным диаметром 29 мм. Эффективная площадь открытия также оказалась близка к значениям из указанной статьи: 1,97 см2 в [43] и 1,91 см2 в наших расчётах. В валидационной работе с применением компьютерного моделирования и FSI- подхода [41] авторы получили для Evolut R средний градиент 6,84-9,62 мм рт. ст. и EOA 1,32-1,50 см2, что также хорошо коррелирует с нашими данными для модели Б. Кроме того, Ghosh et al. в [44] при анализе глубины имплантации для оптимального положения получили значения EOA 1,55 см2, близкие к нашим результатам для моделей Б и В, однако эти результаты получены для модели с входным диаметром 26 мм, что соответствует и меньшей EOA. Таким образом, полученные результаты градиентов давления и эффективной площади для модели Б хорошо ложатся в диапазон результатов, представленных другими авторами. Это косвенно подтверждает адекватность выбранных граничных условий и параметров материалов.
Модель А ( SAPIEN 3 ), напротив, показала более низкие скорости потока и градиента давления. Это может быть связано с её интраанулярным позиционированием в нашей модели и особенностями геометрии створок, которые были одного типа для каждого из протезов. В работе [42] отмечались различия в гемодинамике между баллоно-расширяемыми и саморасширяемыми протезами: их аналог SAPIEN 3 ( THV-B ) показал более высокие скорости, что отличается от полученных нами данных. Однако это подчеркивает важность не только типа клапана, но и конкретной геометрии створок, глубины имплантации и индивидуальной анатомии аорты, которые в нашем исследовании были унифицированы для всех моделей. Если говорить про численные различия, то в работе [43] для клапана аналогичного размера градиент давления получился равным 9,28 ± 3,16 мм рт. ст., а в работе [66] для протеза с диметром 26 мм: 9 мм рт. ст., тогда как у нас получился 3,10 мм рт. ст. Площадь EOA также значительно меньше 1,34 см2 в нашей работе против 1,78 см2 и 1,89 ± 0,37 см2 в работах [66; 43] соответственно. Важно отметить, что работа [66] посвящена испытаниям in vitro .
Ключевым выводом работы является сильная зависимость гемодинамических показателей от геометрии каркаса, определяющей положение и раскрытие створок. Модели с большей площадью открытия ( А, Б, В ) ожидаемо показали более низкие градиенты давления и скорости потока, приближаясь к показателям здорового нативного клапана. Однако, несмотря на большую геометрическую площадь открытия, эффективная площадь открытия модели A оказалось сильно ниже ожидаемой. Модели В и Г , разработанные нашей командой, продемонстрировали результаты, сопоставимые с коммерческим аналогом модели Evolut по таким параметрам, как EOA и GOA . Это свидетельствует о потенциале предложенных параметризованных конструкций, детально описанных в работе [48]. С другой стороны, модели Ж и З , обладающие более низким значением эффективной площади открытия створчатого аппарата, показали градиенты давления и скорости, характерные для стенозированных клапанов. Это служит важным ограничивающим фактором: параметризация геометрии должна проводиться в разумных физиологических пределах, чтобы избежать создания заведомо неэффективных протезов. Слишком малая площадь открытия ( EOA <1,5 см2 у моделей Е, Ж, З ) нивелирует саму цель операции ТИАК, оставляя пациента с гемодинамикой, соответствующей стенозу средней или тяжелой степени.
Оценка пристеночных касательных напряжений за сердечный цикл ( TAWSS ) и осцилляторного индекса сдвига ( OSI ) позволила также выделить наиболее эффективные модели. Модели с наилучшей гемодинамикой ( Б, В ) показали умеренные значения TAWSS , которые, с одной стороны, достаточно высоки, чтобы предотвращать застой крови и тромбообразование (в отличие от модели А с низкими TAWSS ), а с другой – не достигают критических значений, способных вызвать повреждение створок и ускорить кальцификацию. Методология расчета этих параметров соответствует подходам, описанным в работе [45] для коронарных артерий, которые мы адаптировали для оценки створок аортального клапана. Локализация максимальных TAWSS у основания створок (рис. 14) полностью соответствует физиологическим данным и механике работы клапана, где область прикрепления испытывает наибольшие нагрузки. Этот факт также коррелирует с клиническими наблюдениями, что первичная кальцификация биопротезов часто начинается именно в зоне комиссур.
Анализ OSI позволил выделить модели с наиболее стабильным, ламинарным потоком ( А, Б, В, Д ). Низкие значения OSI для этих моделей указывают на меньшее колебание направления WSS , что потенциально уменьшает тромбогенность протеза в долгосрочной перспективе. Интересно, что модель Д , не попавшая в лидеры по градиентам давления, показала хорошие результаты по OSI , что делает ее потенциально интересной с точки зрения долговечности. Высокие значения OSI у моделей Г, Е, Ж, З , вероятно, связаны с образованием зон рециркуляции и завихрений за створками, что визуализируется на рис. 8, 9 и 14. Подобные явления, как отмечается в литературе, могут повышать риск тромбообразования [11]. Однако оптимальное значение TAWSS для створчатого аппарата протеза остается вопросом дискуссионным, поскольку створки не имеют эндотелия, как на аорте, который сильно зависите от гемодинамики, определить нужный диапазон напряжений поможет только увеличение клинических данных.
Настоящая работа, как и любое вычислительное исследование, имеет ряд ограничений, которые необходимо учитывать при интерпретации результатов. Одним из таких ограничений является то, что стенка аорты моделировалась как жесткая область. Это упрощение, хотя и общепринятое на начальных этапах, не позволяет оценить демпфирующие свойства аортальной стенки и их влияние на движение потока и деформацию каркаса протеза. Податливость корня аорты может оказывать существенное влияние на долговечность протеза и возможную параклапанную регургитацию. Во-вторых, мы использовали ньютоновскую модель крови. Хотя для крупных сосудов это допущение приемлемо, согласно [50], в областях с низкой скоростью сдвига (например, в синусах Вальсальвы, за створками) неньютоновские свойства могут влиять на характер течения и, следовательно, на TAWSS и OSI. Еще одним допущением, является то, что мы моделировали только один сердечный цикл, что не позволяет оценить усталостные свойства материала и долгосрочную миграцию стента. Так же, как отмечено во введении, долгосрочные последствия различных конструкций створок остаются недостаточно изученными [16; 17], и наше исследование пока не может полностью восполнить этот пробел. Наконец, мы не учитывали наличие нативного стенозированного клапана, который в реальности остается на месте и может влиять на расположение стента и поток крови.
В качестве следующего этапа нашей работы мы планируем усложнить модель, включив в нее деформируемую стенку аорты, опираясь на математическую модель и подход к деформации мягких тканей [67], с реалистичными механическими свойствами. Также планируется добавить контактное взаимодействие для оценки анкеровки и провести моделирование для нескольких сердечных циклов, исследовать влияние неньютоновских свойств крови, используя модель Каро, а также учесть наличие нативного кальцинированного клапана, как это сделано в работе [41].
Полученные в данном исследовании результаты позволяют нам сузить круг наиболее перспективных из рассматриваемых геометрий (модели Б, В и Г ) для дальнейшего, более детального анализа с учетом указанных факторов. Полученные результаты служат основой для дизайна, проектирования и производства персонализированных протезов ТИАК с учетом анатомических и физиологических особенностей конкретного пациента.
Заключение
В рамках текущего исследования нами были построены 8 геометрий биологических протезов аортального клапана, два из которых были коммерческими, часто применимые в медицине. Каждый из имплантатов имел свой створчатый аппарат, отличающийся высотой расположения и площадью створок, что оказало существенное влияние на результаты моделирования. Используя компьютерное моделирование и ALE-FSI -подход, в программном пакете COMSOL Multiphysics , нами были получены распределения скоростей кровеносного потока в течение одного сердечного цикла для каждой конструкции. Для здорового нативного клапана максимальное значение скорости во время систолы характерно менее 2 м/с, более высокие скорости соответствуют стенозированному клапану. Подходящие результаты показали модели А, Б, В, Г, Е . Градиенты давления дают схожие результаты, поскольку высокие скорости потока напрямую связаны с повышенным градиентом давления. По известным данным [43], после проведения ТИАК значение перепада давлений лежит в диапазоне от 7–12 мм. рт. ст. В данный диапазон попадают показатели моделей Б, В, Г, Е . График перемещений демонстрирует, что створки каждого клапана перемещались менее чем на 10 мм, соответствуя экспериментальным значениям. Анализируя эффективную площадь открытия
( EOA ), нами были выделены модели Б, В, Г как модели, имеющие максимальную EOA, данный показатель должен быть выше отметки 1,5, более низкие значения не приведут к улучшению при установке такого клапана, поскольку площадь открытия будет примерно такой же, как и при стенозе. Стоит также отметить, что выделенные модели имеют и одну из самых больших максимальных геометрических площадей открытия ( GOA ), что является ожидаемым в рамках текущей постановки.
Чтобы оценить долговечность клапана и риски появления тромбов после проведения ТИАК, нами были получены результаты пристеночных касательных напряжений ( WSS ) на створках протезов и коэффициенты колебания их направлений ( OSI ). Несмотря на то что значения WSS получились достаточно высокими, коэффициенты осцилляции позволяют понять, какие модели будут меньше влиять на тромбогенность, поскольку чем меньше OSI , тем реже сменяются направления напряжений, отражая более плавное течение без вихрей, которое является более оптимальным для организма человека. Нами были выбраны модели А, Б, В, Д , имеющие наименьшие значения рассматриваемого параметра. Также на рис. 13 отражены максимальные напряжения, которые появляются у основания створок, что является физически обоснованным, поскольку высокие напряжения влияют на вероятность образования кальция на створках, а стеноз обычно и начинается с основания. Таким образом, анализируя все результаты, наилучшими моделями, имеющими приемлемые показатели, оказались модель Б – коммерческий протез Evolut Pro и модель В – одна из разработанных в нашей лаборатории. Данные модели имеют корректные значения для каждого из изучаемых параметров, однако для более точного исследования в дальнейшем планируется дополнительно проанализировать влияние деформации каркаса в процессе сердечных циклов на влияние гемодинамических характеристик после проведения ТИАК.


