Влияние на бактериальный гидролитический комплекс гумусо-аккумулятивного горизонта техноурбанозема пассажа через кишечник дождевого червя Aporrectodea caliginosa
Автор: Фролов О.А., Якушев А.В.
Журнал: Бюллетень Почвенного института им. В.В. Докучаева @byulleten-esoil
Статья в выпуске: 94, 2018 года.
Бесплатный доступ
Изучены экофизиологические особенности транзитного (прошедшее через кишечную полость) бактериального гидролитического комплекса Aporrectodea caliginosa : проведено сравнение в почве и копролитах биоразнообразия, преобладающих экологических стратегии и физиологических состояний среди его членов. Исследование проводили комплексным структурно-функциональным методом, основанном на кинетическом анализе сукцессии инициированных гидролитических бактериальных сообществ, возникающих после инокуляции набора селективных жидких питательных сред суспензией исследуемых образцов. В инициированные сообщества помимо гидролитических микроорганизмов входят негидролитические бактерии-спутники (олиготрофы и копиотрофы). Рост инициированных бактериальных сообществ на восьми средах с биополимерами (хитине, целлюлозе, пектине, крахмале, ксилане, декстране 500, твине 20, казеине) измеряли по оптической плотности. Описывали его двумя кинетическими параметрами, применяемыми для описания чистых культур микроорганизмов: максимальная удельная скорость роста и начальное физиологическое состояние...
Зоомикробные взаимодействия, кинетика роста, физиологическое состояние микроорганизмов, экологические стратегии микроорганизмов
Короткий адрес: https://sciup.org/143165447
IDR: 143165447 | УДК: 631.46 | DOI: 10.19047/0136-1694-2018-94-57-73
The impact of passage through the intestine of the earthworm Aporrectodea caliginosa on the bacterial community
Ecophysiological features of the transit (passed through the intestinal lacune) bacterial hydrolytic complex Aporrectodea caliginosa were studied: a comparison of biodiversity was made in the soil and coprolites, the prevailing ecological strategy and physiological states among its members. The study was conducted by a complex structural and functional method based on the succession kinetic analysis of initiated hydrolytic bacterial communities that occur after the inoculation of a set of selective liquid nutrient media with a suspension of the test samples. In addition to hydrolytic microorganisms, non-hydrolytic bacterial satellites (oligotrophs and copyotropes) are included in initiated communities. The growth of initiated bacterial communities on eight media with biopolymers (chitin, cellulose, pectin, starch, xylan, dextran 500, tween 20, casein) was measured by optical density. It was described by two kinetic parameters used to describe the pure cultures of microorganisms: the maximum specific growth rate and the initial physiological state...
Текст научной статьи Влияние на бактериальный гидролитический комплекс гумусо-аккумулятивного горизонта техноурбанозема пассажа через кишечник дождевого червя Aporrectodea caliginosa
Почвенные животные и микроорганизмы влияют на плодородие почвы (Звягинцев и др. 2005). Это влияние часто реализуется через зоомикробные взаимодействия (Byzov at al., 1993; Bi at al., 2018). В частности, почвенные животные в ассоциации с микроорганизмами в почве проводят трансформацию (минерализацию и гумификацию) органических остатков, в том числе и биополимеров (Chang at al., 2016), мобилизацию–иммобилизацию элементов питания (Бызов, 2005). От содержания и качества гумуса значительно зависит плодородие (Hargitai,1993). Животные-сапрофаги измельчают, перемещают, перемешивают подстилку и переваривают ее совместно с кишечными микроорганизмами. В дальнейшем их экскременты трансформируются (“стареют”) под воздействием микробиологических, физических и химических процессов. В результате образуются гумусовые горизонты (Bal, 1970). Одним из востребованных и перспективных подходов к изучению вклада микробного комплекса в преобразования органических остатков в почве является оценка экофизиологических особенностей его членов: физиологического разнообразия, преобладающих физиологических состояний и экологических стратегий (Благодатская, 2004; Благодатская, 2008; Córdova, 2018). Подход основан на анализе кинетических характеристик микроорганизмов. Определение кинетики роста и построение моделей, описывающих его, востребовано в прикладных научных исследованиях, в медицинской и пищевой промышленности, оценке экологического состояния окружающей среды (Panikov, 2016; Stanbury at al., 2017; Atungulu at al., 2016; Dev at al., 2016). Проводятся исследования влияния на скорость роста микроорганизмов плотности биомассы (AlSayed at al., 2017; Krichen et al., 2018), кислотности среды (Akkermans, Van Impe, 2018) и др. Экологические стратегии, преобладающие среди кишечных микроорганизмов, и их физиологическое состояние позволяют понять механизмы трансформации органического вещества в пищеварительной системе животных и зоомикробных взаимодействий.
Дождевые черви – одни из наиболее значимых для плодородия почвенных животных (Huang, Xia, 2018; Peigné at al., 2018; Sanchez-Hernandez at al., 2018; Sanchez-Hernandez, 2018) . Им посвящено множество работ по физиологии (Laverack, 1963; Satchell, 1983) , экологии (Юрков и др., 2008; Тихонов и др., 2011; Кутовая, 2012; Храмченкова и др., 2012) и применению в сельском хозяйстве (вермикомпостирование) (Бызов, Якушев, 2008) .
Цель исследования – изучение транзитного (полостного) бактериального комплекса кишечника Aporrectodea caliginosa : сравнение в почве и копролитах разнообразия бактериального комплекса, преобладающих среди его членов экологических стратегии и физиологических состояний.
ОБЪЕКТЫ И МЕТОДЫ
В г. Москве на территории Ботанического сада МГУ им. М.В. Ломоносова на Воробьевых горах собрано 20 особей (15 ювенильных и 5 половозрелых) эврибионтных эндогейных дождевых червей Aporrectodea caliginosa , определенных по специализированной литературе (Всеволодова-Перель, 1997) . Черви содержались неделю в условиях лабораторного микрокосма при постоянной весовой влажности почвы 45% и температуре 25°C в образце (0.8 кг) гумусово-аккумулятивного горизонта техноурбанозема (Розанова и др., 2016) , в котором они обитали в природе. Для получения экскрементов червей отмывали от почвы, помещали в чашку Петри и выдерживали сутки при температуре +10°. Количество бактерий на поверхности червей несопоставимо меньше, чем в копролитах, и их влиянием можно пренебречь. После этого копролиты собирали и анализировали одновременно с образцами почвы (корма).
Экофизиологическую характеристику бактериальных комплексов проводили комплексным структурно-функциональным Таблица 1. Набор полимеров, использованных в селективных средах
Метод не исследует микроорганизмы на классических для почвенной микробиологии уровнях изучения: операционных таксономических единицах, целых сообществах или биохимических процессах, проводимых микробным комплексом. Он изучает не исследованные ранее, временно возникающие в микролокусе из пула ассоциации (смешанные культуры), которые непосредственно осуществляют большинство процессов в природе. В комплексном методе эти консорции микроорганизмов воссоздаются посредством создания инициированных сообществ в лабораторных микрокосмах после внесения суспензии исследуемого природного сообщества в набор селективных жидких питательных сред. При этом анализируются возникающие кинетические параметры сукцессионных изменений. Поскольку процесс происходит в более контролируемых условиях, чем в классических почвенных инициированных сообществах, то его можно представить как рост и отмирание смешанной периодической культуры, описываемой классическими кинетическими параметрами: микробным экономическим коэффициентом, максимальной удельной скоростью роста, метаболическим коэффициентом и т.д. В данной работе исследовали инициированные бактериальные сообщества, содержащие аэробные и факультативно-анаэробные культивируемые микроорганизмы, использующие как трудно-, так и легкодоступные полимеры (филумы Cytophaga-Flavibacterium-Bacteroides, Firmicutes, Proteobacteria, Actinobacteria). В эти ассоциации входят не только гидролитические бактерии, но и их спутники, представленные как копиотро-фами, так и олиготрофами. Поведение инициированных гидролитических сообществ в лаг-фазе и фазе экспоненциального роста описывали уравнением комплексной модели периодической культуры (Якушев, 2015), которая для этих стадий роста идентична модели Н.С. Паникова (1991, 1996):
x(t) = X o (l - P0 + р 0 е ^ т1), где х ( t ) – экспериментально установленная по оптической плотности концентрация клеток (кл./мл) в момент времени t (ч) в селективных жидких питательных средах; x 0 – экспериментально установленная концентрация клеток бактерий в момент инокуляции питательных сред почвенной суспензией (КОЕ/мл); μ m – максимальная удельная скорость ассоциации на среде с полимером (ч-1); ρ 0 – начальное физиологическое состояние растущей смешанной культуры, характеризующее физиологическое состояние бактерий еще в почве – на момент инокуляции ими питательной среды. Чем ρ 0 выше, тем активность бактерий выше.
Биоразнообразие бактерий в инициированных гидролитических сообществах, сформировавшихся на жидких средах с полимерами, определяли по индексам Бергера–Паркера и Шеннона, рассчитанным по данным встречаемости морфотипов бактерий на чашках Петри на среде “Rich” (разбавленной глюкозо-пептоннодрожжевой среде). В результате получено по 7 индексов для инициированных сообществ из почвы и копролитов. Использование слабоселективной среды позволяет более полно учесть биоразнообразие инициированных гидролитических сообществ, чем высев на агаризованные варианты селективных сред, так как помимо гидролитических бактерий в данные сообщества входят копио-трофные и олиготрофные негидролитические бактерии, не способные вырасти на среде с полимерами.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Распределения частот встречаемости значений индексов Шеннона и Бергера–Паркера инициированных гидролитических бактериальных сообществ (табл. 2) имеет ненормальный характер (рис. 1). Поэтому информативно применить непараметрический статистический анализ. Медианный и непараметрический дисперсионный анализы не выявили достоверных различий в биоразнообразии инициированных сообществ на средах с биополимерами, возникших из природных сообществ почвы и экскрементов.
Таблица 2. Морфотипы выделенных бактериальных сообществ
|
Среда |
Корм |
копролиты |
||
|
морфотип № |
доля |
морфотип № |
доля |
|
|
Крахмал |
03 |
0.72 |
2 |
0.66 |
|
04 |
0.26 |
4 |
0.30 |
|
|
08 |
0.02 |
8 |
0.02 |
|
|
КМЦ |
13 |
1 |
2 |
0.75 |
|
9 |
0.25 |
|||
|
Пектин |
05 |
1 |
2 |
0.90 |
|
100 |
0.08 |
|||
|
120 |
00.013 |
|||
|
Ксилан |
06 |
0.66 |
2 |
0.68 |
|
11 |
0.3 |
4 |
0.06 |
|
|
6 |
0.03 |
|||
|
8 |
0.20 |
|||
|
Казеин |
01 |
0.61 |
1 |
0.34 |
|
0 |
0.38 |
2 |
0.13 |
|
|
3 |
0.52 |
|||
|
Твин 20 |
02 |
0.10 |
2 |
0.10 |
|
08 |
0.21 |
3 |
0.45 |
|
|
09 |
0.68 |
4 |
0.02 |
|
|
8 |
0.37 |
|||
|
9 |
00.027 |
|||
|
Декстран-500 |
02 |
0.86 |
2 |
00.091 |
|
0 |
0.03 |
4 |
0.47 |
|
|
07 |
0.38 |
6 |
0.11 |
|
|
08 |
0.05 |
8 |
0.08 |
|
|
100 |
0.24 |
|||
A
Индекс Бергера-Паркера
В
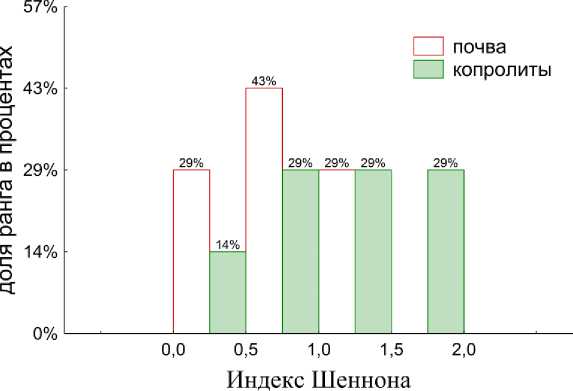
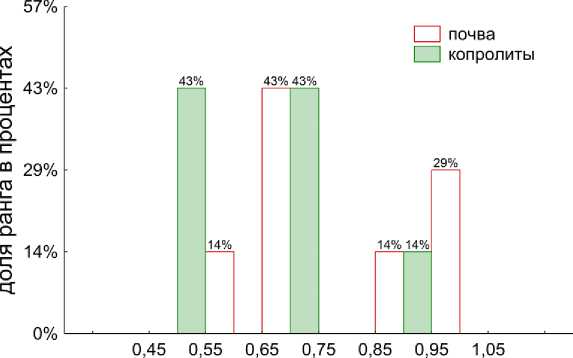
Рис. 1. Ранговое распределение частот встречаемости индексов биоразнообразия инициированных гидролитических сообществ (А – индекс Бергера–Паркера, B – индекс Шеннона).
Поэтому был проведен непосредственный анализ ранговых распределений выявивший тенденцию к смещению в ходе пассажа доли встречающихся значений индекса Шеннона в сторону больших значений и меньших значений по индексу Бергера–Паркера. Увеличение биоразнообразия инициированных сообществ указывает на увеличение биоразнообразия бактериального комплекса копролитов: видовой состав становится более выровненным и разнообразным, а следовательно и более устойчивым. Возможно, слабые величины эффектов связаны с тем, что почва уже была сильно переработана червями. Семь дней для этого вполне достаточно. И по сути, анализировались старые копролиты, смешанные с почвой, и свежие копролиты, собранные в чашке Петри.
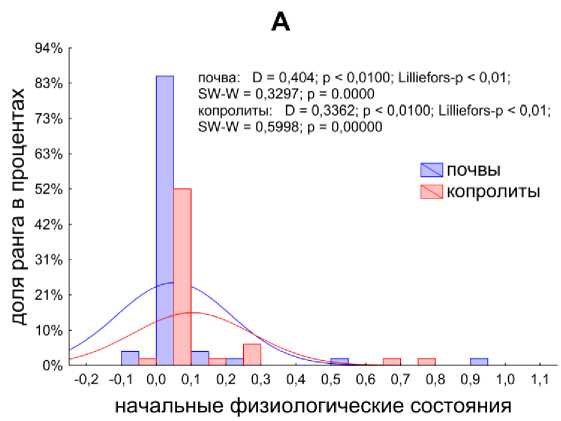
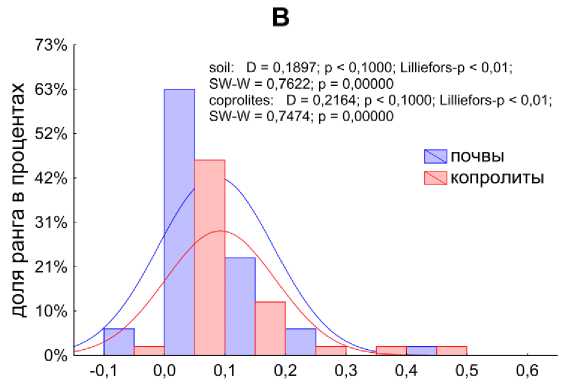
Максимальная удельная скорость роста (μ m ) и начальное физиологическое состояние гидролитических ассоциаций (ρ 0 ) распределены не нормально (рис. 2). Поскольку данные не подчиняются закону нормального распределения, то для сравнения использовались медианный и непараметрический дисперсионный анализы.
Непараметрический однофакторный дисперсионный анализ на основании критерия Краскела—Уоллиса (H (1, N = 80) = 13.9, p = 0.0002) и медианный тест по критерию согласия Пирсона (χ2 = 13.3, df = 1, p = 0.0003) установили увеличение медианных значений ρ 0 для инициированных сообществ в ходе пассажа почвы через кишечник дождевого червя (рис. 3).
Эти анализы не выявили достоверных различий медианных значений μ m . Поэтому был проведен анализ ранговых распределений (рис. 4). При пассаже почвы через кишечник увеличивается доля быстрорастущих бактерий в бактериальном сообществе ко-пролитов (увеличивается доля класса со значениями μ m от 0.05 до 0.1 с 23 до 38% и уменьшается доля класса 0–0.05 с 46 до 34%).
максимальная удельная скорость роста
Рис. 2. Проверка на нормальность ранговых распределений (А – начальных физиологических состояний (безразмерная величина), B – максимальной удельной скорости роста (1/ч)) инициированных гидролитических сообществ.
Начальные физиологические состояния
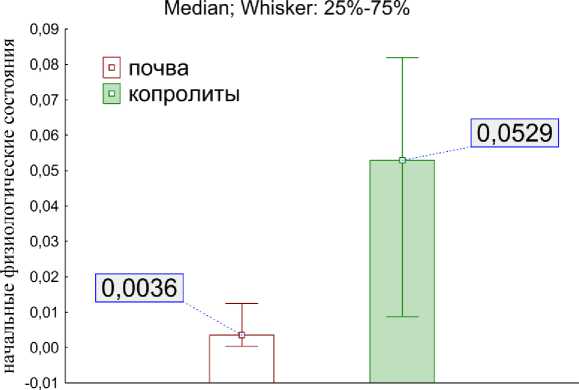
Рис. 3. Начальные физиологические состояния (медиана и квартили) инициированных гидролитических сообществ, сформировавшихся на жидких средах с полимерами.
ЗАКЛЮЧЕНИЕ
При пассаже через кишечник дождевого червя транзитный почвенный бактериальный гидролитический комплекс становится более устойчивым, более выровненным и разнообразным. Происходит его активизация – начальное физиологическое состояние инициированных гидролитических сообществ выше. Среди его членов увеличивается доля быстрорастущих бактерий r -стратегов: на жидких средах с полимерами доля быстрорастущих инициированных гидролитических ассоциации повышается.
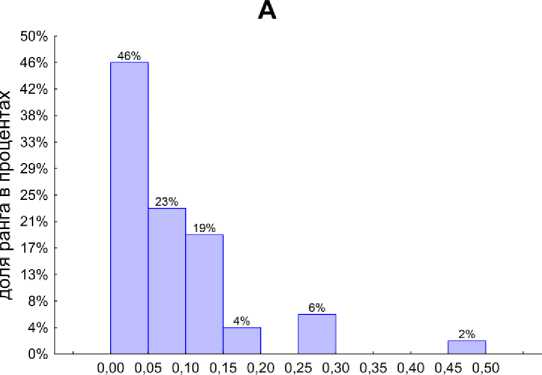
максимальная удельная скорость роста (почва)
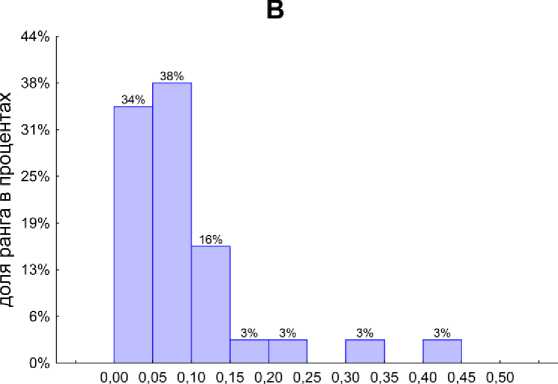
максимальная удельная скорость роста (копролиты)
Рис. 4 Ранговые распределения частоты встречаемости максимальных удельных скоростей роста инициированных гидролитических бактериальных сообществ, сформировавшихся на средах с полимерами (A – почва, B – копролиты).
Список литературы Влияние на бактериальный гидролитический комплекс гумусо-аккумулятивного горизонта техноурбанозема пассажа через кишечник дождевого червя Aporrectodea caliginosa
- Благодатская Е.В., Ермолаев А.М., Мякшина Т.Н. Экологические стратегии микробных сообществ почв под растениями луговых экосистем//Изв. РАН. Сер. биологическая. 2004. №. 6. С. 740-748.
- Благодатский С.А., Богомолова И.Н., Благодатская Е.В. Микробная биомасса и кинетика роста микроорганизмов в черноземах при различном сельскохозяйственном использовании//Микробиология. 2008. Т. 77. № 1. С. 113-120.
- Бызов Б.А. Зоомикробные взаимодействия в почве. М.: ГЕОС, 2005. 213 с.
- Бызов Б.А., Якушев А.В., Микробиологическая характеристика вермикомпостирования методом мультисубстратного тестирования//Почвоведение. 2008. № 11. С. 1381-1387 DOI: 10.1134/S1064229308110112
- Всеволодова-Перель Т.С. Дождевые черви фауны России. Кадастр и определитель. М.: Наука, 1997. 102 с.
- Звягинцев Д.Г., Бабьева И.П., Зенова Г.М. Биология почв. М.: Изд-во Моск. ун-та, 2005. 445 с.
- Кутовая О.В. Характеристика гумусовых веществ агродерново-подзолистой почвы и копролитов дождевых червей//Бюл. Почв. ин-та им. В.В. Докучаева. 2012. Вып. 69. С. 46-59.
- Розанова М.С., Прокофьева Т.В., Лысак Л.В., Рахлеева А.А. Органическое вещество почв ботанического сада МГУ им. М.В. Ломоносова на Ленинских горах//Почвоведение. 2016. № 9. С. 1079-1092 DOI: 10.7868/S0032180X16090124
- Паников Н. С. Синтетическая хемостатная модель как средство описания сложного динамического поведения микроорганизмов//Микробиология. 1991. Т. 60. № 3. С. 431-441.
- Тихонов В.В., Бызов Б.А., Завгородняя Ю.А., Демин В.В. Дождевые черви преобразователи структуры и биологической активности гуминовых кислот//Изв. РАН. Сер. биологическая. 2011. № 1. С. 24-32 DOI: 10.1134/S1062359010061032
- Храмченкова О., Веремеев В., Бачура Ю. Водоросли почв и копролитов дождевых червей в луговых экосистемах//Наука и инновации. 2012. Т. 2. № 108.
- Юрков А.М., Чернов И.Ю., Тиунов А.В Влияние дождевых червей lumbricus terrestris на структуру дрожжевого сообщества лесной подстилки//Микробиология. 2008. Т. 77. № 1. С. 121-125 DOI: 10.1134/S0026261708010153
- Якушев А.В. Комплексный структурно-функциональный метод характеристики микробных популяций//Почвоведение. 2015. № 4. С. 429-446 DOI: 10.7868/S0032180X15040115
- Akkermans S., Van Impe J.F. Mechanistic modelling of the inhibitory effect of pH on microbial growth//Food Microbiol. 2018. Т. 72. P. 214-219 DOI: 10.1016/j.fm.2017.12.007
- AlSayed A., Fergala A., Eldyasti A. Influence of biomass density and food to microorganisms ratio on the mixed culture type I methanotrophs enriched from activated sludge//J. Environ. Sci. 2017 DOI: 10.1016/j.jes.2017.11.017
- Atungulu G.G., Thote S., Wilson S. Storage of hybrid rough rice-Consideration of microbial growth kinetics and prediction models//J. Stored Products Res. 2016. Т. 69. С. 235-244 DOI: 10.1016/j.jspr.2016.09.003
- Bal L. Morphological investigation in two moder-humus profiles and the role of the soil fauna in their genesis//Geoderma. 1970. Т. 4. № 1. С. 5-36 DOI: 10.1016/0016-7061(70)90030-3
- Bi Y.M., Tian G.L., Wang C., Zhang Y., Wang D.N., Zhang F.F., Sun Z.J. Differential effects of two earthworm species on Fusarium wilt of strawberry//Appl. Soil Ecology. 2018. V. 126. P. 174-181 DOI: 10.1016/j.apsoil.2018.02.024
- Byzov B.A., Thanh V.N., Babjeva I.P. Interrelationships between yeasts and soil diplopods//Soil Biol. Biochem. 1993. Т. 25. № 8. С. 1119-1126 DOI: 10.1016/0038-0717(93)90160-D
- Chang C.H., Szlavecz K., Buyer J.S. Species-specific effects of earthworms on microbial communities and the fate of litter-derived carbon//Soil Biol. Biochem. 2016. V. 100. P. 129-139 DOI: 10.1016/j.soilbio.2016.06.004
- Córdova O. et al. Influence of growth kinetics of microalgal cultures on biogas production//Renewable Energy. 2018. Т. 122. С. 455-459 DOI: 10.1016/j.renene.2018.01.125
- Dev S., Roy S., Bhattacharya J. Understanding the performance of sulfate reducing bacteria based packed bed reactor by growth kinetics study and microbial profiling//J. Environ. Management. 2016. Т. 177. С. 101-110 DOI: 10.1016/j.jenvman.2016.03.049
- Hargitai L. The role of organic matter content and humus quality in the maintenance of soil fertility and in environmental protection//Landscape and Urban Planning. 1993. Т. 27. № 2-4. С. 161-167 DOI: 10.1016/0169-2046(93)90044-E
- Huang G., Chen S., Dai C., Sun L., Sun W., Tang Y., Xiong F., He R., Ma H., Effects of ultrasound on microbial growth and enzyme activity//Ultrasonics Sonochemistry. 2017. Т. 37. С. 144-149 DOI: 10.1016/j.ultsonch.2016.12.018
- Huang K., Xia H. Role of earthworms' mucus in vermicomposting system: Biodegradation tests based on humification and microbial activity//Sci. Total Environ. 2018. V. 610. 703-708 DOI: 10.1016/j.scitotenv.2017.08.104
- Krichen E., Harmand J., Torrijos M., Godon J.J., Bernet N., Rapaport A. High biomass density promotes density-dependent microbial growth rate//Biochem. Engin. J. 2018. Т. 130. С. 66-75 DOI: 10.1016/j.bej.2017.11.017
- Laverack M.S. The Physiology of Earthworms. N.Y.: Macmillan, 1963. 230 p.
- Laverack N.S. Mechanistic mathematical models of microbial growth in bioreactors and in natural soils: explanation of complex phenomena//Mathematics and Computers in Simulation. 1996. Т. 42. № 2-3. С. 179-186 DOI: 10.1016/0378-4754(95)00127-1
- Panikov N.S. Kinetics of Microbial Processes, Reference Module in Earth Systems and Environmental Sciences. Elsevier, 2016. P. 1-19 DOI: 10.1016/B978-0-12-409548-9.09733-5
- Peigne J., Vian J.F., Payet V., Saby N.P. Soil fertility after 10 years of conservation tillage in organic farming//Soil and Tillage Res. 2018. V. 175. 194-204 DOI: 10.1016/j.still.2017.09.008
- Sanchez-Hernandez J. C. Biochar activation with exoenzymes induced by earthworms: A novel functional strategy for soil quality promotion//J. Hazardous Materials, 2018. V. 350. 136-143 DOI: 10.1016/j.jhazmat.2018.02.019
- Sanchez-Hernandez J.C., del Pino J.N., Capowiez,Y., Mazzia C., Rault M. Soil enzyme dynamics in chlorpyrifos-treated soils under the influence of earthworms//Sci. Total Environ. 2018. V. 612. P. 1407-1416 DOI: 10.1016/j.scitotenv.2017.09.043
- Satchell J.E. Earthworm microbiology//Earworm ecology from Darwin to vermiculture. London, N.Y, 1983. P. 315-364 DOI: 10.1007/978-94-009-5965-1
- Stanbury P.F., Whitaker A., Hall S.J. Principles of Fermentation Technology. Elsevier, 2017 P. 21-74 DOI: 10.1016/B978-0-08-099953-1.00002-8


