Влияние наночастиц диоксида кремния на морфологию внутренних органов у крыс при пероральном введении
Автор: Зайцева Н.В., Землянова М.А., Звездин В.Н., Довбыш А.А., Гмошинский И.В., Хотимченко С.А.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Экспериментальные модели и инструментальные исследования для оценки риска в гигиене и эпидемиологии
Статья в выпуске: 4 (16), 2016 года.
Бесплатный доступ
Объектом исследования являлся аморфный диоксид кремния (SiO2), который широко используется в качестве пищевой добавки (Е551), вспомогательного компонента в фармацевтических препаратах, в парфюмерно-косметической продукции и т.п. В спецификации JECFA на диоксид кремния отутствует информация о размере его частиц, что допускает использование в качестве пищевой добавки высокодисперсного аморфного SiO2, полученного газофазным гидролизом тетрахлорсилана. Данный материал, известный как «Аэросил», характеризуется размером удельной площади поверхности 300-380 м2/г и размером своих относительно слабо агломерированных частиц 6-30 нм, то есть является наноматериалом. На биологической модели исследованы морфологические изменения тканей органов и систем при пероральном введении наноразмерных частиц диоксида кремния. Крысы-самцы линии Вистар получали на протяжении 92 суток наноразмерный диоксид кремния с удельной площадью поверхности 300 м2/г и размером первичных наночастиц по данным электронной, атомно-силовой микроскопии и динамического рассеяния света в интервале 20-60 нм. Светооптическое морфологическое исследование органов крыс выявило относительно слабо выраженные воспалительные явления в структуре паренхиматозных органов (печень, почки), не демонстрирующие определенной зависимости от дозы наночастиц. Наиболее выраженными были изменения морфологии подвздошной кишки, состоящие в массивной лимфомакрофагальной и эозинофильной инфильтрации ворсинок, без видимого нарушения структуры их эпителиального пласта, что косвенно указывает на отсутствие нарушений барьерной функции кишечного эпителия. При максимальной из доз (100 мг/кгмассы тела) усиление иммунной реакции в стенке подвздошной кишки было наиболее значительным. Полученные результаты указывают на возможные риски для здоровья человека при использовании SiO2 с удельной площадью поверхности 300 м2/г и выше в составе пищевой продукции в качестве пищевой добавки.
А: наночастицы, диоксид кремния, морфологические исследования, пероральное поступление, подострая токсичность, риск здоровью
Короткий адрес: https://sciup.org/14237981
IDR: 14237981 | УДК: 615.9, | DOI: 10.21668/health.risk/2016.4.10
Impact of silica dioxide nanoparticles on the morphology of internal organs in rats by oral supplementation
The object of the study was amorphous silica dioxide (SiO2), which is widely used as a food additive (E551), a subsidiary component in pharmaceutical preparations, perfumery and cosmetic products etc. In the specification of JECFA silica dioxide does not have information about the size of its particles, which allows the use of fine amorphous SiO2, obtained by gas phase hydrolysis of tetrachlorosilane as a food additive. This material, known as the "Aerosil", is characterized by the size of the specific surface area of 300-380 m2/g and the size of its relatively weakly agglomerated particles of 6-30 nm, i.e., it is a nanomaterial. In the biological model the morphological changes in organs and tissue systems on oral supplementation of nanoscale particles of silica dioxide were studied. Wistar male rats were given nanosized silica dioxide with specific surface area of 300 m2/g and primary nanoparticle size on the basis of data of electrical, atomic-powered microscopy, and dynamic light scattering in the range of 20-60 nm during 92 days. Light microscopic morphological examination of organs of rats showed a relatively mild inflammation in the structure of parenchymal organs (liver, kidney), not showing a certain dose-dependent nanoparticles. The most pronounced changes were in ileum morphology, consisting of a massive lymph macrophage and eosinophil infiltration of villi, without any apparent violation of their epithelial layer structure, which indirectly indicates the absence of violations of the barrier function of the intestinal epithelium. At the maximum dose of 100 mg/kg bw, the increased immune response was the most significant in the wall of the ileum. The results indicate the potential risks to human health when using SiO2 having a specific surface area of 300 m2/g or higher in the composition of food products as a food additive.
Текст научной статьи Влияние наночастиц диоксида кремния на морфологию внутренних органов у крыс при пероральном введении
Аморфный диоксид кремния (SiO 2 ) широко используется в качестве пищевой добавки (Е551), а также вспомогательного компонента в фармацевтических препаратах и в парфюмерно-косметической продукции. В спецификации JECFA на диоксид кремния [25] отсутствует информация о размере его частиц, что допускает использование в качестве пищевой добавки высокодисперсного аморфного SiO 2 , полученного газофазным гидролизом тетра-хлорсилана. Данный материал, известный как «Аэросил», характеризуется удельной площадью поверхности 300–380 м2/г и размером своих относительно слабо агломерированных частиц 6–30 нм, то есть является наноматериалом (НМ).
Необходимость оценки безопасности и рисков НМ для здоровья человека обосновывается в Постановлении главного государственного санитарного врача Российской Федерации № 54 от 23.07.2007 г. «О надзоре за продукцией, полученной с использованием нанотехнологий и содержащей наноматериалы» и информационном письме Роспотребнадзора «О надзоре за производством и оборотом продукции, содержащей наноматериалы» [2, 6].
Предварительная оценка степени потенциальной опасности наночастиц диоксида кремния, согласно действующим МР 1.2.2522-09, указывает на среднюю потенциальную опасность данного наноматериала, что требует проведения его развернутого токсиколого-гигиенического исследования в тестах in vivo на лабораторных животных с использованием комплекса интегральных, морфологических, биохимических и других показателей и маркеров токсичности.
Целью настоящей работы являлось изучение влияния наноразмерного SiO 2 на морфологию внутренних органов крыс при пероральном введении в течение 92 суток.
Материалы и методы. В работе использован высокодисперсный аморфный SiO2, приобретенный в фирме ООО «Силика» (Россия, Московская обл., г. Долгопрудный) под торговым наименованием «Орисил 300», соответствующий ГОСТ 14922-77. Представляет собой легкий белый порошок, дающий при диспергации ультразвуком в воде опалесцирующий бесцветный коллоидный раствор, стабильный в течение не менее 2 суток. Удельная площадь поверхности продукта, определенная методом изотерм адсорбции инертных газов, составила по данным изготовителя 300 м2/г. Выполненная в ФГБНУ «Научно-исследовательский институт питания»
и ФГБУН «Институт биохимии им. А.Н. Баха» характеристика наноматериала с использованием методов трансмиссионной электронной микроскопии, атомно-силовой микроскопии и динамического рассеяния света (ДРС) [8], показала (рис. 1), что в составе сухого продукта представлены преимущественно агломераты первичных частиц размером от 5 до 100 нм. Анализ распределения частиц образца по размеру в обработанной ультразвуком водной суспензии в концентрации 1 % по массе выявил, что преобладающая фракция наночастиц (НЧ) имела среднечисловой гидродинамический диаметр 56,6 ± 32,1 нм, 90-й перцентиль размера – 91,7 нм. Содержание частиц с диаметром более 100 нм при этом не превышало 10 % от общего числа частиц.
Работу с животными проводили в соответствии с «Руководством по уходу и использованию лабораторных животных» (ILAR, DELS) и «Правилами лабораторной практики» [5, 17]. Исследования выполнены в соответствии с [4]. Эксперимент выполнен на 75 крысах-самцах линии Вистар исходной массой 80 г, полученных из питомника «Столбовая». На протяжении всего эксперимента животные получали сбалансированный полусинтетический рацион. Крыс размещали в клетках группами по три особи, рацион и воду предоставляли в режиме свободного неограниченного доступа. В начале эксперимента животные были случайным образом разделены на пять групп равной численности (по 15 крыс), совпадающих по исходной средней массе тела. Животным 1-й (контрольной) группы вводили носитель (деионизованную воду). Крысы групп со 2-й по 5-ю получали наноразмерный SiO 2 в виде обработанной ультразвуком суспензии в деионизованной воде (время обработки 5 мин, частота 44 кГц, мощность 1 Вт/см3). В течение первых 30 суток введение НМ осуществляли внутрижелудочно через зонд, а на протяжении последующих 62 суток суспензию SiO2 добавляли к корму животных; дозу при этом рассчитывали, исходя из поедаемости рациона. Вводимая доза SiO 2 в группах 2–5 составляла 0,1; 1,0; 10 и 100 мг/кг массы тела соответственно. Выведение животных из эксперимента осуществляли на 93-е сутки опыта путем обескровливания из нижней полой вены под эфирной анестезией. Отобранные пробы внутренних органов (печень, почки, подвздошная кишка) немедленно помещали в фиксатор (3,7 % раствор формальдегида в 0,1 М натрий-фосфатном буфере рН = 7,00 ± 0,05) и транспортировали в лабора-
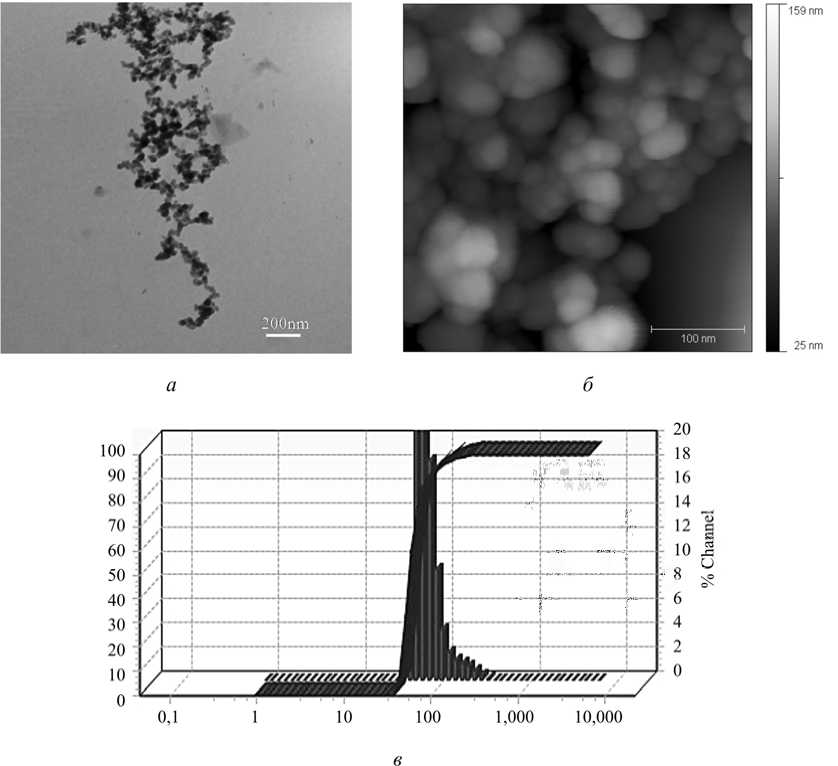
Рис. 1. Размер частиц аморфного диоксида кремния «Орисил-300»: а – метод электронной микроскопии (микроскоп «JEM-100СХ», JEOL, Япония), микроскопия образца без ультразвуковой обработки; б – метод атомно-силовой микроскопии (микроскоп «SmartSPM», «АИСТ-НТ», Россия), микроскопия образца без ультразвуковой обработки; в – метод динамического рассеяния света (прибор «Nanotrack Wave», Microtrack Inc., США), распределение по размеру частиц образца, обработанного звуком. Воспроизведено из работы [5] с разрешения авторов
торию для исследования. Подготовка гистологических препаратов включала дегидратацию фрагментов органов в спиртах восходящей концентрации, пропитку хлороформом и парафином в автоматическом гистологическом процессоре «Excelsior ES» (Thermo Scientific, Германия). Далее образцы заливали гомогенизированной парафиновой средой «Histomix» [1] на станции заливки блоков «Histo Star» (Thermo Scientific, Германия). Парафиновые срезы толщиной 3–4 мкм изготавливали на санном микротоме «JUNG SM 2000R» (Leica, Германия) и окрашивали их по общепринятой методике [3] гематоксилином и эозином в роботе-окрашивате-ле «Varistain Gemini ES» (Thermo Scientific, Германия). Полученные микропрепараты исследовали на светооптическом микроскопе «MEIJI» (Techno,
Япония) при увеличении ×50, ×100, ×200, ×400, ×800, ×1000. Микрофотографии выполняли с помощью камеры «Microscopy VISION» (VISION, Канада). Из каждого органа готовили не менее 9 микропрепаратов. Общее число проанализированных микропрепаратов (срезов) органов составило 400 штук.
Результаты и их обсуждение. Как показали результаты исследования внутренних органов, у всех животных 1-й группы (контрольной) определена персистирующая гиперплазия лимфоидной ткани подвздошной кишки с формированием вторичных фолликулов. На отдельных микропрепаратах в портальных трактах печени выявлена слабо выраженная лимфоидная инфильтрация, одиночные эозинофилы. В почках животных видимые морфологические изменения не установлены. В целом состояние морфологии внутренних органов крыс контрольной группы в основном соответствует норме для животных данного пола и возраста. Репрезентативные микрофотографии срезов печени, почки и подвздошной кишки крыс контрольной группы приведены на рис. 2.
Во 2-й группе животных (доза диоксида кремния 0,1 мг/кг массы тела) в печени выявлена слабо выраженная очаговая пылевидная и мелкокапельная жировая паренхиматозная дистрофия, эозинофилия инфильтрата портальных трактов (рис. 3, а). В части почечных клубочков отмечалась слабо выраженная пролиферация мезангиальных клеток (до 6 в дольке) без увеличения объема мезангиального матрикса; очаговое набухание клеток наружного листка капсулы нефрона (рис. 3, б). В основании крипт слизистой оболочки подвздошной кишки определяются крупные трапециевидные клетки с крупными эозинофильными гранулами в апикальной части и темным ядром в ба- зальных отделах – клетки Панета. Солитарные лимфатические узелки - крупные с большими реактивными центрами, широкими клеточными мантийными зонами, из собственной пластинки они проникают в подслизистую основу. Пейеровы бляшки распространяются из собственной пластинки слизистой в подслизистую основу. В месте расположения крупных пейеровых бляшек просвет кишки резко сужен. Лимфатические узелки между ворсинами выпячивают слизистую оболочку в просвет кишки в виде купола, который покрыт низкими эпителиоцитами с большим количеством лимфоцитов, макрофагов (рис. 3, в). В подслизистой основе небольшой отек, умеренная инфильтрация из эозинофилов, макрофагов, лимфоцитов и плазматических клеток.
У животных 3-й группы (доза диоксида кремния 1 мг/кг массы тела) гепатоциты печени находятся в состоянии очаговой пылевидной и мелкокапельной жировой дистрофии: в цитоплазме клеток множественные мелкие прозрачные
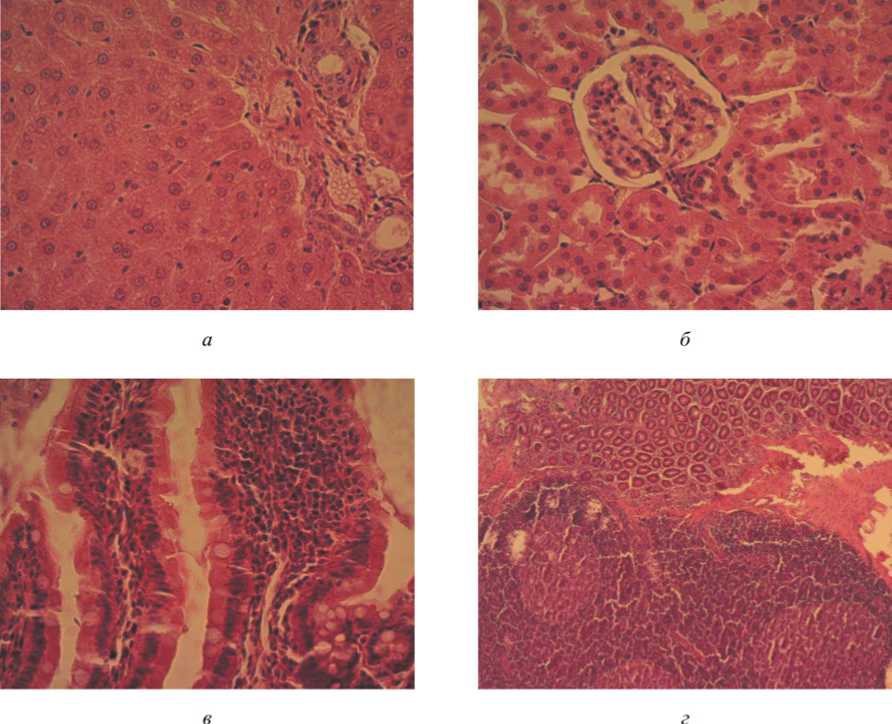
Рис. 2. Репрезентативные микрофотографии крысы группы 1 (контроль) (окраска гематоксилином и эозином, ув. ×200 ( а , г ), ×400 ( б , в )): а – печень, б – почки; в, г – подвздошная кишка
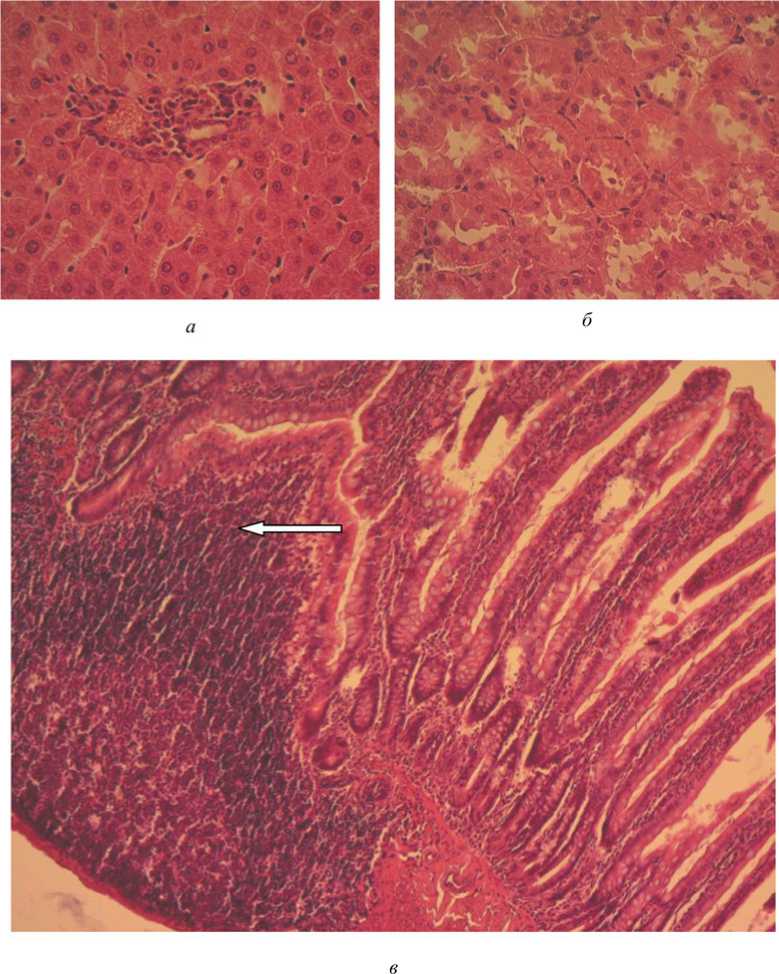
Рис. 3. Репрезентативные микрофотографии крысы группы 2 (диоксид кремния 0,1 мг/кг массы тела) (окраска гематоксилином и эозином, ув. ×200 ( а , б ); ×400 ( в )): а – печень; б – почки;
в – подвздошная кишка. Стрелкой показана межузелковая лимфоидная ткань
капли с четкими контурами, встречаются гепатоциты с двумя ядрами. В портальных трактах и синусоидах отмечается инфильтрация лимфоцитов, макрофагов, плазматических клеток с примесью единичных эозинофилов (рис. 4, а). В почках животных данной группы признаков пролиферации мезангиальных клеток и клеток наружного листка капсулы не наблюдалось. В единичных клубочках отмечено очаговое набухание клеток наружного листка капсулы (рис. 4, б). В слизистой оболочке подвздошной кишки ворсины разной формы и ширины из-за неравномерного отека и клеточной инфильтрации из лимфоцитов, макрофагов и многочисленных эозинофилов (рис. 4, в). В собственной пластинке присутствуют скопления лимфоцитов, макрофагов, плазматических клеток, множественные эозинофилы. В основании крипт большие скопления клеток Панета. Солитарные фолликулы и фолликулы пейеровых бляшек крупные, с большими реактивными центрами и широкими мантийными зонами, переходящими в межузелковую лимфоидную ткань. Фолликулы из слизистой оболочки распространяются на
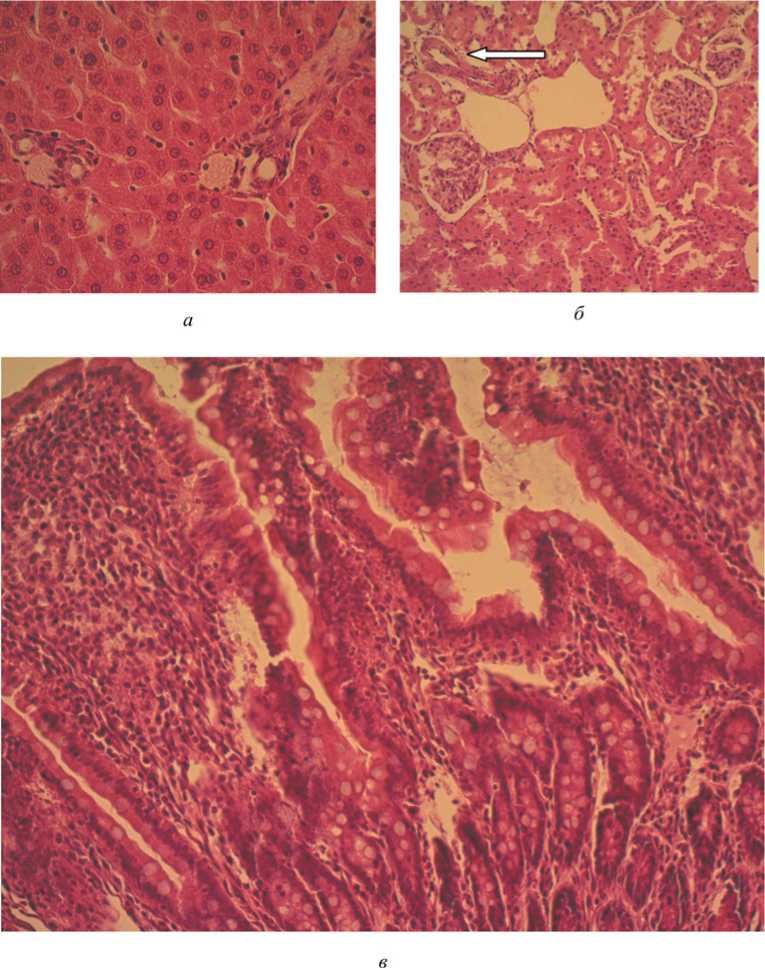
Рис. 4. Репрезентативные микрофотографии крысы группы 3 (диоксид кремния 1,0 мг/кг массы тела) (окраска гематоксилином и эозином, ув. ×200 ( а , б ), ув. ×400 ( в )): а – печень; б – почки, стрелкой показана вена; в – подвздошная кишка
подслизистую основы и резко истончают мышечную оболочку. В проекции пейеровых бляшек крипты неглубокие или отсутствуют, а ворсины короткие и неправильной формы. Лимфоидные узелки образуют выпячивания слизистой оболочки между ворсин в виде купола, покрытого низкими эпителиоцитами с большим количествам лимфоцитов, макрофагов. В подслизистой основе скопления лимфоцитов, макрофагов, плазматических клеток и большого количества эозинофилов.
У животных 4-й группы (доза диоксида кремния 10 мг/кг массы тела) гепатоциты име- ют многоугольную форму, одно или два ядра с мелкодисперсным хроматином, конденсированным у ядерной мембраны, хорошо видимыми ядрышками. Цитоплазма гепатоцитов зернистая (рис. 5, а). Портальные тракты содержат выраженную инфильтрацию из эозинофилов, макрофагов, лимфоцитов и плазматических клеток, часть клеток инфильтрата проникает в перипортальные синусоиды. В почках в части клубочков слабо выраженная пролиферация мезангиальных клеток (до 6 в дольке) без увеличения объема мезангиального матрикса (рис. 5, б). Признаков пролиферации клеток
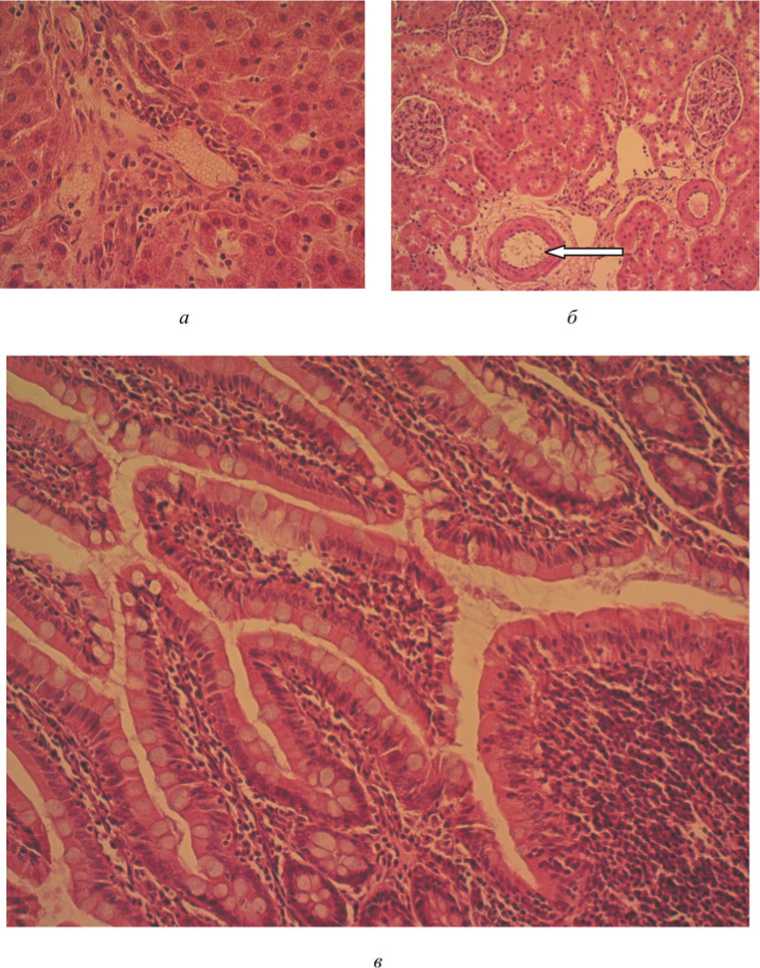
Рис. 5. Репрезентативные микрофотографии крысы группы 4 (диоксид кремния 10 мг/кг массы тела) (окраска гематоксилином и эозином, ув. ×200 ( а , б ); ув. ×400 ( в )): а – печень; б – почки, стрелкой показана артерия; в – подвздошная кишка, стрелкой показаны клетки Панета
наружного листка капсулы нет. В подвздошной кишке в собственной пластинке слизистой небольшой отек, умеренно выраженная лимфомакрофагальная инфильтрация с примесью значительного количества эозинофилов и плазматических клеток. В основании крипт кишечного эпителия хорошо дифференцируются скопления клеток Панета (рис. 5, в). Солитарные фолликулы крупные, из собственной пластинки проникают в подслизистую основу. Пейеровы бляшки содержат широкие клеточные скопления межузелковой лимфоидной ткани. В про- екции пейеровых бляшек крипты неглубокие или отсутствуют, ворсины короткие и неправильной формы. Лимфатические узелки образуют выпячивания слизистой оболочки между ворсин в виде купола, который покрыт низким призматическим эпителием с большим количеством лимфоцитов, макрофагов. В подслизистой основе умеренно выраженный отек, диффузная лимфомакрофагальная инфильтрация с примесью большого количества эозинофилов. Мышечная оболочка в проекции лимфатических фолликулов резко истончена.
■-•; *•■•.,• .эдй»
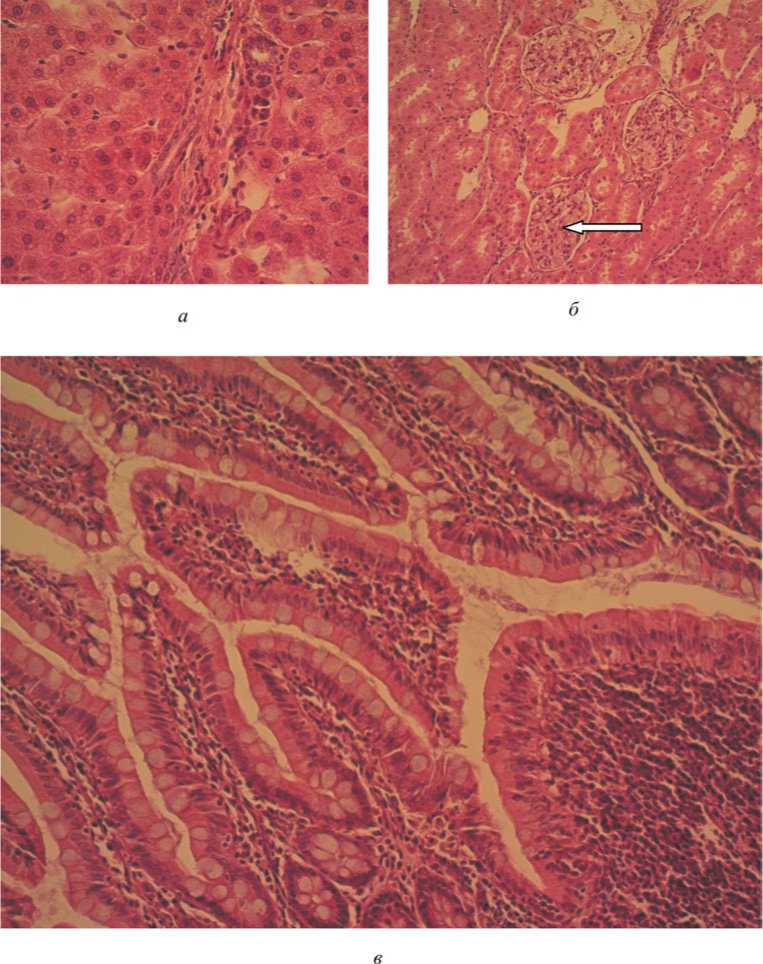
Рис. 6. Репрезентативные микрофотографии крысы группы 5 (диоксид кремния 100 мг/кг массы тела) (окраска гематоксилином и эозином, ув. ×200 ( а , б ); ув. ×400 ( в )): а – печень; б – почки, стрелкой показана артерия; в – подвздошная кишка
У животных 5-й группы (доза диоксида кремния 100 мг/кг массы тела) в печени гепатоциты имеют многоугольную форму, одно или два ядра с мелкодисперсным хроматином, конденсированным у ядерной мембраны, хорошо видимыми ядрышками. Цитоплазма гепатоцитов грубо зернистая эозинофильная (рис. 6, а). Портальные тракты содержат умеренно выраженную инфильтрацию из эозинофилов, макрофагов, лимфоцитов. Клетки Купфера крупные, неправильной формы, преобладают пери-портально. В почках в части клубочков слабо выраженная пролиферация мезангиальных кле- ток (до 6 в дольке) с незначительным увеличением объема мезангиального матрикса. Признаков пролиферации клеток наружного листка капсулы нет (рис. 6, б). В подвздошной кишке на всем протяжении эпителия слизистой оболочки хорошо дифференцируется интраэпителиальная лимфоидная ткань, представленная одиночно расположенными лимфоцитами. У ворсин варьируются ширина и форма из-за разной выраженности отека и воспалительной инфильтрации, состоящей из макрофагов, лимфоцитов, эозинофилов (рис. 6, в). Собственная пластинка слизистой содержит большое коли- чество макрофагов, лимфоцитов, плазматических клеток, эозинофилов. В основании крипт хорошо дифференцируются скопления клеток Панета. Солитарные лимфатические узелки крупные, с большими светлыми преобладающими реактивными центрами, широкими клеточными мантийными зонами; из собственной пластинки проникают в подслизистую основу. Пейеровы бляшки содержат до 8 крупных вторичных фолликулов и скопления межузелковой лимфоидной ткани, располагаются не только в собственной пластинке, но и в подслизистой основе. В проекции пейеровых бляшек крипты неглубокие или вообще отсутствуют, а ворсины короткие и неправильной формы. Лимфатические узелки между ворсин выпячивают слизистую оболочку в просвет в виде купола, который покрыт низкими эпителием (М-клетки) с большим количеством лимфоцитов, макрофагов. Реактивные центры фолликулов содержат центроциты, центробласты, иммунобласты, большое количество макрофагов. Мантийные зоны и межузелковая лимфоидная ткань представлены малыми лимфоцитами с мелкими темными ядрами, узким ободком цитоплазмы, макрофагами. Подслизистая основа представлена рыхлой волокнистой соединительной тканью, местами содержит скопления лимфоцитов, диффузно расположенные эозинофилы, макрофаги, плазматические клетки. В проекции лимфатических фолликулов мышечная оболочка резко истончена.
Результаты показывают, что в органах животных всех опытных групп отмечаются определенные изменения по сравнению с контрольной группой. В печени они представлены эозинофильной инфильтрацией портальных трактов, зернистостью цитоплазмы энтероци-тов (печень), в почках – относительно слабо выраженной очаговой дистрофией наружного листка капсулы нефрона. Эти изменения не демонстрируют определенной зависимости от дозы вводимого наноматериала и, как можно предположить, находятся в пределах возрастных изменений в указанных органах у животных старше 4 месяцев. Тем не менее направленность этих изменений, особенно в печени, свидетельствует об определенном усилении иммунной реакции, вызванной введением НЧ SiO2.
Наиболее выраженными являются изменения морфологии подвздошной кишки, состоящие в массивной лимфомакрофагальной и эозинофильной инфильтрации ворсинок, подслизистого слоя и собственной пластинки. Указанное усиление интенсивности иммунной реакции в стенке кишки, которое, возможно, является результатом раздражающего действия НЧ SiO2, нарастает монотонно во всем интервале доз НМ, что не позволяет с уверенностью установить его дозу, при которой эти изменения заведомо выходят за пределы показателей контрольной группы. Тем не менее достаточно очевидно, что при максимальной из доз (100 мг/кг массы тела) усиление иммунной реакции в стенке подвздошной кишки становится весьма значительным.
Таким образом, исследованный в работе аморфный SiO 2 широко используется в пищевой промышленности в качестве пищевой добавки Е551 с функцией антислеживающего агента и носителя. Согласно ТР ТС 029/2012, допускается использование Е551 в составе таких видов пищевой продукции, как пряности (не более 30 г/кг), продукты, плотно обернутые фольгой (30 г/кг), продукты сухие порошкообразные, включая сахарную пудру (10 г/кг), сыры и их заменители (10 г/кг), соль и ее заменители (10 г/кг), ароматизаторы (50 г/кг). В составе продуктов детского питания допускается использование Е551 в количестве до 10 г/кг, если эта пищевая добавка вносится в готовый продукт в составе другого сырьевого продукта. Норматив использования Е551 в составе сухих продуктов из зерновых (каш) для детского питания составляет 2 г/кг. В БАД к пище, сахаристых кондитерских изделиях (кроме шоколада) содержание Е551 не регламентируется и устанавливается технической документацией изготовителя. В подавляющем большинстве случаев наноразмерная структура применяемого диоксида кремния не декларируется производителями пищевой продукции, в связи с чем установить более или менее точные объемы потребления этого наноматериала с пищей не представляется возможным.
Как показало изучение острой токсичности наноразмерного SiO2 в эксперименте на мышах [7], при однократном внутрижелудоч-ном введении этого вещества через зонд в дозе до 10 000 мг/кг оно не вызывает гибели и явлений интоксикации животных. В гистологических препаратах ободочной и тощей кишки морфологические изменения отсутствовали.
С другой стороны, согласно результатам исследований на большом числе модельных систем in vitro, НЧ SiO2 цитотоксичны при контакте с клетками различных типов. Так, в работе [16] под действием этого НМ выявлено снижение жизнеспособности клеток эпителия бронхов человека линии Beas-2B, развитие процессов перекисного окисления, сдвиги в протеомном профиле ферментов внутриклеточного киназного каскада. Усиление продукции провоспалитель-ных цитокинов под действием НЧ аморфного SiO2 было установлено в двух линиях эпителиальных и эндотелиальных клеток легкого [19]. Нарушение баланса синтеза окиси азота и пероксинитрита в клетках эндотелия сосудов, обработанных этими НЧ, было обнаружено в исследовании [14]. Согласно результатам работы [20], НЧ аморфного SiO2 в клетках человека линии MCF-7 были дозозависимо цитотоксичны, а в нелетальных концентрациях вызывали гиперэкспрессию глутатион-S-трансферазы-1. Под действием НЧ SiO2 наблюдался эффект агрегации тромбоцитов, опосредуемый влиянием на баланс окиси азота и пероксинитрита [13].
НЧ SiO2 вызывали повреждение клеток линии EAHY926, притом, что аналогичные частицы субмикронного размера (100–330 нм) не были токсичны [26]. В культуре стволовых клеток эмбриона мыши наноразмерный SiO 2 с диаметром частиц 10 и 30, но не 80 нм, подавлял дифференцировку в кардиомиоциты [18]. Апоптоз и изменения в экспрессии р53, Вах и Bcl-2 под действием НЧ SiO 2 размером 21 нм были выявлены в гепатоцитах линии L-02 [21]. В культуре Купферовских макрофагов печени крыс данный вид НЧ вызывал высвобождение больших количеств реакционноспособных форм кислорода, оксида азота и TNF- α [15]. Способность рассматриваемых НЧ стимулировать процессы аутофагии в клетках эндотелия установлена в исследовании [24].
При внутрибрюшинном введении НЧ аморфного SiO2 в очень высоких дозах (вплоть до 2 г/кг массы тела) отмечали сдвиги в функции перитонеальных макрофагов, повышение продукции IL-1β, TNF-α, NO, экспрессию генов IL-1,6, TNF-α, синтазы окиси азота, циклооксигеназы-2 [22]. При внутривенном введении НЧ кремнезема диаметром 70 нм были гепатотоксичны для крыс в дозе 30 мг/кг [23]. При таком же способе введения наноматериала мышам в дозе 2–50 мг/кг массы тела были выявлены изменения пропорции CD3+, CD45+, CD4+ и CD8+ клеток в селезенке, сдвиги в уровнях общих иммуноглобулинов классов IgG и IgM [28]. По данным [29] НЧ SiO2 были способны усиливать интраназальную аллергическую сенсибилизацию мышей модельным аллергеном овальбумином. Аналогичные данные на модели бронхиальной астмы у крыс, вызываемой сенсибилизацией к овальбумину, получены в исследовании [12].
В работе [27] изучали подострую (в 84-дневном эксперименте) токсичность двух видов на-ноструктурированного SiO2 при пероральном введении крысам в дозах от 100 до 2500 мг/кг массы тела. Попытка количественно оценить всасывание и бионакопление SiO2 в органах и тканях методом масс-спектрометрии привела к неоднозначным результатам ввиду высокого фонового уровня кремния в органах животных контрольной группы. Однако качественно было констатировано достоверное увеличение содержания кремния в печени и селезенке животных, получавших НЧ в наибольшей дозе. Было отмечено дозозависимое усиление фиброза и экспрессии генов, ответственных за этот процесс, в печени. По этим показателям авторы оценивают пороговую дозу (LOAEL) НЧ SiO2 при подострой пероральной экспозиции величиной 2500 мг/кг массы тела, а максимальную недействующую дозу (NOAEL) – более 100 мг/кг массы тела. Недостатком цитируемой работы (отмечаемым самими авторами) являются очень высокие дозы вводимых животным НЧ, которые ни в каком отношении не соотносятся с возможной реальной экспозицией через пищу, составляющей, по оценкам авторов, около 1,8 мг/кг массы тела в день.
В совместных исследованиях ФГБНУ «Научно-исследовательский институт питания» и ФБУН «Федеральный научный центр медикопрофилактических технологий управления рисками здоровью населения» была проанализирована подострая пероральная токсичность для крыс и мышей производимого промышленностью наноструктурного SiO 2 типа «Аэросил» (с размером НЧ 20–60 нм) в эксперименте продолжительностью до 92 суток. Как показали результаты исследований, представленные в работах [7–11], у животных, получавших НЧ SiO 2 , отмечалась выраженная лейкопения, достоверное снижение доли Т-хелперов и возрастание доли цитотоксических лимфоцитов, уменьшение иммунорегуляторного индекса (CD4/CD8), дисбаланс цитокинов, проявлявшийся в достоверном многократном возрастании уровня TNF- α и выраженном снижении IL-10. Пороговая доза токсического воздействия НЧ SiO 2 при 92-суточной пероральной экспозиции у крыс составила в соответствии с изученными показателями 100 мг/кг массы тела в сутки.
Полученные в настоящем исследовании морфологические данные свидетельствуют о том, что при введении в этих же условиях нанораз-мерного SiO2 в желудочно-кишечный тракт животных в их подвздошной кишке развивается выраженная иммунная реакция, распространяющаяся на ассоциированную со стенкой кишки лимфоидную ткань и состоящая в массивной лимфомакрофагальной и эозинофильной инфильтрации ворсинок, без видимого нарушения структуры их эпителиального пласта, что косвенно указывает на отсутствие нарушений барьерной функции кишечного эпителия и согласуется с ранее полученными данными работы [8]. Исходя из вышеприведенных данных исследования НЧ SiO2 в системах in vitro и in vivo, можно предположить, что пусковым механизмом такой реакции является поглощение НЧ межэпителиальными и (или) входящими в состав лимфатических фолликул макрофагами, с последующей реакцией «респираторного взрыва», гиперпродукцией реакционноспособных свободнорадикальных производных кислорода и выработкой провоспалительных цитокинов и хемоки-нов, вызывающих привлечение и активацию им- мунных клеток различных типов. Следствием такой реакции может быть развитие системного воспаления, проявляющегося в вышеуказанных сдвигах в функции Т-клеточного иммунитета. Вместе с тем для выяснения деталей процесса развития местной иммунной реакции в стенке тонкой кишки под действием НЧ SiO2 необходимы дополнительные исследования, в том числе на ультраструктурном уровне.
Выводы. Проведенные исследования на светооптическом уровне выявили признаки токсического действия НЧ SiO2 с удельной площадью поверхности 300 м2/г на организм животных при пероральном введении в дозах 0,1–100 мг/кг массы тела в течение 92 суток, проявляющиеся, в первую очередь, в развитии иммунной и (или) воспалительной реакции в тонкой кишке. Полученные результаты указывают на возможные риски для здоровья человека при использовании диоксида кремния (SiO 2 ) с удельной площадью поверхности 300 м2/г и выше в составе пищевой продукции в качестве пищевой добавки.
Список литературы Влияние наночастиц диоксида кремния на морфологию внутренних органов у крыс при пероральном введении
- Меркулов Г.А. Курс патологогистологической техники. -Л.: Медицина, Ленинградское отделение, 1969. -424 с.
- Методические подходы к оценке безопасности наноматериалов/Г.Г. Онищенко, А.И. Арчаков, В.В. Бессонов, Б.Г. Бокитько, А.Л. Гинцбург, И.В. Гмошинский, А.И. Григорьев, Н.Ф. Измеров, М.П. Кирпичников, Б.С. Народицкий, В.И. Покровский, А.И. Потапов, Ю.А. Рахманин, В.А. Тутельян, С.А. Хотимченко, К.В. Шайтан, С.А. Шевелева//Гигиена и cанитария. -2007. -№ 6. -С. 3-10.
- Микроскопическая техника: руководство/под ред. Д.С. Саркисова и Ю.Л. Петрова. -М.: Медицина, 1996. -544 с.
- МУ 1.2.2520-09. Токсиколого-гигиеническая оценка безопасности наноматериалов: методические указания. -М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2009. -35 с.
- Об утверждении правил лабораторной практики: Приказ Минздравсоцразвития России № 708Н от 23.08.2010 г. . -URL: http://www.consultpharma.ru/index.php/ru/documents/drugs/299-708-23-2010 (дата обращения: 10.10.2016).
- Онищенко Г.Г., Тутельян В.А. О концепции токсикологических исследований, методологии оценки риска, методов идентификации и количественного определения наноматериалов//Вопросы питания. -2007. -Т. 76, № 6. -С. 4-8.
- Токсикологическая оценка наноструктурного диоксида кремния. Параметры острой токсичности/Н.В.Зайцева, М.А.Землянова, В.Н. Звездин, Довбыш А.А., И.В. Гмошинский, С.А. Хотимченко, И.В. Сафенкова, Т.И. Акафьева//Вопросы питания. -2014. -Т. 83, № 2. -С. 42-49.
- Токсикологическая оценка наноструктурного диоксида кремния. I. Интегральные показатели, аддукты ДНК, уровень тиоловых соединений и апоптоз клеток печени/А.А. Шумакова, Е.А. Арианова, В.А. Шипелин, Ю.С. Сидорова, А.В. Селифанов, Э.Н. Трушина, О.К. Мустафина, И.В. Сафенкова, И.В. Гмошинский, С.А. Хотимченко, В.А. Тутельян//Вопросы питания. -2014. -Т. 83, № 3. -С. 52-62.
- Токсикологическая оценка наноструктурного диоксида кремния. II. Энзимологические, биохимические показатели, состояние системы антиоксидантной защиты/А.А. Шумакова, Л.И. Авреньева, Г.В. Гусева, Л.В. Кравченко, С.Х. Сото, И.В. Ворожко, Т.Б. Сенцова, И.В. Гмошинский, С.А. Хотимченко, В.А. Тутельян//Вопросы питания. -2014. -Т. 83, № 4. -С. 58-66.
- Токсикологическая оценка наноструктурного диоксида кремния. III. Микроэкологические, гематологические показатели, состояние системы иммунитета/А.А. Шумакова, Н.Р. Ефимочкина, Л.П. Минаева, И.Б. Быкова, С.Ю.Батищева, Ю.М. Маркова, Э.Н. Трушина, Мустафина О.К., Н.Э. Шаранова, И.В. Гмошинский, Р.А. Ханферьян, С.А. Хотимченко, С.А.Шевелева, В.А. Тутельян//Вопросы питания. -2015. -Т. 84, № 4. -С. 55-65.
- Токсикологическая оценка наноструктурного диоксида кремния. IV. Иммунологические и аллергологические показатели у животных, сенсибилизированных пищевым аллергеном, и заключительное обсуждение/А.А. Шумакова В.А. Шипелин, Э.Н. Трушина, О.К. Мустафина, И.В. Гмошинский, Р.А. Ханферьян, С.А. Хотимченко, В.А. Тутельян//Вопросы питания. -2015. -Т. 84, № 5. -С. 102-111.
- Adverse Effect of Nano-Silicon Dioxide on Lung Function of Rats with or without Ovalbumin Immunization/B. Han, J. Guo, T. Abrahaley //PLoS One. -2011. -Vol. 6, № 2. -P. e17236.
- Amorphous silica nanoparticles aggregate human platelets: potential implications for vascular homeostasis/J.J. Corbalan, C. Medina, A. Jacoby //Int. J. Nanomedicine. -2012. -Vol. 7. -P. 631-639.
- Amorphous silica nanoparticles trigger nitric oxide/peroxynitrite imbalance in human endothelial cells: inflammatory and cytotoxic effects/J.J. Corbalan, C. Medina, A. Jacoby //Int. J. Nanomedicine. -2011. -Vol. 6. -P. 2821-2835.
- Chen Q., Xue Y., Sun J. Kupffer cell-mediated hepatic injury induced by silica nanoparticles in vitro and in vivo//Int. J. Nanomedicine. -2013. -Vol. 8. -P. 1129-1140.
- Eom H.-J., Choi J. SiO2 Nanoparticles Induced Cytotoxicity by Oxidative Stress in Human Bronchial Epithelial Cell, Beas-2B//Environ. Health Toxicol. -2011. -Vol. 26. -P. e2011013.
- Guide for the care and use of laboratory animals. Eighth Edition/Committee for the Update of the Guide for the Care and Use of Laboratory Animals; Institute for Laboratory Animal Research (ILAR); Division on Earth and Life Studies (DELS); National Research Council of the national academies. -Washington: The National Academies Press, 2011. -246 p. . -URL: https://grants.nih.gov/grants/olaw/Guide-for-the-Care-and-use-of-laboratory-animals.pdf (дата обращения: 10.10.2016).
- In vitro developmental toxicity test detects inhibition of stem cell differentiation by silica nanoparticles/M.V. Park, W. Annema, A. Salvati, A. Lesniak, A. Elsaesser, C. Barnes, G. McKerr, C.V. Howard, I. Lynch, K.A. Dawson, A.H. Piersma, W.H. de Jong//Toxicol. Appl. Pharmacol. -2009. -Vol. 240, № 1. -P. 108-116.
- Inflammatory and cytotoxic responses of an alveolar-capillary coculture model to silica nanoparticles: Comparison with conventional monocultures/J. Kasper, M.I. Hermanns, C. Bantz //Part. Fibre Toxicol. -2011. -Vol. 8. -Р. 6.
- Microsomal glutathione transferase 1 protects against toxicity induced by silica nanoparticles but not by zinc oxide nanoparticles/J. Shi, H.L. Karlsson, K. Johansson //ACS Nano. -2012. -Vol. 6, № 3. -P. 1925-1938.
- Nano-SiO2 induces apoptosis via activation of p53 and Bax mediated by oxidative stress in human hepatic cell line/Y. Ye, J. Liu, J. Xu, L. Sun, M. Chen, M. Lan//Toxicol. In Vitro. -2010. -Vol. 24, № 3. -P. 751-758.
- Park E.J., Park K. Oxidative stress and pro-inflammatory responses induced by silica nanoparticles in vivo and in vitro//Toxicol. Lett. -2009. -Vol. 184, № 1. -P. 18-25.
- Silica nanoparticles as hepa-totoxicants/H. Nishimori, M. Kondoh, K. Isoda //Eur. J. Pharm. Biopharm. -2009. -Vol. 72, № 3. -P. 496-501.
- Silica nanoparticles enhance autophagic activity, disturb endothelial cell homeostasis and impair angiogenesis/J. Duan, Yo. Yu, Ya. Yu, Y. Li, P. Huang, X. Zhou, S. Peng, Z. Sun//Part. Fibre Toxicol. -2014. -Vol. 11, № 1. -P. 50.
- Silicon dioxide, amorphous. Rome: JECFA. -1973-1992. -2 p. . -URL: http://www. fao.org/fileadmin/user_upload/jecfa_additives/docs/Monograph1/Additive-385.pdf (дата обращения: 10.10.2016).
- Size-dependent cytotoxicity of monodisperse silica nanoparticles in human endothelial cells/D. Napierska, L.C. Thomassen, V. Rabolli, D. Lison, L. Gonzalez, M. Kirsch-Volders, J.A. Martens, P.H. Hoet//Small. -2009. -Vol. 5, № 7. -P. 846-853.
- Sub-chronic toxicity study in rats orally exposed to nanostructured silica/M. van der Zande, R.J. Vandebriel, M.J. Groot, E.Kramer, Z.E.H. Rivera, K.Rasmussen, J.S.Ossenkoppele, P. Tromp, E.R. Gremmer, R.J.B. Peters, P.J. Hendriksen, H.J.P. Marvin, R.L.A.P. Hoogenboom, A.A.M. Peijnenburg, H. Bouwmeester//Part. Fibre Toxicol. -2014. -Vol. 11. -P. 8.
- The comparative immunotoxicity of mesoporous silica nanoparticles and colloidal silica nanoparticles in mice/S. Lee, M.-S. Kim, D. Lee, T.K. Kwon, D. Khang, H.-S.Yun, S.-H. Kim//Int. J. Nanomedicine. -2013. -Vol. 8. -P. 147-158.
- Yoshida T., Yoshioka Y., Fujimura M. et al. Promotion of allergic immune responses by intranasally-administrated nanosilica particles in mice//Nanoscale Res. Lett. -2011. -Vol. 6, № 1. -P. 192-204.


