Влияние нестероидных противовоспалительных препаратов (диклофенака, целекоксиба, нимесулида, диацереина) на ренальный транспорт мочевой кислоты у больных оксалатной нефропатией с сопутствующим гонартритом
Автор: Воронина Наталья Владимировна, Гельмутдинов Данир Данисович, Лемещенко Ольга Валентиновна
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 1, 2023 года.
Бесплатный доступ
Цель. Оценка экскретируемой фракции мочевой кислоты у больных оксалатной нефропатией на ранних стадиях хронической болезни почек с гонартритом при курсовом лечении нестероидными противовоспалительными препаратами. Материалы и методы. В открытое сравнительное рандомизированное исследование было включено 192 женщины с оксалатной нефропатией и первичным гонартритом. Скорость клубочковой фильтрации составила более 60 мл/мин, ИМТ 23,4±1,8, возраст 51,4±2,3 года. Первая группа больных получала диклофенак натрия (4500 мг/мес.), вторая группа целекоксиб (6000 мг/мес.), третья группа нимесулид (6000 мг/мес.), четвертая группа диацереин (6000 мг за 2 мес.). Контрольную группу по каждому препарату составили больные с гонартритом, но без нефропатии и гиперурикемии, принимавшие препараты в тех же курсовых дозах. Оценку экскретируемой фракции мочевой кислоты у обследуемых проводили на 15, 30, 60-й дни наблюдения по общепринятым методикам. Результаты. При применении диклофенака наблюдались снижение экскретируемой фракции мочевой кислоты и гиперурикемия, снижение скорости клубочковой фильтрации. После отмены диклофенака показатели через месяц не вернулись к первоначальным значениям. Целекоксиб и нимесулид оказали незначительное влияние на изменение экскретируемой фракции мочевой кислоты и снижение скорости клубочковой фильтрации. Через месяц после их отмены показатели вернулись к исходным. Диацереин не влиял на ренальный транспорт мочевой кислоты. В контрольной группе больных достоверных изменений показателей не отмечено.
Диклофенак, целесоксиб, нимесулид, диацереин, мочевая кислота, оксалатная нефропатия
Короткий адрес: https://sciup.org/14127222
IDR: 14127222 | УДК: 616.61:615.276:616.72-007.248 | DOI: 10.34014/2227-1848-2023-1-27-42
Effect of non-steroidal anti-inflammatory drugs (diclofenac, celecoxib, nimesulide, diacerein) on renal transport of uric acid in patients with oxalate nephropathy and concomitant gonarthritis
The aim of the study is to evaluate the excreted uric acid fraction in patients with oxalate nephropathy in the early stages of chronic kidney disease with gonarthritis under non-steroidal anti-inflammatory drug therapy. Materials and Methods. An open, comparative, randomized study included 192 women, aged 51.4±2.3, with oxalate nephropathy and primary gonarthritis. The glomerular filtration rate was >60 ml/min, BMI 23.4±1.8. The first group of patients was taking Diclofenac Sodium (4500 mg/month), the second group Celecoxib (6000 mg/month), the third group Nimesulide (6000 mg/month), the fourth group -Diacerein (6000 mg/2 months). The control group for each drug consisted of patients with gonarthritis, but without nephropathy and hyperuricemia. The patients of the control groups were treated similarly. The excreted fraction of uric acid in the subjects was assessed on Day 15, Day 30, and Day 60 according to generally accepted methods. Results. A decrease in the excreted fraction of uric acid, hyperuricemia, and a decrease in the glomerular filtration rate were observed in patients taking Diclofenac. After one-month Diclofenac withdrawl, the parameters did not return to their original levels. Celecoxib and Nimesulide had margical effect on the changes of the excreted uric acid fraction and a decrease in glomerular filtration rate. A month after their withdrawl, the parameters returned to their original levels. Diacerein had no effect on the renal transport of uric acid. No significant changes were noted in the control.
Текст научной статьи Влияние нестероидных противовоспалительных препаратов (диклофенака, целекоксиба, нимесулида, диацереина) на ренальный транспорт мочевой кислоты у больных оксалатной нефропатией с сопутствующим гонартритом
Введение. В российских клинических рекомендациях по рациональному использованию нестероидных противовоспалительных препаратов (НПВП) [1] подчеркивается важность клинического мониторинга состояния больных, принимающих НПВП, для своевременного выявления неблагоприятных явлений, особенно у пациентов с факторами риска возможных осложнений (артериальная гипертония, гиповолемия, хроническая сердечная недостаточность, хроническая болезнь почек, прием ряда препаратов – ингибиторов АПФ, блокаторов медленных кальциевых каналов, диуретиков и др.) и с нефропатиями различного генеза.
НПВП в эквивалентных дозах обладают сходной анальгетической и противовоспалительной эффективностью, но их выбор должен определяться безопасностью в конкретных клинических условиях [2–5]. Применение НПВП у больных с уже имеющимися нефропатиями может вызывать прогрессирование почечного повреждения, негативно влиять на процессы, протекающие на уровне клубочков, снижая скорость клубочковой фильтрации (СКФ), и проксимальных канальцев, вызывая ренальную гиперурикемию [6–9].
Сформирована общая модель почечного транспорта уратов, согласно которой мочевая кислота, профильтровавшись в клубочках, подвергается активной реабсорбции, а затем активной секреции в проксимальных канальцах почек [10]. В настоящее время модель дополняется результатами исследований геномных ассоциаций (GWAS), экспрессионных систем биологических моделей, позволивших предположить взаимосвязь почечного транспорта мочевой кислоты и его нарушения с изменением функционирования уратных транспортеров URAT1 и GLUT9 в проксимальных канальцах почек человека [10–12]. НПВП, являясь слабыми органическими кислотами, секретируются в мочу через эпителий почечных канальцев с участием транспортеров органических анионов из семейства SLC22, располагающихся на базолатеральной мембране проксимальных почечных канальцев, и могут приводить к изменению их функционирования [12–15].
Диацереин является новым представителем НПВП, не относящимся к нефротоксичным препаратам, представляет собой ацетилированную форму реина, который, блокируя интерлейкин-1, снижает концентрацию металло-протеаз в хондроцитах при остеоартритах, стимулирует синтез простагландинов, гликозо-аминогликанов и гиалуроновой кислоты [3, 4]. Его рекомендуют в терапии хронической боли при остеоартрите у пациентов с противопоказаниями к НПВП [1]. Однако возможность его влияния на экскретируемую фракцию мочевой кислоты (EFUA) у больных с тубулоинтерстициальными нарушениями и кристаллу-рией целенаправленно не изучалась.
Нефропатия с оксалатно-кальциевой кри-сталлурией, именуемая оксалатной нефропатией (ОН), у взрослых чаще встречается при синдроме рецидивирующей вторичной гипероксалурии, характеризуется медленно прогрессирующим течением, клинически проявляется в периоды обострения заболевания умеренной гипероксалурией с оксалатно-кальцие-вой кристаллурией, микрогематурией и/или альбуминурией, прогрессирующим снижением функции канальцев, а в последующем и клубочков [16]. При давности болезни более 20 лет морфологически выявляются признаки хронического тубулоинтерстициального нефрита с вторичным поражением клубочков с исходом в фиброз с отложением кристаллов оксалата кальция в интерстиции [16].
К факторам риска прогрессирования ОН у пациентов с коморбидной патологией (остеоартрит, дорсопатии) относят применение НПВП, что было показано на небольшой когорте пациентов [17]. Описана клиника абак-териального цистита, связанного с увеличением оксалатно-кальциевой кристаллурии при приеме диклофенака. Феномен хронической боли у пациентов с остеоартритом и современные фармакологические подходы к лечению, основанные не только на курсовом, но и на непрерывном длительном приеме НПВП, обусловливают необходимость учета профиля их безопасности при использовании больными оксалатной нефропатией.
Следует также отметить, что в последние годы придают все большее значение гиперу-рикемии как фактору риска прогрессирования хронических неинфекционных заболеваний и роста смертности вследствие сердечно-сосудистых заболеваний [18–20].
Цель исследования. Оценка экскретируемой фракции мочевой кислоты у больных оксалатной нефропатией на ранних стадиях хронической болезни почек с гонартритом при курсовом лечении нестероидными противовоспалительными препаратами.
Материалы и методы. В открытое сравнительное рандомизированное исследование было включено 192 женщины с оксалатной нефропатией на стадии хронического тубулоинтерстициального нефрита, давностью болезни 20–30 лет, сопоставимые по индексу массы тела (ИМТ 23,4±1,8) и возрасту (51,4±2,3 года), с СКФ выше 60 мл/мин (1–2 стадия ХБП), наличием первичного гонартрита 2–3 стадии по Kellgren – Lawrence, выраженностью боли по индексу WOMAC более 400 мм. В исследование вошли больные, которые не получали НПВП, мочегонные и другие нефротоксические препараты в течение 2 мес. до момента включения в исследование, соблюдали гипо-оксалатную диету и подписали информированное согласие на участие.
Больные оксалатной нефропатией с остеоартритом были рандомизированы на 4 группы: 1-я группа (53 чел.) получала диклофенак натрия в дозе 150 мг/сут (курсовая доза за месяц – 4500 мг), 2-я группа (47 чел.) – целекок-сиб («Целебрекс», Pfizer HCP Corporation) в дозе 200 мг/сут (курсовая доза за месяц – 6000 мг), 3-я группа (42 чел.) – нимесулид («Найз», Dr. Reddy’s Laboratoris Ltd.) в дозе 200 мг/сут (курсовая доза за месяц – 6000 мг), 4-я группа (50 чел.) – диацереин («Диафлекс», Rompharm Company) по 100 мг/сут (курсовая доза за 2 мес. – 6000 мг).
В группу контроля (К) входили 120 женщин в возрасте 52,3±2,1 года с ИМТ 22,9±2,2, остеоартритом без оксалатной нефропатии и гиперурикемии, не имеющих других сопутствующих заболеваний, в т.ч. метаболического синдрома, артериальной гипертонии, сахарного диабета, нарушений функций почек, которые также были распределены на 4 группы по 30 чел. и принимали: 1-я группа – диклофенак (месячная курсовая доза – 4500 мг), 2-я группа – целекоксиб (месячная курсовая доза – 6000 мг), 3-я группа – нимесулид (месячная курсовая доза – 6000 мг), 4-я группа – диацереин (курсовая доза за 2 мес. – 6000 мг).
Оценка ренального транспорта мочевой кислоты в сопоставлении с СКФ у больных и в контрольной группе проводилась на 15-й и 30-й дни лечения диклофенаком, целекокси-бом, нимесулидом и через 30 дней после отмены препаратов (60-й день наблюдения). Длительность лечения указанными НПВП определялась наличием хронической боли в суставах. Больные, принимавшие диацереин в непрерывном режиме, оценивались на 15, 30 и 60-й дни лечения.
Для оценки ренального транспорта мочевой кислоты исследовалось содержание мочевой кислоты в плазме (Рua) и моче (Uua), рассчитывались скорость клубочковой фильтрации и экскретируемая фракция мочевой кислоты. Исследование мочевой кислоты в плазме и моче проводилось уриказным методом на биохимическом анализаторе Hitachi-912 (Hoffman la Roche, Швейцария). Уровень креатинина в сыворотке крови (Pcr) и моче (Ucr) определялся общепринятым кинетическим методом Яффе. Скорость клубочковой фильт- рации рассчитывалась по формуле СКD-EPI [18]. EFUA рассчитывалась по общепринятой формуле [7, 19].
Статистический анализ результатов проводился с использованием пакета прикладных программ StatSoft Statistica v.8.0. Результаты представлены в виде M ± σ. В зависимости от характера распределения для сравнения групп использовался t-критерий Стьюдента. Межгрупповые отличия рассчитывались по непараметрическому критерию Манна – Уитни (Mann – Whitney U-test). Статистически значимыми считались отличия при p<0,05. Для оценки статистической значимости межгрупповых различий в частоте событий использовался точный критерий Фишера. Для оценки динамики показателей на фоне лечения применялся парный непараметрический метод анализа по Вилкоксону. Достоверными считались различия при p<0,05. Наличие или отсутствие связи определялось с помощью критерия /2, при наличии связи проводилось измерение с помощью коэффициентов корреляции Пирсона.
Результаты и обсуждение. До назначения НПВП у больных ОН СКФ была не ниже 82 мл/мин/1,73 м2, уровень Рua достоверно превышал значения контрольной группы лиц и был не выше 0,37 ммоль/л, EFUA исходно была снижена, но не ниже 8 %, в группе контроля EFUA была не ниже 13 %. Результаты исследования в группах сравнения представлены в табл. 1–4.
При анализе динамики показателей в ходе лечения препаратом диклофенак (табл. 1) у пациентов с ОН отмечено достоверное снижение СКФ (р<0,001), Uua (р<0,01) и EFUA (р<0,01), что повлияло на повышение Рua (р<0,01). Через 30 дней после отмены диклофенака выявлена тенденция к снижению ги-перурикемии, увеличению EFUA и СКФ (р<0,01). У пациентов контрольной группы показатели Рua, Uua и EFUA весь период оставались практически на одном уровне, а СКФ снизилась на 10 %, но после отмены препарата нормализовалась (рис. 1, 2).
Таблица 1
Table 1
Динамика показателей ренального транспорта мочевой кислоты и скорости клубочковой фильтрации у больных оксалатной нефропатией, принимающих диклофенак, в сравнении с контрольной группой (М±σ)
Parameters of renal transport of uric acid and glomerular filtration rate in patients with oxalate nephropathy taking Diclofenac in comparison with the control
|
Период Period |
Рua, ммоль/л Рua, mmol/l |
Uua, ммоль/л Uua, mmol/l |
EFUA, % |
СКФ, мл/мин/1,73 м2 GFR, ml/min/1,73 m2 |
||||
|
ОН ON |
К Control |
ОН ON |
К Control |
ОН ON |
К Control |
ОН ON |
К Control |
|
|
До лечения Before treatment |
0,36 ± 0,03* |
0,28 ± 0,03 |
2,82 ± 0,41** |
3,20 ± 0,52 |
8,09 ± 0,25* |
13,13 ± 0,94 |
83,74 ± 3,80* |
116,06 ± 4,10 |
|
Через 15 дней Day 15 |
0,41 ± 0,04* |
0,29 ± 0,03 |
2,64 ± 0,40* |
3,20 ± 0,52 |
7,24 ± 0,41* |
12,72 ± 0,88 |
64,33 ± 7,62* |
108,92 ± 4,71 |
|
Через 30 дней Day 30 |
0,47 ± 0,03* |
0,29 ± 0,03 |
2,40 ± 0,38* |
3,22 ± 0,53 |
6,16 ± 0,12* |
12,46 ± 0,91 |
48,42 ± 3,46* |
105,86 ± 4,51 |
|
Через 60 дней Day 60 |
0,39 ± 0,03* |
0,28 ± 0,02 |
2,61 ± 0,41* |
3,22 ± 0,53 |
6,97 ± 0,36* |
12,72 ± 0,88 |
65,01 ± 4,42* |
113,05 ± 4,79 |
Примечание . * – р<0,001; ** – р<0,01 при сравнении показателей в группах.
Note. * – p<0.001; ** – the differences are significant when comparing similar parameters in the groups p<0.01; GFR – glomerular filtration rate; ON – patients with oxalate nephropathy and osteoarthritis; Control – control group (patients with osteoarthritis without oxalate nephropathy).
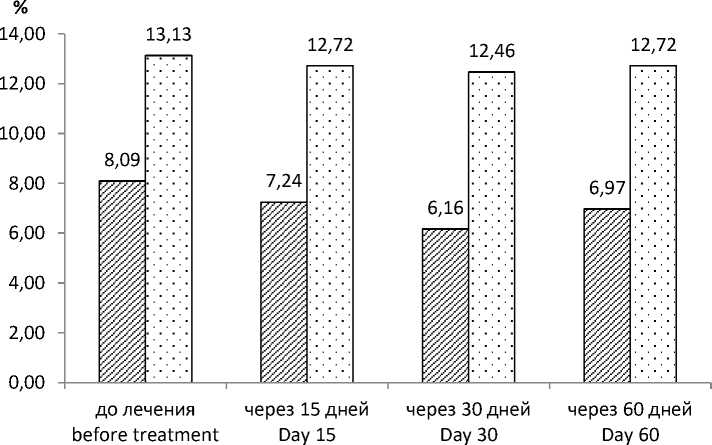
и EFUA ( с ОН) / EFUA (with ON) □ EFUA ( без ОН) / EFUA (without ON)
Рис. 1. Изменение EFUA у пациентов, применяющих диклофенак
Fig. 1. Changes in EFUA in patients taking Diclofenac
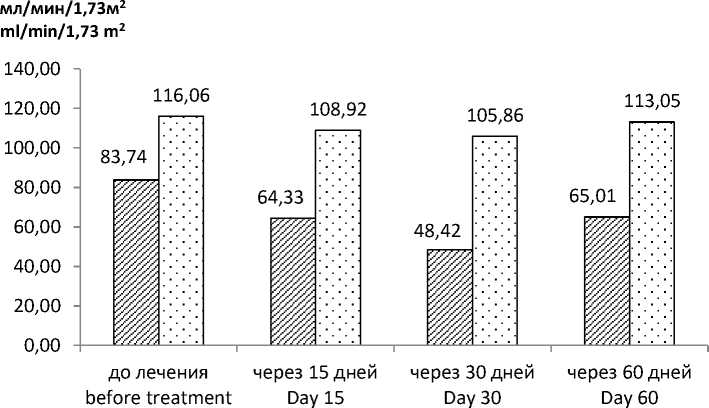
0 СКФ (с ОН) / GFR (with ON) □ СКФ (без ОН) / GFR (without ON)
Рис. 2. Изменение СКФ у пациентов, применяющих диклофенак
Анализ корреляционной зависимости показал наличие сильной прямой связи между Uua, EFUA и СКФ (r xy =0,99), сильной обратной связи между Рua и Uua (r xy =-0,95), Pua и EFUA (r xy =-0,92), Рua и СКФ (r xy =-0,96).
При анализе изменения показателей в процессе лечения нимесулидом (табл. 2) у пациентов с ОН отмечено достоверное снижение
СКФ (р<0,001), Uua (р<0,01), EFUA (р<0,01) и повышение Рua (р<0,01). Через 30 дней после отмены препарата выявлена тенденция к снижению гиперурикемии, увеличению EFUA и СКФ (р<0,01) (рис. 3, 4). У пациентов контрольной группы (без ОН) показатели Рua, Uua, EFUA и СКФ весь период оставались практически на одном уровне.
Таблица 2
Table 2
Динамика показателей ренального транспорта мочевой кислоты и скорости клубочковой фильтрации у больных оксалатной нефропатией, принимающих нимесулид, в сравнении с контрольной группой (М±σ)
Parameters of renal transport of uric acid and glomerular filtration rate in patients with oxalate nephropathy taking Nimesulid in comparison with the control (М±σ)
|
Период Period |
Рua, ммоль/л Рua, mmol/l |
Uua, ммоль/л Uua, mmol/l |
EFUA, % |
СКФ, мл/мин/1,73 м2 GFR, ml/min/1,73 m2 |
||||
|
ОН ON |
К Control |
ОН ON |
К Control |
ОН ON |
К Control |
ОН ON |
К Control |
|
|
До лечения Before treatment |
0,36 ± 0,02* |
0,27 ± 0,03 |
2,81 ± 0,36** |
3,14 ± 0,52 |
8,04 ± 0,29* |
13,16 ± 0,67 |
82,69 ± 4,30* |
118,35 ± 2,33 |
|
Через 15 дней Day 15 |
0,39 ± 0,02* |
0,27 ± 0,03 |
2,75 ± 0,35** |
3,13 ± 0,53 |
7,65 ± 0,33* |
12,93 ± 0,71 |
78,03 ± 4,70* |
117,48 ± 1,86 |
|
Через 30 дней Day 30 |
0,42 ± 0,02* |
0,27 ± 0,03 |
2,68 ± 0,35* |
3,13 ± 0,53 |
7,37 ± 0,35* |
12,82 ± 0,66 |
74,10 ± 3,89* |
117,79 ± 1,96 |
|
Через 60 дней Day 60 |
0,38 ± 0,02* |
0,28 ± 0,03 |
2,75 ± 0,36* |
3,15 ± 0,53 |
7,72 ± 0,29* |
12,90 ± 0,69 |
79,19 ± 4,28* |
117,98 ± 1,82 |
Примечание . * – р<0,001; ** – р<0,01 при сравнении аналогичных показателей в группах.
Note. * – p<0.001; ** – the differences are significant when comparing similar parameters in the groups p<0.01; ON – patients with oxalate nephropathy and osteoarthritis; Control – control group (patients with osteoarthritis without oxalate nephropathy).
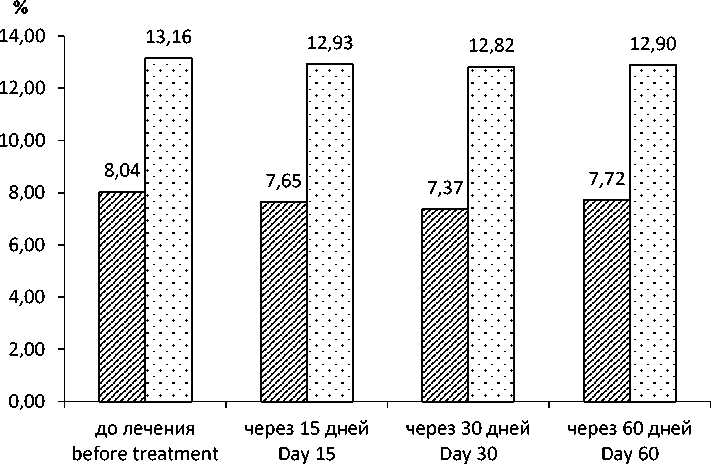
0 EFUA ( с ОН) / EFUA (with ON) □ EFUA ( без ОН) / EFUA (without ON)
Рис. 3. Изменение EFUA у пациентов, применяющих нимесулид
Fig. 3. Changes in EFUA in patients taking Nimesulid
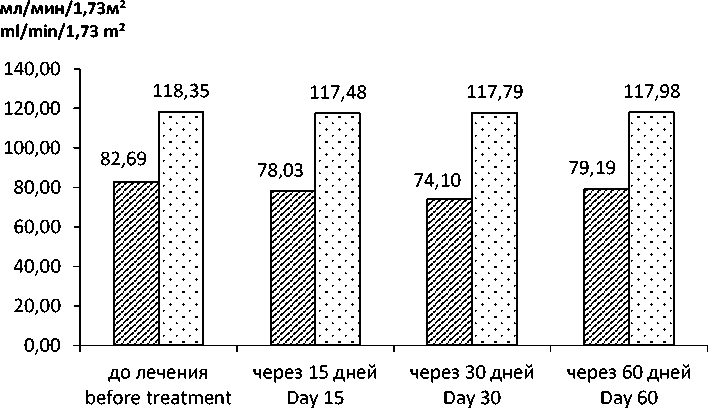
0 СКФ (с ОН) / GFR (with ON) □ СКФ (без ОН) / GFR (without ON)
Рис. 4. Изменение СКФ у пациентов, применяющих нимесулид
Анализ корреляционной зависимости показал наличие сильной прямой связи между Uua и EFUA (r xy =0,99), Uua и СКФ (r xy =0,98), сильной обратной связи между Рua и Uua, EFUA и СКФ (r xy =-0,99).
Изменения лабораторных показателей в течение 30 дней лечения целекоксибом (табл. 3) у пациентов с ОН были аналогичны таковым при приеме нимесулида. Отмечено достовер- ное снижение СКФ (р<0,001), Uua (р<0,01), EFUA (р<0,01) и динамическое повышение Рua (р<0,01). Через 30 дней после отмены препарата выявлена тенденция к снижению гипе-рурикемии, увеличению EFUA и СКФ (р<0,01) (рис. 5, 6). У пациентов контрольной группы значения Рua, Uua, EFUA и СКФ весь период оставались практически на одном уровне.
Таблица 3
Table 3
Динамика показателей ренального транспорта мочевой кислоты и скорости клубочковой фильтрации у больных оксалатной нефропатией, принимающих целекоксиб, в сравнении с контрольной группой (М±σ)
Parameters of renal transport of uric acid and glomerular filtration rate in patients with oxalate nephropathy taking Celecoxib in comparison with the control (М±σ)
|
Период Period |
Рua, ммоль/л Рua, mmol/l |
Uua, ммоль/л Uua, mmol/l |
EFUA, % |
СКФ, мл/мин/1,73 м2 GFR, ml/min/1,73 m2 |
||||
|
ОН ON |
К Control |
ОН ON |
К Control |
ОН ON |
К Control |
ОН ON |
К Control |
|
|
До лечения Before treatment |
0,37 ± 0,02* |
0,28 ± 0,03 |
2,86 ± 0,32*** |
3,20 ± 0,69 |
8,08 ± 0,41* |
13,21 ± 0,87 |
82,10 ± 4,72* |
118,35 ± 2,33 |
|
Через 15 дней Day 15 |
0,39 ± 0,02* |
0,29 ± 0,04 |
2,82 ± 0,31** |
3,20 ± 0,68 |
7,82 ± 0,45* |
12,98 ± 0,86 |
76,36 ± 5,06* |
117,48 ± 1,86 |
|
Через 30 дней Day 30 |
0,41 ± 0,02* |
0,28 ± 0,04 |
2,75 ± 0,33** |
3,19 ± 0,68 |
7,57 ± 0,45* |
12,89 ± 0,92 |
71,62 ± 5,24* |
117,79 ± 1,96 |
|
Через 60 дней Day 60 |
0,38 ± 0,02* |
0,28 ± 0,04 |
2,82 ± 0,31** |
3,19 ± 0,69 |
7,95 ± 0,42* |
12,94 ± 0,83 |
79,20 ± 4,76* |
117,98 ± 1,82 |
Примечание . * – р<0,001; ** – р<0,01; *** – р<0,05 при сравнении аналогичных показателей в группах.
Note. * – p<0.001; ** – р<0.01; *** – the differences are significant when comparing similar indicators in the groups р<0.05; ON – patients with oxalate nephropathy and osteoarthritis; Control – control group (patients with osteoarthritis without oxalate nephropathy).
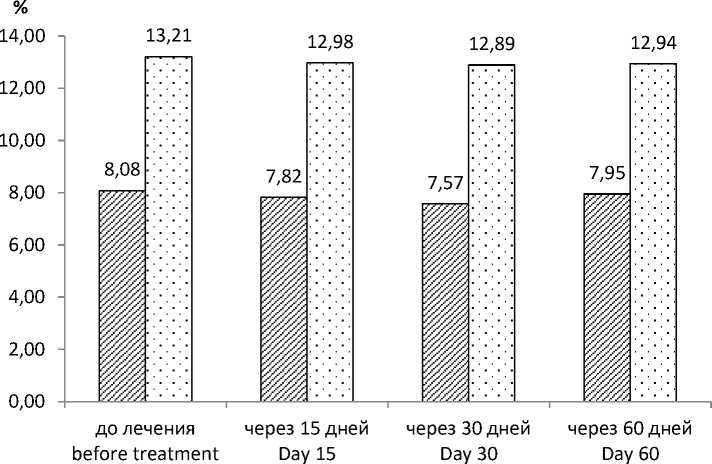
0 EFUA ( с ОН) / EFUA (with ON) □ EFUA ( без ОН) / EFUA (without ON)
Рис. 5. Изменение EFUA у пациентов, применяющих целекоксиб
Fig. 5. Changes in EFUA in patients taking Celecoxib
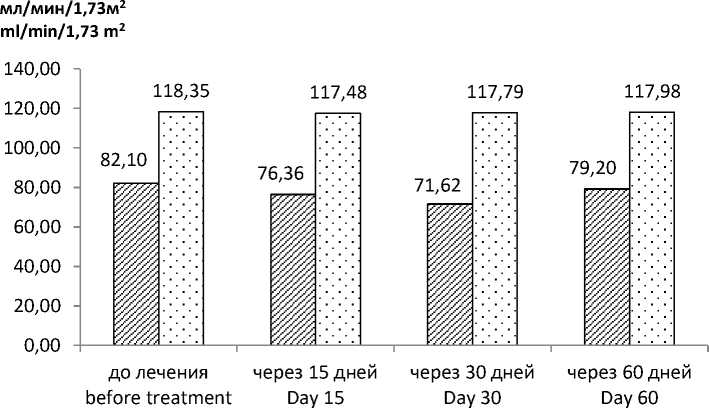
0 СКФ (с ОН) / GFR (with ON) □ СКФ (без ОН) / GFR (without ON)
Рис. 6. Изменение СКФ у пациентов, применяющих целекоксиб
Fig. 6. Changes in GFR in patients taking Celecoxib
Анализ корреляционной зависимости показал наличие сильной прямой связи между Uua и EFUA (r xy =0,97), Uua и СКФ (r xy =0,96), сильной обратной связи между Рua и Uua (r xy =-0,97), EFUA и СКФ (r xy =-0,99).
Динамика показателей ренального транспорта мочевой кислоты и СКФ у пациентов с ОН, принимающих диацереин, представлена в табл. 4 и на рис. 7, 8. При исходно несколько более высоких значениях Рua и сниженных, по сравнению с контрольной группой, показателях Uua, EFUA и СКФ не отмечено значимого изменения исследуемых показателей во время приема диацереина. Значения Рua, Uua, EFUA и СКФ в контрольной группе также весь период оставались практически на одном уровне с незначимым снижением EFUA на 1,6 % от исходных значений за 2 мес.
Таблица 4
Table 4
Динамика показателей ренального транспорта мочевой кислоты и скорости клубочковой фильтрации у больных оксалатной нефропатией, принимающих диацереин, в сравнении с контрольной группой (М±σ)
Parameters of renal transport of uric acid and glomerular filtration rate in patients with oxalate nephropathy taking Diaflex in comparison with the control (М±σ)
|
Период Period |
Рua, ммоль/л Рua, mmol/l |
Uua, ммоль/л Uua, mmol/l |
EFUA, % |
СКФ, мл/мин/1,73 м2 GFR, ml/min/1,73 m2 |
||||
|
ОН ON |
К Control |
ОН ON |
К Control |
ОН ON |
К Control |
ОН ON |
К Control |
|
|
До лечения Before treatment |
0,30 ± 0,04** |
0,27 ± 0,03 |
3,13 ± 0,41 |
3,22 ± 0,53 |
8,17 ± 0,33* |
12,67 ± 0,71 |
82,88 ± 4,31* |
113,91 ± 5,07 |
|
Через 15 дней Day 15 |
0,30 ± 0,04*** |
0,28 ± 0,03 |
3,15 ± 0,42 |
3,20 ± 0,54 |
8,15 ± 0,33* |
12,61 ± 0,70 |
82,10 ± 4,18* |
113,84 ± 4,18 |
|
Через 30 дней Day 30 |
0,31 ± 0,03** |
0,28 ± 0,03 |
3,15 ± 0,43 |
3,21 ± 0,54 |
8,14 ± 0,3* |
12,55 ± 0,78 |
81,40 ± 4,47* |
112,99 ± 4,29 |
|
Через 60 дней Day 60 |
0,30 ± 0,04 |
0,28 ± 0,03 |
3,16 ± 0,42 |
3,23 ± 0,52 |
8,13 ± 0,33* |
12,47 ± 0,76 |
81,37 ± 4,46* |
113,46 ± 4,85 |
Примечание . * – р<0,001; ** – р<0,01; *** – р<0,05 при сравнении аналогичных показателей в группах.
Note. * – p<0.001; ** – р<0.01; *** – the differences are significant when comparing similar indicators in the groups р<0.05; ON – patients with oxalate nephropathy and osteoarthritis; Control – control group (patients with osteoarthritis without oxalate nephropathy).
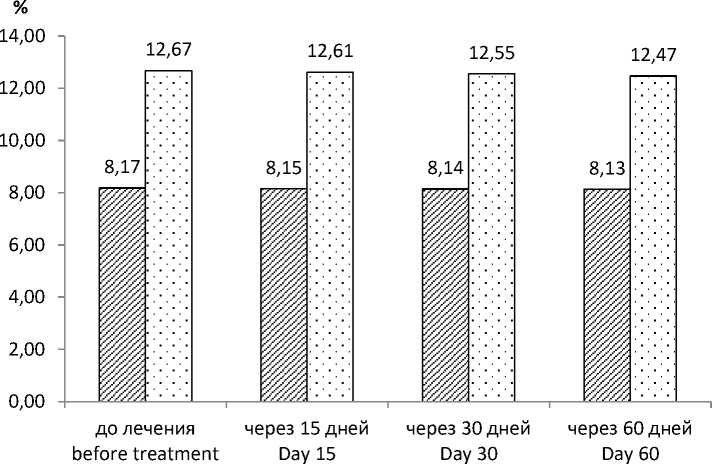
0 EFUA ( с ОН) / EFUA (with ON) □ EFUA ( без ОН) / EFUA (without ON)
Рис. 7. Изменение EFUA у пациентов, применяющих диацереин
Fig. 7. Changes in EFUA in patients taking Diaflex
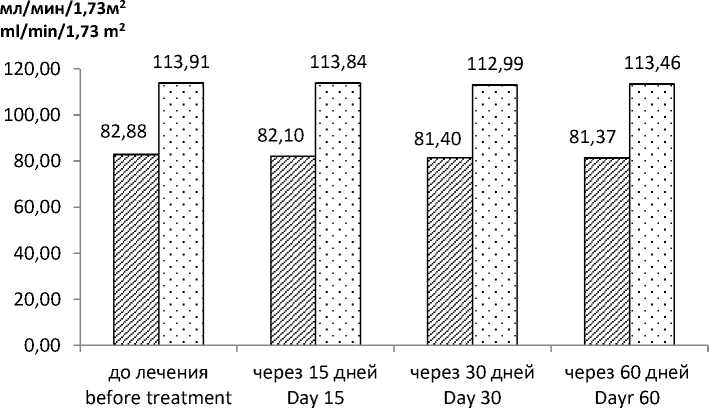
0 СКФ (с ОН) / GFR (with ON) □ СКФ (без ОН) / GFR (without ON)
Рис. 8. Изменение СКФ у пациентов, применяющих диацереин
Fig. 8. Changes in GFR in patients taking Diaflex
Анализ корреляционной зависимости показал отсутствие значимой связи между Uua, EFUA, СКФ и Рua и наличие сильной обратной связи между Uua и EFUA (r xy =0,91), Uua и СКФ (r xy =-0,89).
Сравнение препаратов между собой по эффектам воздействия на ренальный транспорт мочевой кислоты показало значимые различия (рис. 9). Так, при применении диклофенака наблюдались достоверно более выраженные подъем Рua и снижение Uua, EFUA и СКФ, продолжавшиеся до отмены препарата (р<0,001). После отмены препарата диклофенак показатели и через месяц не вернулись к первоначальным значениям. Целекоксиб и ни- месулид оказывали сходное влияние на ренальный транспорт мочевой кислоты и СКФ, но целекоксиб, тем не менее, оказывал более слабое воздействие и показатели быстрее возвращались к исходным после отмены препарата (р<0,05). Наиболее безопасным для применения оказался диацереин, который не нуждался в отмене после второго месяца использования и практически не изменял исходные показатели, не оказывал значимого влияния на ренальный транспорт мочевой кислоты (р<0,01). В контрольной группе лиц статически значимых изменений ренального транспорта мочевой кислоты и СКФ не наблюдали.
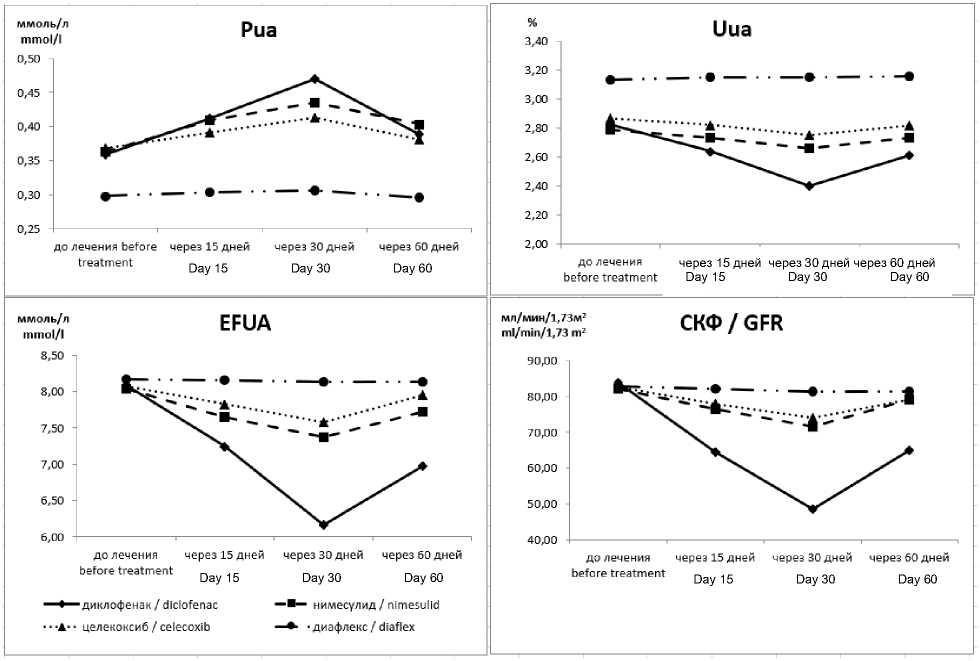
Рис. 9. Динамика показателей ренального транспорта мочевой кислоты и скорости клубочковой фильтрации у больных оксалатной нефропатией
Fig. 9. Parameters of renal transport of uric acid and glomerular filtration rate in patients with oxalate nephropathy
Заключение. Таким образом, у больных оксалатной нефропатией на 1–2 стадии ХБП при приеме нестероидных противовоспалительных препаратов (диклофенак, нимесулид, целекоксиб) наблюдали снижение СКФ и
фракционной экскреции мочевой кислоты. Наиболее выраженные изменения лабораторных показателей были отмечены при приеме диклофенака, причем они сохранялись и в течение месяца после его отмены. Прием диаце-
реина не вызывал нефротоксических эффек- имеет большое практическое значение при тов, не влиял на уровень СКФ и экскретируе- выборе безопасной терапии.
мую фракцию мочевой кислоты (EFUA), что
Список литературы Влияние нестероидных противовоспалительных препаратов (диклофенака, целекоксиба, нимесулида, диацереина) на ренальный транспорт мочевой кислоты у больных оксалатной нефропатией с сопутствующим гонартритом
- Рациональное использование нестероидных противовоспалительных препаратов. Клинические рекомендации. Научно-практическая ревматология. 2018; 56 (прил. 1): 1-29.
- Алексеева Л.И., Таскина Е.А., Кашеварова Н.Г. Остеоартрит: эпидемиология, классификация, факторы риска и прогрессирования, клиника, диагностика, лечение. Современная ревматология. 2019; 13 (2): 9-21.
- Алексеева Л.И., Кашеварова Н.Г., Таскина Е.А., Шарапова Е.П., Аникин С.Г., Короткова Т.А., Стребкова Е.А. Эффективность и безопасность диацереина у пациентов с остеоартритом коленных суставов. Современная ревматология. 2017; 11 (3): 1-8.
- Наумов А.В., Ховасова Н. О. Рекомендованная терапия остеоартрита: новые решения старых задач. РМЖ. 2016; 3: 1-4.
- Каратеев А.Е., Алексеева Л.И. Оценка переносимости диацереина в реальной клинической практике. Результаты исследования РОКАДА (Ретроспективная оценка клинических аспектов применения Диафлекса при остеоартрозе). Научно-практическая ревматология. 2015; 53 (2): 169-174.
- Сатыбалдыев А.М. Выбор нестероидных противовоспалительных препаратов у пожилого пациента с острой и хронической болью. Клиническая геронтология. 2020; 26 (5-6): 49-57. DOI: 10/26347/1607-2499202005-06049-057.
- Клинические рекомендации ассоциации нефрологов. Тубулоинтерстициальные болезни почек. Москва; 2021: 7-11.
- КутыринаИ.М. Оценка функционального состояния почек. В кн.: Тареева И.Е., ред. Нефрология: руководство для врачей. Т. 1. Москва: Медицина; 1995: 173-194.
- Zhang X., Donnan P.T., Bell S., Guthrie B. Non-steroidal antiinflammatory drug induced acute kidney injury in the community dwelling general population and people with chronic kidney disease: systematic review and meta-analysis. BMC Nephrol. 2017; 18 (1): 256. DOI: 10.1186/s12882-017-0673-8).
- Hsu C. C., Wang H., Hsu Y.H. Use of Nonsteroidal Anti-Inflammatory Drugs and Risk of Chronic Kidney Disease in Subjects with Hypertension: Nationwide Longitudinal Cohort Study. Hypertension. 2015; 66 (3): 524-533. DOI: 10.1161/Hypertensionaha.114.05105.epub 2015jul 13.
- Зверев Я. Ф., Брюханов В.М. Современные представления о механизмах почечного транспорта мочевой кислоты. Клиническая нефрология. 2016; 1: 42-49.
- Anton Ivanyuk, Francoise Livio, Jerome Biollaz, Thierry Buclin. Renal Drug Transporters and Drug Interactions. Clin Pharmacokinet. 2017; 56 (8): 825-892. DOI: 10.1007/s40262-017-0506-8.
- Tisdale J.E., Miller D.A. Drug Induced Diseases: Prevention, Detection, and Management. 3rd Ed. Be-thesda, Md.: American Society of Health-System Pharmacists; 2018; 41: 941-966.
- Endou H., Anzai N. Urate transport across the apical membrane of renal proximal tubules. Nucleosides Nucleotides Nucleic Acids. 2008; 27: 578-584.
- Harirforoosh S., Jamali F. Renal adverse effects of non-steroidal anti-inflammatory drugs. Expert Opin Drug Saf. 2009; 8 (6): 669-681. DOI: 10.1517/14740330903311023.
- Lipworth L., Abdel-Kader K., Morse J. High prevalence of non-steroidal anti-inflammatory drug use among acute kidney injury survivors in the southern community cohort study. BMC Nephrol. 2016; 17 (1): 189. DOI: 10.1186/s12882-016-0411-7.
- Воронина Н.В., Грибовская Н.В., Евсеев А.Н., Езерский Д.В. Особенности мочевого синдрома у больных оксалатной нефропатией в сопоставлении с результатами нефробиопсии. Дальневосточный медицинский журнал. 2013; 3: 15-20. 18 Воронина Н.В., Гельмутдинов Д.Д., Маркина О.И. Влияние нестероидных противовоспалительных препаратов - ингибиторов и не ингибиторов ЦОГ-2 на состояние почек у больных оксалатной нефро-патией, коморбидных по остеоартрозу. Дальневосточный медицинский журнал. 2016; 1: 14-19.
- Хроническая болезнь почек (ХБП): клинические рекомендации ассоциации нефрологов. Москва; 2021. 25.
- Арутюнов Г.П., Драгунов Д.О., Соколова А.В., Арутюнов А.Г. Фракционная экскреция мочевой кислоты как альтернативный маркер низкого уровня натрийуреза. Клиническая нефрология. 2014; 5: 20-24.
- Молчанова О.В., Бритов А.Н., Платонова Е.В. Значение повышенного уровня мочевой кислоты в развитии и профилактике хронических неинфекционных заболеваний. Профилактическая медицина. 2020; 23 (2): 102-108. DOI: 10.17116/profmed/ 202023021102.


