Влияние органических растворителей на определение содержания токоферолов в растительных маслах
Автор: Кищенко B.А., Левчук И.В., Ефименко С.Г.
Статья в выпуске: 1 (138), 2008 года.
Бесплатный доступ
Приводятся экспериментальные данные о воздействии органических растворителей, используемых для извлечения токоферолов при приготовлении образцов растительного масла. Количественный и качественный анализ токоферола проводили методом высокоэффективной жидкостной хроматографии. В качестве контроля точности данных использовался сертифицированный справочный материал.
Короткий адрес: https://sciup.org/142171292
IDR: 142171292 | УДК: 547.915:634.0892.6:581.19:577.161.3
An impact of organic solvents on determination of tocopherols in oils
The experimental data on impact of organic solvents used for extraction of tocopherols at preparation of vegetable oil samples are resulted. The quantitative and qualitative tocopherol analyses were done with high effective liquid chromatography method. A certified reference material was used as a control for data accuracy.
Текст обзорной статьи Влияние органических растворителей на определение содержания токоферолов в растительных маслах
ГНУ ВНИИ масличных культур
ВЛИЯНИЕ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ НА ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ТОКОФЕРОЛОВ В РАСТИТЕЛЬНЫХ МАСЛАХ
Растительные масла являются ценным источником биологически активных соединений, в том числе токоферолов (витамина Е). Масла применяются как комплексные компоненты питания, а при создании косметических, лечебно-профилактических препаратов и специальных продуктов питания являются источником витаминов. Естественные токоферолы, как и их синтетические аналоги, применяют в пищевых продуктах и косметических изделиях. В природе токоферолы синтезируются только растениями и представляют собой жирорастворимые вещества, которые переходят в масла в процессе их получения.
Токоферолы и их эфиры – это прозрачные, светло-желтые, вязкие субстанции, растворимые в органических растворителях и разрушающиеся под действием ультрафиолетовых лучей. Витамин Е достаточно устойчив к действию растворов едких щелочей, поэтому он не разрушается при проведении процесса щелочной рафинации жиров и может быть извлечён из них вместе с неомыляемыми веществами. Именно на этих свойствах основаны способы получения натуральных токоферолов. Однако выпускаемые химической промышленностью органические растворители содержат примеси, которые искажают точность определения содержания токоферолов и разрушают их в процессе анализа [1].
Многолетний опыт сотрудников лаборатории биохимии ВНИИМК по определению состава токоферолов в семенах подсолнечника с помощью тонкослойной хроматографии показывает, что используемые органические растворители в различной степени могут влиять на объективность результатов определений. В большей степени их претензии адресованы диэтиловому эфиру.
Диэтиловый эфир часто содержит примеси, которые являются результатом недостаточной очистки при получении, а иногда появляются в нём при использовании и последующем хранении, в результате которого образуются перекись водорода, ацетальдегид, этилпероксид, диоксиэтил-пероксид, озон и другие [2].
Целью настоящей работы стало изучение влияния различных органических растворителей, которые могут быть использованы для экстракции токоферолов из образцов растительных масел для последующего измерения методом высокоэффективной жидкостной хроматографии на обращенно-фазной колонке.
Для достижения этой цели были поставлены следующие задачи:
― определить степень извлечения токоферолов из образцов растительных масел с помощью различных органических растворителей;
― изучить влияние органических растворителей на точность определения содержания токоферолов в маслах на основании испытаний сертифицированного образца.
Материалы и методы. Для исследований использовался жидкостный хроматограф производства фирмы Hewlett-Packard НР 1100 с флуоресцентным и диодно-матричным детекторами, обращенно-фазная колонка Hypersil MOS (диаметр 2,1 мм, длина 200 мм). Мобильная фаза – ацетонитрил : вода (70:80), скорость потока 0,4 мл/мин, температура термостата колонок 40 С. Флуоресцентный детектор – длина волны возбуждения 295 нм, поглощения – 330 нм.
Органические растворители: гексан (Fluka), диэтиловый эфир (Ridel-de Haеn), диэтиловый эфир по ТУ ОП, хлористый метилен (Sigma), а также смесь гексана и диэтилового эфира в соотношении 80:20. Реактивы квалификации «х.ч.» производства фирм Aldrich, Fluka и др. Стандарты витаминов – чистые вещества производства фирмы Supelco. Сертифицированный образец арахисового масла с подтвержденным значением массовой доли витамина Е (Standard Reference Material Peanut Butter, каталожный № 2387, производства NIST).
Подготовку хроматографической системы к работе проводили соответственно инструкции по эксплуатации жидкостного хроматографа НР1100. Градуировочные растворы токоферолов готовили из исходного раствора в метаноле и анализировали при тех же самых условиях, что и образцы. По полученным данным строили градуировочную зависимость площади пика от концентрации компонента [3].
Рабочий диапазон массовой доли витамина Е, которую можно определять с помощью данного метода, составляет 1-500 мг/кг.
Результаты исследований. Подготовка образца к количественному определению при анализе токоферолов состоит из ряда операций и часто занимает 90 % затрат времени необходимого для проведения анализа. Как правило, она включает щелочной гидролиз образца масла, экстракцию органическими растворителями, промывку водой, сушку натрием сернокислым безводным, отгонку экстракта до сухого остатка и растворение его в соответствующем растворителе до получения необходимой концентрации для проведения анализа. Все эти операции вносят свои коррективы в проведение анализа и способны снижать его точность. Органические растворители, используемые для экстракции, как правило, содержат примеси, которые искажают точность определения токоферолов. Не исключена также возможность разрушения токоферолов в процессе пробоподготовки и проведения анализа. Так, например, гексан может содержать ненасыщенные углеводороды, диэтиловый эфир – большое количество пероксидов, которые способствуют разрушению токоферолов в процессе анализа. Поэтому при работе с диэтиловым эфиром необходимо убедиться в отсутствии пероксидов. Наличие пероксидов обнаруживают следующим образом: пробу эфира (2-3 мл) встряхивают в пробирке с таким же объемом 2 %-го раствора йодида калия, предварительно подкисленного несколькими каплями разбавленной соляной кислоты. Появление бурого окрашивания эфирного слоя указывает на присутствие пероксидов.
Учитывая вышесказанное, перед использованием органических растворителей для экстракции проводится проверка их на чистоту, и на их основе готовится так называемая «холостая» проба, которая проводится через весь ход анализа. В метанольном экстракте холостой пробы при введении в хроматограф не должно быть пиков, которые совпадают по времени удерживания с пиками токоферолов.
В результате проведенных нами исследований было установлено, что при использовании органических растворителей для экстракции токоферолов процент их извлечения в процессе анализа варьирует в зависимости от выбранного растворителя и степени его чистоты (рис.1). Это подтверждается, результатами испытаний сертифицированного образца арахисового масла с подтвержденным содержанием витамина Е. Нами было проведено шесть испытаний сертифицированного образца. Анализы
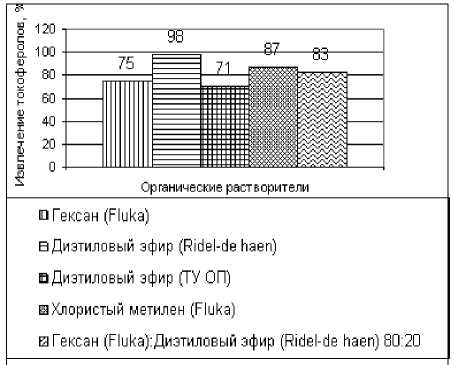
Рисунок 1 – Извлечение токоферолов органическими растворителями при экстракции, % проводили разные операторы в разные дни. В результате проведенных исследований было установлено, что наибольшая полнота извлечения токоферолов была достигнута применением диэтилового эфира (Ridel-de Haеn), свободного от пероксидов (рис. 2).
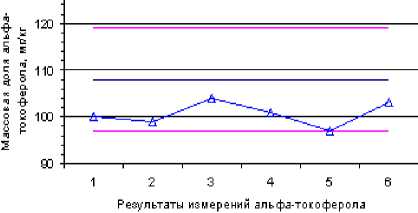
---Среднее подтвержуеноезначение
---Максимальное подтвержденное значение
— Минимальное подтвержденное значение
^а^Полученные результаты
Рисунок 2 – Воспроизводимость результатов измерений α-токоферола при использовании для экстракции диэтилового эфира (Ridel-de Haеn) по сертифицированному образцу
Выводы. Органические растворители, которые используются для экстракции токоферолов, должны быть химически чистыми и не содержать примесей, которые не только снижают точность определения, но и разрушают витамин Е в процессе подготовки образца к анализу. Следует проверять реактивы на чистоту и при необходимости проводить их очистку в условиях лаборатории. Диэтиловый эфир необходимо стабилизировать метанолом в количестве 0,5-1,0 % для предотвращения образо- вания пероксидов. Точность проведения анализа целесообразно контролировать по сертифицированному образцу.
Наибольшая степень извлечения токоферолов из образцов растительных масел достигается применением диэтилового эфира, свободного от пероксидов.


