Влияние особенностей мелкомасштабной структуры молочной железы на распределение глубинной температуры при использовании радиотермометрической диагностики
Автор: Хоперсков Александр Валентинович, Храпов Сергей Сергеевич, Новочадов Валерий Валерьевич, Бурнос Дарья Владимировна
Журнал: Математическая физика и компьютерное моделирование @mpcm-jvolsu
Рубрика: Информационные технологии и математическое моделирование
Статья в выпуске: 6 (25), 2014 года.
Бесплатный доступ
Обсуждается роль сложной мелкомасштабной структуры молочной железы в формировании распределения температуры из-за сильной пространственной неоднородности коэффициента теплопроводности и удельного тепловыделения различных биологических компонентов. В свою очередь пространственные изменения диэлектрической проницаемости и электропроводности в биоткани способны существенно влиять на яркостную температуру биотканей под антенной. Переход от многослойных моделей к многокомпонентной биоткани с учетом ее тонкой структуры и неоднородных параметров (теплопроводность, влагосодержание, удельное тепловыделение, электропроводность, диэлектрическая проницаемость, теплоемкость) может повысить эффективность проведения диагностики опухолей на ранних стадиях.
Перенос тепла, биоткани, радиационный перенос, радиотермометрия, диагностика, молочные железы
Короткий адрес: https://sciup.org/14968972
IDR: 14968972 | УДК: 616.053 | DOI: 10.15688/jvolsu1.2014.6.6
The effect of small-scale mammary glands structure on the distribution of the deep temperature using the microwave radiometry diagnostics
The role of complex small-scale structure of the breast in the formation of the temperature distribution due to the strong spatial inhomogeneity of the thermal conductivity and specific heat of various biological components is discussed. Spatial variations in dielectric permittivity and conductivity in biological tissue can significantly affect the brightness temperature of tissues under the antenna. The effectiveness of diagnosis of tumors at an early stage can be improved by moving beyond multi-layer model to the simulation of multicomponent biological tissues with the fine structure and heterogeneous parameters (conductivity, moisture content, specific heat, conductivity, dielectric constant and specific heat).
Текст научной статьи Влияние особенностей мелкомасштабной структуры молочной железы на распределение глубинной температуры при использовании радиотермометрической диагностики
Микроволновая радиотермометрия (далее – МТ) является важным инструментом диагностики опухолей молочной железы. МТ при всех своих достоинствах имеет низкую нозологическую специфичность [15; 21]. При обследованиях этим методом в «группу риска» попадают как наиболее опасные быстрорастущие опухоли, так и пациенты с выраженной пролиферацией, мастопатией или воспалительными процессами в тканях [14]. Для повышения специфичности необходимо детализировать и усложнить анализ результатов измерения. С этой целью в последней редакции методики микроволновой радиотермометрии для оценки результата требуется учитывать повышение величины термоасимметрии между одноименными точками молочных желез, повышенный разброс температур между отдельными точками в пораженной молочной железе, повышенную дисперсию разности температур между железами и т. д. [1; 3; 6].
Одним из важных признаков здоровой молочной железы клиницисты считают однородность температур как поверхностных (далее – ИК), так и глубоких (далее – РТМ) в пределах молочной железы, что обосновывается строением молочной железы. Большая грудная мышца создает общий температурный фон, отделяя молочную железу от крупных сосудов и органов грудной полости, а симметричное расположение долек железы вокруг соска обусловливает однородность температурного поля. Однако свойства тканей в молочной железе (железистой, жировой, соединительной) могут отличаться по излучению тепла. Например, известно, что температура крови, притекающей по артериям в различные органы, определяется температурой «теплового ядра» тела и составляет около 37 °С. Но за счет конвективного теплообмена одни ткани могут нагреваться, а другие охлаждаться. Подобные изменения температуры могут быть связаны с особенностями строения и кровоснабжения различных тканей в молочной железе, в том числе и опухолевых. Сильная неоднородность строения молочной железы требует построения адекватных компьютерных моделей с очень высоким разрешением. Отметим, например, важнейшую область соска, вблизи которого располагаются наиболее мелкие структуры и где данные о температуре являются наиболее информативными для диагностики онкологических и других заболеваний молочной железы. Первые модели, основанные на определении глубины проникновения плоской волны в однородную биологическую ткань, показали глубину проникновения на несколько сантиметров и сильную зависимость от влагосодержания и параметров и частоты излучения [10; 12]. Учет многослойной структуры тканей человека, поскольку различные параметры биологических тканей (диэлектрическая проницаемость, теплопроводность, электропороводность, удельное тепловыделение, коэффициенты теплообмена, пара- ISSN 2222-8896. Вестн. Волгогр. гос. ун-та. Сер. 1, Мат. Физ. 2014. № 6 (25) 61
метры кровотока, определяющие эффективность передачи тепла от артериальной крови тканям) могут различаться в несколько раз и даже более чем на порядок, позволяет получить более реалистичную картину [2]. Однако такого рода модели учитывают перенос тепла за счет теплопроводности в стационарном приближении. К тому же параметры непрерывно меняются внутри ткани одного типа и эта зависимость всех параметров от координат является существенным фактором.
Наибольшее распространение получил аппликационный радиометрический СВЧ-метод [5; 9; 11], при использовании которого антенна имеет непосредственный контакт с телом человека. Применение СВЧ радиометрии на частотах 1.1–1.6 ГГц демонстрирует достаточную чувствительность, чтобы отслеживать клинически значимые изменения температуры глубоко в тканях (4 см и больше) в отличие от методов инфракрасной термографии [19]. Моделирование тепловых и электромагнитных процессов для почек и мозга указывает на хорошее согласие с экспериментальными результатами [18]. Хорошие результаты дает применение радиотермометрии для ранней диагностики варикозной болезни [8].
Моделирование тепловых процессов
Численное моделирование излучения тканей, включая опухоли, проводится на основе уравнений теплопроводности и уравнений Максвелла в приближении [2; 17]:
V {k(x, y, z) V T(x, y, z)} = - Qbi(x, y, z) - Qmet(x, y, z),(1)
^^^^
V2 E (x, y, z)+ too^oSoe (x, y, z)• E (x, y, z) = 0,(2)
где k – коэффициент теплопроводности; T – температура; Q bl – источник тепла от кровотоков (определяется балансом тепла артериальной Q a и венозной Q v систем); Q met – источник тепла в результате метаболических процессов в тканях (рис. 1); E – вектор электрического поля; ε – диэлектрическая проницаемость; ∇ – оператор набла. Теплообмен с воздухом на границе, задаваемой единичным нормальным к поверхности вектором ^? ( г) , имеем
(^•^) = ^^5^(Г(%'У'2)- т^)- (3)
^VA,y,Z)
На рисунке 1 изображена схема теплообмена между биотканью и окружающей средой с температурой T air , определяющаяся коэффициентом теплопередачи h air , для которого можно принять h air = 13.5 Вт/(м∙оС). Отличительной особенностью биоткани является сильная пространственная неоднородность физических параметров [2; 4; 20]. Изменения электропроводности биоткани варьируются в пределах 0.1–3 см/м. Относительные изменения диэлектрической проницаемости также могут изменяться более чем на порядок: ε ≈ 2–80. Коэффициент теплопроводности варьируется в пределах 0.15–0.7 Вт/(м∙оС). Важнейшим фактором является удельное содержание воды в ткани α w , определяющее теплофизические характеристики из-за сильной зависимости плотности ткани, теплоемкости и температуропроводности от α w . Наличие злокачественной опухоли в наибольшей степени изменяет распределения удельного тепловыделения Q met ≈ 250–70 000 Вт/м3 и параметров кровотока.
Сложная геометрия и многокомпонентность при использовании методов конечноразностных аппроксимаций дифференциальных уравнений в частных производных требует применения специальных неструктурированных численных сеток [16] и задания граничных условий (3) на сложной поверхности (рис. 2). Использование тетраэдров в качестве элементов сетки является удобным и для моделирования распространения излучения в биоткани [7]. Часто ограничиваются приближением многослойной среды [2].
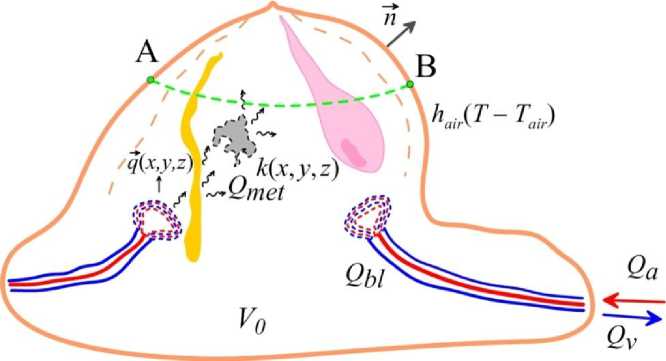
Рис. 1. Неоднородность биоткани и тепловые процессы в ней
Измеряемая яркостная температура T br определяется пространственными распределениями температуры ткани T , коэффициента удельной электрической проводимости о и вектора электрического поля E , создаваемого антенной:
Т ьг = Тд/[(1 - R(f))(JVo C(r,f)T(r)dV + T emi ) + R(nTREC]df, (4) где интегрирование ведется по полосе частот A f и объему биоткани V0 ( Г = { x , y , z } - радиус-вектор), температуры T EMI , T REC характеризуют свойства антенны, а весовая функция C определяется электромагнитным полем и электрофизическими свойствами биоткани [2; 13; 17].
C(x,y,z,f) =
g(f,f)|E(f,f)|2
J yo CT(7V)|E(r,f)|2 dv ’
Мощность электромагнитного излучения на выходе антенны равна P a = kBTbr (1- R ) A f, ( kB -постоянная Больцмана, A f - полоса частоты излучения, R - коэффициент отражения антенны).
Использование в расчетах постоянных электрофизических параметров [2] может давать большую погрешность. Выделяются различные области частот излучения с различной дисперсией ε ( f ), зависящие от преобладания тех или иных физических механизмов (релаксация зарядов на микрососудах, релаксация макромолекул, релаксация молекул воды), причем диэлектрическая проницаемость ε является комплексной величиной [17]. Проводимости крови, лимфы, межклеточной и внутриклеточной жидкостей различаются больше, чем на порядок.
На рисунке 3 приведены модельные одномерные профили основных физических параметров биоткани, определяющих модель (1), (2). Зависимости являются типичными вдоль линии AB на рисунке 1 и учитывают компоненты кожи (эпидерма, дерма, гипердерма), соединительные, жировые ткани, дольки молочной железы, кровотоки, млечный синус. Оценки показывают, что дополнительные неоднородности распределения температуры, обусловленные многокомпонентно-стью биологической ткани, могут заметно влиять на вычисление яркостной температуры T br по формуле (4). В реальных трехмерных условиях картина существенно усложняется.
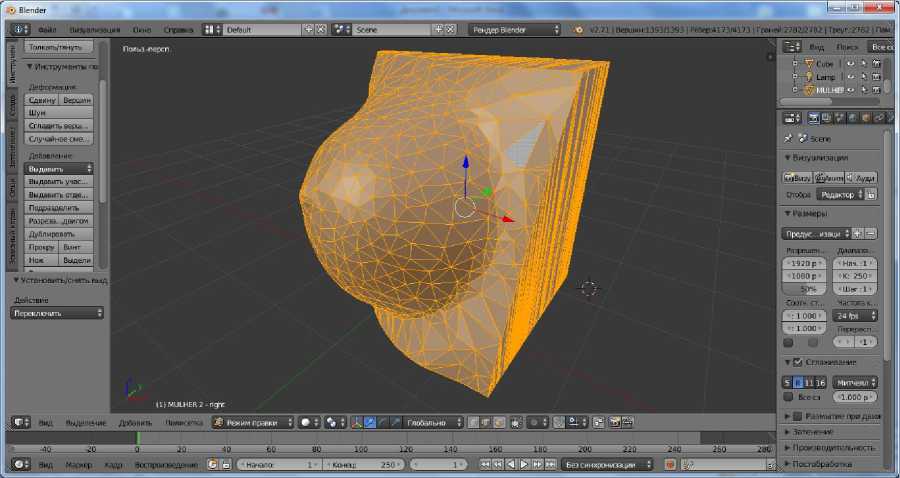
Риc. 2. 3D-модель правой груди
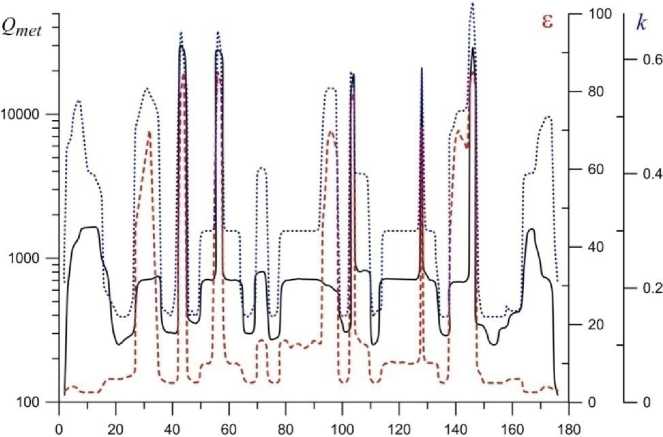
Риc. 3. Модельное распределение физических параметров вдоль линии AB на рис. 1: сплошная черная линия – удельное тепловыделение Q met [Вт/м3]; красная штриховая линия – диэлектрическая проницаемость; синяя пунктирная линия – коэффициент теплопроводности [Вт/(м∙оС)]
Список литературы Влияние особенностей мелкомасштабной структуры молочной железы на распределение глубинной температуры при использовании радиотермометрической диагностики
- Авраменко, Г. В. Использование радиотермометрии в скрининге непальпируемых новообразований молочных желез/Г. В. Авраменко//Вестник рентгенологии и радиологии. -2007. -№ 5. -C. 11-14.
- Веснин, С. Г. Разработка серии антенн-аппликаторов для неинвазивного измерения температуры тканей организма человека при различных патологиях/С. Г. Веснин, М. К. Седанкин//Инженерный журнал: наука и инновации. -2012. -№ 11. -C. 43-61.
- Веснин, С. Г. Современная микроволновая радиотермометрия молочных желез/С. Г. Веснин, А. М. Каплан, Р. С. Авакян//Медицинский альманах.-2008. -№ 3. -C. 82-87.
- Гинзбург, А. С. Теплофизические характеристики пищевых продуктов/А. С. Гинзбург, М. А. Громов, Г. И. Красовская. -М.: Агропромиздат, 1990. -С. 287.
- Маречек, С. В. Радиометрические методы исследования температурного режима приповерхностного слоя биоткани/С. В. Марчек, В. М. Поляков, Ю. Г. Тищенко//Биомедицинские технологии и радиоэлектроника. -2003. -№ 8. -C. 57-64.
- Мустафин, Ч. Н. Опыт использования радиотермометрии в диагностике злокачественных опухолей молочной железы/Ч. Н. Мустафин//Российский онкологический журнал. -2009. -№ 4. -C. 36-42.
- Сетейкин, А. Ю. Трехмерная модель распространения света в биологических тканях/А. Ю. Сетейкин, И. В. Красников, М. С. Павлов//Вестник Санкт-Петербургского университета. Серия 11, Медицина. -2010. -№ 3. -С. 166-172.
- Ставров, Т. А. Математическая модель верификации ранних рецидивов варикозной болезни по данным радиотермометрии/Т. А. Ставров, Е. В. Букина, А. Г. Лосев, Т. В. Замечник//Вестник новых медицинских технологий. -2013. -Т. 20, № 2. -С. 14-18.
- Убайчин, А. В. Печатная антенна для измерения глубинной температуры биологических объектов аппликационным радиометрическим СВЧ-методом/А. В. Убайчин//Доклады Томского государственного университета систем управления и радиоэлектроники. -2013. -№ 3 (29). -С. 47-52.
- Barrett, A. H. Subcutaneous Temperature: A method of Non-invasive Sensing/A. H. Barrett, Ph. C. Myers//Science. -1975. -Vol. 190. -P. 669-671.
- Filatov, A. V. A two-receiver microwave radiometer with high transfer characteristic linearity/A. V. Filatov, A. V. Ubaichin, A. A. Bombizov//Measurement Techniques. -2013. -Vol. 55, № 11. -P. 1281-1286.
- Gautherie, M. Temperature and Blood Flow Patterns in Breast Cancer During Natural Evolution and Following Radiotherapy/M. Gautherie//Biomedical Thermology. -1982. -Vol. 107. -P. 21-64.
- Gonzalez, F. J. Thermal simulation of breast tumors/F. J. Gonzalez//Revista mexicana de fisica. -2007. -Vol. 53, № 4. -P. 323-326.
- Kelly, P. Microwave radiometric signatures of temperature anomalies in tissue/P. Kelly, T. Sobers, B. S. Peter, P. Siqueira, G. Capraro//Proc. SPIE 8313, Medical Imaging 2012: Physics of Medical Imaging. -2012. -Mode of access: Article ID 831368, DOI: DOI: 10.1117/12.910785
- Kelly, P. Temperature anomaly detection and estimation using microwave radiometry and anatomical information/P. Kelly, T. Sobers, B. S. Peter, P. Siqueira, G. Capraro//Proc. SPIE 7961, Medical Imaging 2011: Physics of Medical Imaging. -2011. -Mode of access: Article ID 79614U. -DOI: DOI: 10.1117/12.878136
- Ng, E.Y-K. Computer simulation in conjunction with medical thermography as an adjunct tool for early detection of breast cancer/E. Y-K. Ng, N. M. Sudharsan//BMC Cancer. -2004. -Vol. 4, № 17. -6 p. DOI: DOI: 10.1186/1471-2407-4-17
- Rodrigues, D. B. Numerical 3D modeling of heat transfer in human tissues for microwave radiometry monitoring of brown fat metabolism/D. B. Rodrigues //Proc. SPIE. -2013. -20 p. Mode of access: Article ID 8584. -DOI: DOI: 10.1117/12.2004931
- Stauffer, P. R. Utility of Microwave Radiometry for Diagnostic and Therapeutic Applications of Non-Invasive Temperature Monitoring/P. R. Stauffer, D. B. Rodrigues, P. F. Maccarini//IEEE BenMAS (Benjamin Franklin Symposium on Microwave and Antenna Sub-systems).-2014. -DOI: DOI: 10.13140/2.1.3762.0487
- Umadevi, V.Framework for estimating tumour parameters using thermal imaging/V. Umadevi, S. V. Raghavan, S. Jaipurkar//The Indian Journal of Medical Research. -2011. -Vol. 134, № 5. -P. 725-731. -DOI: DOI: 10.4103/0971-5916.91012
- Valvano, J. W. Tissue Thermal Properties and Perfusion/J. W. Valvano//Optical-Thermal Response of Laser-Irradiated Tissue/еd. by A. J. Welch and van M. J. C. Gemert. -1995. -P. 445-488. -DOI: DOI: 10.1007/978-90-481-8831-4_12
- Wust, P. Thermal monitoring: invasive, minimal-invasive and non-invasive approaches/P. Wust, C. H. Cho, B. Hildebrandt, J. Gellermann//International Journal of Hyperthermia. -2006. -Vol. 22, № 3. -P. 255-262. DOI: DOI: 10.1080/02656730600661149


