Влияние простатических пептидов на трансмембранный перенос ломефлоксацина
Автор: Духанин Александр Сергеевич
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Экспериментальная урология
Статья в выпуске: 3 т.15, 2022 года.
Бесплатный доступ
Введение. Применение пептидов, проникающих в клетку без участия мембранных белков и способных осуществлять внутриклеточный транспорт связанных с ними низкомолекулярных веществ, открывает новый этап в разработке целенаправленной доставки лекарственных веществ к терапевтическим мишеням. Цель. Оценка влияния простатических пептидов препарата Витапрост® (экстракт предстательной железы) на трансмембранный транспорт антимикробного препарата ломефлоксацин. Материалы и методы. В первой серии изучены эффекты простатических пептидов на способность ломефлоксацина проходить через искусственные мембраны путем пассивной диффузии (метод PAMPA -parallel artificial membrane permeability assay). Во второй серии изучены эффекты простатических пептидов на клеточную проницаемость ломефлоксацина в модели Сасо-2. Результаты. Сравнительное исследование эффективной проницаемости мембраны (logPe) для ломефлоксацина в отсутствии (контрольная группа) и присутствии простатических пептидов (экстракт предстательной железы в концентрации 10 мг/мл) показало, что сочетанное применение ломефлоксацина и простатических пептидов приводит к достоверному повышению величины logPe, прирост составляет в среднем 29%. Специфический характер выявленного взаимодействия был подтвержден: добавление бета-меркаптоэтанола (BME) в донорный отсек не влияло на проницаемость чистого ломефлоксацина, но подавляло карго-эффект простатических пептидов. Рассчитанный на модели Caco-2 коэффициент проницаемости (Papp) для ломефлоксацина в комплексе с пептидами составил 13,04±1,80х10-6 см/с, в то время как для ломефлоксацина - 10,31±0,76х10-6 см/с. Заключение. Сопоставление полученных данных двух серий экспериментов свидетельствует о наличии прямого карго-эффекта простатических пептидов на трансмембранный транспорт ломефлоксацина в условиях in vitro.
Ломефлоксацин, простатические пептиды, эффективная проницаемость мембраны, caco-2, карго-эффект
Короткий адрес: https://sciup.org/142236638
IDR: 142236638 | DOI: 10.29188/2222-8543-2022-15-3-28-34
Effect of prostatic peptides on the lomefloxacin transmembrane influx
Introduction. The use of peptides that penetrate the cell without the participation of membrane proteins and are capable of intracellular transport of low molecular weight substances associated with them opens up a new stage in the development of targeted drug delivery to therapeutic targets. Aim. Evaluation of the effect of prostatic peptides of Vitaprost® (prostate extract) on the transmembrane transport of the antimicrobial drug lomefloxacin. Material and methods. In the first series, the effects of prostatic peptides on the ability of lomefloxacin to pass through artificial membranes by passive diffusion (PAMPA method - parallel artificial membrane permeability assay) were studied. In the second series, the effects of prostatic peptides on the cell permeability of lomefloxacin were studied in the Caco-2 model. Results. Comparative study of effective membrane permeability (logPe). for lomefloxacin in the absence (control group) and presence of prostatic peptides (a mixture of prostate extract at a concentration of 10 mg/ml) showed that the combined use of lomefloxacin and prostatic peptides leads to a significant increase in the logPe value, an increase of 29% on average. The specific nature of the identified interaction was confirmed: the addition of beta-mercaptoethanol (BME) to the donor compartment did not affect the permeability of pure lomefloxacin, but suppressed the cargo effect of prostatic peptides. The permeability coefficient (Papp) calculated on the Caco-2 model for lomefloxacin in combination with peptides was 13.04±1.80x10-6 cm/s, while for lomefloxacin it was 10.31±0.76x10-6 cm/s. Conclusion. Comparison of the obtained data of two series of experiments indicates the presence of a direct cargo effect of prostatic peptides on the transmembrane transport of lomefloxacin in vitro.
Текст научной статьи Влияние простатических пептидов на трансмембранный перенос ломефлоксацина
Цитоплазматическая мембрана – важный барьер на пути эффективной доставки в клетку большинства лекарственных соединений, существенно ослабляющий их лечебный потенциал. Разработка новых перспективных инструментов доставки лекарственных препаратов до терапевтических мишеней является актуальной задачей для профилактики и лечения различных урологических заболеваний. Одним из таких перспективных подходов служит применение проникающих в клетку пептидов (cell-penetrating peptide, СРР), которые обладают карго-эффектом – свойством усиливать трансмембранную проницаемость карго-молекулы (терапевтического или диагностического средства) [1-3]. Целенаправленная транспортировка фармакологически активных веществ на основе СРР характеризуется рядом преимуществ по сравнению с другими способами доставки действующего начала лекарственных препаратов: отсутствие у пептидов (молекулярной массой <10кДа) иммуногенных свойств, низкая цитотоксичность, высокая химическая и физическая стабильность в физиологических условиях [4]. Так, применение CPP для доставки противоопухолевых средств (таксол, метотрексат, доксорубицин) способствует увеличению внутриклеточной концентрации химиотерапевтических агентов за счет повышения проницаемости мембран опухолевых клеток, позволяет повысить конечный период их полувыведения и биодоступность [5]. Низкомолекулярный пептид R8, иммобилизованный с молекулой таксола с помощью ковалентных дисульфидных связей, изменял фармакокинетику и фармакодинамику антинеоплатического препарата, увеличивая растворимость в водной среде, позволяя преодолевать множественную лекарственную резистентность [6]. Механизмы трансмембранного переноса, опосредованные СРР, не требуют затрат энергии, происходят без участия белков-адаптеров клатрин-зави-симого эндоцитоза, практически не зависят от экспрессии углеводной части гликолипидов и гликопротеинов наружной плазмолеммы [7]. Такие CPP, как ТАТ и VP22, обладают способностью транслоцироваться через сеть мембран внутриклеточных компартментов, накапливаясь в ядре клетки [8]. С химической точки зрения класс CPP является гетерогенным, объединяя различные по своей природе пептидные последовательности и/или структуры. В то же время общим для всех СРР представляется достаточно высокое содержание основных (положительно заряженных) аминокислот, которое определяет в целом положительный суммарный заряд пептидной молекулы (катионные свойства) [9]. Экспериментальные данные свидетельствуют, что начальные этапы CPP-опосредованного переноса включают связывание пептидов с отрицательно заряженными радикалами липидов и/или протеогликанов клеточной мембраны [9].
Таким образом, поиск новых способов, обеспечивающих доставку лекарственных препаратов в эффекторные клетки, является актуальной задачей биомедицинских исследований. К числу таких перспективных соединений относятся простатические пептиды, которые могут транслоцироваться через мембраны клеток и могут служить переносчиками антимикробных препаратов, повышая эффективность медикаментозной терапии. Субстанция препарата Витапрост® – комплекс биологически активных пептидов предстательной железы крупного рогатого скота – относится к фармакологически активным веществам, улучшающим метаболизм в предстательной железе, и к корректорам уродинамики [10]. Простатические пептиды имеют основной характер, относятся к катионным пептидам, что позволило нам предположить наличие у них карго-свойств.
Цель данной работы – определение влияния простатических пептидов (экстракт предстательной же-лезы)на трансмембранный транспорт антимикробного препарата ломефлоксацин.
МАТЕРИАЛЫ И МЕТОДЫ
Препараты и реактивы
Ломефлоксацина гидрохлорид содержит не менее 89,2% ломефлоксацина в пересчете на сухое вещество (по результатам испытаний – 89,7%). Действующее начало препарата Витапрост® (предстательной железы экстракт): спектр поглощения испытуемого раствора в ультрафиолетовой области (260-350 нм) имеет максимум при длине волны 275±5 нм. Результаты количественного определения (водорастворимые пептиды): 24,7%, рН 5,9. Размер частиц (≤40 мкм) – 99,4. Линия клеток Сасо-2 (АТСС, кат. № НТВ-37, США).
Дизайн исследования включал проведение двух серий экспериментов. В первой из них изучали эффекты простатических пептидов на способность ломе-флоксацина проходить через искусственные мембраны путем пассивной диффузии (PAMPA-parallel artificial membrane permeability assay) [11]. Для этого был использован 96-луночный планшет, конструкция которого состояла из верхней (акцепторной) и нижней (донорной) частей, разделенных с помощью искусственной мембраны на основе изопропилмиристата (30%) и силиконового масла (70%). Время инкубации варьировало от 3 до 24 часов при комнатной температуре, что необходимо для перераспределения исследуемых соединений между двумя отсеками и мембраной. В предварительной серии экспериментов в качестве контрольных образцов использовали верапамил (высокая проницаемость) и ранитидин (низкая проницаемость) – при определении оптимальных условий проведения РАМРА. В первой серии экспериментов для контрольных образцов использовали кетопрофен и феназон, данные по которым отражены в результатах исследования. Комплекс фосфолипидов различного состава наносили на пористую мембрану акцепторного отсека, лунки которого заполняли растворами исследуемых соединений в смеси ДМСО/фосфат-ный буфер. Для заполнения лунок нижнего (донорного) отсека использовали фосфатный буфер. Собранный планшет помещали в термостат при непрерывном перемешивании. Спустя 1-24 ч. по оптической плотности растворов в УФ-диапазоне определяли концентрацию ломефлоксацина в акцепторном отсеке для последующего расчета значений logPe.
Во второй серии были изучены эффекты простатических пептидов на клеточную проницаемость ло-мефлоксацина в модели Сасо-2. На основе рекомендаций для использования коммерческих наборов MultiScreen® Caco-2 Assay System проводили анализ на клетках линии Caco-2, которые культивировали стандартным способом в среде Дульбекко, модифицированной по способу Исков (IMDM) с добавлением 10% термически инактивированной бычьей сыворотки (FBS) при 37 °C в среде 5% CO 2 (об/об) [12].
Целостность клеточного монослоя оценивали по трансэпителиальному электрическому сопротивлению с использованием Millicell ERS-2 в начале и в конце эксперимента. Исследуемые растворы добавляли в верхнюю часть лунки, нижнюю часть лунки заполняли раствором Хэнкса (HBSS). После этого планшеты инкубировали при 37°C и перемешивании (80 об/мин) на орбитальном шейкере. Пробы по 150 мкл отбирали из нижней части лунки через 15, 30, 45, 60, 90 и 120 мин. После отбора пробы, необходимый объем сразу возмещали свежим раствором HBSS. Концентрацию веществ определяли с помощью высокоэффективной жидкостной хроматографии на Agilent 1200 HPLC с УФ-детектором. Хроматографический анализ был проведен на обращенной фазовой колонке (5 μm, 4.6×50 mm, Zorbax Eclipse SB-C18).
Оцениваемые параметры
Содержание ломефлоксацина гидрохлорида в испытуемых растворах определяли спектрофотометрически при длине волны 286 нм (максимум поглощения) в кювете с толщиной слоя 1 см.
Количественное значение logPe, обозначающее эффективную проницаемость мембраны, рассчитывали по формуле:
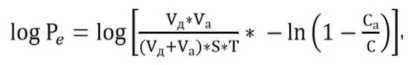
где C – равновесная концентрация вещества в суммарном объеме отсеков, мг/мл; Cа – концентрация вещества в акцепторном отсеке, мг/мл; T – время инкубации, мин.; Vд – объем донорного отсека, см3, S – площадь поверхность мембраны, см2; Vа – объем акцепторного отсека, см3.
Коэффициент клеточной проницаемости рассчитывали согласно формуле [13]:
Papp = Vr*(dC)/(dt)*1/AC0, где Vr – это объем верхней части лунки, dC/dt – это градиент общей концентрации вещества в нижней части лунки в течение времени, А – это площадь мембраны, C0 – это начальная концентрация вещества в верхней части лунки.
Статистическая обработка результатов исследования
Статистическую обработку результатов экспериментов проводили с помощью программ MS Exсel и Sta-tistica 6.0. Полученные экспериментальные данные представляли в виде среднего (mean) и ошибки среднего (standard error of the mean, SEM). Для сравнения количественных данных двух групп применяли двусторонний t-критерий Стьюдента для независимых выборок. Различия считались статистически значимыми при р <0,05.
РЕЗУЛЬТАТЫ
-
I. Изучение влияния простатических пептидов на проницаемость ломефлоксацина с использованием искусственных мембран.
Для определения оптимальной длительности инкубации проведена предварительная серия опытов, в ходе которой оптическую плотность растворов в акцепторных отсеках измеряли спустя 2, 4, 8, 16, 24 и 48 ч. Установлено, что оптимальной продолжительностью инкубации для оценки мембранотропности является интервал в 16 ч.: при уменьшении времени исследуемые активные вещества не успевают в достаточных количествах преодолеть мембрану, при увеличении времени происходит снижение оптической плотности растворов.
В эксперименте PAMPA с использованием фильтр-иммобилизованной искусственной мембраны была оценена способность ломефлоксацина (100 мкг/мл) диффундировать через мембраны при различных значениях рН (диапазон рН от 4 до 10). В качестве препаратов-эталонов были использованы два лекарственных соединения: 1) кетопрофен, как фармакологически активное вещество,хорошо проникающее через
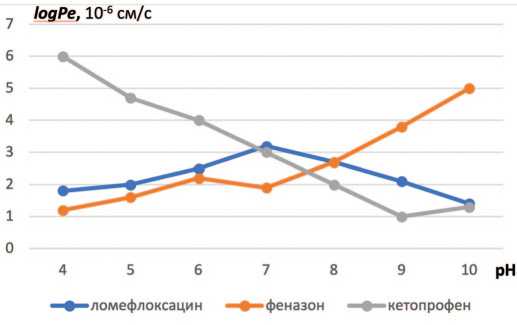
Рис. 1. Влияние рН на эффективную проницаемость мембраны. Ломефлоксацин – 100 мкг/мл, феназон – 50 мкг/мл, кетопрофен – 20 мкг/мл
Fig. 1. Effect of pH on effective membrane permeability. Lomefloxacin – 100 mcg / ml, phenazone – 50 mcg / ml, ketoprofen – 20 mcg / ml биологические мембраны при рН ниже 7,0 (слабая кислота), а также феназон, как лекарственное вещество с низкой проникающей способностью при рН ниже 7 (слабое основание). Результаты исследования приведены на рисунке 1. Видно, что увеличение рН с 4 до 7 существенно снижает проницаемость для кетопрофена, максимальная величина logPe регистрируется при низком уровне рН. Напротив, эффективная проницаемость мембраны для феназона растет с повышением рН, достигая максимальных значений при рН=10. рН-зависимость трансмембранной диффузии ломефлоксацина имеет характерные особенности (рис. 1). При крайних значениях рН величина logPe низкая,высокая проницаемость достигается в интервале рН, равном 6-8. Молекула ломефлоксацина относится к цвиттер-ионам, что, по нашему мнению, лежит в основе установленной нами зависимости проницаемости ломефлоксацина от рН [14].
Изучение влияния липидного состава на трансмембранный перенос включало исследование зависимости проницаемости лекарственных веществ от липидного состава, наносимого на ПВДФ-подложку При выборе экспериментального состава мы исходили из того,что компонентами клеточных мембран чаще всего служат фосфатидилхолин (ФХ) и фосфа-тидилэтаноламин (ФЭ). Особенностью состава липидных экстрактов гистогематических барьеров, в частности ГЭБ,является высокое содержание фосфа-тидилсерина (ФС) [15]. Отталкиваясь от рекомендаций по проведению РАМРА, диапазон концентраций липидного комплекса составлял от 1 до 20 мг/мл. В результате были выбраны и изучены три варианта липидной композиции: 1) 10 мг/мл фосфатидилхолина, 2) 2,52 мг/мл фосфатидилхолина + 6,62 мг/мл фосфа-тидилэтаноламина, 3) 2,52 мг/мл фосфатидилхолина + 6,62 мг/мл фосфатидилэтаноламина + 3,7 мг/мл фос-фатидилсерина. Полученные экспериментальные данные суммированы на рисунке 2.
6 logPe, 106 см/с
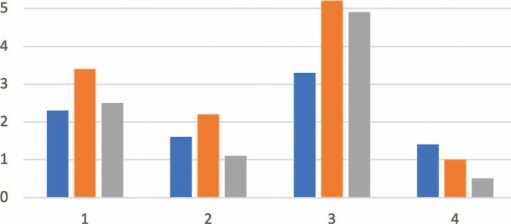
I Состав 1 Состав 2 g Состав 3
Рис. 2. Влияние фосфолипидного состава на эффективную проницаемость мембраны. Обозначения: 1 – ломефлоксацин, 2 – амоксициллин, 3– метронидазол, 4 – нистатин. Концентрация исследуемых соединений составляла 100 мкг/мл Fig. 2. Effect of the phospholipid composition on the effective membrane permeability. Designations: 1 – lomefloxacin, 2 – amoxicillin, 3 – metronidazole, 4 – nystatin. The concentration of the studied compounds was 100 μg/ml
Проведенные исследования позволили нам подобрать оптимальные условия для детекции и количественного определения трансмембранного переноса ломефлоксацина и приступить к главной задаче первой серии экспериментов, а именно, изучению возможности карго-эффекта простатических пептидов в бесклеточной модели. Применимость РАМРА при изучении проницаемости фторхинолонов подтверждена литературными данными [16]. На рисунке 3 представлены значения эффективной проницаемости мембраны для ломефлоксацина в отсутствии (контрольная группа) и присутствии простатических пептидов (экстракт предстательной железы в концентрации 10 мг/мл). Сочетанное применение ломефлоксацина и простатических пептидов приводит к достоверному повышению величины logPe, прирост составляет в среднем 29%.
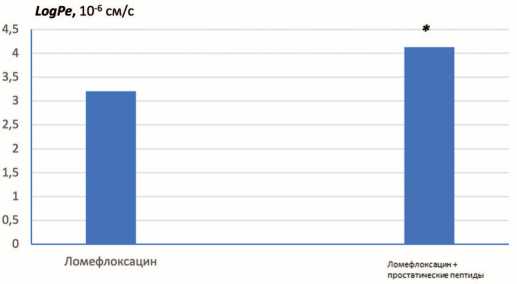
Рис. 3. Влияние простатических пептидов на эффективную проницаемость мембраны для ломефлоксацина (logPe). Условия: рН=7,2; липидный состав включает 2,52 мг/мл фосфатидилхолина + 6,62 мг/мл фосфатидилэтаноламина. *досто-верные отличия при p ≤0,05
Fig. 3. Effect of prostatic peptides on the effective membrane permeability for lomefloxacin (logPe). Conditions: pH=7.2; the lipid composition includes 2.52 mg/ml phosphatidylcholine + 6.62 mg/ml phosphatidylethanolamine. *significant differences at p ≤0.05
С целью доказать специфичность выявленного карго-эффекта был использован метод частичной денатурации пептидов – восстановления дисульфидных связей – с помощью бета-меркаптоэтанола (рис. 4 ). Добавление бета-меркаптоэтанола (BME) (конечная концентрация 200 мкМ) в донорный отсек не влияло на проницаемость чистого ломефлоксацина,но подав- ляло карго-эффект простатических пептидов.
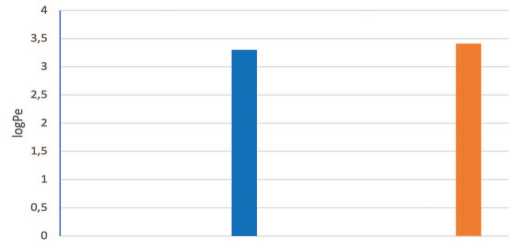
■ Ломефлоксацин + ВМЕ ■ Ломефлоксацин + простатические пептиды + ВМЕ
Рис. 4. Влияние бета-меркаптоэтанола (200 мкМ) на проницаемость ломеф-локсацина в отсутствии и в присутствии простатических пептидов. Условия как на рис. 3
Fig. 4. Effect of beta-mercaptoethanol (200 μM) on the permeability of lomefloxacin in the absence and presence of prostatic peptides. Conditions as in Fig. 3
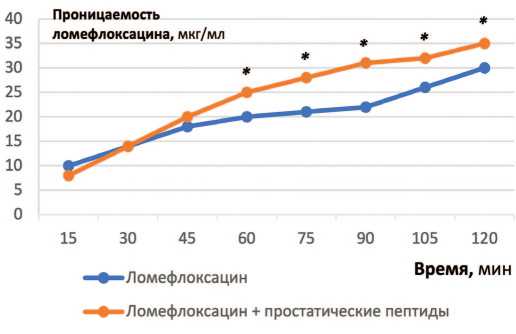
Рис. 5. Проницаемость ломефлоксацина через монослой клеток Сасо-2. * p ≤0,05 по сравнению с ломефлоксацин+пептиды в аналогичной точке. Ломефлоксацин – 20 мкг/мл, простатические пептиды – 10 мг/мл
Fig. 5. Permeability of lomefloxacin through a monolayer of Caco-2 cells. * p ≤0.05 compared to lomefloxacin+peptides at similar point. Lomefloxacin – 20 mcg / ml, prostatic peptides – 10 mg / ml
-
II. Определение клеточной проницаемости ломефлоксацина в модели Сасо-2.
Для выяснения молекулярного механизма повышения биодоступности ломефлоксацина в присутствии простатических пептидов были проведены эксперименты in vitro на клеточной линии Caco-2 (клетки эпителиальной колоректальной аденокарциномы человека) [17, 18]. При изучении сочетанного применения простатических пептидов + ломефлокса-цин было обнаружено значительное увеличение ( p ≤0,05) абсорбции ломефлоксацина по сравнению с чистым препаратом (рис. 5).
Рассчитанный нами коэффициент проницаемости (Papp) для ломефлоксацина в комплексе с пептидами составил 13,04±1,80×10-6 см/сек, в то время, как для ломефлоксацина – 10,31±0,76×10-6 см/сек. Важно отметить,что показатель трансэпителиального электрического сопротивления, который отражает ток ионов через плотные межклеточные контакты,досто-верно не изменялся в исследованном временном диапазоне, что служит подтверждением конфлюэнтности монослоя клеток [19].
ОБСУЖДЕНИЕ
Изучена возможность карго-эффекта активного начала препарата Витапрост® – олигопептидов,выде-ленных из предстательной железы крупного рогатого скота, которые состоят из нескольких аминокислот (от 2 до 100), с низкой молекулярной массой (от 175 до 5000 Да) и высокой специфической активностью.
Подобраны оптимальные условия для детекции и количественного определения трансмембранного переноса и внутриклеточного транспорта ломефлок-сацина; оценена возможность применения культуры клеток для исследования карго-эффекта в терапевтическом диапазоне концентраций активных компонентов препарата Витапрост®;установлены закономер- ности трансмембранного переноса и внутриклеточного транспорта ломефлоксацина в отсутствии (контрольная группа) и присутствии простатических пептидов (экстракт предстательной железы).
На первом этапе исследования был использован метод PAMPA, основанный на применении искусственно сконструированных клеточных мембран [20]. Искусственная мембрана состоит из липидной мембраны, поддерживаемой пористой гидрофобной фильтрующей пластиной. В начале эксперимента тестируемое соединение разводят в буфере и помещают в донорскую ячейку. Скорость проникновения определяют по эффективной проницаемости соединения (Ре). Значения Pe измеряются и рассчитываются с использованием планшетного ридера с интегрированной УФ спектрометрией, что существенно сокращает затраты по сравнению с клеточными моделями [21]. Недавние исследования доказали возможность применения PAMPA для изучения механизмов карго-эффекта [22].
Изучение временной зависимости переноса ло-мефлоксацина с помощью РАМРА показало, что оптимальным интервалом для оценки мембранотроп-ности является интервал в 16 ч. Полученные нами экспериментальные результаты согласуются с литературными данными. H . Yu и соавт., изучая временную зависимость проницаемости различных лекарственных веществ в модели PAMPA, установили, что для представителя фторхинолонов норфлоксацина оптимальным временем является диапазон 14-18 ч. [23]. Чем длиннее гидрофобная цепь, тем лучше проницаемость для лекарственного соединения,при этом для большинства изученных веществ наиболее благоприятной для условий эксперимента была 16-часовая длительность инкубации [24].
Полученные нами данные показали, что роль липидной композиции в эффективной трансмембранной доставке модифицируется в зависимости от химической природы исследуемых соединений. Экспериментальный состав мембраны оказывает сходное влияние на проницаемость ломефлоксацина,метронидазола и амоксициллина.Отличия между ними касается степени проницаемости: проницаемость метронидазола предсказуемо оказалась выше. Наибольшую чувствительность к составу мембраны продемонстрировал амоксициллин,для которого присуща индивидуальная структурная особенность в виде нескольких гидроксильных групп, способных образовывать водородные связи или участвовать в таутомерных равно-весиях.Сочетанное применение ломефлоксацина и простатических пептидов приводило к достоверному повышению величины logPe, прирост составляет в среднем 29%. На специфический характер выявленного карго-эффекта указывает его нивелирование в присутствии бета-меркаптоэтанола, который вызы- вает частичную денатурацию пептидов,не влияя на эффективную проницаемость самого ломефлоксацина.
Адекватной моделью in vitro для оценки проницаемости лекарственного вещества через стенку желудочно-кишечного тракта ЖКТ in vivo заслуженно является клеточная линия Caco-2. Особенностью данных клеток считается способность сохранять практически полные морфо-функциональные свойства, присущие клеткам кишечного эпителия,в том числе экспозиция в клеточных мембранах белков множественной лекарственной устойчивости (таких, как Р-гликопротеин). Как правило, полученные в таких экспериментах данные имеют хорошую корреляцию с биодоступностью лекарственных средств в живых организмах [25]. Оценка влияния простатических пептидов на активность трансмембранного переноса ломефлок-сацина в модели Caco-2 позволила установить достоверное увеличение коэффициента проницаемости (Papp) для ломефлоксацина в комплексе с пептидами по сравнению с пробами, содержащими только ломеф-локсацин. Рассматриваемый феномен может быть следствием как прямого карго-эффекта пептидов, так и опосредован блокированием/снижением активности P-гликопротеина молекулами простатических пептидов. С учетом результатов первой бесклеточной серии экспериментов, следует отдать предпочтение в пользу прямого карго-эффекта простатических пептидов.
ЗАКЛЮЧЕНИЕ
Изучено влияние простатических пептидов препарата Витапрост® на трансмембранный транспорт ломефлоксацина в двух сериях экспериментов: на бесклеточной РАМРА-модели и в культуре клеток Caco-2.
Оценка трансмембранного переноса ломефлокса-цина с помощью РАМРА выявила, что сочетанное применение ломефлоксацина и простатических пептидов приводит к достоверному повышению эффективной проницаемости (Pe), прирост составляет в среднем 29%. Определение клеточной проницаемости ломефлоксацина в модели Сасо-2 показало, что клеточная абсорбция ломефлоксацина в комбинации с простатическими пептидами значительно выше ( p ≤0,05) по сравнению с монопрепаратом ломефлокса-цином. Наблюдаемый эффект может быть следствием как прямого карго-эффекта пептидов, так и опосредованным влиянием – результатом блокирования/сниже-ния активности P-гликопротеина молекулами простатических пептидов.Сопоставляя полученные данные двух серий экспериментов,следует отдать предпочтение прямому карго-эффекту простатических пептидов препарата Витапрост® на трансмембранный транспорт ломефлоксацина.
Список литературы Влияние простатических пептидов на трансмембранный перенос ломефлоксацина
- Liu J, Afshar S. In vitro assays: friends or foes of cell-penetrating peptides. Int J Mol Sci 2020;21(13):4719. https://doi.org/10.3390/ijms21134719.
- Young Kim H, Young Yum S, Jang G, Ahn DR. Discovery of a non-cationic cell penetrating peptide derived from membrane-interacting human proteins and its potential as a protein delivery carrier. Sci Rep 2015(5):11719. https://doi.org/10.1038/srep11719.
- Vasconcelos L, Pärn K, Langel U. Therapeutic potential of cell-penetrating peptides. Ther Deliv 2013;4(5):573-91. https://doi.org/10.4155/ tde.13.22.
- Sawant R, Torchilin V. Intracellular transduction using cell-penetrating peptides. Mol Biosyst 2010;6(4):628-40. https://doi.org/10.1039/b916297f.
- Borrelli A, Tornesello AL, Tornesello ML, Buonaguro FM. Cell penetrating peptides as molecular carriers for anti-cancer agents. Molecules 2018;23(2):295. https://doi.org/10.3390/molecules23020295.
- Dubikovskaya EA, Thorne SH, Pillow TH, Contag CH, Wender PA. Overcoming multidrug resistance of small-molecule therapeutics through conjugation with releasable octaarginine transporters. Proc Natl Acad Sci U S A 2008;105(34):12128-33. https://doi.org/10.1073/pnas.0805374105.
- Madani F, Lindberg S, Langel U, Futaki S, Gräslund A. Mechanisms of cellular uptake of cell-penetrating peptides. J Biophys 2011;2011:414729. https://doi.org/10.1155/2011/414729.
- Richard JP, Melikov K, Vives E, Ramos C, Verbeure B, Gait MJ, Cher-nomordik LV, Lebleu B. Cell-penetrating peptides. A reevaluation of the mechanism of cellular uptake. J Biol Chem 2003;278(1):585-90. https://doi.org/10.1074/jbc.M209548200.
- Patel LN, Wang J, Kim KJ, Borok Z, Crandall ED, Shen WC. Conjugation with cationic cell-penetrating peptide increases pulmonary absorption of insulin. Mol Pharm 2009;6(2):492-503. https://doi.org/10.1021/ mp800174g.
- Khavinson V, Linkova N, Diatlova A, Trofimova S. Peptide Regulation of Cell Differentiation. Stem Cell Rev Rep 2020;16(1):118-125. https://doi.org/10.1007/s12015-019-09938-8.
- Reis JM, Sinko B, Serra CH. Parallel artificial membrane permeability assay (PAMPA) - Is it better than Caco-2 for human passive permeability prediction? Mini Rev Med Chem 2010;10(11):1071-6. https://doi.org/10.2174/1389557511009011071.
- Phillips, A. Arena. Optimization of Caco-2 cell growth and differentiation for drug transport studies. Millipore Corporation Protocol Note PC1060EN00 2003.
- van Breemen RB, Li Y. Caco-2 cell permeability assays to measure drug absorption. Expert Opin Drug Metab Toxicol 2005;1(2):175-85. https://doi.Org/10.1517/17425255.1.2.175.
- Cramariuc O, Rog T, Javanainen M, Monticelli L, Polishchuk AV, Vattulainen I. Mechanism for translocation of fluoroquinolones across lipid membranes. Biochim Biophys Acta 2012;1818(11):2563-71. https://doi.org/10.1016/j.bbamem.2012.05.027.
- van Meer G, Voelker DR, Feigenson GW. Membrane lipids: where they are and how they behave. Nat Rev Mol Cell Biol 2008;9(2):112-24. https://doi.org/10.1038/nrm2330.
- Bermejo M, Avdeef A, Ruiz A, Nalda R, Ruell JA, Tsinman O, González I, Fernández C, Sánchez G, Garrigues TM, Merino V. PAMPA - a drug absorption in vitro model 7. Comparing rat in situ, Caco-2, and PAMPA permeability of fluoroquinolones. Eur J Pharm Sci 2004;21(4):429-41. https://doi.org/10.1016/j.ejps.2003.10.009.
- Kerns EH, Di L, Petusky S, Farris M, Ley R, Jupp P. Combined application of parallel artificial membrane permeability assay and Caco-2 permeability assays in drug discovery. J Pharm Sci 2004;93(6):1440-53. https://doi.org/10.1002/jps.20075.
- Fujikawa M, Ano R, Nakao K, Shimizu R, Akamatsu M. Relationships between structure and high-throughput screening permeability of diverse drugs with artificial membranes: application to prediction of Caco-2 cell permeability. Bioorg Med Chem 2005;13(15):4721-32. https://doi.org/10.1016/j.bmc.2005.04.076.
- Гребенкин Д.Ю., Станишевский Я.М., Шохин И.Е., Стойнова А.М., Карпова М.А., Корякова А.Г., Рябова А.В., Бровченко Б.В., Смирнов А.А. Исследование кишечной проницаемости и Pgp-транспорта фос-фазида с применением модели Сасо-2. Разработка и регистрация лекарственных средств 2017(4):238-242. [Grebenkin D.Yu., Stanishevskiy Y.M., Shohin I.E., Stoinova A.M., Karpova M.A., Koryakova A.G., Ryabova A.V., Brovchenko B.V., Smirnov A.A. Сасо-2 Intestinal permeability and pgp-affinity of phosphazide. Razrabotka i registratsiya lekarstven-nykh sredstv = Drug development and registration 2017(4):238-242. (In Russian)].
- Di L, Kerns EH, Fan K, McConnell OJ, Carter GT. High throughput artificial membrane permeability assay for blood-brain barrier. Eur J Med Chem 2003;38(3):223-32. https://doi.org/10.1016/s0223-5234(03)00012-6.
- Kansy M, Senner F, Gubernator K. Physicochemical high throughput screening: parallel artificial membrane permeation assay in the description of passive absorption processes. J Med Chem 1998;41(7):1007-10. https://doi.org/10.1021/jm970530e.
- Balimane PV, Pace E, Chong S, Zhu M, Jemal M, Pelt CK. A novel high-throughput automated chip-based nanoelectrospray tandem mass spectrometric method for PAMPA sample analysis. J Pharm Biomed Anal 2005;39(1-2):8-16. https://doi.org/10.1016/j.jpba.2005.03.043.
- Yu H, Wang Q, Sun Y, Shen M, Li H, Duan Y. A new PAMPA model proposed on the basis of a synthetic phospholipid membrane. PLoS One 2015;10(2):e0116502. https://doi.org/10.1371/journal.pone.0116502.
- Kim AV, Shelepova EA, Evseenko VI, Dushkin AV, Medvedev NN, Polyakov NE. Mechanism of the enhancing effect of glycyrrhizin on nifedipine penetration through a lipid membrane. J Mol Liq 2021;344:117759. https://doi.org/10.1016/j.molliq.2021.117759.
- Artursson P, Palm K, Luthman K. Caco-2 monolayers in experimental and theoretical predictions of drug transport. Adv Drug Deliv Rev 2001;46(1-3):27-43. https://doi.org/10.1016/s0169-409x(00)00128-9.


