Воспаление, гипоксия и склероз как основные модуляторы эволюции эндометриоидной кисты яичника
Автор: Украинец P.B., Корнева Ю.С., Абросимов С.Ю.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Патологическая анатомия
Статья в выпуске: 1 т.19, 2023 года.
Бесплатный доступ
Цель: оценить особенности клеточного инфильтрата эндометриоидных кист (ЭК) яичника на различных морфологических стадиях их формирования (эволюции). Материал и методы. Изучены 57 пациенток с гистологически верифицированным диагнозом «ЭК яичника»; морфологически ЭК поделены на «молодые», «зрелые» и «старые». Результаты. В тканях «молодой» ЭК подлежащая фиброзная прослойка (ФП) представлена рыхлой соединительной тканью, с небольшим количеством гранулоцитов, сидерофаги единичные. Увеличение количества гранулоцитов в области ФП по границе ткани ЭК (/-/=17,10; р
Воспаление, нарушение кровообращения, склерозирование, эндометриоидные кисты яичников
Короткий адрес: https://sciup.org/149143250
IDR: 149143250 | УДК: 618.11-006.2:616-002.2 | DOI: 10.15275/ssmj1901083
Inflammation, hypoxia and sclerosis as the major modulators of endometrioid cyst evolution
Objective: to estimate the peculiarities of cellular infiltrate of endometrioid ovarian cysts (EC) at various morphological stages of their formation (during evolution). Material and methods. 57 patients with histologically verified diagnosis of ovarian EC were studied; morphologically, endometrioid cysts were divided into types conventionally designated as "immature", "mature" and "old". Inflammatory cells were counted in the EC wall. Results. In the tissues of the "immature" EC, the underlying fibrous layer is represented by loose connective tissue, with a small number of granulocytes, single siderophages. An increase in the number of granulocytes in the fibrous layer along the border of the EC tissue (/-/=17.10; p
Текст научной статьи Воспаление, гипоксия и склероз как основные модуляторы эволюции эндометриоидной кисты яичника
EDN: ILSBAS
-
1 Введение. Эндометриоз является распространенным гинекологическим заболеванием, поражающим примерно 5-10% женщин репродуктивного возраста и характеризующимся наличием ткани эндометрия вне полости матки. Наиболее часто мишенью данной патологии становятся яичники. Верификация ЭК яичника занимает в среднем 7–8 лет с момента появления симптомов, что может привести к необратимому повреждению функциональных тканей. Помимо того, длительный период течения данной патологии оставляет отпечаток и на морфологии самой ЭК, которая в результате может превратиться в так называемую склерозированную ЭК яичника, что затрудняет морфологическую верификацию по операционному материалу [1]. По мнению ряда исследователей, в патогенезе эндометриоза важная роль отводится воспалению [2]. Однако, согласно некоторым литературным данным, оно влечет за собой и неблагоприятные последствия [3]. Данное исследование направлено на уточнение роли острой воспалительной реакции в патогенезе эндометриоза на примере ЭК яичника путем морфологического и статистического анализа их клеточного микроокружения.
Цель — оценить особенности клеточного инфильтрата эндометриоидных кист яичника на различных морфологических стадиях их формирования (эволюции).
Материал и методы. В исследование включены 57 пациенток с гистологически верифицированным диагнозом «ЭК яичника» (средний возраст — 33,5 года в возрастном интервале от 19 до 47 лет), находившиеся на лечении в гинекологическом отделении ОГБУЗ «Клиническая больница скорой медицинской помощи» г. Смоленска в 2018 г. Гистологическое исследование операционного материала с окраской гематоксилином и эозином проводилось на базе отделения клинической патологии № 2 имени профессора В. Г. Молоткова ОГБУЗ «Смоленский областной институт патологии». Предварительно на основании ряда морфологических признаков все ЭК были поделены на «молодые», «зрелые» и «старые» (рис. 1) [4]. «Молодая» ЭК: поверхностный отдел эндометриоидной выстилки имеет множество сосочкообразных выростов; покровный маточный эпителий высокий с вытянутыми гиперхромными ядрами; внутриэпителиально располагается множество макрофагов и лимфоцитов; строма эндометриоидной выстилки также преимущественно инфильтрирована макрофагами и лимфоцитами с примесью небольшого количества нейтрофилов и единичных эозинофилов; сидерофаги чаще отсутствуют или единичные; в строме эндометриоидной выстилки можно встретить маточные железы; подлежащая ФП, отделяющая эндометриоидную гетеротопию (ЭГ) от теки — стромы яичника представленная рыхлой соединительной тканью с неравномерно выраженными очагами уплотнения. «Зрелая» ЭК: поверхностный отдел эндометриоидной выстилки ровный, не имеет сосочкообразных выростов; покровный маточный эпителий уплощен; внутриэпителиально располагается множество макрофагов, лимфоцитов и нейтрофилов; строма эндометриоидной выстилки имеет полиморфноклеточную инфильтрацию; имеются группы сидеро-фагов; маточные железы отсутствуют; подлежащая ФП, отделяющая ЭГ от теки — стромы яичника, представлена плотной соединительной тканью. «Старая» ЭК: поверхностный отдел эндометриоидной выстилки ровный, не имеет сосочкообразных выростов; покровный маточный эпителий уплощен, в части полей зрения отсутствует; внутриэпители-ально располагается множество макрофагов, лимфоцитов и нейтрофилов; строма эндометриоидной выстилки истончена, имеет полиморфноклеточную инфильтрацию; определяются группы сидерофагов; маточные железы отсутствуют; подлежащая ФП, отделяющая ЭГ от теки — стромы яичника, представлена плотной соединительной тканью.
В стенке ЭК после окраски гематоксилином и эозином на увеличении ×400 подсчитывали количество лимфоцитов, нейтрофилов, эозинофилов, макрофагов и сидерофагов в 10 полях зрения для каждой гистологической области, обозначенные как зона 1 — маточный эпителий; зона 2 — строма эндометриоидной выстилки; зона 3 — подлежащая ФП.
На рис. 2 представлены пояснения к встречающимся по тексту схематичным изображениям структуры корреляций.
Статистическая обработка данных выполнена с использованием программы Statistica 10.0. Корреляционный анализ проведен с использованием критерия ранговой корреляции Спирмена с оценкой результатов по шкале Чеддока. Сравнение количественных показателей в группах проведено с помощью критерия
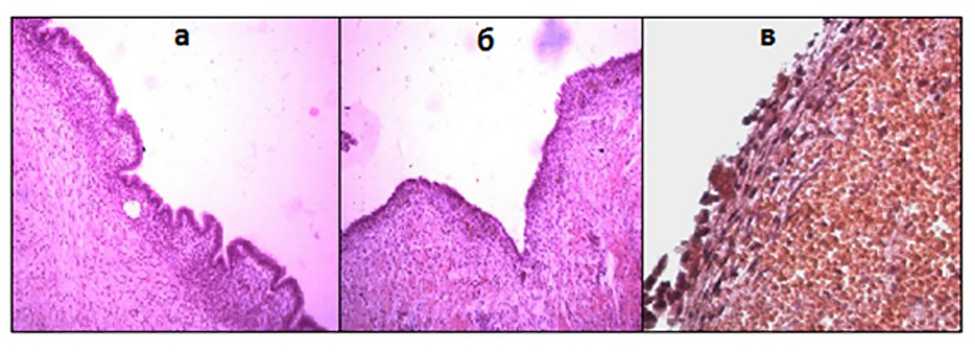
Рис. 1. Типы эндометриоидных кист яичника: а — «молодая» эндометриоидная киста; б — «зрелая» эндометриоидная киста; в — «старая» эндометриоидная киста
Corresponding author — Roman V. Ukrainets
Тел.: +7 (919) 2930849

сила корреляции положительная корреляция отрицательная корреляция
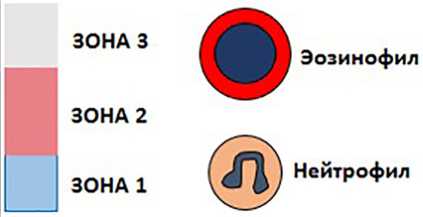

Рис. 2. Условные обозначения для встречающихся далее по тексту схематических изображений структур корреляций в тканях эндометриоидных кист
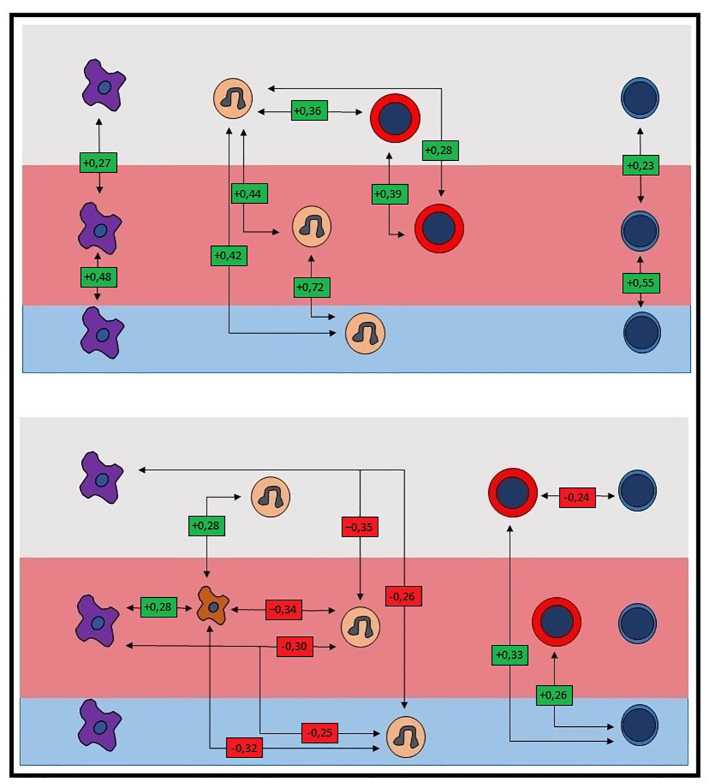
Рис. 3. Корреляции между клеточными популяциями в тканях «молодой» эндометриоидной кисты
Краскела — Уоллиса ( Н ). Результаты считались статистически значимыми при р ≤0,05.
Результаты.
Структура корреляций клеточного микроокружения «молодой» эндометриоидной кисты.
Статистический анализ выявил большое количество корреляций между клеточными популяциями в тканях «молодой» ЭК (рис. 3). Гранулоциты 1–3 зон формируют между собой исключительно положительные корреляции различной силы в количестве шести,
Сравнение количественных показателей клеточных популяций в исследуемых типах эндометриоидных кист с учетом гистологических зон (только статиcтически значимо различающиеся параметры)
Таким образом, гранулоцитарная инфильтрация подлежащей ФП в тканях «молодой» ЭК достаточно скудная (таблица), при этом сама подлежащая ФП преимущественно представлена рыхлой соединительной тканью, а сидерофаги в строме эндометриоидной выстилки единичные. В совокупности эти факты указывают на стабильность гомеостаза ткани ЭГ в условиях отграничения острой воспалительной реакции со стороны прилежащих тканей.
Структура корреляций клеточного микроокружения «зрелой» эндометриоидной кисты. В строении стенки «зрелой» ЭК наблюдается ряд изменений, что отражается на результатах статистического анализа. В сравнении с «молодой» ЭК в зоне 1 количество лимфоцитов и макрофагов значимо снижается, в то время как количество нейтрофилов возрастает; в зоне 2 в «зрелой» ЭК значимо больше лимфоцитов, макрофагов, нейтрофилов и эозинофилов; в зоне 3 количество нейтрофилов и эозинофилов также значимо больше (см. таблицу). По мере «созревания» ЭК наблюдаются изменения корреляций между клеточными популяциями (рис. 4). Гранулоциты 1– 3 зон так же, как и в ткани «молодой» ЭК, образуют между собой исключительно положительные корреляции, однако их количество увеличивается до девяти. Наибольшее количество связей формируют нейтрофилы зоны 1 и эозинофилы зоны 3. Корреляции между гранулоцитами и макрофагами остаются отрицательными. Сидерофаги теряют положительную корреляцию с гранулоцитами и теперь формируют только отрицательные корреляции. При всем том при увеличении количества сидерофагов в строме эндометриоидной выстилки значительно увеличилось и количество корреляций с другими клеточными популяциями. Так, помимо положительной корреляции с макрофагами зоны 2, сидерофаги образуют еще одну положительную корреляцию с макрофагами зоны 3. Обратим внимание на то, что сидерофаги имеют положительные корреляции с лимфоцитами зоны 2 и 3, а также отрицательную корреляцию с лимфоцитами зоны 1; лимфоциты и нейтрофилы зоны 2 формируют между собой отрицательную корреляцию. Изменения наблюдаются и для корреляций между лимфоцитами 1– 3 зон. Лимфоциты зоны 1 ранее в ткани «молодой» ЭК имели одну положительную корреляцию с лимфоцитами зоны 2, тогда как при «созревании» ЭК лимфоциты зоны 1 образуют две отрицательные корреляции с лимфоцитами 2–3 зон.
Структура корреляций клеточного микроокружения «старой» эндометриоидной кисты. В ходе эволюции «старая» ЭК также приобретает ряд морфологических особенностей. Количество нейтрофилов и лимфоцитов в зоне 1 в «старой» ЭК значимо меньше, чем в «молодой» и «зрелой», а макрофагов значимо больше, чем в «зрелой», но меньше, чем в «молодой». В зоне 2 количество лимфоцитов, макрофагов, нейтрофилов и эозинофилов значимо меньше, чем в «зрелой» ЭК, но макрофагов тоже больше, чем в «молодой». Обнаруженные для зоны 3 значимые различия в количестве эозинофилов и нейтрофилов также были меньше в группе «старых» ЭК (см. таблицу).
По мере «старения» ЭК яичника наблюдается прогрессирующая дезорганизация межклеточных взаимоотношений (рис. 5). Между макрофагами 1– 3 зон полностью отсутствуют положительные корреляции, которые определялись в «молодых» и «зрелых» ЭК, но все еще сохраняются исключительно отрицательные корреляции между макрофагами и гранулоцитами. Сидерофаги образуют единственную положительную корреляцию с макрофагами зоны 3, где, вероятнее всего, сохраняются остатки макрофагального пула, трансформирующегося в си-дерофаги за счет поляризации. Лимфоциты 1 и 2 зон имеют одну положительную корреляцию. Между гранулоцитами 1–3 зон также остаются исключительно отрицательные корреляции, изменяется незначительно только их количество (7 вместо 9).
Обсуждение. Увеличения количества сидерофа-гов в строме эндометриоидной выстилки «молодой» ЭК по мере увеличения количества нейтрофилов подлежащей ФП косвенно подтверждает неблагоприятное влияние острого воспаления на микроциркуляцию и трофику эндометриоидной выстилки кисты. Отрицательные корреляции между гранулоцитами и макрофагами указывают на их противоположную
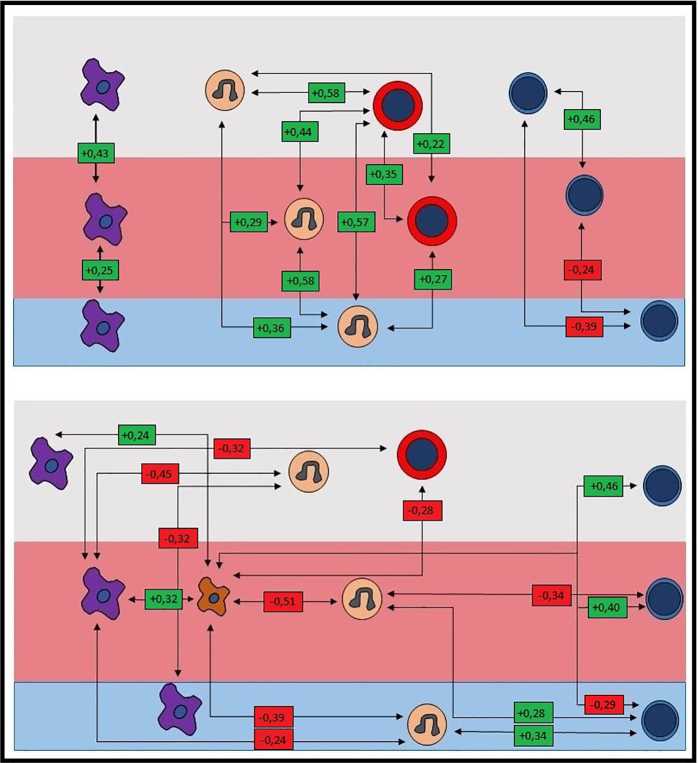
Рис. 4. Корреляции между клеточными популяциями в тканях «зрелой» эндометриоидной кисты
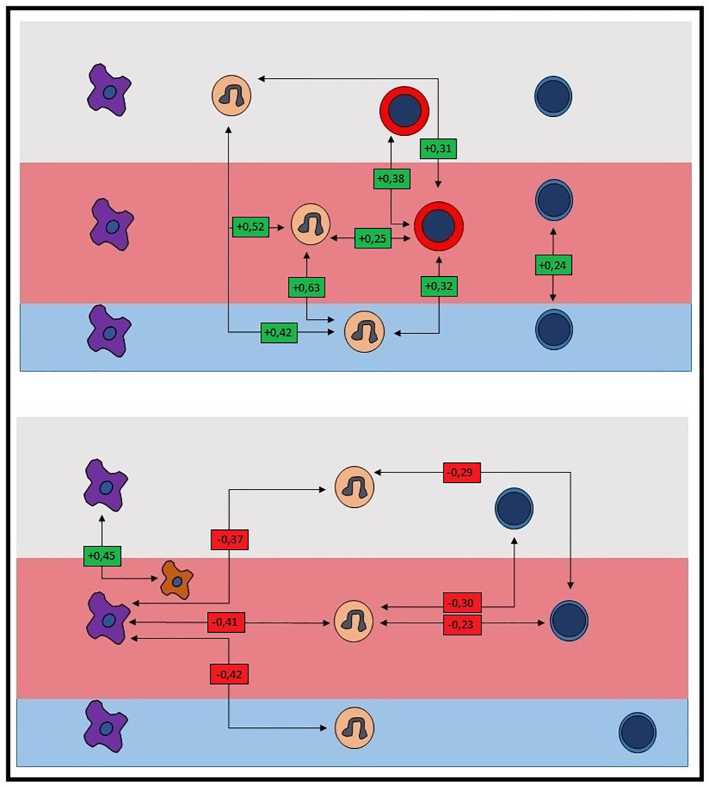
Рис. 5. Корреляции между клеточными популяциями в тканях «старой» эндометриоидной кисты функциональную направленность, в таком случае макрофаги должны быть представлены противовоспалительной субпопуляцией (М2). Интересно, что, по данным исследователей, именно эта субпопуляция преимущественно инфильтрирует ЭГ [5], способствуя сохранению их гомеостаза за счет регуляции процессов регенерации и ангиогенеза [6, 7]. Заметим, что настоящий макрофагальный фенотип имеет слабовыраженную способность к фагоцитозу, что особенно заметно в условиях нарушения кровообращения. Однако положительная корреляция между макрофагами и сидерофагами в пределах зоны 2 свидетельствует о поляризации макрофагального фенотипа с образованием группы провос-палительных макрофагов (М1), обладающих более выраженной способностью к фагоцитозу, поскольку они необходимы для ликвидации последствий усугубляющихся нарушений кровоснабжения в пределах стромы эндометриоидной выстилки. Следовательно, смена макрофагального фенотипа дает возможность восстановления гомеостаза за счет появления сиде-рофагов в условиях нарушенной трофики.
В стенке «зрелой» ЭК наибольшее количество связей формируют нейтрофилы зоны 1 и эозинофилы зоны 3. Это может быть связано с тем, что нейтрофилы преодолели подлежащую ФП и накапливаются в ней, что приводит к ее отеку и постепенному уплотнению; кроме этого, проникновение нейтрофилов в маточный эпителий способствует постепенной атрофии эндометриоидной выстилки. Так, помимо положительной корреляции с макрофагами зоны 2, сидерофаги образуют еще одну положительную корреляцию с макрофагами зоны 3, что может указывать на продолжающуюся поляризацию макрофагов вследствие нарастающих нарушений кровоснабжения. Заметим, что коммуникации ткани ЭГ несостоятельны и не могут обеспечить восполнения макрофагального пула из периферической крови так же эффективно, как в нормальном эндометрии. Следовательно, со временем происходит истощение клеточной субпопуляции противовоспалительных макрофагов (М2), что в конечном итоге еще больше способствует расстройству гомеостаза ЭГ. Перечисленные особенности положения и направления корреляций указывают на постепенную хронизацию воспалительной реакции с одновременным усугублением расстройств кровоснабжения в тканях «зрелой» ЭГ.
В «старой» ЭК уменьшается количество корреляций, сформированных лимфоцитами, вероятная функция которых на данном этапе — это регуляция апоптоза эндометриоидной выстилки по мере усугубления гипоксии и реперфузионных повреждений, обусловленных нарушением кровоснабжения данной области [8]: имеется одна положительная корреляция между лимфоцитами 1 и 2 зон. Вполне очевидно, что гранулоцитарная инфильтрация как морфологический субстрат острого воспаления неблагоприятно влияет на гомеостаз ЭГ, что подтверждается относительной сохранностью количества корреляций между гранулоцитами 1-3 зон на всех этапах существования ЭК при разрушении связей между другими клетками в стенке. Ранее N. M. Nowak с соавт. показали то, что экспериментально воспроизведенный перитонит у мышей негативно влияет на имплантацию взвеси ткани эндометрия и последующее формирование ЭГ, из чего следует, что острое воспаление в брюшной полости блокирует возникновение эндометриоза [3]. Таким образом, происходит дальнейшая хрони-зация воспалительной реакции, что в итоге приведет к полной атрофии эндометриоидной выстилки кисты яичника и формированию так называемой склерозированной ЭК яичника [1].
Заключение. Нарастание плотности гранулоцитарного инфильтрата в области ФП на границе теки — стромы ЭГ способствует ее постепенному уплотнению за счет отека и склероза с последующим нарушением кровоснабжения ткани и истощением макрофагального пула за счет поляризации противовоспалительной субпопуляции макрофагов (М2) с увеличением количества сидерофагов, что неблагоприятно отражается на поддержании гомеостаза ЭГ. Таким образом, острая воспалительная реакция, последующая ее хронизация с исходом в склероз приводят к нарастанию гипоксии, являясь основными модуляторами эволюции ЭК яичника с формированием в конечном итоге так называемой склерозированной ЭК яичника.
Список литературы Воспаление, гипоксия и склероз как основные модуляторы эволюции эндометриоидной кисты яичника
- Нейштадт Э.Л., Ожиганова И.Н. Опухоли яичника. СПб.: Фолиант, 2017; 352 с.
- Jiang L, Yan Y, Liu Z, Wang Y. Inflammation and endo-metriosis. Front Biosci (Landmark Ed). 2016; (21): 941-8. DOI: 10.2741/4431. PMID: 27100482.
- PMID: 27100482
- Nowak NM, Fischer OM, Gust TC, et al. Intraperitoneal inflammation decreases endometriosis in a mouse model. Human Reproduction. 2008; 23 (11): 2466-74.
- Украинец P.В., Корнева Ю.С. Поляризация макрофагального клеточного центра в процессе эволюции эндометриоидной кисты яичника. Сибирский журнал клинической и экспериментальной медицины. 2021; 36 (2): 84-91.
- Smith КА, Pearson СВ, Hachey AM, et al. Alternative activation of macrophages in rhesus macaques (Macaca mulatta) with endometriosis. Comp Med. 2012; 62 (4): 303-10.
- Mantovani A, Sica A, Sozzani S, et al. The chemokine system in diverse forms of macrophage activation and polarization. Trends Immunol. 2004; 25 (12): 677-86. 10.1016/j.it. 2004.09.015.
- Mantovani A. Macrophage diversity and polarization: in vivo veritas. Blood. 2006; 108 (2): 408-9.
- Kim JS, Choi YS, Park JH, et al. Role of B-cell translocation gene 1 in the pathogenesis of endometriosis. Int J Mol Sci. 2019; 20 (13): 3372.


