Воздействие наносекундных электромагнитных импульсов на кинетику фазового перехода у-А1(ОН)3 -» У-AlOOH в гидротермальных условиях
Автор: Лопушан В.И., Крымский В.В., Клещев Д.Г.
Рубрика: Физика
Статья в выпуске: 7 (62), 2006 года.
Бесплатный доступ
Выявлен эффект инициирующего влияния наносекундных электромагнитных импульсов на кинетику фазового перехода гиббсит → бемит в гидротермальных условиях.
Короткий адрес: https://sciup.org/147158473
IDR: 147158473 | УДК: 541.1
Текст научной статьи Воздействие наносекундных электромагнитных импульсов на кинетику фазового перехода у-А1(ОН)3 -» У-AlOOH в гидротермальных условиях
Типичными представителями таких систем являются мелкодисперсные оксиды р- и 3d-металлов, которые широко используются в качестве неорганических пигментов, катализаторов химических реакций, магнитных порошков, полировальных и ионообменных материалов, компонентов для получения пластмасс, керамики и др. В зависимости от механизма и типа протекающих физико-химических реакций можно выделить следующие группы методов синтеза оксидных МДС: а) термического разложения солей или гидратированных оксидов р- и Зд-металлов; б) окисления металлических или восстановления оксидных порошкообразных объектов; в) твердофазного взаимодействия в системе порошкообразных оксидов; г) конденсации из газовой фазы; д) кристаллизации из растворов, в том числе, осложненной протеканием химических реакций; е) основанные на различного рода превращениях неравновесных гидратированных оксидов металлов при термообработке в растворах: кристаллизация рентгеноаморфных фаз, фазовые превращения (ФП).
Каждый из этих методов имеет присущие ему ограничения в фазовом, химическом и дисперсном составе формирующихся продуктов, которые детально проанализированы в [2]. В частности, из-за активации при высоких температурах процессов коалесценции и спекания твердофазные методы не позволяют получать нанокристаллические объекты. Напротив, при конденсации труднорастворимых оксидов из газовой фазы или растворов образуются нанокристаллические продукты, склонные к коагуляции с образованием плотных агрегатов из-за высокой дефектности их кристаллической структуры.
Показано [2, 5-7], что близкие к монодисперсным, не склонные к коагуляции оксидные МДС формируются при ФП или ХП неравновесных гидратированных оксидов металлов в процессе их термообработки в растворах, в том числе, в гидротермальных условиях. При этом средний размер кристаллов МДС можно варьировать в широком диапазоне (от десятков до тысяч нанометров) путем изменения параметров термообработки, фазового и дисперсного состава неравновесных соединений.
Отметим, что с заметной скоростью превращения неравновесных МДС протекают при относительно высоких температурах и давлениях, что требует разработки автоклавов специальной конструкции и препятствует широкому внедрению новых технологий. Известно [3, 8], что физические методы воздействия инициируют протекание в МДС процессов, приводящих к понижению ее свободной энергии. К таким методам, в частности, относится воздействие на МДС наносекундных электромагнитных импульсов (НЭМИ), которые влияют на протекание различных процессов в твердых и жидких телах [9—11]. Целью данной работы является выявление воздействия НЭМИ на кинетику ХП гиббсита (у-А1(ОН)3) в бемит (у-АЮОН), которое согласно [12, 13] в системе А12О3 - Н2О макроскопически проявляется при температурах термообработки выше 170 °C.
Методика эксперимента. В качестве исходного образца гиббсита использовали фракцию минус 40 мкм технического гидроксида алюминия, который, по данным химического анализа, содержал (мае. %): А12О3 - 64,2±0,5; Н2О - 35,5±0,5; М2О (М1- -К+, Na+) - 0,4±0,1. Образец предварительно тщательно отмывали от примесей гидроксидов щелочных металлов сначала 0,1 N раствором серной кислоты, а затем дистиллированной водой, высушивали при НО °C до постоянной массы и измельчали. По данным РФА, отмытый образец был однофазным - у-А1(ОН)3, а его состав А12О3 3,12Н2О - близок к стехиометрическому. Фазово-чистый образец бемита (состав А12О31,05Н2О) был получен термообработкой гиббсита в парах воды при 300 °C при парциальном давлении паров воды ~6 МПа.
Для исследования кинетики ФП у-А1(ОН)3 -> у-АЮОН образец гиббсита репульпировали в дистиллированной воде при массовом соотношение Т.Ж = 1:5. В первой серии опытов суспензию в количестве 2,4±0,1 мл загружали в автоклавы с рабочим объемом 3,0 см3, изготовленные из нержавеющей стали, и герметизировали. Для максимального исключения влияния кинетики нагрева и температурного градиента в печи на ФП гидротермальную обработку суспензий проводили в двух муфельных печах. Вторую печь с широкой изотермической зоной (линейные размеры -150x150 мм2; разность температур на границах зоны - не более 0,5 °C) нагревали до заданной температуры Т и термостатировали (точность поддержания температуры - ±0,3 °C), а первую- до температуры Тх = Т + АГ, где АТ * 150 °C. Кассету из 12 автоклавов с термопарами, вставленными в просверленные отверстия в верхних крышках крайних двух автоклавов, сначала помещали в первую печь, в которой их за время тх, не превышающее 15 мин, нагревали до температуры Т, а затем - во вторую печь. С момента достижения автоклавами температуры Т начинали отсчет времени г термообработки. Температуру Т варьировали от 180 до 220 °C, длительность т - от 0,1 до 30 ч. По окончании термообработки автоклавы вынимали из печи, быстро охлаждали под струей воды и разгерметизировали.
Для изучения влияния НЭМИ на кинетику ХП был изготовлен автоклав объемом 10 см3 с двумя коаксиальными электродами. Одним из электродов служил корпус автоклава, который был заземлен. На второй центральный электрод, изолированный фторопластовой прокладкой, подавался положительный потенциал от генератора НЭМИ. Во второй серии опытов в автоклав загружали 8 мл суспензии у-А1(ОН)3, его герметизировали, нагревали в первой печи до температуры 200+3 °C, подключали к электродам генератор НЭМИ, помещали в первую печь, термостатированную при 200 °C, и включали генератор импульсов. Термообработку вели в течение 0,5 ч при следующих режимах работы генератора: длительность импульса 0,5 нс; амплитуда импульсов 8 кВ; частота повторения импульсов 1000 Гц. Была проведена серия из трех параллельных опытов.
Фазовый состав образцов контролировали методом порошковой дифрактометрии (рентгеновский аппарат ДРОН-3, фильтрованное Cu^a-излучение). Идентификацию фазового состава исходного и подвергнутых термообработке образцов проводили путем сопоставления экспериментально определенных значений межплоскостных расстояний (1«а и относительных интенсивностей /ьи дифракционных максимумов с табличными данными [14]. Для обнаружения следовых количеств бемита в подвергнутых термообработке образцах проводили сканирование рефлекса (020) бемита по точкам (время счета - 40 с; шаг сканирования по 20-0,1 град на крыльях и 0,02 град в центральной части дифракционного максимума). Степень химического превращения гиббсита в бемит рассчитывали из данных РФА по стандартной методике [15]. В качестве аналитических использовали рефлексы (002) у-А1(ОН)3 и (020) у-АЮОН. Химический состав объектов контролировали методами объемного химического анализа и термогравиметрии (дериватограф Paulik-Erdey).
Результаты и обсуждение. Для выявления эффекта влияния НЭМИ на кинетику ФП гиббсита в бемит и определения условий проведения эксперимента в первой серии опытов была изучена кинетика данного ХП в отсутствии внешних воздействий.
Рентгенограммы всех исследованных образцов в зависимости от температуры Т и продолжительности т термообработки содержали только рефлексы гиббсита, или бемита, или смеси вышеуказанных фаз. При Т = const с ростом г, либо при т = const и увеличении Т, проявляется тенденция к уменьшению относительных интенсивностей рефлексов у-А1(ОН)3 и, напротив, возрастание интенсивности рефлексов фазы у-А1ООН, что свидетельствует о протекании ФП гиббсита в бемит.
Кинетические кривые этого ФП имеют сигмоидный вид (см. рисунок) с ярко выраженным латентным периодом. С увеличением Т наблюдалось сокращение длительности латентного периода, а при т = const - возрастание полноты а ФП, что свидетельствует об его активационном характере.
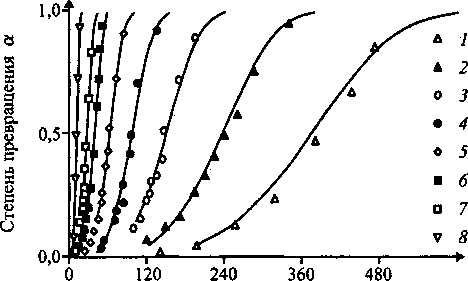
Время термообработки т, мин
Кинетические кривые фазового превращения гиббсит -* бемит: температуры термообработки 1 -180, 2 -185, 3 - 190,4 -192, 5 - 195, 6-200,7-205,8-210 °C
Согласно [16] кинетические уравнения ФП можно представить в виде
^а(т,т^ = кт, (1) где g - интегральная функция кинетического уравнения, аналитический вид которой зависит от механизма реакции; к - константа скорости реакции. Математическую обработку экспериментальных данных проводили согласно рекомендациям [17, 18] с учетом наиболее распространенных кинетических моделей ФП (см. таблицу). Для этого на первом этапе кинетические кривые линеаризовали в координатах g(a) - т, для каждой из моделей рассчитывали выборочные статистики Фишера Fi^i (см. таблицу), по значению которых судили о возможности реализации данного механизма ХП.
Аналитический вид интегральных функций д(а) и средние значения выборочных статистик Фишера F^_2 для ФП гиббсит -» бемит
|
' Лимитирующая стадия (символ модели) |
||
|
Одномерная диффузия (D0 |
a2 |
56,3 |
|
Двумерная диффузия (D2) |
a + (l-a)'ln(l-a) |
93,9 |
|
Трехмерная диффузия (D3) |
[1 _(1 -a)1/3]2 |
35,8 |
|
Топохимические реакции на границе раздела фаз (R=: 1<н<3) |
l-(l-a)1/n |
190,4 |
|
Зародышеобразование и рост кристаллов (модель Аврами-Ерофеева-Колмагорова - Ап: 0,5 < п < 4,0) |
[-ln(l-a)]l/" |
429,3 |
Из проведенных расчетов следует (таблица), что во всем исследованном температурном интервале наибольшие значения F^ достигаются для модели Аврами-Ерофеева-Колмагорова (А-Е-К), лимитирующими стадиями которой выступают процессы зародышеобразования и (или) роста кристаллов равновесной фазы.
На втором этапе математической обработки в модель А-Е-К была введена поправка, учитывающая возможную погрешность начала отсчета времени т0.
Из линеаризованных по скорректированной модели кинетических кривых для каждой из температур определены значения константы скорости к ФП гиббсита в бемит и параметра реакции п. Зависимости к = КТ) линеаризуются в координатах 1пА(7) - 1/Г, что свидетельствует об активационном характере протекающих ХП:
КТ) = А-е* ЕГ№\, (2)
где А - некоторая постоянная для данного ФП величина; Е - кажущаяся энергия активации ФП; R - универсальная газовая постоянная. Экспериментально определенное значение энергии активации: Е = 157±12 кДж/моль. По своей величине Е согласуется с суммарным изменением энтальпии (148,49+2,20) при ФП у-А1(ОН)3 -> у-А1ООН и у-АЮОН-> у-А12О3 [19], а также с энергиями активациями ХП при прокалке на воздухе гидроксидов и оксигидроксидов других металлов [2, 18].
С учетом полученных данных по кинетике ФП (см. рисунок) были выбраны следующие режимы термообработки у-А1(ОН)з: Т * 200 °C; т = 0,5 ч. Для исключения артефакта, связанного с изменением объема и конструкции автоклава, сначала была проведена серия из трех контрольных опытов с выключенным генератором. Сканирование по точкам образцов, подвергнутых термообработке, в области углов дифракции рефлексов бемита на обнаружение его следовых количеств дали отрицательный результат: все три образца были однофазными - у-А1(ОН)з.
На рентгенограммах всех трех образцов, полученных при тех же режимах термообработки с включенным генератором НЭМИ, наряду с рефлексами гиббсита присутствуют отчетливые дифракционные максимумы бемита. Степень превращения а гиббсита в бемит, определенная из данных количественного РФА, в них составила: 29; 20 и 36 мае. %. Таким образом, полученные результаты позволяют сделать вывод об инициирующем влиянии НЭМИ на ФП гиббсита в бемит.
Обратимся к анализу возможных причин данного явления. Как показано в работах [2, 5-8], фазовые и химические превращения неравновесных гидратированных оксидов р- и 3 d-элементов при термообработке в растворах осуществляются по механизму «растворение-осаждение» (РОМ), путем растворения кристаллов неравновесной фазы, образования зародышей и роста (через раствор) кристаллов равновесной фазы. При относительно низких температурах термообработки лимитирующей стадией этих превращений выступает процесс растворения кристаллов неравновесной фазы, связанный с разрывом связей между атомами (ионами) поверхностного слоя кристаллов. При воздействии НЭМИ с высокой напряженностью электрического поля (до 109 В/м) происходит деформация валентных орбиталей атомов (ионов), что ведет к снижению энергии разрыва связей. Проявлением этого является ускорение процесса фазовых и химических превращений неравновесных фаз, снижение температуры макроскопического проявления превращений.
Выводы. Установлено инициирующее влияние наносекундных электромагнитных импульсов на кинетику химического превращения гиббсита в бемит.
Робота выполнена при финансовой поддержке Российского фонда фундаментальных исследований: грант 05-08-01356.
Список литературы Воздействие наносекундных электромагнитных импульсов на кинетику фазового перехода у-А1(ОН)3 -» У-AlOOH в гидротермальных условиях
- Петров Ю.И. Кластеры и малые металлические частицы. -М. Наука, 1986. -368 с.
- Клещев Д.Г., Шейнкман А.И., Плетнев Р.Н. Влияние среды на фазовые и химические превращения в дисперсных системах. -Свердловск: УрО АН СССР, 1990. -248 с.
- Бучаченко А.И. Химия на рубеже веков: свершения и прогнозы//Успехи химии. -1999. -Т.68.-№2.-С.99-117.
- Основы физикохимии веществ в метастабильном состоянии и перспективы их использования/И.А. Тананаев, В.Б. Федоров, И.Д. Морохов, Л.В. Малюкова//Изв. АН СССР. Неорган. материалы. -1984. -Т. 20. -№ 6. -С. 1026-1033.
- Клещев Д.Г. Получение нанокристаллических оксидов Ti, Mn, Co, Fe и Zn в водных растворах при термообработке//Неорган. материалы.-2005.-Т. 41.-№ 1.-С. 46-53.
- Толчев А.В., Багаутдинова Р.Р., Клещев Д.Г. Кристаллохимический аспект фазообразования в системе γ-FeOOH -Н2O -NaOH//Журн. прикл. химии. -2001. -Т. 74. -№ 1. -С. 3 89-394.
- Агафонов Г.И., Клещев Д.Г., Толчев А.В. Универсальная гидротермальная технология синтеза железоокисных пигментов//Лакокрасочные материалы и их применение. -1999. -№ 7-8.-С. 41-46.
- Бажал И.Г., Куриленко О.Д. Переконденсация в дисперсных системах. -Киев: Наукова думка, 1975. -287 с.
- Взаимопревращения различных элементов/В.Ф, Балакирев, В.В. Крымский, Б.В. Болотов и др.; Под ред. В.Ф. Балакирева. -Екатеринбург: УрО РАН, 2003. -96 с.
- Наносекундные импульсы и их применение/B.C. Белкин, В.А. Бухарин, В.К. Дубровин и др.; Под ред. В.В. Крымского. -Челябинск: Изд-во Татьяны Лурье, 2001. -119 с.
- Крымский В.В., Балакирев В.Ф. Воздействие наносекундных электромагнитных импульсов на свойства веществ//Доклады РАН. -2002. -Т. 385. -№ 6. -С. 786-787.
- Ervin G., Osborn E.P. А12O3 -Н2O system//J. Geol. -1951. -V. 59. -№ 2. -P. 381-394.
- Химическая энциклопедия/Под ред. Кнунянц И.Л. и др. -Т. 1. М.: Сов. энциклопедия, 1988.-623 с.
- Powder Diffraction File: Search Manual Fink Method Inorganic. Swarthmore, 1978.
- Китайгородский А.И. Рентгеноструктурный анализ мелкокристаллических и аморфных тел. -М.-Л.: ГИТТЛ, 1952. -588 с.
- Третьяков Ю.Д., Лепис X. Химия и технология твердофазных материалов. -М.: Издательство МГУ, 1985.-251 с.
- Koga N, Haruhiko Tanaka. A physico-geometric approach to the kinetics of solid-state reactions as exemplified by the thermal dehydration and decomposition of inorganic solids//Thermochimica Acta. -2002. -V. 388. -№ 1. -P. 41-61.
- Koga N., Takemoto S., Okado S., Tanaka H. A kinetic study the thermal decomposition of iron(III) oxides. Part I. α-FeOOH in banded iron formations//Thermochimica Acta. -1995. -V. 254. -№2.-P. 193-207.
- Wenming Z., Nianya C., Qiyuan С. Thermodinamics of thermal decomposition of aluminium hydroxide//Trans. Noneferrous Metals Soc. China. -1997. -V. 7. -№ 3. -P. 132-139.


