Возможности диагностики костных метастазов у больных люминальным раком молочной железы с помощью таргетной GRPR-визуализации
Автор: Иванова А.Г., Брагина О.Д., Варвашеня Р.Н., Ларькина М.С., Чернов В.И., Романова А.А., Фролова И.Г., Табакаев С.А., Паталяк С.В., Бритвина М.А.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 1 т.25, 2026 года.
Бесплатный доступ
Актуальность. Люминальный рак молочной железы встречается в 60–80 % случаев и характеризуется высокой частотой метастазирования в кости, что определяет необходимость своевременного выявления отдаленных очагов. Традиционные методы визуализации имеют ограниченную чувствительность, особенно в отношении очагов малого размера. В связи с этим актуальна разработка высокочувствительных методов более ранней диагностики метастазов в кости. Перспективным направлением является таргетная радионуклидная визуализация рецептора гастрин-высвобождающего пептида (GRPR), гиперэкспрессия которого ассоциирована с рецептором эстрогена, с использованием радиофармацевтического лекарственного препарата (РФЛП) на основе антагонистов GRPR. Доклинические исследования продемонстрировали перспективность использования для этих целей РФЛП [99mTc]Tc-DB8. Цель исследования – демонстрация возможностей РФЛП [99mTc]Tc-DB8 в диагностике костных метастазов у больных люминальным РМЖ. Описание клинических случаев. Клинический случай № 1. Пациентка К., 51 год, диагноз: Рак правой молочной железы, IIIC стадия (T2N3M0), мультицентричный рост, метастатическое поражение аксиллярных и подключичных лимфоузлов. ОФЭКТ/КТ выполнена через 2 ч после внутривенного введения РФЛП [99mTc]Tc-DB8 в дозировке протеина 80 мкг. По результатам исследования помимо первичной опухоли и метастатических лимфоузлов выявлен высокий уровень аккумуляции препарата [99mTc]Tc-DB8 в проекции V ребра справа по средней аксиллярной линии. Повторный анализ компьютерных томограмм органов грудной клетки (КТ ОГК) подтвердил наличие очага литической деструкции, расцененного как возможный метастаз и взятого под наблюдение. При КТ ОГК в динамике в указанной проекции визуализировался участок неравномерных склеротических изменений, что интерпретировано как ответ на терапию. Клинический случай № 2. Пациентка Д., 42 года, диагноз: Рак правой молочной железы IV стадии (T1N1M1), метастаз в аксиллярный лимфоузел, множественные метастазы в костях. ОФЭКТ/КТ проведена через 2 ч после инъекции РФЛП [99mTc]Tc-DB8 в дозировке 80 мкг, при которой помимо визуализации первичного очага и метастатически измененного лимфоузла выявлена высокая аккумуляция РФЛП в проекции LII-SII, в подвздошной и седалищной костях, в заднем отрезке VII ребра справа. Заключение. Результаты клинического исследования с использованием препарата [99mTc]Tc-DB8 продемонстрировали высокую диагностическую эффективность метода в визуализации костных метастазов у больных люминальным РМЖ.
Люминальный рак молочной железы, DB8, GRPR, радионуклидная диагностика
Короткий адрес: https://sciup.org/140314357
IDR: 140314357 | УДК: 618.19-006.6-033.2:611.71]-073.916 | DOI: 10.21294/1814-4861-2026-25-1-170-178
Potential of targeted GRPR imaging for the detection of bone metastases in patients with luminal breast cancer
Background. Luminal breast cancer, comprising 60–80 % of cases, is characterized by a high frequency of bone metastasis, necessitating continuous surveillance for early detection of distant metastases. Traditional imaging methods have limited sensitivity, especially for small lesions. Therefore, the development of highly sensitive methods for early diagnosis is relevant. Targeted radionuclide imaging of the gastrin-releasing peptide receptor (GRPR) using antagonist-based radiopharmaceuticals, such as [99ᵐTc]Tc-DB8 is a promising non-invasive method for detecting small lesions. The aim of the study was to demonstrate the potential of [99ᵐTc]Tc-DB8 for detecting bone metastases in patients with luminal breast cancer. Case report 1. A 51- year-old woman diagnosed with stage IIIC right breast cancer (T2N3M0), with multicentric growth, metastatic involvement of the axillary and subclavian lymph nodes, underwent SPECT/CT 2 hours after the intravenous administration of [99ᵐTc]Tc-DB8 at a protein dose of 80 μg. The detection of a high-uptake [99ᵐTc]Tc-DB8 lesion in the right 5th rib, confrmed as a lytic bone destruction on CT, indicated a high suspicion of bone metastasis. Followup chest CT showed an area of uneven sclerotic changes, interpreted as a response to therapy. Case report 2. A 42-year-old woman was diagnosed with stage IV right breast cancer (T1N1M1), metastatic involvement of the axillary lymph node, and multiple bone metastases. A SPECT/CT performed 2 hours after the intravenous injection of [99ᵐTc]Tc-DB8 at a dose of 80 μg revealed high uptake of the radiopharmaceutical in the primary tumor, metastatic lymph nodes, and extensive bone metastases. Specifcally, the radiopharmaceutical accumulated in the L2-S2 vertebrae, the right ilium and ischium, and the posterior segment of the 7th rib on the right, identifying these as metastatic sites. Conclusion. Results of the clinical study on [99ᵐTc]Tc-DB8 demonstrated its high effcacy in detecting bone metastases in patients with luminal breast cancer.
Текст научной статьи Возможности диагностики костных метастазов у больных люминальным раком молочной железы с помощью таргетной GRPR-визуализации
Люминальный рак является наиболее распространенным молекулярно-биологическим подтипом (60–80 %) рака молочной железы (РМЖ), который характеризуется относительно благоприятным прогнозом и чувствительностью к гормональной терапии [1]. В то же время данный подтип обладает более высокой частотой выявления метастазов в кости. Ретроспективное исследование J.H. Fan et al. [2], включавшего 2 393 пациентки с распространенным РМЖ, продемонстрировало, что наибольшая склонность к развитию костных метастазов отмечалась при люминальных формах: костное поражение диагностировано у 51,1 % пациенток с люминальным А и у 44,7 % с люминальным В подтипом. Наличие отдаленных метастазов оказывает значительное влияние на общую выживаемость пациенток с раком молочной железы. При этом медиана выживаемости при изолированном поражении костей составляет
26–30 мес, пятилетняя выживаемость варьирует в пределах 22–38 % [3–5].
В настоящее время для оценки состояния костей у больных РМЖ в клинической практике используются остеосцинтиграфия с 99mTc-мечеными дифосфонатами (чувствительность – 62–90 %, специфичность – 74–91 %), магнитно-резонансная томография (чувствительность – 94 %, специфичность – 98 %), компьютерная томография (чувствительность – 70 %, специфичность – 98 %), а также позитронно-эмиссионная томография с 18F-дезоксиглюкозой (чувствительность – 94 %, специфичность – 98 %) [6–8]. Однако несмотря на широкую доступность и высокую диагностическую эффективность, данные методы визуализации обладают рядом недостатков: высокой стоимостью, потребностью в большинстве случаев проведения дополнительных уточняющих исследований (необходимость включения нескольких анатомических областей), а также, прежде всего, ограниченной чувствительностью в оценке распространенности опухолевого поражения (включая первичную опухоль и метастазы в регионарные лимфоузлы и отдаленные органы и ткани) [9, 10].
Важно отметить, что у больных люминальным раком молочной железы в ряде случаев может наблюдаться различный уровень экспрессии рецепторов между первичной опухолью и метастатическими очагами [11]. Согласно данным S. Shiino et al. [12], проанализировавших показатели несоответствия экспрессии рецепторов эстрогенов (РЭ) и прогестерона (РП) у больных РМЖ в 11 исследованиях, различия в экспрессии РЭ составили 19,7 %, для РП – 32,5 %. Аналогичный метаанализ, проведенный W.A.M.E. Schrijver et al. [13], продемонстрировал сопоставимые результаты у 6 118 пациентов в 39 исследованиях, при этом суммарные показатели несоответствия для РЭ и РП составили 19,3 и 30,9 % соответственно. К сожалению, проведение морфологической верификации метастазов не всегда возможно из-за технических трудностей забора материала и высокой вероятности развития осложнений.
Учитывая мировые тенденции, большое внимание уделяется изучению методов таргетной радионуклидной визуализации, открывающей перспективы для оптимизации диагностического этапа за счет сокращения числа исследований и связанных с ними экономических затрат, а также способствующей реализации персонализированного подхода к выбору терапевтической тактики. Данный метод основан на использовании радиофармацевтических лекарственных препаратов (РФЛП), состоящих из таргетного модуля и радиоизотопа. Нацеливающий модуль взаимодействует с внеклеточной частью опухолевого рецептора, в то время как электромагнитное излучение, испускаемое радионуклидом, фиксируется используемой аппаратурой (однофотонная эмиссионная компьютерная томография (ОФЭКТ) или позитронная эмиссионная томография (ПЭТ)). Такой подход обеспечивает не только анатомическую визуализацию опухолевых очагов, но и предоставляет ценную информацию о биологических характеристиках опухоли [14]. Полученные к настоящему моменту результаты в отношении рецептора эпидермального фактора роста 2 типа (HER2/ neu) с использованием альтернативных каркасных протеинов продемонстрировали эффективность в анатомической детекции опухолевых очагов и молекулярной оценке экспрессии HER2/neu в выявленных анатомических структурах [14, 15].
Актуальным для больных люминальным РМЖ направлением является радионуклидная визуализация рецептора гастрин-высвобождающего пептида (GRPR, Gastrin-Releasing Peptide Receptor) – трансмембранного белка, оказывающего влияние на рост и пролиферацию как нормальных, так и атипичных клеток посредством активации внутриклеточных сигнальных каскадов. Установлено, что экспрессия GRPR в злокачественных опухолях молочной железы достоверно выше, чем в нормальных тканях, при этом она положительно коррелирует с уровнем экспрессии рецептора эстрогена. Наибольшая частота гиперэкспрессии GRPR регистрируется при люминальных формах: у 86,2 % пациенток с люминальным А, у 70,5 % – с люминальным В HER2-негативным и у 82,8 % – с люминальным В HER2-положительным РМЖ, значительно реже этот рецептор экспрессируется при HER2-положительном (21,3 %) и трижды негативном (7,8 %) подтипах, что подчеркивает потенциальную значимость GRPR в качестве мишени для оценки распространенности опухолевого процесса у больных с эстроген-положительными опухолями [16].
Учитывая опыт в разработке радиофармацевтических лекарственных препаратов в отделении радионуклидной терапии и диагностики НИИ онкологии ТНИМЦ, направленных на детекцию различных молекулярных мишеней, в том числе рецептора HER2/neu, а также отсутствие РФЛП, отвечающего оптимальным характеристикам для обнаружения GPRP в опухолях молочной железы и метастатических очагах, отделением радионуклидной терапии и диагностики в коллаборации с Томским политехническим и Уппсальским (г. Уппсала, Швеция) университетами синтезирован новый радиофармацевтический лекарственный препарат на основе антагониста GRPR – [99mTc] Tc-DB8 [14–17]. По результатам in vitro и in vivo доклинических исследований молекула продемонстрировала высокую специфичность и аффинность к GRPR, а также отсутствие токсического действия при введении РФЛП лабораторным животным. Полученные экспериментальные данные послужили обоснованием для запуска I фазы клинических исследований, в рамках которой была подтверждена безопасность [99mTc]Tc-DB8 при внутривенном введении пациентам, а также продемонстрирован высокий уровень его накопления в первичных опухолях с положительным статусом рецептора эстрогена с использованием дозировки 80 мкг и проведением ОФЭКТ/КТ через 2 ч после инъекции по сравнению с опухолями, не экспрессирующими данный маркер [17].
Цель исследования – демонстрация возможностей радиофармацевтического лекарственного препарата [99mTc]Tc-DB8 в диагностике костных метастазов у больных люминальным раком молочной железы.
Клинический случай № 1
Пациентка К., 51 год, поступила в амбулаторнополиклиническое отделение НИИ онкологии ТНИМЦ в декабре 2023 г. с диагнозом: Рак правой молочной железы, IIIC (сТ2N3M0) стадия, мульти-центричный рост, метастатическое поражение аксиллярных и подключичных лимфатических узлов справа. Гистологическое заключение: инвазивная дольковая карцинома молочной железы, G2. ИГХ: рецептор эстрогена – 6 баллов, рецептор прогестерона – 8 баллов, HER2/neu отрицательный (0), Ki65 25 % – люминальный В подтип. Поражение регионарных лимфоузлов подтверждено результатами цитологического исследования. Пациентке выполнен полный объем клинико-инструментальных исследований согласно Российским клиническим рекомендациям [18]. По результатам остеосцинтиграфии с 99mTc-Пирофосфатом и компьютерной томографии органов грудной клетки данных за отдаленные метастазы не получено.
При однофотонной эмиссионной компьютерной томографии (ОФЭКТ) органов грудной клетки и верхнего этажа брюшной полости через 2 ч после внутривенной инъекции РФЛП [99mTc]Tc-DB8 в дозировке протеина 80 мкг все выявленные ранее опухолевые очаги были визуализированы (SUV max
ПО=2,97, SUVmax мЛУ=2,16), а их расположение соответствовало данным, полученным при стандартных методах диагностики. Дополнительно при анализе полученных результатов обратила на себя внимание высокая аккумуляция препарата [99mTc]Tc-DB8 в проекции V ребра справа по средней аксиллярной линии (рис. 1) (SUVmax = 1,29).
При пересмотре компьютерной томограммы органов грудной клетки (ОГК) в указанной проекции был выявлен участок литической деструкции, размером 19×5 мм (рис. 2А), который был оставлен на динамическое наблюдение.
На базе НИИ онкологии ТНИМЦ пациентка получила комбинированное лечение в объеме предоперационной химиотерапии и радикальной мастэктомии справа. По результатам планового гистологического исследования операционного материала выявлены признаки слабого лечебного патоморфоза. Следующим этапом назначены дистанционная лучевая терапия на область передней грудной стенки и зоны регионарного лимфооттока и последующая адъювантная гормонотерапия ингибиторами ароматазы на фоне лекарственной овариальной супрессии.
При контрольной компьютерной томографии ОГК после комбинированного лечения в проекции V ребра справа по средней аксиллярной линии отмечался участок неравномерных склеротических изменений, размером 26×5 мм (рис. 2Б), что расценено как терапевтический эффект. Остеосцинтиграфия после проведения лечения не выполнялась.
В настоящее время пациентка принимает ингибиторы ароматазы и находится на динамическом наблюдении в НИИ онкологии ТНИМЦ без признаков прогрессирования заболевания.
Клинический случай № 2
Пациентка Д., 42 года, обратилась в амбулаторно-поликлиническое отделение Томского областного онкологического диспансера (ТООД) в
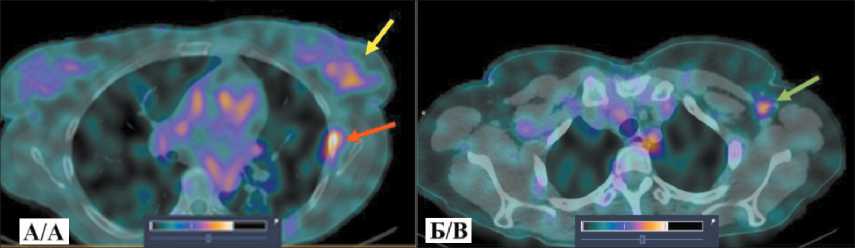
Рис. 1. ОФЭКТ/КТ органов грудной клетки больной К. через 2 ч после инъекции [99mTc]Tc-DB8 в дозировке протеина 80 мкг: А – желтая стрелка указывает на первичную опухоль, красная стрелка – на участок гиперфиксации РФЛП в проекции V ребра по средней аксиллярной линии справа; Б – зеленая стрелка указывает на метастатический аксиллярный лимфоузел.
Примечание: рисунок выполнен авторами
Fig. 1. Chest SPECT/CT performed 2 hours after injection of [99mTc]Tc-DB8 at a protein dose of 80 μg: A – yellow arrow indicates the primary tumor, red arrow indicates the area of increased radiopharmaceutical uptake in the projection of the 5th rib along the right mid-axillary line; B – green arrow indicates the metastatic axillary lymph node. Note: created by the authors
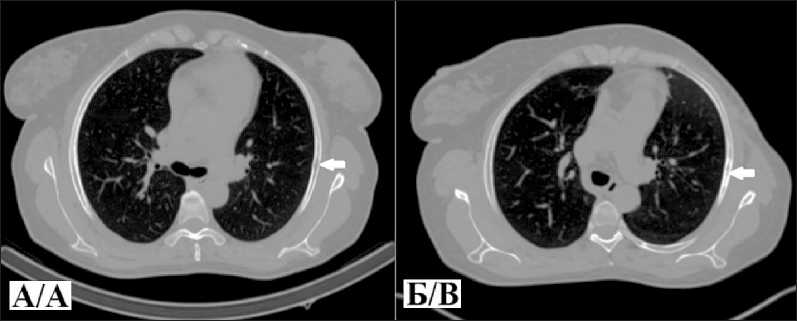
Рис. 2. А – компьютерная томография органов грудной клетки в аксиальной проекции (костное окно) больной К. до лечения (белой стрелкой указан участок литической деструкции в V ребре по средней аксиллярной линии справа, размером 19×5 мм); Б – исследование через 11 мес после лечения (белой стрелкой указан участок неравномерных склеротических изменений в V ребре по средней аксиллярной линии справа, размером 26×5 мм). Примечание: рисунок выполнен авторами
Fig. 2. A – chest CT in axial projection (bone window) performed before treatment (white arrow indicates an area of lytic destruction measuring 19×5 mm in the 5th rib along the right mid-axillary line); B – chest CT performed after treatment (white arrow indicates an area of uneven sclerotic changes measuring 26×5 mm in the 5th rib along the right mid-axillary line). Note: created by the authors
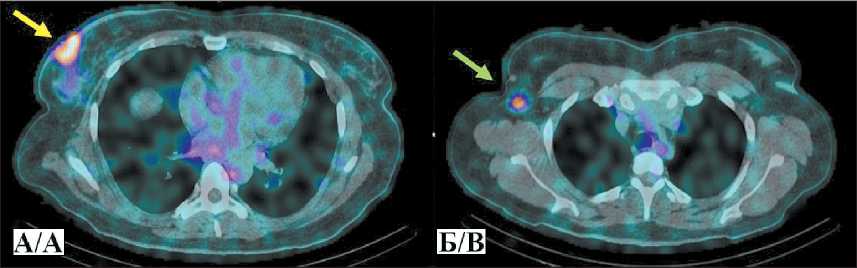
Рис. 3. ОФЭКТ/КТ органов грудной клетки больной Д. через 2 ч после инъекции [99mTc]Tc-DB8 в дозировке протеина 80 мкг: А – желтая стрелка указывает на первичную опухоль; Б – зеленая стрелка указывает на метастатический аксиллярный лимфоузел.
Примечание: рисунок выполнен авторами
Fig. 3. Chest SPECT/CT performed 2 hours after injection of [99mTc]TcDB8 at a protein dose of 80 μg: A – yellow arrow indicates the primary tumor; B – green arrow indicates the metastatic axillary lymph node. Note: created by the authors
марте 2025 г. после обследования по поводу образования правой молочной железы, был верифицирован рак правой молочной железы. Гистологическое заключение: инвазивная протоковая карцинома, степень злокачественности – G2. ИГХ: рецептор эстрогена – 6 баллов, рецептор прогестерона – 5 баллов, HER2/neu – отрицательный (1+), Ki67 – 37 %, что соответствует люминальному B молекулярному подтипу. При УЗИ регионарных лимфатических узлов в аксиллярной области выявлен гипоэхогенный лимфоузел с утолщением коркового слоя, после чего проведена тонкоигольная аспирационная биопсия, метастатическое поражение лимфоузла подтверждено цитологически.
По данным остеосцинтиграфии, выполненной в марте 2025 г., в проекции тел L2, L3, L4, L5, S1, S2, седалищной и подвздошной костей, заднего отрезка VII ребра справа определялись участки гиперфиксации радиофармпрепарата 99mTc-Пирофосфата.
Окончательный диагноз поcле завершения обследования: Рак правой молочной железы, IV
(cT1N1M1) стадия. Пациентка направлена в НИИ онкологии ТНИМЦ для однофотонной эмиссионной компьютерной томографии, по результатам которой через 2 ч после внутривенного введения [99mTc] Tc-DB8 в дозе протеина 80 мкг зарегистрировано интенсивное накопление препарата в первичной опухоли, метастатическом аксиллярном лимфатическом узле (SUVmax ПО=3,45, SUVmax мЛУ=2,52) (рис. 3), а также в проекции L2-L5 (SUV =3,06), S1, S2 (SUVmax=5,92), подвздошной (SUVmamxa=x 3,48) и седалищной (SUVmax=5,97) костей справа, заднего отрезка VII ребра справа (SUVmax=1,54) (рис. 4). При анализе результатов компьютерной томографии на снимках определялись участки литической деструкции в телах L2, L3, L4 с формированием патологического компрессионного перелома, а также в L5, S1, S2, в подвздошной и седалищной костях, в заднем отрезке VII ребра справа.
По результатам онкологического консилиума принято решение начать лечение с курсов полихимиотерапии на первом этапе. В настоящее время
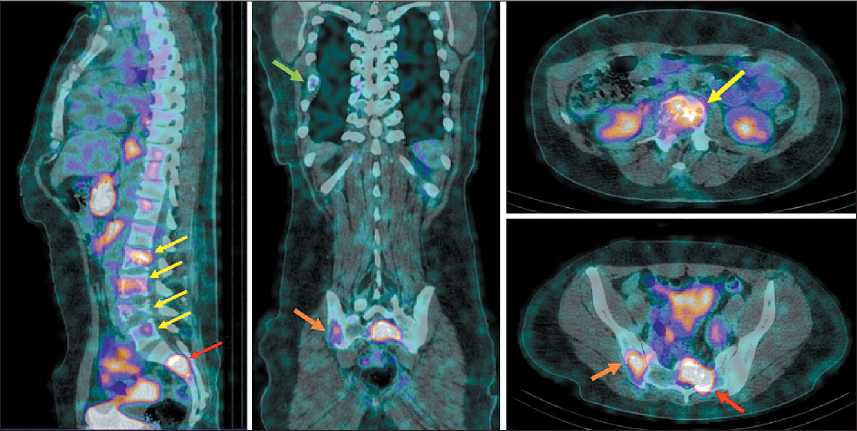
Рис. 4. ОФЭКТ/КТ больной Д. через 2 ч после инъекции [99mTc]Tc-DB8 в дозировке протеина 80 мкг. Стрелками отмечены участки гиперфиксации РФЛП в проекции тел LII-LV (желтая стрелка), S1-SII (красная стрелка), подвздошной и седалищной костей справа (оранжевая стрелка), заднего отрезка VII ребра справа (зеленая стрелка). Примечание: рисунок выполнен авторами
Fig. 4. SPECT/CT performed 2 hours after injection of [99mTc]TcDB8 at a protein dose of 80 μg. The arrows indicate areas of increased radiopharmaceutical uptake in the projection of the L2–L5 vertebral bodies (yellow arrow), S1–S2 vertebral bodies (red arrow), the right ilium and ischium (orange arrow), and the posterior segment of the 7th rib on the right (green arrow). Note: created by the authors
пациентка продолжает назначенное лечение на базе ТООД.
Обсуждение
Люминальный рак молочной железы характеризуется наиболее высокой частотой метастазирования в костную ткань, что оказывает существенное влияние на прогноз у данной категории больных, в связи с чем своевременная диагностика костных метастазов приобретает особую важность [1–5]. Поскольку традиционные методы диагностики (остеосцинтиграфия, магнитно-резонансная, компьютерная томография и позитронно-эмиссионная томография) обладают ограниченной чувствительностью в визуализации метастатических очагов и сопряжены с необходимостью многоэтапного обследования, это затрудняет выбор персонализированного подхода к лечению и повышает риск назначения недостаточно оптимальных схем терапии [6–13]. В связи с этим возникает необходимость в разработке более чувствительных методик, способных обеспечить точную оценку распространенности опухолевого процесса. Такие диагностические возможности предоставляет таргетная радионуклидная визуализация [14, 15]. Значимым достижением в области ядерной медицины стало выявление рецептора гастрин-высвобождающего пептида, поскольку


