Возможности эндоваскулярного лечения пациентов с окклюзией инфраренального отдела аорты
Автор: Жолковский Александр Владимирович, Ермоленко Вячеслав Владимирович, Боронджиян Тигран Сергеевич, Тимофеева Лариса Леонидовна, Чубаров Виталий Ервантович, Урусов Идар Анатольевич
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 1 (29), 2017 года.
Бесплатный доступ
Окклюзия терминального отдела аорты чаще всего обусловлена атеросклерозом и при развитии ишемии нижних конечностей требует оперативного лечения. Помимо открытой хирургии аорты могут также быть использованы реканализация и стентирование. В статье представлен первый опыт эндоваскулярного лечения больных с хорошими непосредственными и среднеотдаленными результатами. Данная методика целесообразна в использовании пациентам с противопоказаниями к общей анестезии.
Хроническая окклюзия брюшной аорты, эндоваскулярное лечение, реканализация, стентирование
Короткий адрес: https://sciup.org/143164623
IDR: 143164623
The quality of life in patients with coronary heart disease
Occlusion of terminal aorta is mostly often caused by atherosclerosis and the development of lower limb ischemia requires prompt treatment. In addition to the open aortic surgery recanalization and stenting can also be used. The article presents the first experience of endovascular treatment in patients with good immediate and mid-term results. This method is suitable to use in patients with contraindications to general anesthesia.
Текст научной статьи Возможности эндоваскулярного лечения пациентов с окклюзией инфраренального отдела аорты
Введение. Окклюзия инфраренального отдела аорты сопровождается типичным симп-томокомплексом, впервые описанным в 1923 г. R.Leriche [1]. При этом основной (88-94 %) причиной развития синдрома Лериша является атеросклероз [2, 3]. При развитии у больных с поражением терминального отдела аорты и подвздошных артерий ишемии нижних конечностей IIБ, III и IV степени по Фонтейну– Покровскому показано оперативное лечение в объеме резекции аорты с протезированием, аортобедренного шунтирования или экстраанатомических операций. При высокой окклюзии аорты часто необходимо выполнять тромбэктомию из интерренального сегмента аорты, что может потребовать более травматичного тора-кофреноперитонеального доступа [4]. По данным Покровского А.В. и соавт. 10-летняя выживаемость после реконструкции терминального отдела аорты составляет 61 % , что связывается с превалированием пациентов с мультифокальным атеросклерозом [5]. Несмотря на то, что традиционно данной категорией больных занимаются в отделениях сосудистой хирургии, развитие эндоваскулярных технологий в последние годы значительно меняет структуру вмеша- тельств, показаны хорошие непосредственные и отдаленные результаты стентирования подвздошных артерий [6]. Также появились отдельные публикации, посвященные эндоваскулярному лечению окклюзий аорты и подвздошных артерий [7].
Материал и методы. В 2008-2016 гг. 13 пациентов были прооперированы по поводу хронической окклюзии инфраренального отдела аорты и подвздошных артерий. Пациенты разделены на 3 группы: 1-я группа: 4 пациента в возрасте 47-70 лет (среднее – 59,3), которым было выполнено аортобедренное шунтирование/протезирование из срединной лапаротомии; 2-я группа: 5 больных 51-67 лет (среднее – 58), им реконструкция выполнена из мини-лапаротомного доступа; 3-я группа: 4 больных от 49 до 67 лет (средее – 56,5), которым выполнено эндоваскулярное лечение в объеме реканализации и стентирования. У всех больных анализировался характер поражения аорты, в т.ч. выявлялась высокая окклюзия с закрытием устья нижней брыжеечной артерии, исследовались артерий нижних конечностей для исключения многоэтажных поражений (дистальный блок), определялась степень хронической ишемии нижних конечностей и критическая ишемия (КИНК) – III и IV степень по Фонтейну-Покровскому). Также проводилось комплексное обследования для выявления сопутствующей патологии: клинически значимые формы ишемической болезни сердца (ИБС), дисциркуляторной энцефалопатии (ДЭП). По этим признакам существенных различий в характеристиках пациентов при ретроспективном анализе не выявлено (таблица 1), но в 3-й группе было 2 больных с хронической обструктивной болезнью легких (ХОБЛ) с противопоказаниями к эндотрахеальному наркозу.
Таблица 1
Характеристика больных до операции
|
Группа |
КХИНК |
Высокая окклюзия аорты |
Дисталь-ный блок |
ИБС |
ДЭП |
|
1 группа (4) |
3 |
2 |
3 |
2 |
1 |
|
2 группа (5) |
5 |
4 |
2 |
3 |
2 |
|
3 группа (4) |
3 |
3 |
2 |
2 |
- |
Всем пациентам 3-й группы выполнялась мультиспиральная компьютерно-томографическая ангиография для планирования вмешательства (рис.1).
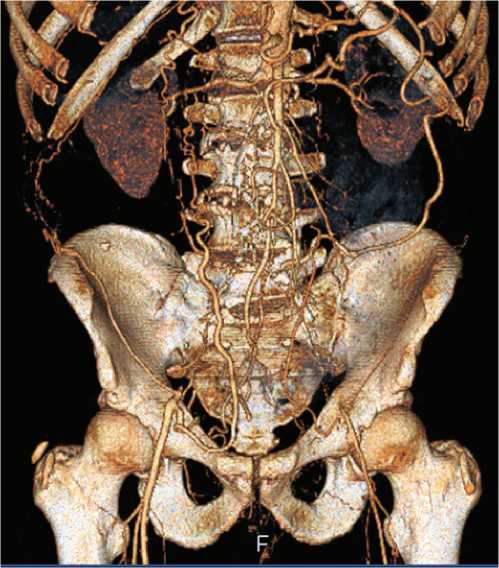
Рис. 1. МСКТ – ангиография субренальной окклюзии аорты и подвздошных артерий
Операции в 1 и 2 группе выполнялись под эндотрахеальным наркозом, в ходе лапаротомии (длиной 27-30 см в 1-й группе и 8-14 см – во 2-й группе), выделялся субренальный отдел аорты и устья почечных артерий, выполнялась перевязка аорты над бифуркацией в 1-й группе, либо полное поперечное пересечение во 2-й (рис. 2); тромбэктомия с формированием проксимального анастомоза бифуркационного протеза соответственно конец-в-конец или конец-в-бок. Бранши протеза проводились забрюшинно к доступам на бедрах, где формировались дистальные анастомозы с общими бедренными артериями.
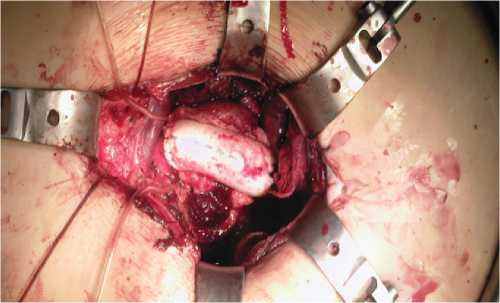
Рис. 2. Протезирование аорты из минилапаротомного доступа
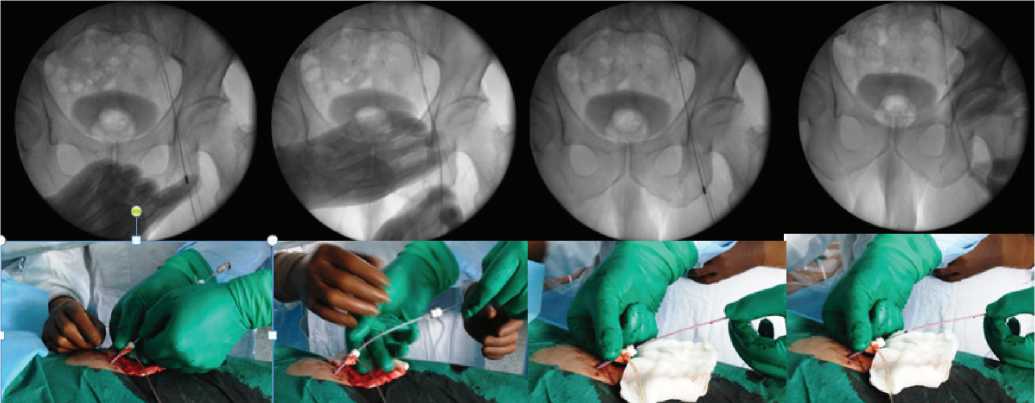
Рис. 3. Экстернализация гидрофильного проводника
Операции в 3-й группе выполнялись у 3 из 4 больных под спинномозговой анестезией, начинались с пункции и катетеризации плечевой артерии, проведением катетера в нисходящую и брюшную аорту, антеградной реканализации инфраре-нальной аорты и левой подвздошной артерии с использованием гидрофильного 0,035 проводника HiWi («COOK», США) ретроградной пункции левой и правой общей бедренных артерий (в 3 из 4 случаев) под ультразвуковым наведением.
Экстернализация проводника, необходимая для усиления поддержки и сохранения просвета реканализированного сегмента, потребовалась у 3 из 4 пациентов и проводилась путем проведения гидрофильного проводника под рентгеноскопическим контролем через ретроградно установленный интродьюсер диаметром 7 French и коаксильно проведенный в его клапан интро-дьюсер диаметром 5 French (рис.2), ретриверы не использовались.
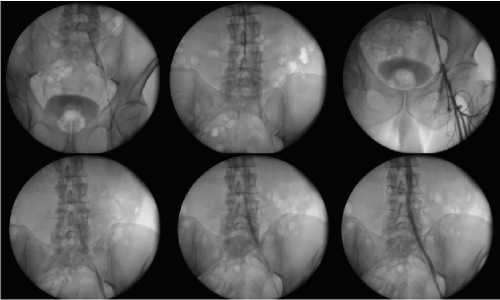
Рис. 4. Ангиографическое изображение этапов реканализации аорты и подвздошной артерии
В дальнейшем проводилась замена проводника на жесткий диагностический, баллонная ангиопластика, последовательная имплантация нитиноловых стентов и их постдилатация.
Ретроспективно были проанализированы особенности вмешательства, длительность пребывания в отделении реанимации, объем крово-
Таблица 2
|
Группа |
П/о - к/д (средн.) |
АРО, час (средн.) |
Крово-потеря, мл (сред.) |
Гемотрансфузия (средн.) мл |
|
1 группа (4) |
13-21 (15,5) |
16-288 (84) |
500-2000 (950) |
0-1500 (950) |
|
2 группа (5) |
10-17 (13,4) |
15-17 (16) |
300-1200 (710) |
0-640 (313) |
|
3 группа (4) |
5-7 (6) |
4-6 (4,8) |
0-200 (125) |
0 |
Таблица 3
|
Пациент |
ХИНК, ст. |
Бифуркация |
Рост, см |
Количество ВО и диаметр стентов |
|
№ 1 |
III |
- |
176 |
3: 10,9, 8 мм |
|
№ 2 |
II Б |
да |
178 |
4: 10, 9, 8 мм |
|
№ 3 |
III |
да |
172 |
4: 12,10, 9 мм |
|
№ 4 |
IV |
- |
188 |
4: 12, 10, 9, 8 мм |
потери, гемотрансфузии, длительность госпитализации после операции, отдаленная проходимость, повторные вмешательства.
Результаты и обсуждения
Течение периоперационного периода отличалось во всех группах.
У одного из пациентов 1-й группы в связи с прорезыванием швов возникло кровотечение, потребовавшее массивных гемотрансфузий и длительного пребывания в анестезиологореанимационном отделении (АРО). У пациентов 2-й группы функция кишечника восстанавливалась самостоятельно на вторые сутки, в то время как у большинства (3 из 4) больных 1-й группы требовалась полная его стимуляция на 2-3 сутки. Пребывание пациентов 3-й группы было менее продолжительным и обуславливалось необходимостью ликвидации спинального блока. У одного пациента 2-й группы с ХОБЛ возникла пневмония в послеоперационном периоде, потребовавшая антибактериальной терапии в течение 7 суток. Послеоперационный койко-день (П/о к/д), пребывание в АРО, кровопотеря, объем гемотрансфузии отражены в таблице 2.
В ходе операций в 3-й группе, в 2-х случаях из 4-х, помимо аорты была реканализирована только левая подвздошная артерия (1 – запланировано, 1 – из-за невозможности ретроградной реканализации), имплантировались нити-ноловые стенты, рентгеноконтрастный препарат вводился вручную в объеме 250-320 мл, не отмечено нарушения функции почек и местных осложнений в местах доступов (гематом). Особенности вмешательств в этой группе отражены в таблице 3.
У всех пациентов ишемия была купирована. Проходимость реконструированных сегментов контролировалась ультразвуковым дуплексным сканированием при выписке, а также через 3, 6 и 12 месяцев, затем – по клиническим показаниям. 2 пациентам из 3-й группы для уточнения результатов стентирования выполнялась контрольная МСКТ – ангиография (рис. 5).
Пациенты 1-й и 2-й групп принимали вар-фарин (4 из 9) или препараты ацетилсалициловой кислоты. Пациентам 3-й группы назначалась стандартная двойная антиаггрегантная терапия на 6 месяцев с последующим переходом на аспирин.
В 1-й группе в сроки наблюдения 39-60 месяцев (средн. – 54,8): 1 пациент дважды (через 32 и 43 месяца после первой операции) оперирован по поводу тромбоза протеза аорты на фоне пароксизмальных нарушений ритма, с третьим
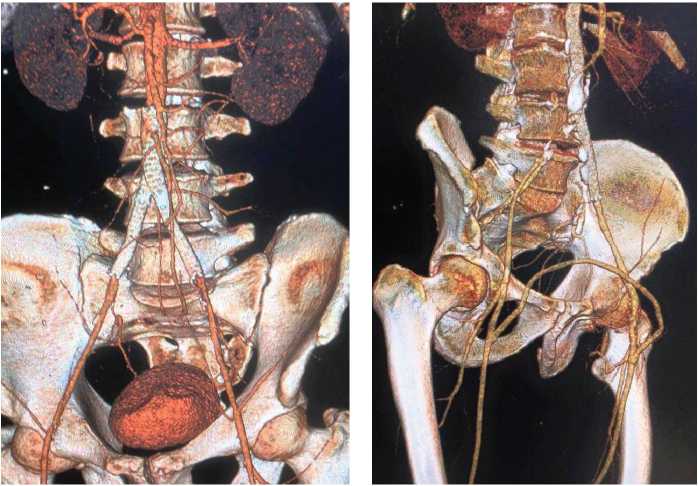
Рис. 6. Результат реканализа ции и унилатерального стентирования аорты и левой подвздошной артерии и отсроченного перекрестного бедренно-бедренного аутовенозного шунтирования
Рис. 5. Результат реканализации и бифуркационного стентирования аорты повторным тромбозом и рецидивом ишемии конечности; 1 пациент скончался от инфаркта миокарда чрез 3 года после операции на аорте.
Во 2-й группе в сроки наблюдения от 3 до 60 месяцев (средн. – 31,8) 1 пациент оперирован по поводу острой спаечной тонкокишечной непроходимости через 6 месяцев после операции из мини-доступа.
В 3-й группе в сроки наблюдения от 3 до 37 месяцев (средн. – 19,3): 1 пациент сразу после выписки самостоятельно прекратил прием анти-аггрегантов и через 35 дней был экстренно госпитализирован с рецидивом критической ишемии и реокклюзией аорты и левой подвздошной артерии. Ему была успешно выполнена эндоваскулярная операция – баллонная ангиопластика, регионарный тромболизис с восстановлением просвета сосудов; 1 пациенту через 18 месяцев после реканализации и стентирования аорты и левой подвздошной артерии планово выполнено перекрестное бедренно-бедренное аутовенозное шунтирование слева-направо по поводу хронической ишемии правой нижней конечности II Б ст. (рис. 6).
Заключение. Первый опыт эндоваскулярного лечения окклюзий инфраренального отдела брюшной аорты показал высокий процент технического успеха при унилатеральном решении, хорошие непосредственные и среднеотдаленные результаты, отсутствие кровопотери, нарушений функции почек, короткий период пребывания пациента в отделении реанимации и стационара, возможность выполнения повторных опе- раций и реализации гибридного подхода. Отмечена необходимость строгого соблюдения схемы приема двойной антиаггрегантной терапии. Использование саморасширяющихся нитиноло-вых стентов, местной анестезии, наряду с вышеперечисленными особенностями, выгодно отли- чающими от операции открытого протезирования, делает эти операции по-видимому и экономически целесообразными, что требует отдельного анализа. Использование данной методики целесообразно у пациентов с противопоказаниями к общей анестезии.
Список литературы Возможности эндоваскулярного лечения пациентов с окклюзией инфраренального отдела аорты
- R. Leriche. Des obliterations arterielles hautes (obliteration de la terminaiso de l`aorte) comme cause des insuffisances circulatoires des members inferieurs/Bull Mem Soc Chir (Paris) 1923; 49:1404-1406
- Шалимов А.А., Дрюк Н.Ф. Хирургия аорты и магистральных артерий. Киев: Здоровье. 1979. 346 с.
- Покровский А.В. Клиническая ангиология. М.: Медицина, 1979. 400 с.
- Покровский А.В. Клиническая ангиология Т.2: Руководство/Под ред. А.В. Покровского. М.: ОАО «Издательство «Медицина», 2004. 888 с: ил. ISBN 5-225-04857-9
- Покровский А.В., Зотиков А.Е., Перспективы и действительность в лечении атеросклеротических поражений аорты. М.: BGC. 1996 г. 534 c.
- Cuong Lam; Ripal T Gandhi; Geogy Vatakencherry, et al. Iliac Artery Revascularization Overview of Current Interventional Therapies Katzen Interventional Cardiol. 2010;2(6):851-859
- Moise MA, Alvarez-Tostado JA, Clair DG, Greenberg RK, et.al. Endovascular Management of Chronic Infrarenal Aortic Occlusion. J Endovasc Ther. 2009 Feb;16(1):84-92 DOI: 10.1583/08-2526.1


