Возможности магнитно-резонансной томографии сердца в дифференциальной диагностике острого коронарного синдрома у пациентов с необструктивным атеросклерозом коронарных артерий
Автор: Гомбоева Саяна Баировна, Рябов Вячеслав Валерьевич, Шелковникова Татьяна Александровна, Усов Владимир Юрьевич, Баев Андрей Евгеньевич
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.32, 2017 года.
Бесплатный доступ
Цель исследования: оценить возможности магнитно-резонансной томографии (МРТ) сердца в дифференциальной диагностике острого коронарного синдрома (ОКС) у пациентов с необструктивным коронарным атеросклерозом (НОКА). Материал и методы. Проводимое исследование нерандомизированное, открытое, контролируемое. Зарегистрировано на ClinicalTrials.gov: NCT02655718. Мы представляем результаты субанализа исследования, который включает данные пациентов с ОКС, госпитализированных в отделение неотложной кардиологии (ОНК) в 2015-2016 гг. Критерии включения: 1. Клиника ОКС. 2. НОКА (нормальные коронарные артерии / атеросклеротические бляшки
Острый коронарный синдром, необструктивный коронарный атеросклероз, магнитно-резонансная томография сердца
Короткий адрес: https://sciup.org/14920297
IDR: 14920297 | УДК: 616-12-008.
Capabilities of cardiac magnetic resonance imaging in the differential diagnosis of acute coronary syndrome in patients with nonobstructive coronary atherosclerosis
The aim of the study was to evaluate the capabilities of cardiac MRI in the differential diagnosis of acute coronary syndrome (ACS) in patients with nonobstructive coronary atherosclerosis. Material and Methods. This non-randomized open controlled study was registered on ClinicalTrials.gov: NCT02655718. This article presents the results of the subanalysis of the study. Analysis included data of ACS patients admitted to the Emergency Department of Cardiology Research Institute in 2015-2016. Inclusion criteria were nonobstructive coronary atherosclerosis (normal coronary arteries / plaques
Текст научной статьи Возможности магнитно-резонансной томографии сердца в дифференциальной диагностике острого коронарного синдрома у пациентов с необструктивным атеросклерозом коронарных артерий
Актуальность
Ранняя инвазивная стратегия лечения пациентов с ОКС выявила проблему увеличения частоты обнаружения клинических случаев, в которых морфологическим субстратом ОКС является невыраженный атеросклероз коронарных артерий или его отсутствие [1–3]. Согласно результатам мета-анализа 28 публикаций, распространенность этих случаев составляет 6% (95% CI, 5–7%) [4].
Эксперты Европейского общества кардиологов предлагают ввести понятие Myocardial infarction with nonobstructive coronary atherosclerosis – MINOCA, которое является “рабочим” диагнозом, аналогично понятию сердечной недостаточности – ОКС. Предпосылкой к внедрению данного определения явилась необходимость дообследования пациентов для выявления ведущих причин развития ОКС при НОКА [5]. Механизмы развития MINOCA могут быть как кардиальными, так и некардиальными, и требуют специфического лечения [6–7].
Высокая разрешающая способность МРТ сердца и возможность оценки функционального и структурного состояния миокарда позволяют говорить о высокой диагностической значимости его применения в дифференциальной диагностике ОКС у пациентов с НОКА и расценивать МРТ сердца как виртуальную биопсию миокарда [8].
В настоящее время усовершенствование методик визуализации МРТ сердца выявляет основные патофизиологические процессы в миокарде: отек, гиперемию и фиброз, что позволяет дифференцировать ишемические, воспалительные и генетические заболевания сердца [8].
Цель проводимого исследования: оценить возможности МРТ сердца в дифференциальной диагностике ОКС у пациентов с НОКА.
Материал и методы
Исследование утверждено локальным этическим комитетом НИИ кардиологии, Томский НИМЦ РАН, протокол №139 от 18.11.2015 г. Пациенты, включенные в исследование, подписали добровольное информированное согласие.
В проводимое исследование включены пациенты с клиникой ОКС [9] и НОКА (нормальные коронарные артерии / атеросклеротические бляшки <50%), подтвержденным инвазивной КАГ, старше 18 лет на момент рандомизации. Больные с ранее проведенной реваскуляризацией коронарных артерий были исключены из исследования.
Определены первичные конечные точки: госпитальная летальность, ОИМ [6], нестабильная стенокардия [9], синдром Такоцубо [10] и миокардит [11]. Смерть, рецидив инфаркта, инсульты, развитие сердечной недостаточности и повторные госпитализации в течение 6 мес. после выписки из стационара определялись как вторичные конечные точки.
Всем пациентам проводилась КАГ с целью оценки атеросклеротического повреждения коронарного русла, динамическое измерение количественного/качественного тропонина I, КФК, КФК–МВ с целью оценки закономерной динамики снижения кардиоспецифических ферментов.
Исследования сердца выполнялись на магнитно-резонансном томографе Vantage Titan (Toshiba) 1,5 Тл с ЭКГ-синхронизацией и получением изображений миокарда по короткой и длинной осям до и после введения контрастного препарата. Срезы выполнялись от верхушки до основания сердца толщиной 8 мм. Протокол МРТ-иссле-дования включал использование Т1-, Т2-взвешенных последовательностей и последовательности с подавлением сигнала от жировой ткани для визуальной оценки состояния миокарда (наличие области отека, жировой перестройки и т.д.), динамических SSFP последовательностей с задержкой дыхания для функционального исследования сердца, оценки его региональной и общей сократимости. Для определения характера контрастирования миокарда использовалась градиентная последовательность “инверсия–восстановление” (GR–IR) c получением изображений сердца в 2-, 4-камерных проекциях через 8–20 мин после внутривенного введения контрастного препарата.
Анализ полученных результатов проводился в программе STATISTICA 10. Сравнение между группами проводилось с использованием U-критерия Манна–Уитни и точного критерия Фишера. Значение р ≤ 0,05 рассматривалось как статистически значимое.
|
Таблица 1 Клиническая характеристика пациентов |
|||
|
Показатели |
Всего |
ОКСпST |
ОКСбпST |
|
Количество больных, n (%) |
23(100) |
11(48) |
12(52) |
|
Мужчины, n (%) |
17(73) |
7(41) |
10(59) |
|
Средний возраст, среднее ± стд. откл. |
55,7±9,4 |
54,9±10,4 |
56,5±8,8 |
|
Гипертоническая болезнь, n (%) |
19(83) |
9(47) |
10(53) |
|
Дислипидемия, n (%) |
15(65) |
7(47) |
8(53) |
|
Ожирение, n (%) |
8(35) |
2(25) |
6(75) |
|
Наследственность, n (%) |
8(34) |
4(50) |
4(50) |
|
Курение, n (%) |
12(52) |
4(33) |
8(67) |
|
Сахарный диабет, 2-й тип, n (%) |
3(13) |
1(33) |
2(67) |
|
ХБП, n (%) |
1(4) |
1(100) |
0 |
|
СКФ, среднее ± стд. откл., (мл/мин/1,73 м2) |
70,04±13,9 |
71,1±11,4 |
69±16,3 |
|
Атеросклероз, n (%) |
18(78) |
7(39) |
11(61) |
|
Стенозирующий, n (%) |
1(4) |
0 |
1(100) |
|
Стенокардия в анамнезе, n (%) |
12(52) |
5(42) |
7(58) |
|
Инсульт в анамнезе, n (%) |
2(9) |
0 |
2(100) |
|
Перенесенный ИМ, n (%) |
1(4) |
0 |
1(100) |
|
Врожденный порок сердца, n (%) |
3(13) |
1(33) |
2(67) |
|
Примечание: ХБП – хроническая болезнь почек, СКФ |
скорость клубочковой фильтрации, ОКСпST – |
ОКС с подъемом ST, ОКСбпST – |
ОКС без подъема ST. |
Таблица 2
Характеристика острого коронарного синдрома
|
Показатели |
Всего |
ОКСпST |
ОКСбпST |
р |
|
Шкала GRACE |
||||
|
Высокий риск, n (%) |
6(26) |
4(67) |
2(33) |
p>0,05 |
|
Средний риск, n (%) |
2(9) |
2(10) |
0 |
p>0,05 |
|
Низкий риск, n (%) |
15(65) |
5(33) |
10(67) |
p>0,05 |
|
Кардиоспецифические маркеры |
||||
|
Повышение ферментов при поступлении, n (%) |
13(57) |
8(62) |
5(38) |
p<0,05 |
|
Нет повышения ферментов при поступлении, n (%) |
10(44) |
2(20) |
8(80) |
|
|
КФК–МВ при поступлении |
Максимум, ед/л |
Минимум, ед/л |
||
|
1930 |
9 |
|||
|
Увеличение КФК–МВ в течение суток n (%) |
3(13) |
2(67) |
1(33) |
p>0,05 |
|
Вч. Тропонин I в течение первых суток |
Максимум, нг/мл |
Минимум, нг/мл |
||
|
7,71 |
0,01 |
|||
|
Повышение тропонина I в течение суток, n (%) |
17(74) |
8(47) |
9(53) |
p>0,05 |
|
Нет повышения тропонина I в течение суток, n (%) |
5(22) |
3(60) |
2(40) |
p>0,05 |
|
Время поступления в стационар от начала симптомов |
||||
|
6 ч от начала симптомов, n (%) |
10(43) |
6(60) |
4(40) |
p>0,05 |
|
6–24 ч, n (%) |
8(35) |
4(50) |
4(50) |
p>0,05 |
|
Более 24 ч, n (%) |
5(22) |
1(20) |
4(80) |
p>0,05 |
|
Инвазивная стратегия |
||||
|
КАГ в течение 2 ч, n (%) |
4(17) |
4(100) |
0 |
p>0,05 |
|
КАГ в течение 24 ч, n (%) |
10(43) |
2(20) |
8(80) |
p>0,05 |
|
КАГ в течение 72 ч, n (%) |
3(13) |
3(100) |
0 |
p>0,05 |
|
КАГ плановая, n (%) |
6(26) |
2(33) |
4(67) |
p>0,05 |
|
ТЛТ на догоспитальном этапе/эффективная, n (%) |
3/1(13/4) |
3/1(100/33) |
0 |
p>0,05 |
|
ТЛТ в стационаре/эффективная, n (%) |
2/2(9/9) |
1/1(50/50) |
1/1(50/50) |
p>0,05 |
|
Результаты коронарной ангиографии |
||||
|
Стеноз менее 50%, n (%) |
5(22) |
4(80) |
1(20) |
p>0,05 |
|
Стеноз менее 30%, n (%) |
6(26) |
2(33) |
4(67) |
p>0,05 |
|
Неизмененные коронарные артерии, n (%) |
12(52) |
5(42) |
7(58) |
p>0,05 |
|
Спазм коронарной артерии, n (%) |
1(4) |
1(100) |
0 |
p>0,05 |
|
Замедление коронарного кровотока выявлено/не выявлено, n (%) |
15/8(65/35) |
5/6(33/75) |
10/2(67/25) |
p>0,05 |
Примечание: КФК МВ – креатинфосфокиназа МВ, Вч. Тропонин I – высокочувствительный тропонин I, NKN – тромболитическая терапия.
Клиническая характеристика пациентов
В 2015–2016 гг. с клиникой ОКС в ОНК было госпитализировано 604 человека. В 23 (3,8%) случаях выявлен НОКА по результатам КАГ. В исследуемой группе пациентов преобладают мужчины – 17 (73%), средний возраст составил 56±9 лет. Клинико-анамнестические характеристики в обеих группах статистически не различались (p ≥ 0,05), таблица 1.
Риск госпитальных сердечно-сосудистых событий и смерти по шкале GRACE низкий у большинства пациентов – 15 (65%), повышение кардиоспецифических ферментов при поступлении отмечено у половины пациентов – 13 (57%). В группе с ОКСпST выявлено статистически значимое повышение уровня кардиоспецифических ферментов при поступлении. 10 (43%) больных госпитализировалось в течение первых 6 ч от начала заболевания, позднее поступление (6–24 ч/ ≥ 24 ч) характерно для пациентов с ОКСбпST – 4 (80%).
По результатам КАГ, интактные коронарные артерии выявлены у половины пациентов – 12 (52%). Замедление коронарного кровотока определялось у 15 (65%), выраженный спазм коронарной артерии до уменьшения просвета сосуда на 75% выявлен у 1 (9%) в группе с ОКСпST (табл. 2).
У пациентов с ОКСпST и ОКСбпST не было статистически значимой разницы в госпитальных исходах ОКС. 22 пациента выписано из стационара, один умер; у половины больных – 13 (56%) диагностирован ОИМ; у 3 (13%) пациентов диагностирована нестабильная стенокардия; псевдокоронарный вариант течения миокардита – у 7 (30%) человек (табл. 3).
Среднее количество дней, через которое проводилась МРТ сердца, от момента развития ОКС составило 10±6 дней (от 3 до 24 дней). Одному пациенту МРТ-исследова-ние не проведено из-за тяжести состояния, обусловлен- ного дыхательной недостаточностью и нестабильностью гемодинамики, второму не удалось выполнить инфузию контрастного вещества (КВ) из-за панической атаки. Среднее значение фракции выброса (ФВ) левого желудочка 59±9%.
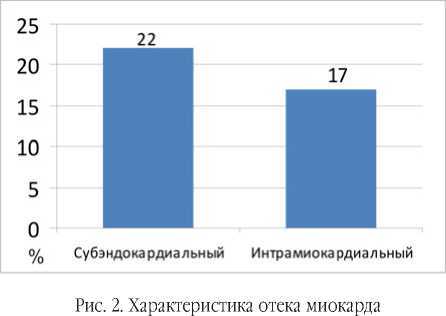
По полученным данным, усиление интенсивности Т2-сигнала, свидетельствующее об отеке миокарда, определяется у 39% человек, накопление контраста в раннюю фазу контрастирования/гиперемия – в 26%, в позднюю фазу/фиброз – в 96% (рис. 1). Субэндокардиальный отек выявлялся в 22%, интрамиокардиальный – в 17%, субэпикардиальный отек не визуализировался (рис. 2). Фиброз миокарда выявлялся в 96% случаев. В четверти случаев определялся интрамиокардиальный (26%) и в четверти случаев – сочетание субэндокардиального и интрамио-кардиального фиброза. В 17% выявлена комбинация субэпикардиального и интрамиокардиального накопления контраста в позднюю фазу контрастирования (рис. 3).
Все пациенты получали стандартную терапию ОКС согласно национальным рекомендациям: двойную дезаг-регантную терапию (100%), бета-адреноблокаторы (96%), статины (91%), ингибиторы ангиотензинпревращающе-го фермента (70%) или сартаны (17%), нефракциониро-ванный гепарин (91%) с последующим переводом на низкомолекулярные гепарины (78%). Необходимость в инотропной поддержке дофамином, внутриаортальной баллонной контрпульсации была у 4% (1) пациентов. Терапия корректировалась согласно результатам клиникоинструментального исследования.
Обсуждение
В группе исследуемых больных распространенность НОКА составляет 3,8%, что несколько ниже результатов мета-анализа 28 публикаций, где распространенность
Таблица 3
Диагноз больных при выписке из стационара
|
Показатели |
Всего |
ОКСпST |
ОКСбпST |
p |
|
Пациенты, n(%) |
23(100) |
11(48) |
12(52) |
|
|
ОИМ, n (%) |
13(56) |
7(54) |
6(46) |
p>0,05 |
|
С подъемом ST, n (%) |
5(22) |
5(100) |
о |
|
|
Без подъема ST, n (%) |
8(35) |
2(25) |
6(75) |
|
|
Нестабильная стенокардия, n (%) |
3(13) |
1(33) |
2(67) |
p>0,05 |
|
Миокардит, n (%) |
7(30) |
3(43) |
4(57) |
p>0,05 |
|
Псевдокоронарный вариант, n (%) |
7(30) |
3(43) |
4(57) |
|
|
Миокардит+ возможный АФС, n (%) |
2(9) |
2(100) |
0 |
|
|
ОИМ + миокардит, n (%) |
1(4) |
1(100) |
0 |
|
|
Миокардит + ТЭЛА, n (%) |
1(4) |
0 |
1(100) |
|
|
Миокардит + ФП, n (%) |
2(9) |
0 |
2(100) |
|
|
Врожденный порок сердца, n (%) |
3(13) |
1(33) |
2(67) |
p>0,05 |
|
Смерть, n (%) |
1(4) |
1(100) |
0 |
p>0,05 |
|
ТЭЛА, n (%) |
1(4) |
0 |
1(8) |
p>0,05 |
|
Гипертоническая болезнь, n (%) |
21(91) |
10(48) |
11(52) |
p>0,05 |
|
Тромбоз вен нижних конечностей, n (%) |
1(4) |
0 |
1(100) |
p>0,05 |
|
Рак легких, n (%) |
1(4) |
1(100) |
0 |
p>0,05 |
Примечание: АФС – антифосфолипидный синдром, ТЭЛА – тромбоэмболия легочной артерии, ФП – фибрилляция предсердий.
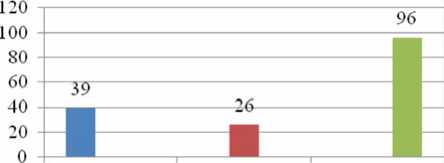
У сипение ПС в Накоппениев Накоппениев Т2-ВПотек EGE гиперемия LGE/фпброз
Рис. 1. Характеристика МРТ сердца
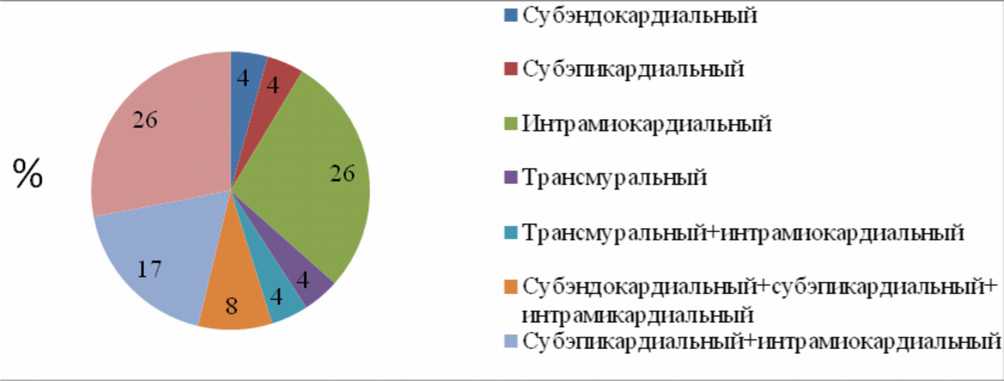
■ Субэндокардиальный
■ Субэпикардиальный
■ I 1нтр ам! юкард! 1ал ьнып
■ Трансмуральный
■ Трансмур ал ьнып+i играм! юкард! мл ьнып
■ Су бэнд окар Д11ал ьный+су бэт жар Д11альный+
I штрам! жард] ьал ьнып
■ Субэго жар Д11ал ьнып+i шц) акп юкард! мл ьнып
Рис. 3. Характеристика фиброза миокарда
MINOCA составляет 6% (ДИ 95%, 5–7%). Средний возраст больных составил 56±9 лет, что сопоставимо с данными S. Pasupathy et al., 2015. Доля женщин составила 27%, что ниже ранее полученных данных – 40% [4].
По результатам сравнительных исследований, которые включали пациентов с MINOCA и ИМ и обструктивным коронарным атеросклерозом (ОКА), выявлено, что пациенты с MINOCA менее склонны к дислипидемии по сравнению с пациентами с ИМ с ОКА: 21% (95% доверительный интервал, 6–35%) против 32% (95% доверительный интервал, 30–59%) соответственно. Другие сердечно-сосудистые факторы, в том числе артериальная гипертензия, сахарный диабет, курение, отягощенный семейный анамнез сходны в группах с MINOCA и ИМ ОКА [4]. По результатам мета-анализа G.M. De Ferrari et al. (2014), пациенты с MINOCA реже страдали сахарным диабетом, заболеваниями периферических сосудов или ишемической болезнью в анамнезе, что соответствует полученным данным: стенокардии (52%), перенесенного ИМ (4%), инсультов (9%) [12].
Высокая разрешающая способность, возможность оценки анатомических структур и функционального состояния сердца и миокарда определяют пользу внедре- ния в рутинную клиническую практику МРТ сердца для выявления ведущих причин развития ОКС у пациентов с НОКА. Возможность выявления отека, гиперемии и фиброза миокарда позволяет определить как ишемические, так и неишемические причины повреждения миокарда [13–17].
Повреждение миокарда ишемического генеза характеризуется его отеком и формированием очага некроза, соответствующего бассейну кровоснабжения определенной коронарной артерии [15–17]. Отек миокарда в острую фазу инфаркта может быть визуализирован в виде субэндокардиального усиления интенсивности сигнала в Т2-взвешенных изображениях, определяемым как “myocardium at risk”. Преимуществом этого метода является возможность дифференцировать ОИМ от постинфарктного кардиосклероза. Позднее накопление контраста на Т1-взвешенных изображениях в режиме инверсия– восстановление наблюдается при необратимых изменениях в миокарде – фиброзе/некрозе. Данный феномен позволяет дифференцировать постинфарктный некроз, локализующийся субэндокардиально или трансмураль-но (рис. 4), от фиброза неишемического генеза, при котором отмечается интрамуральное или субэпикардиаль-
MPT критерии ИМ:
-
> Локальное усиление Т2-сигнала/отек (позволяет дифференцировать ОИМ от перенесенного)
-
> Субэндокардиальное/трансмуральное накопление КВ при позднем контрастировании/ рубец
RSNA, 2013,1383-1412
Рис. 4. Критерии Lake–Louise
Крит ерии Lake-Louise (при выявлении 2 из 3 критериев диагностируется миокардит):
-
1. Локальное /ди(|х|)узнос усиление интенсивности Т2-сигнала/отск (рис. 1)
-
2. Увеличение отношения интенсивности раннего Т1-сигнала от миокарда к сигналу от скелетных мышц /гиперемия
-
3. Повышенное накопление КВ на отсроченных Т1 -взвешенных изображениях/фиброз (рис. 2) Cajorio A.L., Pankuweit S., ArbustiniE, European Heart Journal, 2013: 34 (33): 2636-48.
Рис. 5. МРТ-критерии ИМ ное распределение контраста, или миокардит, при котором регистрируется субэпикардиальное или фокальное контрастирование [8, 13, 14]. При микрососудистой ангиопатии внутри зон накопления контраста может быть ослабление интенсивности сигнала, что вызвано обструкцией капилляров некротизированными клетками [8, 17].
По результатам КАГ у 7 (30%) пациентов выявлены интактные коронарные артерии и увеличение кардио-специфических ферментов. Применение МРТ сердца у этой группы больных позволило определить наличие ишемических изменений в миокарде и поставить диагноз ОИМ 2-го типа. По МРТ сердца визуализировалась картина субэндокардиального усиления Т2-сигнала в сочетании с субэндокардиальным, субэпикардиальным и интрамиокардиальным накоплением контраста в позднюю фазу накопления в 1 (4%) случае.
Раннее накопление контраста субэндокардиально в сочетании с поздним субэпикардиальным и интрамио-кардиальным накоплением отмечено у 1 (4%) пациента, субэндокардиальное и интрамиокардиальное позднее накопление выявлено в 1 (4%) случае, субэндокардиальное позднее контрастирование – в 1 (4%), интрамиокар-диальное позднее накопление КВ – в 2 (8%). У всех этих пациентов имелись некоронарогенные причины повреждения миокарда, такие как пароксизм фибрилляции предсердий, гипертрофия левого желудочка, эритроцитоз в периферической крови, развитие ишемии на фоне коро-нариита в результате миокардита. У одного пациента ОИМ развился на фоне паранеопластического синдрома, подтвержденного на аутопсии.
При повреждении миокарда воспалительного генеза на МРТ выявляется усиление интенсивности Т2-сигнала. Для данного феномена характерно мезо- или субэпикардиальное распределение, и встречается оно только у 7 (30%) пациентов [13, 14]. Раннее накопление КВ на Т1- взвешенных изображениях, локализованное интрамио-кардиально или субэпикардиально, свидетельствует о гиперемии миокарда при острых воспалительных заболеваниях. Согласно разработанным Lake–Louise критериям (рис. 5), наличие 2 из 3 феноменов является диагностическим признаком для миокардита [11]. У 2 (8%) пациентов был выставлен диагноз миокардита на основании МРТ-критериев.
В настоящее время эндомиокардиальная биопсия является “золотым стандартом” диагностики миокардита, позволяя определить патофизиологические процессы в миокарде согласно дополненному определению A.L.P. Caforio еt al., миокардит верифицируется при обнаружении ≥ 14 лейкоцитов в 1 мм2 биоптата, в том числе до 4 моноцитов в 1 мм2, 7 и более CD 3+ T-лимфоцитов в 1 мм2. Однако, принимая во внимание возможные осложнения манипуляции, такие как гемотампонада, нарушения ритма и проводимости сердца, тромбоэмболические осложнения, показания к ее проведению ограничены [11].
По результатам клинико-инструментальных исследований, у 7 (30%) пациентов было подозрение на миокардит. По МРТ сердца визуализировалось интрамиокарди-альное и субэпикардиальное накопление КВ при отсроченном контрастировании у 3 (13%) пациентов, интра-миокардиальное усиление Т2-сигнала в сочетании с инт-рамиокардиальным накоплением КВ в позднюю фазу контрастирования – у 1 (4%); субэндокардиальное и интра-миокардиальное распределение КВ при позднем контрастировании – у 1 (4%); субэндокардиальное усиление Т2-сигнала в сочетании с субэндокардиальным, субэпикардиальным и интрамиокардиальным накоплением в позднюю фазу контрастирования – у 1 (4%); субэндокардиальное усиление Т2-сигнала в сочетании с субэндокардиальным накоплением в раннюю фазу контрастирования и интрамиокардиальным накоплением при отсроченном контрастировании – у 1 (4%) пациента.
По результатам эндомиокардиальной биопсии миокарда у 6 (26%) пациентов подтвержден вирусный миокардит. При иммунногистохимическом исследовании биоптатов миокарда выявлена экспрессия ВПГ-6, цитомегаловируса, энтеровируса и вируса Эпштейна–Барра. У 1 (4%) миокардит не подтвердился, по МРТ сердца у него выявлены признаки ОИМ в сочетании с интрамуральным и субэпикардиальным фиброзом миокарда.
Принимая во внимание полученные данные, есть основание говорить о пользе применения МРТ сердца в дифференциальной диагностике ОКС у пациентов с НОКА.
Выводы
Доля пациентов с ОКС и НОКА, госпитализированных в ОНК с ноября 2015 г. по май 2016 г., составляет 3,8%. Эти больные представляют гетерогенную группу пациентов с ОИМ, миокардитом, ТЭЛА, нестабильной стенокардией, гипертонической болезнью.
Возможности МРТ сердца визуализировать миокард позволяют безопасно применять его в дифференциальной диагностике ОКС у пациентов с НОКА.
Список литературы Возможности магнитно-резонансной томографии сердца в дифференциальной диагностике острого коронарного синдрома у пациентов с необструктивным атеросклерозом коронарных артерий
- Гомбожапова А.Э., Роговская Ю.В., Рябова Т.Р. и др. Случай псевдокоронарного варианта клинического течения воспалительной вирусной кардиомиопатии//Сиб. мед. журн. (Томск). -2015. -Т. 30(4). -С. 60-65.
- Planer D., Mehran R., Ohman E.M. et al. Prognosis of рatients with non-ST-segment-elevation myocardial infarction and nonobstructive coronary artery disease propensity-matched analysis from the acute catheterization and urgent intervention triage strategy trial//Circulation. -2014. -Vol. 7. -P. 285-293.
- Tornvall P., Gerbaud E., Behaghel A. et al. Myocarditis or "true" infarction by cardiac magnetic resonance in patients with a clinical diagnosis of myocardial infarction without obstructive coronary disease//Atherosclerosis. -2015. -Vol. 241(1). -P. 87-91.
- Pasupathy S., Air T.M., Dreyer R.P. et al. Systematic Review of Patients Presenting With Suspected Myocardial Infarction and Nonobstructive Coronary Arteries//Circulation. -2015. -Vol. 131. -P. 861-870.
- Agewall S., Beltrame J.F., Reynolds H.R. et al. ESC working group position paper on myocardial infarction with non-obstructive coronary arteries//Eur. Heart J. - (дата обращения 24.11.2016) DOI: 10.1093/eurheartj/ehw149
- Третье универсальное определение инфаркта миокарда//Рос. кардиол. журн. -2013. -№ 2(100).
- Pasupathy S., Tavella R., Beltrame J.F. The What, When, Who, Why, How and Where of Myocardial Infarction with Non-Obstructive Coronary Arteries (MINOCA)//Circulation. -2016. -No. 80. -P. 11-16.
- Rajiah P., Desai M.Y., Kwon D. et al. MR Imaging of Myocardial Infarction//RSNA. -2013. -P. 1383-1412.
- Roffi M., Patrono C., Collet J.P. et al. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation //Eur. Heart J. -2015. - DOI: 10.1093/eurheartj/ehv320
- Pilgrim T.M., Wyss T.R. Takotsubo cardiomyopathy or transient left ventricular apical ballooning syndrome: A systematic review//Int. J. Cardiol. -2008. -No. 124(3). -P. 283-292.
- Caforio A.L., Pankuweit S., Arbustini E. et al. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases//Eur. Heart J. -2013. -No. 34(33). -P. 2636-2648.
- De Ferrari G.M., Fox K.A., White J.A. et al. Outcomes among non-ST-segment elevation acute coronary syndromes patients with no angiographically obstructive coronary artery disease: observations from 37,101 patients//Eur. Heart J. Acute Cardiovasc. Care. -2014. -Vol. 3(1). -P. 37-45.
- Esposito A., Francone M., Faletti R. Lights and shadows of cardiac magnetic resonance imaging in acute myocarditis//Insights Imaging. -2016. -No. 7. -P. 99-110.
- Ferreira V.M., Piechnik S.K., Dall’Armellina E. T1-mapping for the diagnosis of acute myocarditis using CMR//JACC Cardiovasc. Imaging. -2013. -No. 6(10). -P. 1048-1058.
- Herzog B., Greenwood J., Plein S. CMR Pocket Guide, 2013 . -URL: https://www.escardio.org/static_file/Escardio/Subspecialty/EACVI/CMR-guide-2013.pdf (дата обращения 01.12.2016).
- Mulia E., Wicaksono S.H., Kasim M. Role of cardiac MRI in acute myocardial infarction//Med. J. Indones. -2013. -Vol. 22. -P. 46-53.
- Стукалова О.В., Староверов И.И., Жукова Н.А. и др. Магнитно-резонансная томография сердца у больных инфарктом миокарда//Кубанский научн. мед. вестн. -2010. -№ 6. -С. 134-139.


