Возможности повышения периоперационной безопасности пациентов при раке толстой кишки
Автор: Карсанов А.М., Маскин С.С., Слепушкин В.Д., Карсанова Ф.Д., Дербенцева Т.В., Худиева Э.М.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.10, 2015 года.
Бесплатный доступ
Представлены результаты внедрения концепции периоперационой безопасности пациентов с раком толстой кишки, основными элементам которой являлась комплексная профилактика инфекций области хирургического вмешательства и эскалация мер профилактики венозных тромбоэмболических осложнений на основе протокола ускоренного восстановления. В результате было достигнуто сокращение продолжительности лечения до 8,9 против 13,1 дней, частоты послеоперационных осложнений с 26,9% до 14,8%, а хирургических с 11,7% до 3,5%.
Периоперационная безопасность, рак толстой кишки, хирургия, осложнения, раневая инфекция, венозная тромбоэмболия
Короткий адрес: https://sciup.org/140188453
IDR: 140188453
Opportunity increase perioperative safety with colon cancer surgery
The results of the introduction of the concept of perioperative patient safety with colon cancer, whose main elements are integrated prevention of infections and surgical site escalation prevention of venous thromboembolic complications based on the protocol of early recovery. The result was a shortening of the treatment achieved to 8.9 vs. 13.1 days, postoperative complications from 26.9% to 14.8% and from 11.7 surgical% to 3.5%.
Текст научной статьи Возможности повышения периоперационной безопасности пациентов при раке толстой кишки
Обеспечение хирургической безопасности пациентов должно быть основой оказания медицинской помощи. На фоне возрастающей потребности в хирургической помощи безопасность имеет ключевое значение в оценке ее эффективности. Многие национальные программы повышения безопасности хирургического лечения базируются на структурированной по видам осложнений системе профилактики, позволяющей, при соблюдении определенных стандартов, предотвратить половину всех послеоперационных осложнений (ПО) и случаев смерти [7].
Рак толстой кишки (РТК), занимая 2–3-е место в общей структуре онкологической заболеваемости человека, имеет тенденцию стабилизации в индустриально-развитых и неуклонного роста в развивающихся странах [2, 13], являясь 4-й причиной канцерспецифичной смертности в мире [13].
Негативной тенденцией современности является то, что число первичных больных с осложненным течением рака не уменьшается, а в нашей стране даже увеличивается, что повсеместно является неблагоприятным фактором онкологического прогноза [2, 3]. Ввиду наличия у этих пациентов исходной полиморбидности даже отсроченное хирургическое лечение сопровождается ПО на уровне 26–37%, с летальностью 1–4%, с высокой долей (до 70%) инфекций области хирургического вмешательства (ИОХВ) и экстраабдоминальных осложнений [1, 3, 10].
В онкохирургии риск венозных тромбоэмболических осложнений (ВТЭО), в том числе фатальной тромбоэмболии легочной артерии (ТЭЛА), в 2–3 раза выше, чем в элективной хирургии доброкачественных заболеваний толстой кишки [8, 9]. Высокая вероятность, проблемы ранней диагностики венозного тромбоза (ВТ) и ТЭЛА, а также низкая эффективность лечебных мероприятий позволяют заключить, что самым главным в борьбе с ВТЭО является профилактика [8, 12], что однако не позволяет на практике полностью исключить риск возникновения послеоперационных ВТЭО и диктует необходимость поиска объективных критериев адекватности выбранной стратегии периоперационной профилактики ВТЭО [11, 12].
В качестве одной из современных доктрин, направленных на нивелирование последствий хирургической агрессии, в мировой практике широко апробируется модель с внедрением протокола ускоренного восстановления (ПУВ) после хирургии – «Fast track surgery» [10].
Цель исследования – изучение возможности реализации на практике целостной концепции периопера-ционой безопасности пациентов с компенсированной степенью нарушения кишечной проходимости при РТК, основными элементам которой являлась комплексная профилактика ИОХВ и эскалация мер профилактики ВТЭО.
Материал и методы
В основу работы положены результаты планового хирургического лечения 260 больных с компенсированной формой нарушения проходимости при РТК, оперированных открытым способом на клинических базах кафедры госпитальной хирургии Волгоградского ГМУ и Северо-Осетинской ГМА с 2007 по 2013 гг. Пациенты распределены на две группы сравнения. В основной группе

(115 больных) периоперационный комплекс лечебных мероприятий реализовывался на основе адаптированного варианта ПУВ и эскалации мер профилактики ВТЭО. В контрольной группе (145 больных) использовали традиционную методику ведения больных (табл. 1).
Пациенты исключались из исследования при условии: обструктивного характера операции, превентивного колостомирования, мультивисцеральных резекций и сочетанных операций (за исключением случаев, когда вторая операция относилась к I классу по Аltemeier), массивного канцероматоза брюшины, класса IV по оценке физического статуса по шкале Американского общества анестезиологов (ASA). Фактор трансфузии препаратов крови (ПК) признавался значимым только в случаях необходимости периоперационного использования двух и более доз.
В различных сочетаниях значимые сопутствующие заболевания имели место у 58,5% пациентов основной и у 62,7% контрольной групп (рис. 1).
В зависимости от частоты воспроизводимости в конкретном исследовании, компоненты ПУВ были нами отнесены к трем уровням. Уровень воспроизводимости (УВ) «А» включал мероприятия, воспроизведенные нами с частотой 81–100%; УВ «В» – 61–80%, УВ «C» – ≤ 60% от всех пациентов основной группы.
В результате на дооперационном этапе УВ «А» соответствовали: информирование и наставления (100,0%), введение низкомолекулярного гепарина (НМГ) эноксапарина по 40 мг за 12 часов до операции – 100%, внутривенное введение разовой дозы цефалоспоринов II–III поколения без антисинегнойной активности за 30 МИНУТ до разреза (100%), отказ от очистительных клизм и использование слабительных на основе многоатомных спиртов, пробиотиков, дюфалака (98%).
УВ “В” соответствовали: селективная деконтаминация с включением пероральной формы препаратов с антианаэробной активностью в день, предшествующий операции (76,5%), отказ от предоперационного голодания с разрешением пить богатые углеводами смеси для энтерального питания и прозрачные высококалорийные жидкости вплоть до 3-х часов до начала операции (71%), ультразвуковое компрессионное ангиосканирование (УЗАС) вен нижних конечностей (70,4%), создание адекватного режима регидратации путем инфузии кристаллоидов по 2 мл/кг/ч (61,7%).
УВ «С» соответствовали: прием перорального прокинетика в течение 5 дней до операции (50,4%), эхокардиография при сочетании нескольких факторов риска для выявления нефлебогенных потенциальных источников тромбоэмболов (10,4%).
На операционном этапе УВ «А» соответствовали: выполнение операции путем срединой лапаротомии (100%) (в контрольной группе 20,6% оперированы параректальным доступом), ограничение режима интраоперационно инфузируемой жидкости в виде инфузии по 5 мл/кг/ч (100%) (в контрольной группе все больные получали по
Табл. 1. Характеристики пациентов в группах сравнения
|
Параметры |
Основная n = 115 |
Контрольная n = 145 |
|
Стадия рака: II; III; IV (%) |
23,5; 68,7; 7,8 |
20,0; 73,1; 6,9 # |
|
Медиана возраста, годы (диапазон) |
63,5 (32-89) |
60 (36-86) # |
|
Мужчины (n/%) |
47/41 |
66/45,5# |
|
Женщины |
68/59 |
79/54,5# |
|
Риск по ASA (n) (I/II/III) |
20/79/16 |
14/103/28# |
|
Медиана индекса массы тела, (диапазон) кг/м2 |
24,5 (18-34) |
26,7 (17-35) # |
|
Анемия (Hв<100 г/л) (n/%) |
21/18,2 |
31/21,4 # |
|
Трансфузия препаратов крови (n/%) |
17/15 |
25/17,2 # |
|
Вид операции: Гемиколэктомия справа |
35 |
36 |
|
Резекция поперечно-ободочной кишки |
8 |
5 |
|
Гемиколэктомия слева и резекция сигмы |
72 |
104 |
|
Интраоперационная кровопотеря > 400 мл в группе (%) |
18,5 |
22# |
|
Продолжительность операции > 120 мин в группе (%) |
29,4 |
36,6# |
Примечание: # – отсутствие достоверных различий по критерию Mann-Whitney.
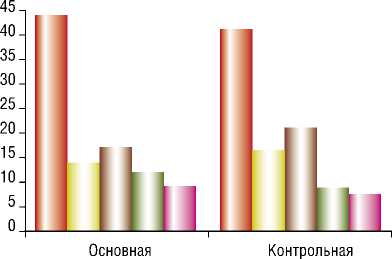
I ■ Сердечно-сосудистой системы
Эндокринной системы
-
■ ■ Респираторной системы
-
■ ■ Мочевыделительной системы
I ■ Центральной нервной системы
Рис. 1. Частота встречаемости интеркуррентных заболеваний в группах (%)
10 мл/кг/ч), недопущение интраоперационной гипотермии путем инфузии подогретых растворов и применение согревающих одеял (100%), комплекс профилактики ИОХВ с включением после герметизации апоневроза последовательного лаважа 3% раствором перекиси водорода и водным раствором хлоргексидина, полнослойной герметизации покровных тканей I–II уровней шовными материалами с нулевой сорбционной активностью (100%), удаление назогастрального зонда перед экстубацией (82,7%).
УВ «В» соответствовали: интраоперационный мониторинг с включением оценки уровня сознания по БИС-монитору для дозирования гипнотиков и электро-

миографии для дозирования миорелаксантов [4] (78,2%), формирование ручных анастомозов продольным однорядным экстрамукозным абсорбируемым швом (77,4%) (в контрольной группе все анастомозы сформированы двухрядным швом Альберта-Ламбера).
К мероприятию в соответствии с УВ «С» относилась протекция операционной раны силиконовым полотном (45,2%).
Среди послеоперационных мероприятий к высокому УВ «А» относились: ограничение режима послеоперационного введения жидкости в виде инфузии по 5 мл/кг/ч (100%), бесповязочное ведение послеоперационной раны со 2-х суток (96,5%), ограничение показаний к трансфузии ПК уровнем гематокрита менее 25% (91%), подача насыщенного кислорода в течение 2-х часов после операции для поддержания SpO2 > 95% (88%), дискретная коррекция висцерального кровотока путем внутрибрюшинного введения анестетика и антисептика с 1-х суток (85,7%), удаление центрального венозного и уретрального катеров в течение 48 часов (85%), инфузионная терапия на основе применения сбалансированных многокомпонентных электролитных растворов, рассчитанных для одновременной коррекции водно-электролитных и кислотно-щелочных параметров [5] (84%).
Средняя частота воспроизводимости (ЧВ) оказалась у таких мероприятий как: начало энтерального приема жидкости к концу 1-х суток (80%) и изокалорических энтеральных смесей в середине 2-х суток после операции (71%), дополнительная инфузия при гипотонии или олигурии (77,4%), использование с целью анальгезии инфузий раствора парацетамола 1000 мг через 8 часов и инъекций кеторола по требованию, что позволило у 77,4% пациентов ограничиться 1-й инъекцией наркотического анальгетика с коротким периодом действия в течение 12 часов после операции, с полным исключением их в дальнейшем, а у 40% вовсе обойтись без них, активизация в виде принятия сидячего, а то и вертикального положения к исходу 1-х суток (68%), со ступенчатым удлинением периода активизации.
Низкой ЧВ – «С» соответствовали: удаление дренажей из брюшной полости (41,7%), УЗАС вен нижних конечностей на 3-и сутки после операции (39%), прекращение инфузионной терапии по истечении 2-х суток (28%), повышение суточной профилактической дозы НМГ на 25–50% на 3-и сутки, при отсутствии увеличения активированного частичного тромбопластинового времени (АЧТВ) как минимум в 1,2 раза от исходного у конкретного больного и при ухудшении гемостазио-логических показателей более чем на 20% от исходных, пролонгирование инъекций НМГ до 30 суток на основе добровольного информированного согласия при сочетании нескольких факторов риска [11, 12] (14,8%).
Для общей оценки ПО (в течение 30 суток после операции), была использована классификация Dindo-Clavien [6], а для ИОХВ – интегральная шкала ASEPSIS [14] на- чиная с 3-х и через каждые 2-е суток послеоперационного периода, при этом фиксировали наихудший показатель за неделю. Статистический анализ проводили с помощью программы Statistica 6.1., с применением U-критерия Манна-Уитни.
Результаты и обсуждение
При анализе осложнений в группах сравнения были получены статистически достоверные отличия, в первую очередь за счет хирургических осложнений. Внутригрупповые особенности проявились тем, что в основной группе преобладали общие осложнения (табл. 2), в том числе преходящее нарушение мозгового кровообращения – 1; дисэлектролитные нарушения сердечного ритма – 4; тахиаритмия и сердечная недостаточность, потребовавшая назначения бета-блокаторов – 4, обострение хронического пиелонефрита – 2, дистальный тромбоз глубоких вен (ТГВ) голени – 1, локальный варикотромбофлебит голени (ВТФ) – 1. В 5 случаях потребовалась повторная кратковременная катетеризация мочевого пузыря. Небезупречное заживление послеоперационной раны было в 4-х случаях (3,5%), из них 2 серомы (1,7%) и 2 случая (1,7%) кожной гиперемии менее 20% площади раны, купированных без применения антибиотиков.
В контрольной группе наблюдался абсолютный рост частоты хирургических осложнений (11,7%), по сравнению с основной (3,5%). Наряду с тяжестью, достоверно возросла доля хирургических ПО в общей структуре осложнений по сравнению с основной группой (с 23,5% до 43,6%). К осложнениям класса IIIв по Dindo-Clavien (требующим повторного хирургического пособия под общей анестезией) относились такие, как несостоятельность толстокишечных анастомозов (2), абсцесс брюшной полости и повторная эвентрация у того же больного (1), послеоперационная механическая непроходимость (1), глубокая инцизионная ИОХВ (2, одна из которых при
Табл. 2. Общая характеристика осложнений в группах
|
Осложнения |
Основная n = 115 |
Контрольная n = 145 |
|
Всего осложнений1 (n/%) |
17/14,8 |
39/26,9* |
|
Общие осложнения (n/%) |
13/11,3 |
22/15,2 |
|
Хирургические осложнения (n/%) |
4/3,5 |
17/11,7* |
|
Тип осложнения2 (n) I |
9 |
13* |
|
II |
6 |
9* |
|
IIIа |
2 |
5* |
|
IIIв |
0 |
7 |
|
IVа |
0 |
3 |
|
IVв |
0 |
1 |
|
V |
0 |
1 |
|
Повторная госпитализация (n/%) |
0 |
3 (2,0) |
|
Медиана3 (диапазон) |
8,9 (7-17) |
13,1 (9-41)* |
Табл. 3. Характеристика инцизионых ИОХВ по шкале ASEPSIS
|
Интегральный показатель |
Основная n = 115 |
Контрольная n = 145 |
|
0–10 баллов (n/%) |
111/96,5 |
133/91,7* |
|
11–20 баллов (n/%) |
4/3,5 |
5/4,3* |
|
21–30 баллов (n/%) |
- |
2/1,4 |
|
31–40 баллов (n/%) |
- |
3/2,1 |
|
> 40 баллов (n/%) |
- |
2/1,4 |
Примечание: * – различия не достоверны по критерию Mann-Whitney.
Табл. 4. Частота ВТЭО в группах сравнения
|
Группы сравнения (n) |
Локализация осложнения (n/%) |
||
|
Дистальный ТГВ/ВТФ |
Проксимальный ТГВ |
ТЭЛА |
|
|
Контрольная (145) |
2 (1,4) |
2 (1,4) |
1 (0,7) |
|
Основная (115) |
2 (1,7) * |
0 (0) |
0 (0) |
|
Всего (260) |
4 (1,5) |
2 (0,77) |
1 (0,4) |
Примечание: * – межгрупповые различия недостоверны по критерию Mann-Whitney.
Заключение
Одним из условий обеспечения периоперационной безопасности пациентов с РКТ является внедрение структурированного по видам осложнений протокола профилактики наиболее клинически значимых ПО. Целесообразность применения технологии быстрого восстановления аргументирована достоверным снижением частоты и тяжести ИОХВ и ВТЭО.
Интегральный принцип оценки заживления раны у больных РТК на основе шкалы ASEPSIS демонстрирует большую вариабельность и динамизм анализируемых параметров и хроно-морфологических нюансов репаративного процесса.
Использование тактики активной переоценки и эскалации мер профилактики ВТЭО в основной группе позволило добиться двукратного снижения частоты осложнений.
Список литературы Возможности повышения периоперационной безопасности пациентов при раке толстой кишки
- Белоусова Т.А., Раскин Г.А., Галунова Т.Ю. Прогностические признаки и факторы риска послеоперационных инфекционных осложнений у больных колоректальным раком//Инфекции в хирургии. -2013. -№ 1. -С. 34-39.
- Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные заболевания в России в 2012 году (заболеваемость и смертность). -М., 2014; 249 с.
- Коровин А.Я., Демин Д.И., Андреев А.В. и др. Хирургическая тактика при осложненном раке толстой кишки и сахарном диабете//Кубанский научный медицинский вестник. -2010. -№9. -С. 111-114.
- Слепушкин В.Д., Женило В.М., Осканова М.Ю., Женило М.В. Мониторинг церебральных функций в анестезиологии и интенсивной терапии. Владикавказ -Ростов-на-Дону, Нальчик, 2014. -202 с.
- Слепушкин В.Д., Миндзаева Е.Г., Тотиков В.З., Тотиков З.В. Оптимизация инфузионной терапии при операциях на толстой кишке//Вестник хирургической гастроэнтерологии. -2011. -№3. -С. 70-71.
- Dindo D., Demartines N., Clavien P-A. Classification of Surgical Complications A New Proposal With Evaluation in a Cohort of 6336 Patients and Results of a Survey//Ann. Surg. -2004. -Vol. 240, № 2. -Р. 205-213.
- Hall B.L., Hamilton B.H., Richards K. et al. Does surgical quality improve in the American College of Surgical Quality Improvement Program: an evaluation of all participating hospitals//Ann. Surg. -2009. -Vol. 250, №. 3. -Р. 363-376.
- Hanna N., Bikov K.A., McNally D. et al. Impact of venous thromboembolism on mortality of elderly Medicare patients with stage III colon cancer//Oncologist. -2012. -Vol. 17, № 9. -Р. 1191-1197.
- Kakkar A.K., Cohen A.T., Tapson V.F. et al. Venous thromboembolism risk and prophylaxis in the acute care hospital setting (ENDORSE survey): findings in surgical patients//Ann. Surg. -2010. -Vol. 251, № 2. -Р. 330-338.
- Kehlet Y., Wilmore D.W. Evidence-based surgical care and the evolution of fast-track surgery//Ann. Surg. -2008. -Vol. 248, № 2. -Р. 189-198.
- Lyman G.H., Khorana A.A., Kuderer N.M. et al. Venous Thromboembolism Prophylaxis and Treatment in Patients with Cancer: American Society of Clinical Oncology Practice Guideline Update//J. Clin. Oncol. -2013. Vol. 31, № 17. -Р. 2189-2204.
- Mandala M., Falanga А., Roila F. Management of venous thromboembolism (VTE) in cancer patients: ESMO Clinical Practice Guidelines//Ann. Oncol. -2011. -Vol. 22, № 6. -P. 85-92.
- Whyte S., Harman S. Effectiveness and cost-effectiveness of an awareness campaign for colorectal cancer: a mathematical modeling study//Cancer Causes Control. -2013. -Vol. 25, №. 6. -Р. 647-658.
- Wilson A.P., Helder N., Theminimulle S.K. Comparison of wound scoring methods for use in audit//J. Hosp. Infect. -1998. -Vol. 39, № 2. -Р. 119-126.


