Возможности раннего энтерального питания в кардиохирургии
Автор: Ефремов Сергей Михайлович, Дерягин Михаил Николаевич, Шмырев Владимир Анатольевич, Шилова Анна Николаевна, Кихтенко Николай Андреевич, Ломиворотов Владимир Владимирович
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Послеоперационный период и интенсивная терапия
Статья в выпуске: 3 т.18, 2014 года.
Бесплатный доступ
Цель исследования - сравнительная оценка стандартной изокалорической и иммунной гиперкалори-ческой формул при проведении раннего энтерального питания у кардиохирургических пациентов с синдромом острой сердечной недостаточности. Проведено проспективное рандомизированное исследование 40 пациентов (20 пациентов в группе стандартного питания и 20 пациентов в группе иммунного). Плазменную концентрацию преальбумина и трансферрина анализировали на 1, 3, 5, 7 и 14-е сутки после операции. Среди пациентов иммунной группы отмечена достоверно более высокая концентрация преальбумина на 14-е сутки (0,13±0,01 и 0,21 ±0,1 г/л; р = 0,04) и трансферрина на 5-е сутки (1,21 ±0,33 и 1,85±0,24 г/л; р = 0,0002), 7-е сутки (1,28±0,39 и 1,75±0,37 г/л; р = 0,018) и 14-е сутки (1,58±0,47 и 2,07±0,46 г/л; р = 0,044). Полученные данные свидетельствуют о преимуществах иммунной гиперкалорической смеси при проведении раннего энтерального питания. Дальнейшие исследования необходимы с целью подтверждения клинических преимуществ иммунного ЭП перед стандартным.
Энтеральное питание, сердечно-сосудистая хирургия, интенсивная терапия
Короткий адрес: https://sciup.org/142140617
IDR: 142140617 | УДК: 61
The potential of early enteral nutrition in cardiac surgery
The aim of this study was to assess the effects of standard solution for enteral nutrition (1 kcal/ml) and immune solution for enteral nutrition (1.3 kcal/ml, rich with glutamine) for early enteral nutrition of cardiac surgery patients with acute heart failure syndrome. Prospective randomized study of 40 patients (20 in standard group and 20 in immune group). Plasma concentrations of prealbumin and transferrin were analyzed at 1, 3, 5, 7 and 14 days. Plasma prealbumin was significantly higher at 14 day after surgery in immune group (0.13±0.01 and 0.21 ±0.1 g/l; р = 0.04). Transferrin was significantly higher in immune group on the 5 day (1.21 ±0.33 and 1.85±0.24 g/l; р = 0.0002), 7 day (1.28±0.39 and 1.75±0.37 g/l; р = 0.018) and 14 day (1.58±0.47 and 2.07±0.46 g/l; р = 0.044). Thus, results of study indicated on benefits of hypercaloric solution for enteral feeding enriched with glutamine in compare with standard isocaloric solution for early enteral nutrition of cardiac patients with acute heart failure.
Текст научной статьи Возможности раннего энтерального питания в кардиохирургии
Проблема нутритивной поддержки (НП) пациентов с синдромом острой сердечной недостаточности и нестабильной гемодинамикой особенно актуальна в кардиохирургии. По многочисленным данным, начало энтерального питания (ЭП) у пациентов в течение 24–48 ч после операции (раннее ЭП) позволяет достичь ряд преимуществ, таких как снижение длительности пребывания в отделении интенсивной терапии (ОИТ) и времени госпитализации, сокращение искусственной вентиляции легких (ИВЛ) и уменьшение частоты инфекционных осложнений [1, 2]. Раннее начало нутритивной поддержки рекомендовано многими ассоциациями [3, 4].
Материал и методы
Настоящее проспективное рандомизированное исследование одобрено локальным этическим комитетом. В исследование включено 40 пациентов, оперированных на сердце в условиях искусственного кровообращения.
Критерии включения: возраст старше 18 лет; операция в условиях искусственного кровообращения (ИК); синдром острой сердечной недостаточности в раннем послеоперационном периоде; время после окончания операции менее 24 ч; предполагаемая длительность искусственной вентиляции легких более 2 суток.
Критерии исключения: нестабильная гемодинамика, шок; ацидоз (PH <7,350 или лактат >4 ммоль/л); гипоксемия (SpO2art >60 мм рт. ст.), кровотечение; острое нарушение мозгового кровообращения; парез кишечника; острая мезентериальная ишемия.
Первичной конечной точкой была динамика концентрации преальбумина. Вторичными конечными точками явились: альбумин, трансферрин, церулоплазмин, глюкоза, триглицериды, билирубин общий, билирубин конъюгированный, лактат крови, СРБ, суточные потребности в энергии (метод
Таблица 1
Состав стандартной и иммунной энтеральных смесей
Нутрикомп ликвид, мл
Пациенты рандомизированы на два типа энтеральных смесей (табл. 1): стандартную (С) (Нутрикомп стандарт ликвид [1 ккал/мл, белок 3,8 г/100 мл] (BBraun, Германия)), 20 пациентов, и иммунную (И) (Нутрикомп иммунный ликвид [1,3 ккал/мл, белок 6,67 г/100 мл, из которого глутамин – 2 г/100 мл] (BBraun, Германия)), 20 пациентов. Энтеральное питание начинали не позднее 48 ч после операции со скоростью 25 мл/ч, с увеличением скорости введения на 50% каждые 24–48 часов под контролем остаточного желудочного объема. Парентеральное питание начинали не ранее 3-х суток после операции, в случае если объем доставляемых энтеральным путем калорий не превышал 60% от суточных потребностей. Ежедневное измерение энергетических потребностей проводили с использованием метода непрямой калориметрии при помощи метаболографа Medgraphics CCM Express (Medical Graphics Corporation, USA).
Индекс вазопрессорно-инотропной поддержки считали по формуле: добутамин (мкг/кг/мин) + допамин (мкг/кг/мин) + 100 × адреналин (мкг/кг/мин) + 100 × норадреналин (мкг/кг/мин) + 10 × мезатон (мкг/кг/мин).
Лабораторные показатели оценивали на: 1-е сутки после операции (исходно), 3, 5, 7 и 14-е сутки после операции c использованием соответствующих наборов реагентов на автоматическом анализаторе ELx808 Absorbance Microplate Reader (Biotek Instruments, Winooski, USA).
Полученные параметрические количественные данные представлены в виде среднего значения и в скобках стандартного отклонения; непараметрические данные показаны в виде медианы и в скобках границ межквартильного интервала (МКИ). Качественные признаки описаны простым указанием количества и доли в процентах.
Сравнительный анализ параметрических признаков выполнен с помощью дисперсионного анализа повторных измерений (Repeated measures ANOVA) с последующим поиском межгрупповых различий (post-hoc test). Непараметрический аналог однофакторного дисперсионного анализа проводился с помощью критерия Крускала – Уоллиса с последующим поиском межгрупповых различий критерием Коновера. Сравнения качественных признаков проводились тестом χ 2 или точным критерием Фишера.
Для всех статистических критериев ошибка первого рода устанавливалась равной 0,05. Нулевая гипотеза отвергалась при р <0,05. Статистический анализ данных проведен согласно общепринятым методам c использованием лицензионной программы MedCalc версии 13.0 (MedCalc Software, Бельгия).
Результаты
Средний возраст пациентов составил 61±8 года; 26 (65%) мужчин и 14 (35%) женщин. У 16 (40%) пациентов выполнена операция на сердце по поводу ведущей патологии ишемической болезни сердца (ИБС), у 18 (45%) – по поводу приобретенной патологии сердца (ППС), у двоих (5%) пациентов по поводу острого расслоения восходящего отдела и дуги аорты и четверо (10%) пациентов оперированы по поводу комбинированной патологии (ИБС и ППС). У четырех (10%) пациентов оперативное вмешательс- тво было повторным. Острый периоперационный инфаркт миокарда как причина синдрома острой сердечной недостаточности выявлен у 9 (22,5%) пациентов. У 10 (50%) пациентов группы стандартного и у 10 (50%) группы иммунного энтерального питания проводили внутриаортальную баллонную контрпульсацию.
Характеристики клинического течения послеоперационного периода исследуемых пациентов
Летальность составила 4 (20%) пациента в группе стандартного энтерального питания и 6 (30%) в группе иммунного ЭП. Длительность искусственной вентиляции легких 116 (86–153) и 114 (73–275) ч (р = 0,7) в группах стандартного и иммунного энтерального питания. Продолжительность пребывания в ОИТ 9 (7–11) суток у пациентов, получающих стандартную смесь для энтерального питания, и 11 (7–23) суток для пациентов, получающих иммунное питание, (р = 0,46). Срок госпитализации среди выписанных пациентов составил 26 (19–21) и 30 (25–33) дней в группах стандартного и иммунного питания (р = 0,27). Характеристики тяжести состояния и клинического течения пациентов исследуемых групп представлены в табл. 2. Достоверных межгрупповых различий исследуемых параметров как исходно, так и в динамике не выявлено.
Суточные энергетические потребности
Описание суточных энергетических потребностей (REE) согласно расчетной формуле Харриса – Бенедикта, данные непрямой калориметрии, респираторный коэффициент (RQ), объем усвоенного энтерального питания и общий объем нутритивной поддержки представлены в табл. 3. Обнаружены достоверные межгрупповые различия объема усвоенного энтерального питания и нутритивной поддержки. Так, среди пациентов, получающих иммунное питание, объем доставленных энтеральным путем калорий достоверно больше на 2, 5 и 7-е сутки. Также пациенты этой группы получали больше нутритивной поддержки в целом (энтерально и парентерально) на 2 и 7-е сутки. Кроме того, количество доставленного белка также больше среди пациентов группы иммунного питания и достоверно различалось на 2, 4 и 7-е сутки.
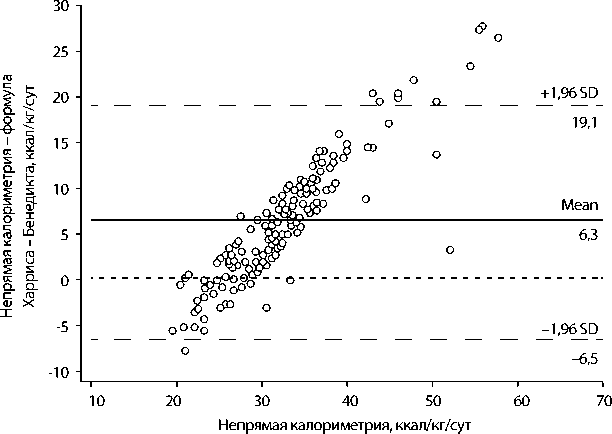
При сравнительном анализе расчета суточных энергетических потребностей по формуле Харриса – Бенедикта с методом непрямой калориметрии выявлены достоверные различия результатов на всех этапах исследования (рис. 1). Уравнение Харриса – Бенедикта недооценивало энергетические потребности исследуемых пациентов в среднем на 6,3 ккал/кг/сут (рис. 2). Так, значения этих параметров на 1-е сутки соответствовали 26 (24,5–28,3) и 32,3 (27,8–36,0) ккал/кг/сут, р = 0,0001; на 2-е – 25,6 (24,4–27,6) и 31,8 (28,5–34,2) ккал/кг/сут, р <0,0001; на 3-е – 25,1 (23,7– 27,6) и 32,6 (27,8–36,2) ккал/кг/сут, р <0,0001; на 4-е – 25,4 (23,7–27,8) и 31,5 (28,1–33,4) ккал/кг/сут, р <0,0001; на 5-е – 25,3 (23,7–26,8) и 31,2 (28,9–34,6) ккал/кг/сут, р <0,0001; на 6-е – 25,3 (24,4–27,7) и 31,4 (25,7–36,3) ккал/кг/сут, р = = 0,002; на 7-е – 25,3 (24,4–26,3) и 33 (28,0–42,5) ккал/кг/сут, р <0,0001 и на 14-е сутки 25,3 (24,5–26,8) и 31 (28,6–38,3) ккал/кг/сут, р = 0,001.
Таблица 2
Тяжесть состояния пациентов исследуемых групп на этапах наблюдения
|
Параметр |
Тип смеси |
Сутки |
|||||||
|
1-е |
2-е |
3-и |
4-е |
5-е |
6-е |
7-е |
14-е |
||
|
С |
23 |
23 |
21 |
19 |
16 |
14 |
12 |
7 |
|
|
Тяжесть по шкале |
(21–25) |
(20–24) |
(17–24) |
(13–23) |
(13–22) |
(8–23) |
(8–24) |
(7–8) |
|
|
APACHE II |
И |
22 |
23 |
21 |
19 |
16 |
11 |
13 |
9 |
|
(18–24) |
(17–24) |
(15–22) |
(11–22) |
(11–21) |
(8–19) |
(8–19) |
(7–14) |
||
|
Тяжесть по шкале |
С |
10 (9–12) |
10 (8–12) |
10 (8–12) |
7 (5–11) |
6 (4–12) |
6 (3–10) |
6 (2–10) |
2 (0–3) |
|
SOFA |
И |
10 (9–10) |
10 (9–12) |
9 (8–11) |
8 (6–10) |
7 (6–9) |
6 (4–8) |
7 (2–9) |
3 (1–8) |
|
Кол-во органных дис- |
С |
4 (3–5) |
4 (3–4) |
4 (3–4) |
3 (2–4) |
3 (2–4) |
2 (1–4) |
2 (1–4) |
0 (0–1) |
|
функций по Baue |
И |
3 (3–4) |
4 (3–5) |
4 (3–5) |
3 (3–4) |
3 (2–4) |
2 (1–3) |
2 (1–3) |
1 (0–2) |
|
Индекс вазопрес- |
С |
19 (13–29) |
12 (8–18) |
7 (1–14) |
2 (0–10) |
0 (0–5) |
0 (0–4) |
0 (0–2) |
0 (0–0) |
|
сорно-инотропной поддержки |
И |
16 (9–22) |
16 (8–22) |
8 (3–16) |
4 (0–11) |
2 (0–6) |
0 (0–2) |
0 (0–0) |
0 (0–0) |
|
С |
5,6 |
2,3 |
2 |
2,1 |
1,4 |
1,9 |
2,0 |
1,3 |
|
|
Лактат крови, |
(4,9–7,9) |
(2,0–2,7) |
(1,6–2,4) |
(1,0–2,8) |
(1,0–2,6) |
(1,3–5,3) |
(1,3–9,0) |
(1,1–2,0) |
|
|
ммоль/л |
И |
4,1 |
2,7 |
1,9 |
2,0 |
1,6 |
1,4 |
1,8 |
1,4 |
|
(3,8–5,3) |
(2,0–3,6) |
(1,6–2,0) |
(1,5–2,2) |
(1,0–2,5) |
(1,0–2,4) |
(1,0–2,3) |
(1,0–1,9) |
||
|
Индекс оксигенации |
С |
199 (153–243) 200 |
182 (150–225) 179 |
232 (174–311) 267 |
277 (169–362) 288 |
241 (198–406) 344 |
292 (187–406) 303 |
210 (194–367) 305 |
|
|
И |
|||||||||
|
(130–256) |
(125–288) |
(176–320) |
(246–386) |
(267–370) |
(217–379) |
(239–374) |
|||
|
С |
66 |
51 |
48 |
48 |
28 |
34 |
42 |
13 |
|
|
Суточный расход |
(45–106) |
(40–79) |
(32–68) |
(18–66) |
(18–50) |
(9–51) |
(7–52) |
(0–24) |
|
|
инсулина, ед./сут |
И |
44 |
62 |
61 |
76 |
32 |
40 |
30 |
10 |
|
(34–72) |
(41–88) |
(41–110) |
(47–109) |
(30–89) |
(22–70) |
(11–62) |
(0–20) |
||
Таблица 3
Характеристика суточного энергобаланса исследуемых пациентов, * р <0,001; ** p <0,01; # p <0,05
|
Параметр |
Тип смеси |
Сутки |
|||||||
|
1-е |
2-е |
3-и |
4-е |
5-е |
6-е |
7-е |
14-е |
||
|
REE (непря- |
С |
2 291 |
2 455 |
2 464 |
2 391 |
2 545 |
2 273 |
2 470 |
2 381 |
|
мая кало- |
(2 090–2 802) |
(1 976–2 755) |
(2 052–2 832) |
(2 037–2 643) |
(2 009–2 651) |
(2 042–2 651) |
(2 209–2 853) |
(2 012–2 565) |
|
|
риметрия), |
И |
2 479 |
2 423 |
2 613 |
2 455 |
2 617 |
2 381 |
2 715 |
2 401 |
|
ккал/сут |
(2 279–2 734) |
(2 171–2 939) |
(2 178–2 994) |
(2 405–2 668) |
(2 354–2 731) |
(2 185–2 862) |
(2 526–2 874) |
(2 248–2 640) |
|
|
RQ (непрямая калориметрия) |
С |
0,93 (0,87–0,98) 0,87 |
0,81 (0,81–0,87) 0,79 |
0,83 (0,8–0,88) 0,77 |
0,86 (0,84–0,99) 0,8 |
0,79 (0,76–0,83) 0,82 |
0,78 (0,74–0,85) 0,8 |
0,85 (0,83–0,98) 0,84 |
0,83 (0,8–0,9) 0,81 |
|
И |
|||||||||
|
(0,8–0,91) |
(0,76–0,82) |
(0,66–0,8) |
(0,76–0,84) |
(0,74–0,9) |
(0,78–0,84) |
(0,8–0,9) |
(0,79–0,85) |
||
|
500 |
1 000 |
1 400 |
1 000 |
1 250 |
1 250 |
||||
|
Объем усвоенного ЭП, |
С |
0 (0–0) |
(350–500) |
(650–1 200) |
(1 000–1 500) |
(350–1 500) |
(1 000–1 500) |
(1 000–1 500) |
|
|
650 |
1 300 |
1 950 |
1 950 |
1 950 |
1 950 |
||||
|
ккал/сут |
И |
0 (0–0) |
(650–650)* |
(650–1 950) |
(1 300–1 950) |
(1 300–2 112)# |
(1 625–2 600) |
(1 300–2 600)# |
|
|
С |
0 (0–0) |
500 |
1 000 |
2 237 |
2 475 |
2 000 |
1 500 |
||
|
Объем НП, |
(350–500) |
(650–1 200) |
(1 975–2 475) |
(2 135–2 856) |
(1 625–2 000) |
(1 000–2 059) |
|||
|
ккал/сут |
И |
0 (0–0) |
650 |
1 300 |
1 950 |
1 950 |
1 950 |
1 950 |
|
|
(650–650)* |
(650–1 950) |
(1 950–2 600) |
(1 950–2 600) |
(1 875–2 600) |
(1 300–2 600)# |
||||
|
19 |
67 |
93 |
110 |
93 |
57 |
||||
|
Доставленный бе- |
С |
0 (0–0) |
(17,5–19,0) |
(43–80) |
(76–110) |
(79–126) |
(76–110) |
(38–90) |
|
|
лок, г/сут |
И |
0 (0–0) |
33,3 |
67 |
100 |
100 |
101 |
100 |
|
|
(33,0–33,0)* |
(33–100) |
(100–133)# |
(100–133) |
(100–133) |
(67–133)** |
||||
Рис. 1.
Суточные энергетические потребности согласно расчетным методам (формула Харриса – Бенедикта) и результатам непрямой калориметрии (n = 40).
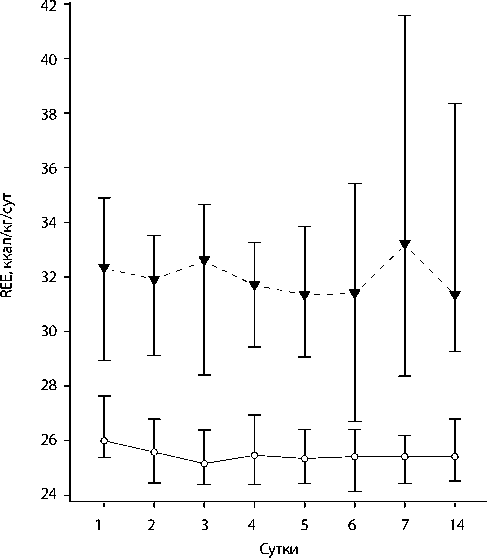
Основной обмен
▼---▼ Непрямая калориметрия
по Харрису – Бенедикту
Рис. 2.
Диаграмма Бленд – Альтмана. Сравнение методов определения основного обмена.
Лабораторные показатели и маркеры нутритивного статуса исследуемых групп
В результате анализа маркеров эффективности нутритивной поддержки выявлены достоверные межгрупповые различия динамики преальбумина, трансферрина и церулоплазмина (табл. 4).
Так, отмечалась достоверно более высокая концентрация преальбумина в группе пациентов, получающих иммунное питание, на 14-е сутки после операции (0,13±0,01 и 0,21±0,1 г/л; р = 0,04).
Кроме того, среди пациентов группы иммунного питания также выявлено более высокое содержание трансферрина на 5-е (1,21±0,33 и 1,85±0,24 г/л; р = 0,0002), 7-е (1,28±0,39 и 1,75±0,37 г/л; р = 0,018) и 14-е (1,58±0,47 и 2,07±0,46 г/л; р = 0,044) сутки. Также в группе иммунного питания отмечали достоверно более высокую концентрацию церулоплазмина на 5-е (0,33±0,09 и 0,46±0,07 г/л; р = =0,0067) и 14-е (0,3±0,06 и 0,4±0,08 г/л; р = 0,018) сутки. Среди прочих исследуемых биохимических показателей достоверных межгрупповых различий не обнаружено.
Таблица 4
Биохимические данные, * р <0,001; ** p <0,01; # p <0,05
|
Параметр |
Тип Сутки смеси 1-е 3-и 5-е 7-е 14-е |
|
Преальбумин, г/л |
С 0,17±0,02 0,12±0,02 0,12±0,03 0,1±0,05 0,13±0,01 И 0,16±0,02 0,14±0,05 0,15±0,04 0,13±0,04 0,21±0,1# |
|
Трансферрин, г/л |
С 1,61±0,35 1,4±0,26 1,21±0,33 1,28±0,39 1,58±0,47 И 1,91±0,32 1,79±0,34# 1,85±0,24* 1,75±0,37# 2,07±0,46# |
|
Церулоплазмин, г/л |
С 0,29±0,11 0,33±0,09 0,33±0,09 0,31±0,09 0,3±0,06 И 0,33±0,1 0,41±0,11 0,46±0,07** 0,41±0,09# 0,4±0,08# |
|
Глюкоза, ммоль/л |
С 9,9±2,9 9,1±1,7 7,8±1,6 8,4±2,1 7,4±1,6 И 10,0±2,0 9,8±2,0 7,9±3,4 7,8±2,6 7,6±3,1 |
|
Триглицериды, ммоль/л |
С 0,84±0,32 1,87±0,73 1,77±1,65 2,19±0,72 1,58±0,4 И 1,1±0,34 1,35±0,57 1,65±0,4 1,69±0,93 1,99±0,89 |
|
СРБ, мг/л |
С 6,9 (4,6–11,9) 9,8 (7,8–18,0) 9,3 (3,8–15,3) 7,7 (5,0–9,2) 3,7 (2,3–7,9) И 7,9 (5,7–12,7) 16,6 (7,7–22,0) 12,2 (8,5–13,9) 8,6 (6,1–10,5) 4,5 (2,8–8,6) |
|
Билирубин общий, мкмоль/л Билирубин конъюгированный, мкмоль/л |
С 25,3 (8,6–31,0) 14,8 (12,6–37,4) 16,9 (14,2–25,1) 23,7 (14,2–27,3) 17,2 (13,0–31,0) И 31,3 (15,0–33,4) 14,4 (9,0–24,0) 10,5 (7,5–14,1) 12,5 (8,8–21,0) 12,4 (7,8–24,0) С 6,9 (3,0–10,5) 14,3 (4,6–26,5) 8,1 (6,6–11,0) 11,1 (5,9–17,4) 11,7 (4,0–18,8) И 13,1 (9,1–16,6) 9,2 (3,4–12,8) 3,6 (2,3–5,0) 6,1 (3,8–8,0) 5,1 (1,8–10,8) |
Обсуждение
Важной находкой представленного исследования являются впервые полученные данные о том, что раннее энтеральное питание гиперкалорической смесью, обогащенной глутамином (иммунная формула), обеспечивает лучшую динамику маркеров нутритивного статуса у наиболее тяжелой категории кардиохирургических пациентов. Так, в группе пациентов, получающих иммунное энтеральное питание, наблюдались достоверно более высокие концентрации преальбумина и трансферрина. Такие результаты объясняет тот факт, что пациентов указанной группы удавалось обеспечить большим количеством энергии и белка при эквивалентном объеме доставленного энтерального питания. Следует отметить, что, несмотря на проводимую нутритивную поддержку, концентрации преальбумина и трансферрина были меньше нормальных значений даже на 14-е сутки после операции, что закономерно в условиях критических состояний, приводящих к гиперкатаболизму, реприоретизации синтеза белков в печени, нарушению сосудистой проницаемости и экстравазации жидкости и белка [8, 9]. Повышенная концентрация СРБ на этапах исследования указывает на значительную выраженность воспалительной реакции среди исследуемых пациентов. Кроме того, у 50% исследуемых пациентов проводилась ПЗТ, ведущая к дополнительным потерям аминокислот через мембрану гемофильтра [10].
Также у пациентов группы иммунного питания отмечали более высокую концентрацию церулоплазмина – фермента, обладающего антиоксидантной активностью и играющего важную роль в метаболизме железа [11]. Известно, что церулоплазмин является основным переносчиком меди и его плазменная концентрация коррелирует с содер- жанием этого микронутриента [12]. Более высокая концентрация церулоплазмина в группе иммунного питания, вероятно, связана с большим содержанием микронутриентов в иммунной смеси для энтерального питания.
В рутинной клинической практике клиницисты часто воздерживаются от проведения энтерального питания у пациентов, находящихся на инотропной поддержке [13]. Наиболее частая причина такого подхода – опасения спровоцировать острую мезентериальную ишемию вследствие возможного дисбаланса между доставкой и потреблением кислорода кишечником, а также увеличивающейся на фоне энтерального питания потребности в нем. Хотя данные немногочисленных исследований свидетельствуют об эффективности и безопасности энтерального питания у кардиохирургических пациентов, которым проводится инфузия инотропных препаратов [7].
В представленном исследовании срок начала энтерального питания среди исследуемых пациентов в среднем составил 27±11 ч, что подтверждает возможность раннего начала энтерального питания у пациентов с синдромом острой сердечной недостаточности. Полученные в рамках исследования результаты не противоречат опубликованным прежде данным о том, что раннее энтеральное питание у пациентов с синдромом острой сердечной недостаточности целесообразно, однако его возможности подвержены негативному влиянию со стороны недостаточности кровообращения и инотропной поддержки [7].
Другой важный результат проведенного исследования – выявленное несоответствие фактических суточных энергетических потребностей расчетным REE (формула Харриса – Бенедикта). Так, REE, измеренные с использованием непрямой калориметрии, в среднем на 30% больше, чем REE, рассчитанные по формуле Харриса – Бенедикта, и составляли в среднем 32 ккал/кг/сут. Эта находка не является новой, ведь погрешность расчетных методик при определении REE в условиях критических состояний хорошо известна [14]. Это связано с тем, что расчетные методики не учитывают ряд условий, оказывающих существенное влияние на REE пациента, таких как шок, седация, экстракорпоральные методы лечения, диагностические и лечебные манипуляции.
Заключение
Таким образом, динамика высокочувствительных маркеров эффективности нутритивной поддержки (преальбумина и трансферрина) указывает на преимущества иммунного энтерального питания у пациентов с синдромом острой сердечной недостаточности после кардиохирургических вмешательств. Дальнейшие исследования необходимы с целью подтверждения клинических преимуществ иммунного энтерального питания перед стандартным.


