Возможности секвенирования нового поколения при исследовании мутационного статуса больных хроническим лимфолейкозом
Автор: Михалева М.А., Мартынкевич И.С., Булдаков И.А., Петров С.В., Кувшинов А.Ю., Чечеткин А.В., Волошин С.В.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Обзорные статьи
Статья в выпуске: 2 т.16, 2020 года.
Бесплатный доступ
Хронический лимфолейкоз (ХЛЛ) - гетерогенное заболевание не только по клиническому течению, иммунофенотипу трансформированных В-лимфоцитов (коэк-спрессия CD5+ c CD19+ и CD20+ c CD23+), но и по генетическим группам риска. Быстрый прогресс в технологиях секвенирования нового поколения позволяет расшифровать мутационный статус заболевания, генетическую и эпигенетическую вариабельность ХЛЛ, и оценивать ее влияние на характер течения заболевания. Идентификация драйверных мутаций позволяет расширить наше понимание патогенеза ХЛЛ и выбрать потенциальные «мишени» для терапии, способствуя разработке и внедрению как новых таргетных препаратов, так и их комбинаций.
Секвенирование нового поколения, таргетное секвенирование, хронический лимфолейкоз
Короткий адрес: https://sciup.org/170172544
IDR: 170172544
New generation sequencing capabilities in determiningmutation status in chronic lymphocytic leukemia
Chronic lymphocytic leukemia (CLL) is a heterogeneous disease not only in the clinical course, immunophenotype of transformed B-lymphocytes (coexpression of CD5+ with CD19+ and CD20+ with CD23+), but also by genetic risk groups. Rapid progress in next generation sequencing technologies allows us to decipher the mutational status of the disease, the genetic and epigenetic variability of CLL, and evaluate its effect on the nature of the disease’s course. Identification of driver mutations allows us to expand our understanding of the pathogenesis of CLL and to select potential “targets” for therapy, contributing to the development and implementation of both new targeted drugs and their combinations
Текст обзорной статьи Возможности секвенирования нового поколения при исследовании мутационного статуса больных хроническим лимфолейкозом
Современные методы молекулярной диагностики лимфопролиферативных заболеваний построены как на уже считающихся классическими исследованиях генома — цитогенетическом анализе (стандартное кариотипирование, флюоресцентная in-situ гибридизация (FISH), методах полимеразной цепной реакции (ПЦР)), так и на стремительно развивающихся методах секвенирования. Новейшая технология расшифровки генома — секвенирование нового поколения (Next Generation Sequencing, NGS), ставшая одним из перспективных направлений среди диагностических методов.
Технология NGS обеспечивает анализ генетического профиля различных лимфопролиферативных заболеваний [1, 2, 3], включая ХЛЛ, с точностью до одного нуклеотида.
Технология NGSи ХЛЛ. Секвенирование нового поколения представляет собой усовершенствованный метод Сэнгера,основанный на электрофорезе и открытый более 40 лет назад [4]. Технологии NGS позволили преодолеть два основных недостатка метода Сэнгера: низкую пропускную способность и относительно высокую себестоимость. Принцип NGSоснован на возможности одновременного прочтения множества генов,в том числе всего генома, увеличивая при этом скорость исследования и объем полученных данных,при снижении себестоимости анализа.
Технология NGS стала генетическим тестом, позволяющим,в зависимости от поставленной задачи, как секвенировать весь геном или экзом, так и использовать таргетные панели генов.
Исследование, выполненное группой ученых Quesada V., et al. (2012) на образцах 105 пациентов с ХЛЛ, позволило выявить 1246
соматических мутаций, потенциально влияющих на функцию генов. При этом более чем в одном образце опухоли идентифицировали 78 функционально измененных генов. Ген SF3B1 был мутирован у 9,7 % больных, а дальнейший анализ полученных данных показал ассоциацию мутаций в гене SF3B1 с быстрым прогрессированием заболевания и сокращением общей выживаемости пациентов [5].
Puente X., et al. провели сочетанное полногеномное и полноэкзомное секвенирование образцов 4-х пациентов с ХЛЛ и выявили 46 соматических мутаций, потенциально изменяющих функцию генов. Дальнейший анализ данных мутаций у 363 пациентов с ХЛЛ выявил реккурентные мутации в 4 генах: NOTCH1, XPO1, MYD88 и KHLH6 [6]. Насколько известно, это первый комплексный анализ клинических данных и результатов полногеномного секвенирования. Было выявлено, что мутации MYD88 и KHLH6 преобладают в случаях ХЛЛ с мутированным статусом вариабельного региона тяжелых цепей иммуноглобулинов, тогда как мутации NOTCH1 и XPO1 — с немутированным статусом.
Работы Landau D., et al., выполненные в 2013 г. [7] и в 2015 г. [8], позволили раскрыть паттерны клональной эволюции ХЛЛ и связать появление новых субклонов трансформированных В-лимфоцитов с неблагоприятными клиническими исходами.
Таким образом, полногеномное и полноэк-зомное секвенирование при ХЛЛ привело к открытию новых драйверных мутаций, включая мутации в некодирующих областях, и позволило пролить свет на роль сигнальных путей в патогенезе ХЛЛ.
В настоящее время, результаты выполненных NGSисследований у больных ХЛЛ свидетельствуют об участии в патогенезе ХЛЛ 8 основных сигнальных путей из известных 12 с выявленными драйверными мутациями в них [9].
Предполагаемые сигнальные пути ХЛЛ (рисунок 1) :
-
1. сигнальный путь NOTCH: NOTCH1, FBXW7 [5, 6, 10].
-
2. сигнальный путь Wnt: LRP1B [5, 6, 10], MED12 [7, 11], FAT1 [12, 13], NkD2 [14].
-
3. путь передачи сигнала через В-клеточный рецептор: BTK и PLCG2 [12, 13], NRAS и KRAS [7, 15], BRAF [16, 17], ITPKB [7, 14, 18], KLHL6 [5, 6, 10].
-
4. врожденный воспалительный ответ: MYD88 [5, 6, 10], RIPK1 [7, 19], BIRC3, MAP2K1 и MAP2K3 [14], MAPK1 [5, 6, 10].
-
5. модификация хроматина: MYM3 [5, 6, 10], CHD2 [6, 7, 20], HIST1H1E [7, 21], HIST1H1C [14].
-
6. процессинг и транспорт мРНК: SF3B1 и DDX3X [5, 6, 10], XPO1 [6, 7, 20]; RPS15, POLR3B и RANBP2 [14].
-
7. дифференцировка В-клеток: BCOR [7, 22], EGR2 [7, 16, 23], IK F3 [14].
-
8. ответ на повреждения ДНК, контроль клеточного цикла: TP53 и ATM [5, 6, 10], SAMHD1 [7, 24], POT1 [6, 7, 20], BRCC3 [14].
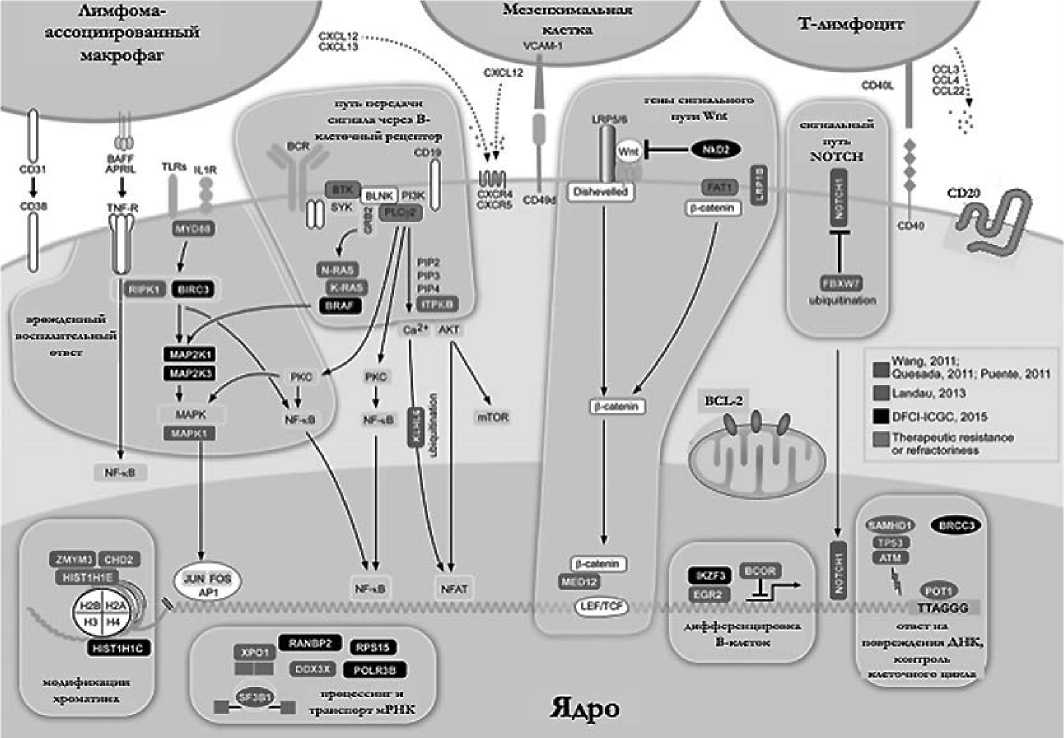
Рисунок 1. Основные предполагаемые клеточные пути ХЛЛ (адаптировано из [25]).
Целью настоящего исследования является разработка таргетной NGS-панели для диагностики мутационного статуса больных ХЛЛ, основанная на опубликованных современных данных (таблица 1).
Таблица 1.
Таргетная NGS-панель для диагностики соматических мутаций ХЛЛ
|
№ |
Название гена |
Локализация гена |
Транскрипт* |
Частота встречаемости |
|
1 |
ATM |
11q22.3 |
NM_000051.3 |
8–25,6 % [7, 8, 26, 27, 29] |
|
2 |
BCOR |
Xp11.4 |
NM_001123385.2 |
2–8,1 % [7, 8, 27] |
|
3 |
BIRC3 |
11q22.2 |
NM_001165.5 |
4–15,5 % [8, 26, 27, 29] |
|
4 |
BRAF |
7q34 |
NM_001374244.1 |
2,5–5 % [8, 28, 29] |
|
5 |
BRCC3 |
Xq28 |
NM_001018055.2 |
1 % [8] |
|
6 |
BTK |
Xq22.1 |
NM_000061.3 |
1–10 % [28] |
|
7 |
CHD2 |
15q26.1 |
NM_001271.4 |
4–5 % [7, 8] |
|
8 |
DDX3X |
Xp11.4 |
NM_001356.5 |
2 % [7, 8] |
Продолжение таблицы
|
№ |
Название гена |
Локализация гена |
Транскрипт* |
Частота встречаемости |
|
9 |
EGR2 |
10q21.3 |
NM_000399.5 |
1–3 % [7, 8] |
|
10 |
FAT1 |
4q35.2 |
NM_005245.4 |
8,1 % [27] |
|
11 |
FBXW7 |
4q31.3 |
NM_001349798.2 |
1,3–5 % [8, 26, 29] |
|
12 |
H1–4 (HIST1H1E) |
6p22.2 |
NM_005321.3 |
1–3 % [7, 8] |
|
13 |
H1–2 (HIST1H1C) |
6p22.2 |
NM_005319.4 |
|
|
14 |
IKZF3 |
17q12–21.1 |
NM_012481.5 |
2 % [8] |
|
15 |
ITPKB |
1q42.12 |
NM_002221.3 |
2 % [7] |
|
16 |
KRAS |
12p12.1 |
NM_033360.4 |
2–4,7 % [7, 8, 27] |
|
17 |
LRP1B |
2q22.1-q22.2 |
NM_018557.3 |
|
|
18 |
MAPK1 |
22q11.22 |
NM_002745.5 |
2 % [8] |
|
19 |
MAP2K1 |
15q22.31 |
NM_002755.4 |
|
|
20 |
MAP2K3 |
17p11.2 |
NM_145109.3 |
|
|
21 |
MED12 |
Xq13.1 |
NM_005120.3 |
2 % [7, 8] |
|
22 |
MYD88 |
3p22.2 |
NM_002468.5 |
1, 5–10 % [7, 8, 25, 27, 29] |
|
23 |
NOTCH1 |
9q34.3 |
NM_017617.5 |
4–24,1 % [7, 8, 26, 27, 29] |
|
24 |
NkD2 |
5p15.33 |
NM_033120.4 |
|
|
25 |
NRAS |
1p13.2 |
NM_002524.5 |
1,5–10 % [7, 8, 26, 27] |
|
26 |
PLCG2 |
16q23.3 |
NM_002661.5 |
|
|
27 |
POLR3B |
12q23.3 |
NM_018082.6 |
|
|
28 |
POT1 |
7q31.33 |
NM_015450.3 |
2,5–7 % [7, 8, 27, 29] |
|
29 |
RANBP2 |
2q13 |
NM_006267.5 |
|
|
30 |
RIPK1 |
6p25.2 |
NM_001354930.2 |
3 % [7] |
|
31 |
RPS15 |
19p13.3 |
NM_001018.5 |
0,88–19,5 % [8, 26] |
|
32 |
SAMHD1 |
20q11.23 |
NM_015474.4 |
2–9,8 % [7, 8, 26] |
|
33 |
SF3B1 |
2q33.1 |
NM_012433.4 |
5–24,9 % [7, 8, 26–29] |
|
34 |
TP53 |
17p13.1 |
NM_000546.5 |
5,3–50 % [7, 8, 26, 27, 29] |
|
35 |
XPO1 |
2p15 |
NM_003400.4 |
1,8–11,5 % [7, 8, 26–28] |
|
36 |
ZMYM3 |
Xq13.1 |
NM_201599.3 |
2–3 % [7, 8, 29] |
Примечания : *Справочные номера транскриптов могут быть обновлены вследствие изменения версии базы данных RefSeq (NCBI Reference Sequence Database, Референсная база данных последовательностей Национального центра биотехнологической информации) [30].
Молекулярное разнообразие ХЛЛ определяет его выраженную клиническую гетерогенность: от наблюдаемых десятилетиями и не нуждающихся в терапии, до быстропрогрессирующих в течение нескольких месяцев,несмотря на активное лечение. Понимание молекулярных характеристик, лежащих в основе патогенеза ХЛЛ, становится приоритетом в свете расширяющихся возможностей современной таргетной терапии ХЛЛ (рисунок 2).
Одним из первых достижений в терапии ХЛЛ стали разработка и применение моноклональных антител: анти-CD20 (ритуксимаб, офатуму-маб, обинутузумаб) и анти-CD52 (алемтузумаб), эффективность которых доказана многочисленными клиническими исследованиями [31–38] и последующей рутинной практикой.
Внедрение таргетных препаратов в клиническую практику стало следующим важным достижением в терапии ХЛЛ. В проводимых исследованиях была доказана высокая эффективность и относительно низкий профиль токсичности ингибиторов В-клеточного сигнального пути (ибрутиниб [39, 40], акалабрутиниб [41, 42], иделалисиб [43]), ингибитора Bcl-2 (венетоклакс [44, 45]) и иммуномодуляторов (леналидомид [46, 47]).
|
Химиотерапия |
Моноклональные антитела |
BCR ингибиторы |
BCL2 ингибиторы |
CAR-T клеточная |
|
Анти-CD20: ✓ Ритуксимаб ✓ Обинтузумаб ✓ Офатумумаб Анти-CD52 Алемтузумаб |
ВТК ингибиторы ✓ Ибрутиниб Акалабрутиниб PI3K ингибиторы Идеалисиб Дувелисиб |
✓ Венетоклакс |
терапия |
|
|
Хлорамбуцил |
||||
|
Флударабин Циклофосфамид Бендамустин |
Иммуномодуляторы Леналидомид |
Аллогенная трансплантация костного мозга |
Сопроводительная терапия
^ - зарегистрированные таргетпые препараты в РФ
Рисунок 2. Возможности терапии ХЛЛ в 2020 г.
Иммунохимиотерапевтические комбинации и новые лекарственные агенты улучшили качество и продолжительность ответов с ожидаемым временем наступления прогрессирования заболевания, превышающим пятилетний порог, тем самым увеличивая время наблюдения, необходимое для оценки клинически значимых различий беспрогрессивной выживаемости и общей выживаемости в проводимых исследованиях [48].
Заключение. Секвенирование нового поколения применяется в онкогематологии как в диагностических,так и в прогностических целях. Полногеномное и полноэкзомное NGS позволило раскрыть выраженную генетическую и эпигенетическую гетерогенность ХЛЛ. Накопленные к настоящему времени данные и их интерпретация еще не достаточны для выяснения прогностической значимости всех выявленных мутаций в генах ХЛЛ, что обосновывает необходимость проведения дополнительных исследований. Разработка панелей генов для анализа их мутационного статуса при ХЛЛ позволяет воссоздавать молекулярный профиль опухоли и выбирать на его основе оптимальные схемы лечения. Кроме того,накопление информации о предполагаемых клеточных путях, задействованных в патогенезе ХЛЛ, способствует опреде- лению драйверных мутаций в генах, которые могут являться потенциальными «мишенями» для разработки новых таргетных препаратов.
Революционные изменения в лечении ХЛЛ с использованием таргетных препаратов в течение последних пяти лет закономерно снизили частоту использования химиопрепаратов. Продолжающиеся в настоящее время разработки таргетных препаратов и их комбинаций направлены, прежде всего, на ограничение длительности терапии с сохранением ее высокой эффективности, при снижении токсичности и частоты возникновения резистентности. Пожалуй, задача на ближайшие годы исследований — молекулярное профилирование опухолевых клонов ХЛЛ и внедрение приемлемых программ таргетной терапии в реальную клиническую практику.
Технология высокопроизводительного секвенирования нового поколения,как часть масштабных трансляционных исследований, позволяет совершенствовать лечение лимфопролиферативных заболеваний, таких как ХЛЛ,в частности и онкогематологических заболеваний в целом, позволяя планировать разработку и применение персонифицированного подхода к терапии.
Список литературы Возможности секвенирования нового поколения при исследовании мутационного статуса больных хроническим лимфолейкозом
- Chapuy B., Stewart C., Dunford A. J., Kim J., Kamburov A., Redd R. A., Lawrence M. S., Roemer M. G. M., Li A., Ziepert M., et al. Molecular subtypes of diffuse large B cell lymphoma are associated with distinct pathogenic mechanisms and outcomes // Nat. Med. — 2018. — Vol. 24. — P. 679–690.
- Bea S., Valdes-Mas R., Navarro A., Salaverria I., Martín-Garcia D., Jares P., Giné E., Pinyol M., Royo C., Nadeu F., et al. Landscape of somatic mutations and clonal evolution in mantle cell lymphoma // Proc. Natl. Acad. Sci. USA. — 2013. — Vol. 110. — P. 18250–18255.
- Bolli N., Avet-loiseau H., Wedge D. C., Van Loo P., Alexandrov L. B., Martincorena I., Dawson K. J., Iorio F., Nik-Zainal S., Bignell G. R., et al. Heterogeneity of genomic evolution and mutational profiles in multiple myeloma // Nat. Commun. — 2014. — Vol. 5. — P. 2997.
- Sanger F., Nicklen S., Coulson A. DNA sequencing with chain-terminating // Proc Natl Acad Sci USA. — 1997. — Vol. 74(12). — P. 5463–5467.
- Quesada V., Conde L., Villamor N. et al. Exome sequencing identifies recurrent mutations of the splicing factor SF3B1 gene in chronic lymphocytic leukemia // Nat Genet. — 2012. — Vol. 44. — P. 47–52.
- Puente X., Pinyol M., Quesada V., et al. Whole-genome sequencing identifies recurrent mutations in chronic lymphocytic leukaemia // Nature. — 2011. — Vol. 475. — P. 101–105.
- Landau D., Carter S., Stojanov P., et al. Evolution and impact of subclonal mutations in chronic lymphocytic leukemia // Cell. — 2013. — Vol. 152(4). — P. 714–726.
- Landau, D., Tausch, E., Taylor-Weiner, A. et al. Mutations driving CLL and their evolution in progression and relapse // Nature. — 2015. — Vol. 526. — P. 525–530.
- Vogelstein B., Papadopoulos N., Velculescu V., Zhou S., Diaz L., Kinzler K. Cancer genome landscapes // Science. — 2013. — Vol. 340(6127). — P. 1546–1558.
- Wang L., Lawrence M. S., Wan Y., Stojanov P., Sougnez C., Stevenson K., Werner L., Sivachenko A., DeLuca D. S., Zhang L., et al. SF3B1 and other novel cancer genes in chronic lymphocytic leukemia // N. Engl. J. Med. — 2011. — Vol. 365. — P. 2497–2506.
- Mäkinen N., Mehine M., Tolvanen J., Kaasinen E., Li Y., Lehtonen H. J., Gentile M., Yan J., Enge M., Taipale M., et al. MED12, the mediator complex subunit 12 gene, is mutated at high frequency in uterine leiomyomas // Science. — 2011. — Vol. 334. — P. 252–255.
- Woyach J., Furman R., Liu T., et al. Resistance mechanisms for the Bruton’s tyrosine kinase inhibitor ibrutinib // N Engl J Med. — 2014. — Vol. 370(24). — P. 2286–2294.
- Messina M., Del Giudice I., Khiabanian H., et al. Genetic lesions associated with chronic lymphocytic leukemia chemo-refractoriness // Blood. — 2014. — Vol. 123(15). — P. 2378–2388.
- Landau D., Stewart C., Reiter J., et al. Novel putative driver gene mutations in chronic lymphocytic leukemia (CLL): results from a combined analysis of whole-exome sequencing of 262 primary CLL samples // Blood. — 2014. — Vol. 124(21). Abstract 1952.
- Bos J. Ras oncogenes in human cancer: a review // Cancer Res. — 1989. — Vol. 49. — P. 4682–4689.
- Damm F., Mylonas E., Cosson A., et al. Acquired initiating mutations in early hematopoietic cells of CLL patients // Cancer Discov. — 2014. — Vol. 4(9). — P. 1088–1101.
- Jebaraj B., Kienle D., Bühler A., Winkler D., Döhner H., Stilgenbauer S., Zenz T. BRAF mutations in chronic lymphocytic leukemia // Leukemia & Lymphoma. — 2013. — Vol. 54. — P. 1177–1182.
- Maréchal Y., Quéant S., Polizzi S., Pouillon V., and Schurmans S. Inositol 1, 4, 5-trisphosphate 3-kinase B controls survival and prevents anergy in B cells // Immunobiology. — 2011. — Vol. 216. — P. 103–109.
- Hosgood H., Baris D., Zhang Y., Berndt S., Menashe I., Morton L., Lee K., Yeager M., Zahm, S., Chanock S., et al. Genetic variation in cell cycle and apoptosis related genes and multiple myeloma risk // Leuk. Res. — 2009. — Vol. 33. — P. 1609–1614.
- Fabbri G., Rasi S., Rossi D., Trifonov V., Khiabanian H., Ma J., Grunn A., Fangazio M., Capello D., Monti S., et al. Analysis of the chronic lymphocytic leukemia coding genome: role of NOTCH1 mutational activation // J. Exp. Med. — 2011. — Vol. 208. — P. 1389–1401.
- Alami R., Fan Y., Pack S., Sonbuchner T., Besse A., Lin Q., Greally J., Skoultchi A., and Bouhassira, E. Mammalian linker-histone subtypes differentially affect gene expression in vivo // Proc. Natl. Acad. Sci. USA. — 2003. — Vol. 100. — P. 5920–5925.
- Grossmann V., Tiacci E., Holmes A. B., Kohlmann A., Martelli M., Kern W., Spanhol-Rosseto A., Klein H., Dugas M., Schindela, S., et al. Whole-exome sequencing identifies somatic mutations of BCOR in acute myeloid leukemia with normal karyotype // Blood. — 2011. — Vol. 118. — P. 6153–6163.
- Unoki M., and Nakamura Y. EGR2 induces apoptosis in various cancer cell lines by direct transactivation of BNIP3L and BAK // Oncogene. — 2003. — Vol. 22. — P. 2172–2185.
- Rice G., Bond J., Asipu A., Brunette R., Manfield I., Carr I., Fuller J., Jackson R., Lamb T., Briggs T., et al. Mutations involved in Aicardi-Goutie` res syndrome implicate SAMHD1 as regulator of the innate immune response // Nat. Genet. — 2009. — Vol. 41. — P. 829–832.
- Guièze R., Wu C. Genomic and epigenomic heterogeneity in chronic lymphocytic leukemia // Blood. — 2015. — Vol. 126(4). — P. 445–453.
- Rodríguez-Vicente A., Bikos V., Hernández-Sánchez M., Malcikova J., Hernández-Rivas J., Pospisilova S. Next-generation sequencing in chronic lymphocytic leukemia: Recent findings and new horizons // Oncotarget. — 2017. — Vol. 8(41). — P. 71234–71248.
- Sandoval-Sus J., Stingo F., Knepper T., et al. Mutational Landscape of Chronic Lymphocytic Leukemia Using Next Generation Sequencing Technologies in the Real World Clinical Setting // Blood. — 2016. — Vol. 128(22). — P. 4366.
- Guillermin Y., Lopez J., Chabane K., et al. What Does This Mutation Mean? The Tools and Pitfalls of Variant Interpretation in Lymphoid Malignancies // Int J Mol Sci. — 2018. — Vol. 19(4). — P. 1251.
- Rigolin G., Saccenti E., Bassi C., et al. Extensive next-generation sequencing analysis in chronic lymphocytic leukemia at diagnosis: Clinical and biological correlations // J Hematol Oncol. — 2016. — Vol. 9(1). — P. 1–9.
- RefSeq (NCBI Reference Sequence Database, Референсная база данных последовательностей Национального центра биотехнологической информации). https://www. ncbi. nlm. nih. gov/refseq/
- Michallet A., Aktan M., Hiddemann W., et al. Rituximab plus bendamustine or chlorambucil for chronic lymphocytic leukemia: primary analysis of the randomized, open-label MABLE study // Haematologica. — 2018. — Vol. 103. — P. 698–706.
- Thompson P., Tam C., O’Brien S., et al. Fludarabine, cyclophosphamide, and rituximab treatment achieves long-term disease-free survival in IGHV-mutated chronic lymphocytic leukemia // Blood. — 2016. — Vol. 127. — P. 303–309.
- Coiffier B., Lepretre S., Pedersen L., et al. Safety and efficacy of ofatumumab, a fully human monoclonal anti-CD20 antibody, in patients with relapsed or refractory B-cell chronic lymphocytic leukemia: a phase 1–2 study // Blood. — 2008 — Vol. 111. — P. 1094–1100.
- Flinn I., Panayiotidis P., Afanasyev B., et al. A phase 2, multicenter study investigating ofatumumab and bendamustine combination in patients with untreated or relapsed CLL // Am J Hematol. — 2016. — Vol. 91. — P. 900–906.
- Cartron G., de Guibert S., Dilhuydy M., et al. Obinutuzumab (GA101) in relapsed/refractory chronic lymphocytic leukemia: final data from the phase 1/2 GAUGUIN study // Blood. — 2014. — Vol. 124. — P. 2196–2202.
- Goede V., Fischer K., Engelke A., et al. Obinutuzumab as frontline treatment of chronic lymphocytic leukemia: updated results of the CLL11 study // Leukemia. — 2015. — Vol. 29. — P. 1602–1604.
- Hillmen P., Skotnicki A., Robak T., et al. Alemtuzumab compared with chlorambucil as first-line therapy for chronic lymphocytic leukemia // J Clin Oncol. — 2007. — Vol. 25. — P. 5616–5623.
- Lozanski G., Heerema N., Flinn I., et al. Alemtuzumab is an effective therapy for chronic lymphocytic leukemia with p53 mutations and deletions // Blood. — 2004. — Vol. 103. — P. 3278–3281.
- Burger J., Barr P., Robak T., et al. Long-term efficacy and safety of first-line ibrutinib treatment for patients with CLL/SLL: 5 years of follow-up from the phase 3 RESONATE-2 study // Leukemia. — 2020. — Vol. 34(3). — P. 787–798.
- Woyach J., Ruppert A., Heerema N., et al. Ibrutinib Regimens versus Chemoimmunotherapy in Older Patients with Untreated CLL // N Engl J Med. — 2018. — Vol. 379. — P. 2517–2528.
- Awan F., Schuh A., Brown J., et al. Acalabrutinib monotherapy in patients with chronic lymphocytic leukemia who are intolerant to ibrutinib // Blood Adv. — 2019. — Vol. 3. — P. 1553–1562.
- Ghia P., Pluta A., Wach M., et al. ASCEND phase 3 study of acalabrutinib vs investigator’s choice of rituximab plus idelalisib (IDR) or bendamustine (BR) in patients with relapsed/refractory (R/R) chronic lymphocytic leukemia (CLL) [abstract]. European Hematology Association Congress; 2019: Abstract LB2606.
- Sharman J., Coutre S., Furman R., et al. Final results of a randomized, phase III study of rituximab with or without idelalisib followed by open-label idelalisib in patients with relapsed chronic lymphocytic leukemia // J Clin Oncol. — 2019. — Vol. 37. — P. 1391–1402.
- Fischer K., Al-Sawaf O., Bahlo J., et al. Venetoclax and obinutuzumab in patients with CLL and coexisting conditions // N Engl J Med. — 2019. — Vol. 380. — P. 2225–2236.
- Seymour J., Kipps T., Eichhorst B., et al. Venetoclax-Rituximab in Relapsed or Refractory Chronic Lymphocytic Leukemia // N Engl J Med. — 2018. — Vol. 378. — P. 1107–1120.
- Ferrajoli A., Lee B., Schlette E., et al. Lenalidomide induces complete and partial remissions in patients with relapsed and refractory chronic lymphocytic leukemia // Blood. — 2008. — Vol. 111. — P. 5291–5297.
- Fink A., Bahlo J., Robrecht S., et al. Lenalidomide maintenance after first-line therapy for high-risk chronic lymphocytic leukaemia (CLLM1): final results from a randomised, double-blind, phase 3 study // Lancet Haematol. — 2017. — Vol. 4(10). — P. e475-e486.
- Волошин С. В., Кувшинов А. Ю., Бессмельцев С. С., и др. Эффективность таргетных лекарственных препаратов как средства эрадикации и контроля за остаточным опухолевым клоном у больных хроническим лимфолейкозом // Биомедицинский журнал Medline.ru. — 2019. — Т. 20, гематология. — С. 229–241.


