Возрастные морфологические изменения глионейронального комплекса первичной зрительной области коры больших полушарий крыс, коррекция n-тирозолом
Автор: Свердева Юлия Олеговна, Варакута Е.Ю., Логвинов С.В., Жданкина А.А., Потапов А.В., Герасимов А.В., Солонский А.В., Суханова Г.А.
Журнал: Сибирский вестник психиатрии и наркологии @svpin
Рубрика: Биологические исследования
Статья в выпуске: 4 (93), 2016 года.
Бесплатный доступ
В эксперименте, проведенном на 30 белых крысах-самцах линии Вистар, показано, что к 18-месячному возрасту в первичной зрительной области коры во II, IV и V слоях увеличивается процентное содержание деструктивно измененных нейронов и глиоцитов, преимущественно по темному типу. Изменяется глионейрональный индекс вследствие уменьшения численной плотности нейронов и закономерного увеличения численной плотности глии. Однако курсовое введение 18-месячным крысам n-тирозола сдерживает деструкцию, что выражается в снижении процентного содержания пикноморфных сморщенных нейронов и глиоцитов. На фоне коррекции у 18-месячных животных снижается также процентное содержание гиперхромных нейронов без сморщивания ядра, что, вероятно, связано с их переходом в нормохромное состояние.
Старение, нейрон, глия
Короткий адрес: https://sciup.org/14295948
IDR: 14295948 | УДК: 591.484.1.068.1:[611.843.1.018.84:611.813.1]-092.9
Age-related morphological changes of glioneyronal complex in primary visual cortex of the brain of rat, correction with n-tyrosol
The experiment on 30 white male Wistar rats shows an increased percentage of neurons and gliacytes with predominantly dark type destructive changes in layers II, IV, V in primary visual cortex by 18 months age. The glioneuronal index changes due to a decreased neuron number and a subsequently increased glial number. However, a course administration of n-tyrosol to 18 months old rats leads to a decline in destructive changes compared to 18 months old rats without n-tyrosol. The percentage of hyperchromatic neurons without shrinking nucleus of 18 months rats on the background of correction also declines, which is likely to be connected with their transition to normochromic condition.
Текст научной статьи Возрастные морфологические изменения глионейронального комплекса первичной зрительной области коры больших полушарий крыс, коррекция n-тирозолом
Введение. В связи с увеличением средней продолжительности жизни и доли пожилого населения [2] возрастает исследовательский интерес как к изучению медико-биологических аспектов старения, так и к поиску лекарственных средств, предотвращающих возрастные патофизиологические изменения в органах и тканях. Известно, что ведущим фактором старения организма являются изменения в различных структурах центральной нервной системы [1, 8]. Определенный вклад в повреждение клеток при старении вносят свободные радикалы [12], что послужило патогенетическим обоснованием для использования антиоксидантов в качестве геропротекторов [10]. n-Тирозол, разработанный в Новосибирском институте органической химии им. Н. Н. Ворожцова СО РАН (НИОХ СО РАН), является синтетическим аналогом природного фенольного антиоксиданта родиолы розовой и, помимо антиоксидантного эффекта, проявляет гемореологические и антитромбоци-тарные свойства [7].
Цель исследования: изучить возрастные морфологические изменения глионейронально-го комплекса первичной зрительной области коры (OC1) у 18-месячных крыс-самцов линии Вистар на фоне коррекции n-тирозолом и без нее.
Материал и методы. Эксперименты выполнены на 30 белых крысах-самцах линии Вистар в возрасте 3 (n=15) и 18 (n=15) месяцев (табл. 1).
Таблица 1
Распределение животных по экспериментальным группам и подгруппам (абс.)
|
Группа |
Подгруппа |
Количество животных |
|
3-месячные крысы-самцы |
3 мес. (интактные) |
n=5 |
|
3 мес. + n-тирозол |
n=5 |
|
|
3 мес. + эквиобъемное к-во дистиллированной воды |
n=5 |
|
|
18-месячные крысы-самцы |
18 мес. (интактные) |
n=5 |
|
18 мес. + n-тирозол |
n=5 |
|
|
18 мес. + эквиобъемное к-во дистиллированной воды |
n=5 |
Животные каждой возрастной группы (3месячные и 18-месячные) были разделены на 3 равные подгруппы, по 5 животных в каждой подгруппе. Животные первой подгруппы – интактные. Животным второй подгруппы каждой возрастной группы (n=5) в течение 14 суток внутрижелудочно вводили n-тирозол в дозе 50 мг/кг массы. Животным из третьей подгруппы вводили эквиобъемное количество дистиллированной воды.
Всех животных содержали в условиях вивария на стандартном пищевом рационе, с искусственным световым режимом 12 часов день, 12 часов ночь, освещенность 25 лк. На 15-е сутки производили декапитацию крыс под эфирным наркозом, выделяли затылочную область коры, фиксировали в 10 % формальдегиде и заливали в парафин. Отвесные срезы толщиной 5—6 мкм окрашивали крезиловым фиолетовым по Нисслю, дифференцировали область OC1, подсчитывали процентное содержание нейронов с очаговым и тотальным хроматолизом, гиперхромных нейронов со сморщиванием ядра и без, процентное содержание глиоцитов с гиперхромией ядра и его пикнозом во II, IV и V слоях.
Все расчеты производили на 200 соответствующих клеток. Рассчитывали численную плотность нейронов и глии с помощью окулярной рамки известной площади на 1 мм² и определяли глионейрональный индекс. Для электронной микроскопии материал фиксировали в 2,5 % растворе глутаральдегида на какодилатном буфере (рН=7,4). Далее производили постфиксацию в 2 % растворе четырехокиси осмия и заливали в смесь эпона и аралдита М. Полутонкие срезы окрашивали азуром II. Значения всех подгрупп 3-месячных животных были объединены на основании морфолого-количественного анализа, показавшего отсутствие достоверных различий по изучаемым показателям, и считались контрольными. В подгруппе интактных 18месячных крыс и в подгруппе крыс с введением дистиллированной воды достоверных различий по изучаемым показателям также не обнаружено, что позволило нам использовать усредненные значения. Для оценки достоверности различий при сравнении средних величин использовали непараметрический критерий Манна-Уитни. Различия считались статистически значимыми при р<0,05.
Результаты и их обсуждение. К 18месячному возрасту в первичной зрительной области коры у крыс наблюдаются морфологические изменения нейронов по темному типу, причем как обратимого, так и необратимого характера. К обратимым изменениям относят ги-перхромию без сморщивания ядра, такие нейроны имеют нормальные размеры и четкие, ровные контуры ядра и цитоплазмы. В группе 18-месячных животных выявлено достоверное увеличение процентного содержания гипер-хромных нейронов без сморщивания ядра во II слое (рис. 1А) до 33,5 % (28,3—35,2) по сравнению с соответствующими показателями контрольной группы – 18,43 % (15,7—20,48) (p≤0,05). Появление темных нейронов является неспецифической реакцией нервной ткани и отражает их функциональное состояние.
Существуют данные, что гиперхромия является эквивалентом заторможенного состояния, углубление и длительное существование которого может приводить к сморщиванию ядра и гибели клетки [5]. Так, процентное содержание пикноморфных нейронов увеличивается у 18-месячных крыс до 3,5 (1,6—3,5) в V слое по сравнению с таковым у крыс контрольной группы – 0,5 (0—1,0) (p≤0,05). При морфологическом анализе глиальной популяции нами обнаружено, что в группе 18-месячных крыс встречаются глиоциты с высокой степенью конденсации хроматина (рис. 1Б), они характеризуются интенсивно прокрашенным, четко дифференцируемым ядром без признаков сморщивания. Процентное содержание таких гипер-хромных глиоцитов без сморщивания ядра увеличивается во всех исследуемых слоях в группе 18-месячных крыс: до 40 % (35,6—47,1) во II слое, до 29,6 % (28,6—32) в IV слое, до 37,5 % (32,5—39,7) в V слое против значений контрольной группы во II слое 26,17 % (21,5—32,7), в IV слое 20 % (19—24,6), в V слое 22 % (21,4— 32,5) соответственно (p≤0,05).
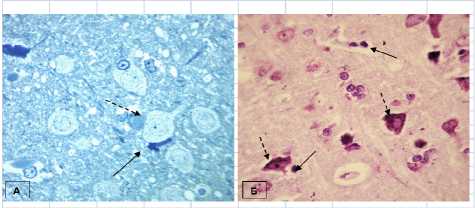
Рис. 1А. Гиперхромный глиоцит со сморщиванием ядра (черная стрелка), нейрон с тотальным хроматолизом (пунктирная стрелка) у 18месячной крысы в IV слое, область OC1. Полутонкий срез. Окраска азур II.
Ув. 1200
Рис. 1Б. Гиперхромные глиоциты (черные стрелки), гипер-хромные нейроны без сморщивания ядра (пунктирная стрелка) у 18-месячной крысы в V слое, область OC1. Парафиновый срез. Окраска крезоловым фиолетовым по Нисс-лю. Ув. 1200
Гиперхромное состояние нейроглии можно объяснить изменением метаболизма и функциональной активности этих клеток. Так, по мнению С. Мори и К. П. Лейблона, гиперхром-ное состояние олигодендроцитов свидетельствует об их зрелости, тогда как наиболее светлые клетки представляют активно делящуюся популяцию [13]. Светлые клетки присутствуют в молодом возрасте, в зрелом возрасте встречаются в норме в основном темные формы [9]. Обнаружено, что гиперхромия свойственна не только олигодендроглии, в области гиппокампа CA1 открыт новый темный тип микроглии, которая обладает повышенной фагоцитарной активностью, главным образом, в области синаптических контактов нейронов. Авторы считают, что такое патологическое состояние связано с развитием окислительного стресса [11].
У 18-месячных крыс во всех исследуемых слоях имеются глиоциты с неправильной угловатой формой, гомогенно интенсивно прокрашенные со сморщенными ядрами. Такие клетки, вероятно, являются исходом длительно существующего гиперхромного состояния. Морфометрический анализ показал, что процентное содержание пикноморфных глиоцитов увеличивается в V слое до 6 % (4—6,25) против соответствующих значений у животных контрольной группы 1,5 % (1—2,8) (p≤0,05).
Для изучения взаимоотношений между глией и нейронами принято использовать глионей-рональный индекс (ГНИ), который значимо увеличивается во всех исследуемых слоях в группе 18-месячных крыс (табл. 2).
Таблица 2
Распределение животных по экспериментальным группам
|
II слой |
IV слой |
V слой |
||||||
|
3 мес. (контроль) |
18 мес. |
18 мес. + n-тирозол |
3 мес. (контроль) |
18 мес. |
18 мес. + n-тирозол |
3 мес. (контроль) |
18 мес. |
18 мес. + n-тирозол |
|
0,25 |
1* |
0,3 |
1 |
1,5* |
1,3 |
0,5 |
0,75* |
0,6 |
|
0-05 |
0,3-0,7 |
0-0,6 |
0,7-1,5 |
0,8-1,5 |
0,5-2 |
0,3-0,8 |
0,5-1 |
0,25-2 |
Примечание. * – Достоверные различия по сравнению с показателями контрольной группы.
Увеличение ГНИ у 18-месячных крыс, наряду с обнаружением в IV и V слоях участков, полностью лишенных нейронов и замещенных глиоцитами, свидетельствует о гибели нейронов и пролиферации глии. Так, во всех исследуемых слоях численная плотность нейронов на 1 мм² среза достоверно уменьшается: до 120 (80—60) во II слое, до 200 (160—220) в IV слое, до 120 (80—160) в V слое по сравнению с соответствующими показателями контрольной группы во II слое 240 (200—240), в IV слое 320 (280—360), в V слое 200 (160—240) (p≤0,05). Численная плотность глии на 1 мм² среза, напротив, значимо увеличивается: до 120 (80— 140) во II слое, до 160 (120—180) в IV слое, до 160 (120—200) в V слое по сравнению с показателями контрольной группы во II слое 40 (40— 80), в IV слое 80 (40—120), в V слое 80 (40— 120) (p≤0,05).
Для коррекции изменений глионейронально-го комплекса был выбран препарат n-тирозол, который как адаптоген повышает сопротивляемость организма к вредному воздействию различных факторов, в том числе и биологических, способствует нормализации энергопродукции мозга в физиологических и стрессовых условиях [6]. При применении n-тирозола у 18месячных крыс отмечается достоверное повышение процентного содержания нейронов с очаговым хроматолизом: в IV слое до 8 % (6,5—10), в V слое до 15 % (9,6—16) по сравнению с таковым показателем у животных той же возрастной группы без коррекции в IV слое 2 % (1—2), в V слое 6 % (4—6,6) (p≤0,05). Очаговый хроматолиз является потенциально обратимым состоянием, которое может отражать повышенную функциональную активность нейрона [3]. Применение n-тирозола снижает процентное содержание гиперхромных нейронов без сморщивания во II слое до 23 % (21—26,5) и процентное содержание сморщенных гиперхром-ных нейронов у 18-месячных крыс в V слое до 1 % (0,8—1,6) по сравнению с аналогичными показателями 18-месячных крыс группы без коррекции (p≤0,05), не достигая при этом соответствующих показателей контроля. При оценке влияния n-тирозола на глиальную популяцию выявлено достоверное снижение процентного содержания гиперхромных пикноморфных глиоцитов: в V слое до 2 % (1,5—2) (p≤0,05), а также гиперхромных глиоцитов без сморщивания ядра в IV слое до 23 % (20,5—28), в V слое до 24 % (20—26,5) (p≤0,05) по сравнению со значениями аналогичных показателей в группе без коррекции, однако значений контроля данные показатели не достигают. Уменьшение содержания пикноморфных глиоцитов и гиперхромных нейронов со сморщиванием ядра на фоне коррекции, вероятно, обусловлено утилизацией погибших клеток и поддержанием адекватного функционального состояния неизмененных и гиперхромных клеток без сморщивания. Похожие результаты были получены нами при исследовании влияния ка-ровертина на радиальную глию сетчатки в условиях яркого света [4].
Выводы. Таким образом, у крыс к 18месячному возрасту без коррекции наблюдается снижение численной плотности нейронов в результате их гибели, главным образом, посредством сморщивания ядра и перикариона. Показано, что n-тирозол препятствует гибели нейронов и глиоцитов, вероятно, за счет своих антиоксидантных и антиагрегантных свойств, проявляя, таким образом, нейропротективный эффект.
Список литературы Возрастные морфологические изменения глионейронального комплекса первичной зрительной области коры больших полушарий крыс, коррекция n-тирозолом
- Анисимов В. Н. Молекулярные и физиологические механизмы старения: в 2-х т. -2-е изд., перераб. и доп. -СПб.: Наука, 2008. -Т. 1. -С. 270.
- Демографический ежегодник России. 2015: Статистический сб./Росстат. -М., 2015. -С. 20-21.
- Коломеец Н. С., Клещинов В. Н. Пластический обмен в нейронах при их изменениях по гипохромному типу//Архив анатомии, гистологии и эмбриологии. -1990. -Т. 98. -С. 30-38.
- Логвинов С. В., Плотников М. Б., Варакута Е. Ю., Жданкина А. А., Потапов А. В., Михуля Е. П. Влияние каровертина на реакцию пигментного эпителия и радиальной глии сетчатки при воздействии яркого света//Бюллетень экспериментальной биологии и медицины. -2007. -№ 7. -С. 112-114.
- Орловская Д. Д., Клещинов В. Н. Нейрон в гиперхром-ном состоянии//Журн. невропатологии и психиатрии. -1986. -Вып. 7. -C. 981-988.
- Саратиков А. С., Краснов Е. А. Родиола розовая. -4-е изд-е, перераб. и доп. -Томск: Изд-во Том. ун-та, 2004. -С. 292.
- Смольякова В. И., Чернышева Г. А., Плотников М. Б., Алиев О. И., Краснов Е. А. Антиоксидантные и кардиопротекторные эффекты n-тирозола при ишемии миокарда с реперфузией у крыс//Кардиология. -2010. -№ 11. -С. 50.
- Солонский А. В., Логвинов С. В. Ультраструктурные и морфометрические особенности синаптогенеза мозга эмбрионов и плодов человека в условиях пренатального воздействия этанола//Бюллетень сибирской медицины. -2008. -Т. 7, № 2. -С. 35-39.
- Хэм А., Кормак Д. Гистология/пер. с англ. -М.: Мир, 1983. -Т. 3. -С. 200-204.
- Ames B. N., Shigenaga M. K., Hagen T. M. Oxidants, antioxidants, and the degenerative diseases of aging//Proceedings of the National Academy of Sciences of the United States of America. -1993. -№ 17 (90). -P. 7915-7922.
- Bisht K., Sharma K. P., Lecours C., Gabriela Sanchez M., El Hajj H., Milior G, Olmos-Alonso A., Gomez-Nicola D., Luheshi G., Vallières L., Branchi I., Maggi L., Limatola C., Butovsky O., Tremblay M. È. Dark microGlia: A new phenotype predominantly associated with pathological states//Glia. -2016. -№ 5 (64). -P. 826-839.
- Miquel J., Juan E. de, Sevila I. Oxygen-induced mitochondrial damage and aging//EXS. -1992. -№ 62. -P. 47-57.
- Mori S., Leblond C. P. Electron microscopic identification of three classes of oligodendrocytes and a preliminary study of their proliferative activity in the corpus callosum of young rats//The Journal of Comparative Neurology. -1970. -№ 1 (139). -P. 1-8.


