Выбор метода анестезии при грыжесечении у пациента с дилятационной кардиомиопатией
Автор: Теплых Б.А., Лисиченко И.А., Левчук А.Л.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 2 т.9, 2014 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/140188297
IDR: 140188297 | УДК: 616-007.43-089.5/.87(063)
Choice of anesthesia in a herniotomy with and dilated cardiomyopathy
Текст статьи Выбор метода анестезии при грыжесечении у пациента с дилятационной кардиомиопатией
УДК: 616-007.43-089.5/.87(063)
CHOICE OF ANESTHESIA IN A HERNIOTOMY WITH AND DILATEDCARDIOMYOPATHY
Врач анестезиолог-реаниматолог при выборе метода анестезиологического пособия у больных с высоким кардиальным риском может использовать различные технологии: общей анестезии с ИВЛ, разновидности нейроаксиальной анестезии (эпидуральная, спинальная), периферические блокады, инфильтрационную анестезию, понимая все особенности, преимущества и недостатки каждой из них.
Настоящее клиническое наблюдение посвящено иллюстрации этой непростой задачи выбора.
Больной К, 35 лет поступил в клинику в феврале 2012 года, для планового оперативного лечения по поводу гигантской пахово-мошоночной грыжи с высоким риском ущемления. Грыжа была таких размеров, что пациенту приходилось придумывать подвесные устройства из подручных средств для обеспечения свободы передвижения (рис. 1).
Из анамнеза известно: до 30 лет 1-2 раза в год страдал ангинами. С 2006 года отмечает кратковременные, приступообразные сердцебиения, перебои в работе сердца, проходящие самостоятельно, к врачам не обращался. В 2008 году при обследовании амбулаторно впервые выявлена дилатация левого желудочка, снижение фракции выброса ЛЖ, нарушение ритма по типу фибрилляции предсердий. Установлен диагноз дилатационной кардиомиопатии. ХСН II А ст. Постоянной формы фибрилляции предсердий. С 2010 года у пациента диагностируется правосторонняя пахово-мошоночная грыжа, в связи с приступообразными болями в этой области в декабре 2011 года обратился к хирургу. Из за наличия тахисистолии пациент был госпитализирован в кардиологическое отделение стационара, для коррекции терапии, предоперационного обследования и решения вопроса о возможности оперативного лечения.
Во время обследования у больного было выявлено:
– по клиническим и биохимическим показателям крови в переделах нормы.
– ЭХО-КГ: ДОЛЖ- 8,0/340 (норма 3,5–5,6/56–154 ), СОЛЖ- 6,6/224
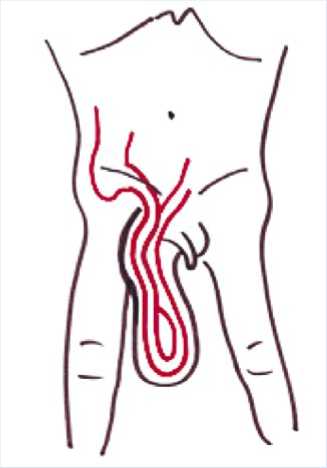
Рис. 1.
(норма 2,5–4,0/22–70 ), УО- 116 мл (норма 45–85), ФВ 34% (55–75), МЖП- 1,2 см, Ао- 3,7 см (норма до 2,8 см), ДРЛП- 7,7 X 8,2 см (норма до 4,0-4,8), ДРПП- 4,9 X 6,3 см (норма до 3,8 X 4,6), СЛА 55 ( норма до 30). Заключение: Значительное диффузное снижение систолической функции ЛЖ. МР 4 ст. ТР 2 ст, АР 0 ст. Признаки легочной гипертензии. Жидкости в плевральных синусах нет.
– Сцинтиграфия миокарда в покое: Сцинтиграфические признаки диффузного снижения перфузии по всему миокарду ЛЖ. Общая зона наиболее выраженной гипоперфузии ( верхуш-

ка, задняя и боковая стенка) порядка 10%. Сократительная способность ЛЖ удовлетворительная: ОФВ ЛЖ-32%. Признаки диффузного снижения регионального систолического утолщения по всему миокарду ЛЖ.
– Холтеровское мониторирование ЭКГ на фоне приема дигоксина 0,25 мг и кардевилола 12,5 мг: Регистрировалось мерцание предсердий с ЧЖС 61-126 в мин, средняя ЧЖС 87 в мин. Частые одиночные желудочковые экстрасистолы, всего 531, из них 1 желудочковый куплет, 14 пауз 2,0–2,3 с - преимущественно в ночные часы.
В предоперационном периоде было решено с целью урежения ЧСС увеличить дозу кардевилола до 13,625 мг, добавить амиодарон 400 мг/сут, спиронолактон заменить на эплеренон 25 мг/сут, но учитывая паузы на ХМ-ЭКГ до 2,3 сек от амиодарона впоследствии решено было отказаться. От дальнейших попыток предоперационной подготовки пациента решено было воздержаться из-за вероятной их бесперспективности.
Выбирая метод анестезии у представленного пациента, мы учитывали, что:
– при общей анестезии сохраняются риски электрической нестабильности, фибрилляции желудочков на фоне частой желудочковой экстрасистолии, увеличения трансторакального давления и как результат декомпенсация легочной гипертензии, увеличения системного сосудистого сопротивления и декомпенсация митральной недостаточности.
– при выборе нейроаксиальных методик обезболивания одними из главных опасностей могли быть неконтролируемое снижение системного сосудистого сопротивления с декомпенсацией сердечной недостаточности, неконтролируемый уровень симпатической блокады, возможное увеличение пауз между желудочковыми сокращениями вследствие системной токсичности.
– перечисленные методики не исключали возможность осложнений в ранний послеоперационный период, а именно резкое увеличение постнагрузки и частоты сердечных сокращений в ответ на послеоперационный болевой синдром.
Учитывая, выше перечисленные риски кардиальных осложнений в периопе-рационном периоде, от «традиционных» методов обезболивания решено было воздержаться, и рассмотреть возмож- ность выполнения оперативного лечение с применением только методов регионарного обезболивания и легкой седации.
Методом регионарной анестезии был избран ТАР-блок (Transversus Abdominis Plane Block). ТАР-блок, впервые описанный А.Рафи в 2001, в настоящее время является наиболее молодой и широко применяемой методикой регионарной анестезии. Целью ТАР-блока являются чувствительные нервы передней брюшной стенки, исходящие из сегментов Tr7-L1, что полностью закрывает зону планируемого грыжесечения. Особенность методики является введение раствора местного анестетика между фасциями внутренней косой мышцы живота и поперечной мышцы живота, где проходят начальные отделы чувствительных нервов (рис. 2).
На заре использования блокады применяли метод «щелчков» для идентификации прокола нужных фасций, что ограничивало распространение ТАР-бло-ка, как трудно повторяемого. В последние годы ТАР-блок используют в условиях УЗИ навигации, и это делает его легко воспроизводимым в руках любого врача знакомого с азами УЗИ, так как слои мышц и фасции легко визуализируются и навигация крайне проста (рис. 3).
Общепризнано, что единственным противопоказанием к проведению этой блокады является лишь аллергическая реакция на местные анестетики. ТАР блок в основном применяется для послеоперационного обезболивания, так как лимитирующим фактором является медленное развитие полной блокады (составляет около 60 минут), однако для описанного больного это не могло явиться лимитирующим фактором, основной нашей задачей было получить наиболее гладкое течение анестезии.
Осложнения методики ТАР-блока включают: неэффективный блок, внутрисосудистое или внутрибрюшное введение анестетика, риск повреждения кишечника и других органов брюшной полости, вероятность развития этих осложнений крайне мала в условиях использования УЗИ навигации.
Описание методики
Цель блокады — введение анестетика в фасциальное пространство между внутренней косой и поперечной мышцами живота, в котором проходят нервы от Тr7 до L1. Для определения мышечных слоев и подтверждения правильного положения иглы использовалась УЗ-на-вигация. Датчик был установлен в попе-
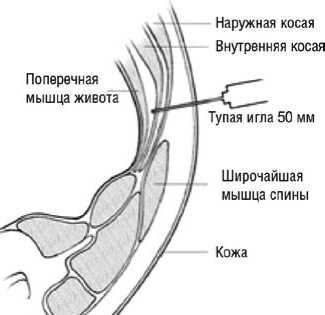
Рис. 2.
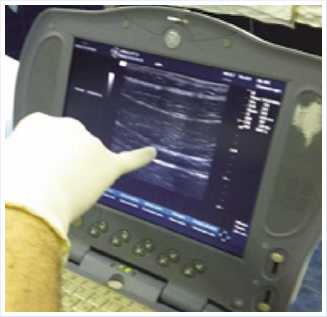
Рис. 3.
речной плоскости между 12- м ребром и гребнем подвздошной кости по передней подмышечной линии. После инфильтрационной анестезии раствором лидокаина 2%- 2 мл, произвели вкол иглой Туохи диаметром 18 G в пространство между фасциями внутренней косой мышцы и поперечной мышцы живота, ввели 30 мл 0,75% раствора наропина, в условиях УЗИ визуализации наблюдали распределение раствора анестетика в межфасциальном пространстве (рис. 4).
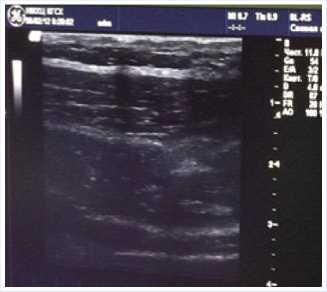
Рис. 4.

Булда О.В., Гаспарян М.В., Алешин П.В., Шахназарян А.М., Шахназарян Н.Г., Паразян А.С., Жовнер Е.В.
СЛУЧАЙ УСПЕШНОГО ОПЕРАТИВНОГО ЛЕЧЕНИЯ РАЗРЫВА ПОСТТРАВМАТИЧЕСКОЙ ЛОЖНОЙ АНЕВРИЗМЫ ПЕРЕШЕЙКА АОРТЫ
Через иглу установили катетер для послеоперационного обезболивания, в который начали инфузию наропина 0,2% со скоростью 8 мл/час. Для достижения максимального эффекта развития блокады ожидали 60 минут.
После развития адекватной анестезии места оперативного вмешательства, на фоне стабильной гемодинамики и адекватной анальгезии, было проведено грыжесечение с ненатяжной пластикой полипропиленовой сеткой.
В раннем послеоперационном периоде, на фоне адекватного обезболивания (инфузия наропина 0,2% – 8мл/час) пациент находясь в палате, уже через 1 час после оперативного вмешательства «нарушал» постельный режим, ведя повседневный образ жизни без ограничений связанных с послеоперационной болью.
ТАР-блок может рассматриваться, как метод выбора, при операциях на передней брюшной стенке у пациентов с высоким кардиальным риском.
СЛУЧАЙ УСПЕШНОГО ОПЕРАТИВНОГО
ЛЕЧЕНИЯ РАЗРЫВА ПОСТТРАВМАТИЧЕСКОЙ ЛОЖНОЙ АНЕВРИЗМЫ ПЕРЕШЕЙКА АОРТЫ
Булда О.В., Гаспарян М.В., Алешин П.В., Шахназарян А.М., Шахназарян Н.Г., Паразян А.С., Жовнер Е.В.
ГБУЗ СК «Ставропольская краевая клиническая больница», г. Ставрополь
УДК: 616.135-02-007.64-089.168
CASE OF SUCCESSFUL SURGICAL
TREATMENT RUPTURE
OF POSTTRAUMATIC FALSE ANEURYSM
OF THE AORTIC ISTHMUS
Bulda O.V., Gasparjan M.V., Aleshin P.V., Shahnazarjan A.M., Shahnazarjan N.G., Parazjan A.S., Zhovner E.V
Одним из вариантов повреждения грудной аорты в результате закрытых травм грудной клетки является разрыв аорты или формирование ложной аневризмы. Разрыв аорты – крайне тяжелое и неблагоприятное по естественному течению состояние [4, 8, 9]. Среди пациентов с острым разрывом аорты приблизительно 2% выживают без операции, и у них формируются посттравматические ложные аневризмы аорты. В настоящее время основными видами закрытой травмы, приводящими к таким аневризмам, являются автомобильные аварии и падение с высоты [10].
В связи с характерным механизмом образования (при резком торможении тела) этот вид повреждения грудной аорты в англоязычной литературе получил название «децелерационный синдром» («decelerative syndrome») [2, 12, 14]. Классическим исследованием деце-лерационного синдрома до сих пор считается работа L. Parmley и соавт. (1958), основанная на 275 аутопсиях, связанных с травматическими повреждениями грудной аорты [12].
Синдром возникает вследствие резкого торможения, вызванного столкновением быстро движущегося тела человека с препятствием, что наблюдается чаще всего при автокатастрофах и падениях с высоты. При большой скорости движения и резком торможении за счет того, что недостаточно фиксированные сегменты аорты продолжают инерционное движение вперед, смещаясь относительно точек прочной фиксации аорты (корень аорты, перешеек в месте прикрепления артериальной связки и уровень аортального отверстия диафрагмы), в последних происходит надрыв внутренней оболочки аорты с образованием су-бинтимальной гематомы, а в последующем – посттравматической аневризмы [4, 7, 10]. Различие в подвижности при резком торможении между дугой аорты и ее нисходящей частью приводит к возникновению максимального напряжения на внутренней поверхности аорты выше точки наибольшей фиксации – аортальной связке. Именно поэтому в 90% случаев надрыв (а впоследствии и ложная аневризма) аорты локализуется в области ее перешейка [9, 12].
Причины высокой летальности при повреждениях грудной аорты вызваны как исходной тяжестью травмы (как правило, имеющей сочетанный ха- рактер), так и отсутствием оптимальной лечебно-диагностической тактики. Абсолютное большинство пострадавших с децелерационным синдромом первично попадают к общему хирургу, подвергаются неоправданно длительному динамическому наблюдению и умирают от прорыва формирующейся аневризмы аорты в плевральную или перикардиальную полость. При этом правильный топический диагноз ставится, как правило, посмертно [9].
В настоящей статье приводим случай успешного хирургического лечения разрыва острой ложной посттравматической аневризмы перешейка аорты.
Пациент Г., 23 лет, поступил в отделение сосудистой хирургии ГБУЗ СК «Ставропольской краевой клинической больницы» 29.10.2013 г. с жалобами на выраженную общую слабость, боль в грудной клетке при глубоком вдохе, боль в животе, охриплость голоса.
Из анамнеза известно, что 27.10.2013 г. в результате автомобильной аварии получил тяжелую сочетанную травму – тупую травму грудной клетки и живота с травматическим шоком 1 степени. Был госпитализирован в хирургическое отделение больницы скорой помощи, где комплексно обследован. Выявлены переломы IV-VII ребер справа, гемопневмоторакс справа, левосторонний гемоторакс, пульмонит справа, подкапсульные гематомы в печени, ушиб левой почки, посттравматическая аневризма нисходящего отдела грудной аорты. Консультирован ангиохирургом. 29.10.2013 г. переведен в отделение сосудистой хирургии ГБУЗ СК «СККБ» с целью дообследования и определения дальнейшей тактики лечения.
При поступлении: общее состояние пациента средней степени тяжести. Сознание ясное. Кожный покров и видимые