Выбор методики эндоскопического удаления субэпителиальных новообразований желудка
Автор: Хворова И. И., Шишин К. В., Недолужко И. Ю., Шумкина Л. В., Курушкина Н. А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Онкология
Статья в выпуске: 1 (83), 2023 года.
Бесплатный доступ
Введение. Современные тенденции развития хирургии характеризуются внедрением эндоскопических внутрипросветных технологий в варианты лечения пациентов с субэпителиальными новообразованиями желудка. Однако, не смотря на растущее число публикаций об успешном опыте выполнения данных операций, единого алгоритма выбора техники, с учетом всех характеристик опухоли, на сегодняшний день не существует. Цель исследования. Улучшить результаты лечения пациентов с субэпителиальными новообразованиями желудка. Материалы и методы. В основу работы положен ретроспективный анализ хирургического лечения 74 пациентов с субэпителиальными новообразованиями желудка в период с 2013 по 2022 гг. Вмешательства включили в себя 27 эндоскопических диссекций в подслизистом слое, 34 тоннельные диссекции, 10 эндоскопических мышечных диссекций и 3 полнослойные резекции.Результаты. Значимых интра- и послеоперационных осложнений, требующих изменения тактики лечения, не было. У 17(50%) пациентов, которым было выполнено тоннельное вмешательство, был выявлен карбоксиперитонеум. Лишь в 8(23,5 %) наблюдениях требовалась декомпрессия брюшной полости с использованием иглы Вереша. При выполнении контрольных ЭГДС и КТ органов грудной и брюшной полости (через 6 месяцев и 1 год) данных за рецидив заболевания не выявлено.Заключение. Разработанный алгоритм выбора методики эндоскопического удаления подслизистого новообразования желудка позволяет осуществить правильный доступ к опухоли, за счет чего операция может быть выполнена с минимальными временными затратами и минимальными рисками возникновения осложнений. Быстрая реабилитация является несомненным преимуществом эндоскопических вмешательств.
Подслизистые опухоли, эндоскопическая подслизистая диссекция, эндоскопическая мышечная диссекция, субэпителиальные новообразования
Короткий адрес: https://sciup.org/142237462
IDR: 142237462 | УДК: 616-072.1 | DOI: 10.17238/2072-3180-2023-1-64-72
Choice of the method of endoscopic resection of subepithelial gastric tumors
Introduction. The introduction of endoscopic intraluminal technologies is one of the current trends in the surgical treatment of patients with gastric subepithelial lesions. The number of publications showing the success of endoscopic operations is growing. Despite this and due to the variable characteristics of these tumors, there is no single algorithm for choosing a technique. Aim. To improve the results of treatment of patients with subepithelial lesions of the stomach.Materials and methods. We retrospectively analysed 74 patients with subepithelial lesions who underwent different endoscopic surgeries in our hospital from 2013 to 2022. 27 patients underwent endoscopic dissections in the submucosal layer, 34 tunnel dissections, 10 endoscopic muscle dissections and 3 full-thickness resections.Results. All surgical interventions were performed as planned. No intra- and postoperative complications requiring changes in therapeutic setting occurred. Carboxyperitoneum was detected in 17 patients (50%) who underwent tunnel intervention. Only 8 cases (23,5%) required decompression of the abdominal cavity using a Veress needle. Upper GI endoscopy and CT of the chest and abdominal cavity were performed at 6 and 12 months. No recurrence was observed.Conclusion. The developed algorithm for choosing a technique of gastric subepithelial lesions endoscopic removal allows to gain the correct access to the tumor. As a result of the operation can be performed with minimal time costs and risks of complications. Rapid rehabilitation is an undoubted advantage of endoscopic interventions.
Текст научной статьи Выбор методики эндоскопического удаления субэпителиальных новообразований желудка
В последнее время отчетливо определяется тенденция увеличения выявляемости субэпителиальных новообразований желудка, представляющих достаточно большую группу различных опухолей и пороков развития. Тактика хирургического лечения пациентов с субэпителиальными новообразованиями желудка в последние десятилетия претерпела определенные изменения и может значительно варьировать в зависимости от размеров новообразования, наличия клинических проявлений, прогнозирования характера опухоли и ее локализации как в различных отделах желудка, так и принадлежности к слоям стенки. Особый интерес вызывают субэпителиальные опухоли миогенного происхождения, среди которых выделяют группу гастроинтестинальных стромальных опухолей (ГИСО), имеющих повышенный злокачественный потенциал. Степень злокачественности, как правило, коррелирует с размерами новообразования более 2 см и наличием негомогенного строения опухоли [1, 2, 3].
Согласно современным представлениям все миогенные опухоли желудка размером более 2 см подлежат удалению. Однако популяризация и возрастающая доступность методов эндоскопической диагностики приводит выявлению опухолей небольшого размера (менее 2 см), которые, как правило, подлежат динамическому наблюдению. Динамическое наблюдение с применением эндоУЗИ позволяет выявить ранние признаки повышенного злокачественного потенциала (структурные изменения в виде наличия включений и негомогенного строения опухоли), которые определяют целесообразность удаления новообразований, не достигших целевых значений по размеру. Удаление малых новообразований, как правило, не требует проведения обширных резекций и выполнения лимфаденэктомии, принимая во внимание гематогенный характер возможного метастазирования [2, 4].
Это обстоятельство делает очень привлекательным применение эндоскопических внутрипросветных методов удаления опухоли. Вместе с тем технологии классической диссекции в подслизистом слое, направленные на сохранение целостности мышечного слоя, требуют усовершенствования и модификации.
Новые методики вмешательства должны минимизировать технические сложности закрытия полнослойного дефекта стенки желудка, возникающего в процессе удаления опухоли или минимизировать прогностические риски его возникновения на основании детального анализа данных предоперационного обследования и применения особых технических и методических приемов выполнения оперативного вмешательства. Сравнительно недавно появились первые сообщения о выполнении тоннельных или карманных методик удаления субэпителиальных новообразований, применения усовершенствованных методик эндоскопического закрытия полнослойных дефектов стенки желудка, технических особенностях контроля и профилактики осложнений [5, 6, 7].
Материалы и методы
Методики эндоскопического удаления новообразований желудка достаточно разнообразны и включают как варианты классической диссекции в подслизистом слое, так и варианты диссекции в мышечном слое (мышечная диссекция), тоннельные вмешательства, полнослойные резекции [8, 9, 10]. Ключевыми параметрами, определяющими выбор оптимального метода удаления, являются размер и особенности расположения опухоли как по отношению к слою стенки желудка, так и локализации ее в различных отделах желудка. По мере накопления опыта с учетом прогностической возможности технической реализации той или иной технологии вмешательства мы сочли целесообразным условно выделить в желудке несколько зон. При этом учитывались факторы аппаратной и инструментальной доступности новообразования, возможность обеспечения оперативного доступа в прямом и инверсивном положении аппарата, особенности анатомического анатомического строения желудка (толщина стенки, структура подслизистого слоя, интенсивность кровоснабжения, возможности закрытия полнослойного дефекта и др.) [11, 12, 13].
Идеальные условия для выполнения любого оперативного вмешательства обеспечиваются при стабильной позиции аппарата, наличии свободного инструментального доступа к опухоли, что в последующем значительно со- кращает временные затраты, риски развития неблагоприятных интраоперационных ситуаций и возможность их коррекции (рис. 1).
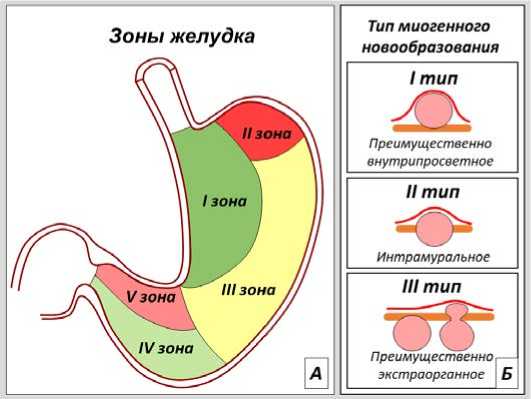
Рис. 1. Особенности локализации субэпителиальной опухоли желудка, влияющие на выбор типа оперативного вмешательства Fig. 1. Features of the localization of a subepithelial lesion of the stomach, influencing the choice of surgical intervention
В процессе работы мы посчитали целесообразным выделить 5 зон желудка. Цветовая маркировка зон желудка в соответствии с аппаратной и инструментальной доступ- ностью, представленная на рисунке 1А, придерживается «принципа светофора». Более доступные зоны отмечены оттенками зеленого цвета, умеренно доступные – желтым, неблагоприятные – оттенками красного цвета. Суммарные характеристики зон желудка в аспекте трудностей создания эндоскопического оперативного доступа суммированы в таблице 1.
I зона захватывает кардиальный отдел желудка, переднюю и заднюю стенки тела по малой кривизне до уровня угла желудка. Расположение опухоли в I зоне является оптимальной локализацией для выполнения любого эндоскопического вмешательства от диссекции в подслизистом слое до удаления опухоли по тоннельной технологии. Оперативный доступ может быть реализован в прямом положении эндоскопа. При этой локализации складываются благоприятные условия для вмешательства, оперативный доступ к области интереса находится под острым углом к стенке желудка, что облегчает работу в подслизистом слое и минимизирует риски полнослойного повреждения. Мышечный слой стенки желудка в I зоне достаточно выражен, что позволяет проводить диссекцию в подслизистом слое с элементами мышечной диссекции. Подслизистый слой как правило не содержит жировой ткани, что делает предсказуемым работу электрохирургического оборудования. Относительно неблагоприятным фактором является достаточно выраженное кровоснабжение подслизистого слоя. Однако работа в нем в условиях благоприятного технологического доступа, как правило, не сопровождается значительными трудностями осуществления гемостаза (рис. 2).
Таблица 1
Характеристика зон желудка в аспекте особенностей реализации оперативного доступа
Table 1
Characteristics of the zones of the stomach
|
Зоны |
Локализация |
Оперативные особенности |
|
|
I |
Кардиальный отдел желудка, передняя и задняя стенки тела по малой кривизне до уровня угла желудка/ The cardial part of the stomach, the anterior and posterior walls of the body along the lesser curvature to the level of the angle of the stomach |
Позиция аппарата/ Endoscope position |
Прямая/ Direct |
|
Стабильность аппарата/ Endoscope stability |
Высокая/ High |
||
|
Инструментальный доступ/ Instrumental access |
Под острым углом/ At an acute angle |
||
|
Маневренность аппарата/ Endoscope maneuverability |
Высокая/ High |
||
|
Толщина мышечного слоя/ Muscle layer thickness |
Средняя/ Medium |
||
|
Кровоснабжение/ Blood supply |
Высокое/ High |
||
|
Жировая ткань/ Fat tissue |
Немного/ Little |
||
Продолжение Таблицы 1
|
II |
Свод желудка/ Fornix of the stomach |
Позиция аппарата/ Endoscope position |
В инверсии/ Inversion |
|
Стабильность аппарата/ Endoscope stability |
Низкая/ Low |
||
|
Инструментальный доступ/ Instrumental access |
Под прямым углом/ At the right angle |
||
|
Маневренность аппарата/ Endoscope maneuverability |
Низкая/ Low |
||
|
Толщина мышечного слоя/ Muscle layer thickness |
Малая/ Little |
||
|
Кровоснабжение/ Blood supply |
Небольшое/ Little |
||
|
Жировая ткань/ Fat tissue |
Немного/ Little |
||
|
III |
Большая кривизна и примыкающие к ней участки передней и задней стенки тела желудка/ Greater curvature and adjacent areas of the anterior and posterior wall of the body of the stomach |
Позиция аппарата/ Endoscope position |
«Длинная» позиция/ “Long” position |
|
Стабильность аппарата/ Endoscope stability |
Низкая/ Low |
||
|
Инструментальный доступ/ Instrumental access |
Индивидуально/ Individual |
||
|
Маневренность аппарата/ Endoscope maneuverability |
Индивидуально/ Individual |
||
|
Толщина мышечного слоя/ Muscle layer thickness |
Толстый/ Thick |
||
|
Кровоснабжение/ Blood supply |
Высокое/ High |
||
|
Жировая ткань/ Fat tissue |
Выражена/ Thick |
||
|
IV |
Большая кривизна и примыкающие к ней участки передней и задней стенки антрального отдела желудка/ Greater curvature and adjacent areas of the anterior and posterior wall of the antrum |
Позиция аппарата/ Endoscope position |
Прямая на «длинной» позиции/ Direct at “long” position |
|
Стабильность аппарата/ Endoscope stability |
Средняя/ Medium |
||
|
Инструментальный доступ/ Instrumental access |
Под острым углом/ At an acute angle |
||
|
Маневренность аппарата/ Endoscope maneuverability |
Средняя/ Medium |
||
|
Толщина мышечного слоя/ Muscle layer thickness |
Толстый/ Thick |
||
|
Кровоснабжение/ Blood supply |
Среднее/ Medium |
||
|
Жировая ткань/ Fat tissue |
Индивидуально/ Individual |
||
|
V |
Малая кривизна и примыкающие к ней участки передней и задней стенки антрального отдела желудка/ Lesser curvature and adjacent areas of the anterior and posterior wall of the antrum of the stomach |
Позиция аппарата/ Endoscope position |
Инверсия на «длинной» позиции/ Inversion at “long” position |
|
Стабильность аппарата/ Endoscope stability |
Низкая/ Low |
||
|
Инструментальный доступ/ Instrumental access |
Под прямым углом/ At the right angle |
||
|
Маневренность аппарата/ Endoscope maneuverability |
Низкая/ Low |
||
|
Толщина мышечного слоя/ Muscle layer thickness |
Толстый/ Thick |
||
|
Кровоснабжение/ Blood supply |
Высокое/ High |
||
|
Жировая ткань/ Fat tissue |
Индивидуально/ Individual |
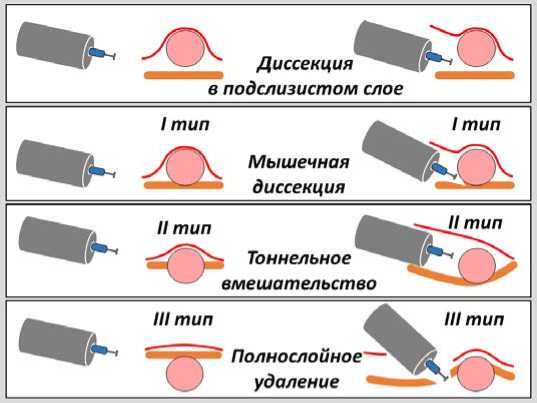
Рис. 2. Типы оперативных вмешательств при локализации опухоли в I зоне желудка Fig. 2. Types of surgical interventions for lesions localized in the I zone of the stomach
II зона желудка представляет собой свод (или фундальный отдел) желудка. Аппаратный и инструментальный доступ к новообразованию возможны только в инверсионой позиции гастроскопа в максимально неудобном положении под прямым углом к области интереса. Область малодоступна для осуществления тоннельного вмешательства. Даже при формировании оперативного доступа из пищевода острый угол не позволяет сделать тоннель без высокого риска повреждения слизистой изгибом аппарата. Кроме этого эндоскопические вмешательства в этой области по поводу миогенных новообразований всегда чреваты развитием перфорации вследствие тонкой мышечной стенки желудка (рис. 3).
III зона – большая кривизна и примыкающие к ней участки передней и задней стенки тела желудка. Эта зона также характеризуется трудностью создания эндоскопического оперативного доступа вследствие наличия технических трудностей достижения стабильности эндоскопа и его изгиба по большой кривизне тела желудка. Подчас создание оперативного доступа к области интереса занимает существенную часть оперативного вмешательства. Подслизистый слой характеризуется большим количеством жировой ткани, затрудняющей работу электрохирургическим инструментом.
IV зона – большая кривизна антрального отдела. Эндоскопический доступ достаточно благоприятный для выполнения диссекции в подслизистом слое, в том числе мышечной диссекции. Условия для реализации тоннельного доступа также достаточно благоприятные. Аппаратная доступность обеспечивается на «длинной» позиции гастроскопа, которая достаточно стабильна при умеренной инсуфляции газа и избегании чрезмерного раздувания желудка. Инструменталь- ный доступ осуществляется под острым углом к плоскости диссекции.
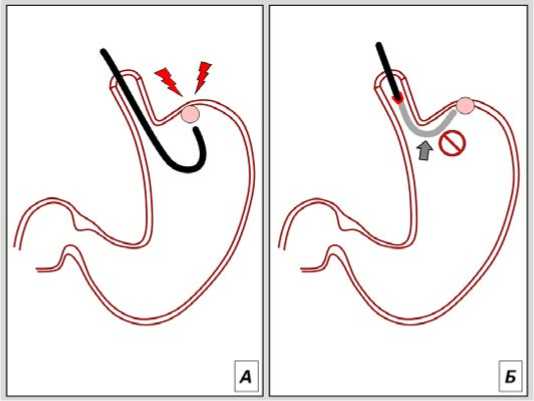
Рис. 3. Оперативный эндоскопический доступ к новообразованиям II зоны желудка. А) Высокий риск перфорации при диссекции.
Б) Сложности создания тоннеля. Стрелкой указан участок вероятной перфорации тоннеля в области изгиба аппарата
Fig. 3. Operative endoscopic access to neoplasms located in the IId zone of the stomach. A) High risk of perforation during dissection.
B) Difficulties in creating a tunnel. The arrow indicates the area of probable perforation of the tunnel in the area of the device bend
V зона – малая кривизна антрального отдела желудка. Очень сложная зона для технической реализации комфортных условий операции. Оперативная доступность реализуется в «длинной» позиции эндоскопа с инверсией. Технические условия для реализации тоннельного вмешательства неблагоприятные как для формирования доступа, так и последующей диссекции в подслизистом слое. Изгиб аппарата, как правило, приводит к разрыву слизистой в области доступа и отсутствию технической возможности завершения операции по тоннельной методике. Кроме этого, повышенное кровоснабжение данной локализации сопровождается рисками развития выраженного кровотечения и сложностями эндоскопического гемостаза.
Следующим важнейшим критерием, который необходимо учитывать при планировании метода эндоскопического удаления опухоли, является характер роста новообразования относительно просвета желудка и принадлежность опухоли к слою желудочной стенки. Информация о локализации новообразования относительно слоев стенки желудка являлась одной из задач при проведении эндоскопической ультрасонографии, особенного для опухолей миогенного характера.
Опухоли, исходящие из 2 и 3 эхо-слоя (мышечная пластинка слизистой и подслизистый слой), стандартно удаляются методом диссекции в подслизистом слое. Зона желудка в данной ситуации не имеет принципиального значения. Исключение составляют новообразования с локализацией во II зоне, где выполнение диссекции сопряжено с большими техническими трудностями. В каждом конкретном случае с учетом индивидуальных особенностей локализации и наличия аппаратноинструментального доступа к опухоли следует рассматривать вопрос о выполнении полнослойного удаления эндоскопическим или лапароскопическим доступом, что подчас технически реализуется с меньшими рисками осложнений.
Выбор оптимальной методики удаления миогенных новообразований, исходящих из 4 слоя (мышечная оболочка стенки), представляет собой ключевой вопрос разумного взвешенного прогнозирования эффективности и безопасности оперативного вмешательства. В зависимости от локализации опухоли в разных отделах желудка и характера роста возможно выполнение 3 типов операции: мышечной диссекции, удаления опухоли по тоннельной технологии и полнослойной резекции. При этом характер роста миогенной опухоли и ее взаимоотношение с мышечной стенкой желудка имеет одно из ключевых значений [14, 15].
Мы предлагаем выделять три типа миогенных новообразований (рис. 1Б).
-
• I тип – преимущественно внутрипросветное. Основной массив опухоли расположен в подслизистом пространстве, однако по ЭУС прослеживается «ножка» новообразования, исходящая из мышечного слоя, толщина которой менее половины диаметра новообразования.
-
• II тип – интрамуральное расположение. При этом центральная часть опухоли располагается в толще мышечные оболочки. Опухоль равномерно распространяется в просвет желудка и экстраорганно.
-
• III тип – преимущественно экстраорганный тип роста опухоли. При этом большая часть новообразования или его больший узел расположены за пределами стенки желудка. Внутрипросветная часть опухоли может едва контурироваться.
Наиболее оптимальные условия для выполнения эндоскопического вмешательства складывались при наличии у пациента опухоли I типа. При локализации новообразования в зонах, благоприятных для выполнения тоннельного вмешательства (I и IV зона), оно имело явный приоритет. Основанием для выбора тоннельного вмешательства являлось возможность реализации максимально безопасного вмешательства с полноценным закрытием слизистой даже при выполнении полнослойной резекции. При выделении опухоли из мышечного слоя стремились к выполнению операции по типу энуклеации с элементами мышечной диссекции. Дозированное рассечение мышечных волокон при выполнении мышечной диссекции позволяло безопасно закончить оперативное вмешательство без применения сложных и дорогостоящих технологий закрытия дефектов стенки желудка.
В случае наличия у пациента опухоли III и V зоны приоритетным методом удаления являлась диссекция в подслизистом слое с мышечной диссекцией или полнослойное удаление. В каждом конкретном случае решение принималось индивидуально в зависимости от особенностей местного статуса.
Эндоскопическое вмешательство при расположении опухоли в II зоне нецелесообразно. В этой ситуации возникали наиболее выраженные трудности, связанные с инверсионным положением гастроскопа и ограничением свободных манипуляций, что делает вмешательство менее безопасным и более трудоемким.
Удаление миогенных опухолей II типа всегда сопровождается формированием полнослойного дефекта стенки желудка. В I и IV зонах желудка, благоприятных для выполнения тоннельного вмешательства, рассматривали эту технологию в качестве приоритетной. Для удаления опухолей другой локализации целесообразно выполнение полнослойного удаления новообразования эндоскопическим или лапароскопическим способом [15].
При экстраорганном расположении миогенной опухоли (III тип) вне зависимости от локализации по зонам приоритет отдавался полнослойной резекции. В настоящее время технология может быть реализована эндоскопически и лапароскопическим доступом. Эндоскопическая полнослойная резекция является достаточно сложной в техническом исполнении, относится к операциям экспертного уровня и, безусловно, не может быть широко рекомендована. Техническая готовность проведения подобных вмешательств заключается не только в наличии большого опыта диссекций у оперирующего хирурга, но и технической возможности применения надежных методов гемостаза и закрытия больших перфораций стенки желудка, согласованной работы с анестезиологической бригадой в условиях неминуемо возникающего карбоксиперитонеума. Подчас в этой ситуации лапароскопическое вмешательство в виде атипичной резекции желудка является более обоснованным выбором в отношении безопасности вмешательства и реализует принцип выбора оптимального метода лечения [13].
В результате комплексного анализа была сформирован следующий алгоритм выбора методики эндоскопического вмешательства, представленный в таблице 2, который хорошо зарекомендовал себя в серии наших практических наблюдений.
Результаты
С 2013 по 2022 гг. в МКНЦ им. А. С. Логинова было прооперировано 74 пациента с подслизистыми опухолями желудка. Стандартный протокол обследования включал в себя выполнение эндоскопической ультрасонографии и компьютерной томографии. Показаниями к хирургическому лечению являлись рост опухоли в процессе динамического наблюдения или изменение ее структуры по данным ЭУС, а также наличие клинических проявлений заболевания (кровотечение, дисфагия, боль в животе).
Таблица 2
Выбор методики удаления подслизистых новообразований в зависимости от расположения и типа роста
Table 2
The choice of methods for resection submucosal tumors depending on the location end type of growth
|
Эхо-слой стенки желудка/ Echo layer of the stomach wall |
|||||
|
2 слой/ 1 layer |
3 слой/ 3 layer |
4 слой I тип/ 4 layer I type |
4 слой II тип/ 4 layer II type |
4 слой III тип/ 4 layer III type |
|
|
I |
ЭДПС/ ESD |
ЭДПС/ ESD |
ЭТВ/ ETD |
ЭТВ/ ETD |
ПУ/ FTR |
|
II |
ЭДПС/ ESD ПУ/ FTR |
ЭДПС/ ESD ПУ/ FTR |
ПУ/ FTR |
ПУ/ FTR |
ПУ/ FTR |
|
III |
ЭДПС/ ESD |
ЭДПС/ ESD |
ЭМД/ EMD ПУ/ FTR |
ПУ/ FTR |
ПУ/ FTR |
|
IV |
ЭДПС/ ESD |
ЭДПС/ ESD |
ЭМД/ EMD ЭТВ/ ETD |
ЭТВ/ ETD |
ПУ/ FTR |
|
V |
ЭДПС/ ESD |
ЭДПС/ ESD |
ЭМД/ EMD ПУ/ FTR |
ПУ/ FTR |
ПУ/ FTR |
|
ЭДПС/ ESD |
эндоскопическая диссекция в подслизистом слое / endoscopic submucosal dissection |
||||
|
ЭМД/ EMD |
эндоскопическая мышечная диссекция / endoscopic muscle dissection |
||||
|
ЭТВ/ ETD |
эндоскопическое тоннельное вмешательство / endoscopic tunnel dissection |
||||
|
ПУ/ FTR |
полнослойн ое удаление / full-thickness remo val |
||||
Все оперативные вмешательства были выполнены под эн-дотрахеальным наркозом. Средний размер опухоли составил 2,6 см. Всего было выполнено 27 эндоскопических диссекций в подслизистом слое, 34 тоннельные диссекции, 10 эндоскопических мышечных диссекций и 3 полнослойные резекции. В серии наших наблюдений был проведен комплексный анализ типа выполненных оперативных вмешательств в зависимости от особенностей локализации опухолей (рис. 4).
Следует отметить, что большинство удаленных новообразований располагались в отделах желудка, наиболее удобных для выполнения эндоскопического вмешательства. В процессе накопления клинического материала при выборе методики оперативного вмешательства преследовали своей целью выбор наиболее оптимального типа операции, соответствующей соблюдению принципа достижения положительного результата с минимальными техническими трудностями и рисками раз- вития осложнений. Послеоперационных осложнений, требующих изменения тактики лечения или увеличивающих койкодень, зафиксировано не было. Основным интраоперационным нежелательным явлением являлся карбоксиперитонеум, который регулировался умеренной подачей газа и активной аспирацией. Лишь 8 пациентам требовалась декомпрессия брюшной полости с использованием иглы Вереша. В день операции пациентам разрешалась пить воду. При отсутствии отклонений от нормального течения послеоперационного периода пациенты выписывались на следующий либо через день после операции.
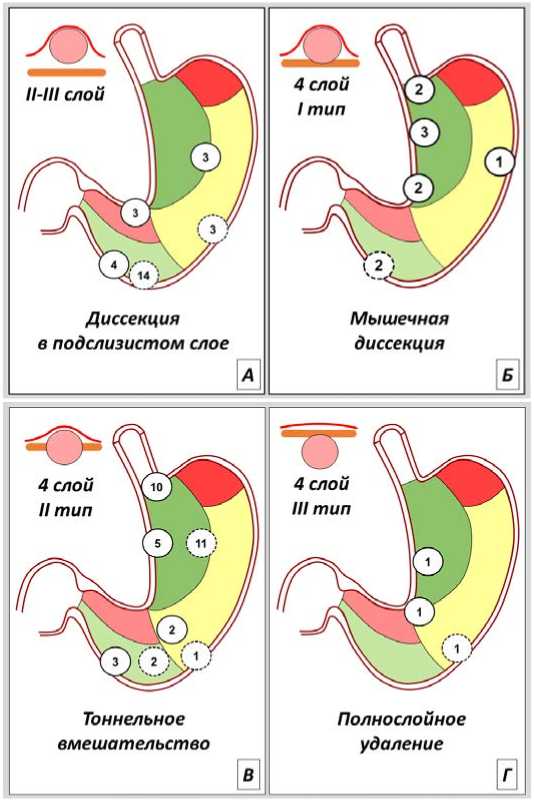
Рис. 4. Типы выполненных вмешательств в зависимости от локализации новообразования. А) Диссекция в подслизистом слое. Б) Мышечная диссекция. В) Тоннельное вмешательство. Г) Полнослойное удаление. Пунктиром обозначены новообразования с преимущественной локализацией на задней стенке желудка Fig. 4. Types of interventions performed depending on the location of the neoplasm. A) Dissection in the submucosal layer. B) Muscular dissection. C) Tunnel dissection. D) Full-thickness removal. The dotted line indicates neoplasms with predominant localization in the posterior wall of the stomach
По результатам гистологического и иммуногистохимического исследований удаленные опухоли чаще всего являлись гастроинтестинальными стромальными опухолями, лейомиомами, фиброзно-воспалительными полипами и липомами. Период наблюдения составил от 2 месяцев до 8 лет. Рецидивов заболеваний за весь период наблюдения не было отмечено.
Заключение
Разработанный алгоритм выбора метода эндоскопического удаления субэпителиальных новообразований желудка хорошо зарекомендовал себя при лечении достаточно большой группы пациентов, показал свою эффективность и может быть рекомендован для практического применения.
Список литературы Выбор методики эндоскопического удаления субэпителиальных новообразований желудка
- Kubota A., Kuwabara S., Yamaguchi K., Kobayashi K., Hashidate H. Gastrointestinal stromal tumor of the stomach with lymph node metastasis treated by laparoscopic and endoscopic cooperative surgery with lymph node pick-up resection: A case report and literature review. Int. J Surg. Case Rep., 2020, № 77, pp. 178-181. https://doi.org/10.1016/j.ijscr.2020.10.131
- Buldanlı M. Z., Yener O. Endoscopic Resection of Upper Gastrointestinal Subepithelial Tumours: Our Clinical Experience and Results. Prague Med Rep., 2022, № 123(1), pp. 20-26. https://doi.org/s://doi:10.14712/23362936.2022.2
- Chen H., Li B., Li L., Vachaparambil C.T., Lamm V., Chu Y., Xu M., Cai Q. Current Status of Endoscopic Resection of Gastric Subepithelial Tumors. Am J Gastroenterol., 2019, № 114(5), pp.718-715. https://doi.org/10.14309/ajg.0000000000000196
- Chen Q., Yu M., Lei Y., Zhong C., Liu Zh., Zhou X. , Li G., Zhou X., Chen Y. Efficacy and safety of endoscopic submucosal dissection for large gastric stromal tumors. Clin. Res. Hepatol Gastroenterol., 2020, № 44(1), pp. 90-100. https://doi.org/10.1016/j.clinre.2019.03.004
- Granata A., Martino A., Amata M., Ligresti D., Tuzzolino F., Traina M. Efficacy and safety of gastric exposed endoscopic full-thickness resection without laparoscopic assistance: a systematic review. Endosc. Int. Open., 2020, № 8(9), pp. E1173-E1182. https://doi.org/10.1055/a-1198-4357
- Goto, E., Koizumi, K. Higuchi, H., Noda, T., Onda , J., Omori J., Kaise M., Iwakiri K. Cutting-Edge Technologies for Gastrointestinal Therapeutic Endoscopy. J Nippon Med. Sch., 2021, № 88(1), pp. 17-24. https://doi.org/s://doi:10.1272/jnms.JNMS.2021_88-109
- Granata A., Martino A., Amata M., Ligresti D., Traina M. Gastrointestinal exposed endoscopic full-thickness resection in the era of endoscopic suturing: a retrospective single-center case series. Wideochir Inne Tech Maloinwazyjne, 2021, № 16(2), pp. 321-328. https://doi.org/10.5114/wiitm.2021.104496
- Nabi, Z., Reddy D. N., Ramchandani M. Recent Advances in Third-Space Endoscopy. Gastroenterol Hepatol (N Y), 2018, № 14(4), pp. 224-232.
- Santos-Antunes J., Marques M., Morais R., Baldaque-Silva F.,Vilas-Boas F., Moutinho-Ribeiro P., Lopes S., Carneiro F., Macedo G. Retrospective analysis of the outcomes of endoscopic submucosal dissection for the diagnosis and treatment of subepithelial lesions in a center with high expertise. Ann Gastroenterol., 2022, № 35(1), pp. 68-73. https://doi.org/10.20524/aog.2021.0675
- Dellatore P., V. Bhagat, Kahaleh M. Endoscopic full thickness resection versus submucosal tunneling endoscopic resection for removal of submucosal tumors: a review article. Transl. Gastroenterol. Hepatol., 2019, № 4, pp. 829-854. https://doi.org/10.21037/tgh.2019.05.03
- Abe S., Wu S., Ego M., Takamaru H., Sekiguchi M., Yamada M., Nonaka S., Sakamoto T., Suzuki H. , Yoshinaga Sh., Matsuda T., Oda I., Saito Y. Efficacy of Current Traction Techniques for Endoscopic Submucosal Dissection. Gut. Liver., 2020, № 14(6), pp. 673-684. https://doi.org/10.5009/gnl19266
- Chang J. , Kim T. J., Hwang N. Y., Sohn I., Min Y. W., Lee H., Min B. H., Lee J. H., Rhee P., Kim J. J. Clinical Outcomes and Adverse Events of Gastric Endoscopic Submucosal Dissection of the Mid to Upper Stomach under General Anesthesia and Monitored Anesthetic Care. Clin. Endosc., 2022, № 55(1), pp. 77-85. https://doi.org/10.5946/ce.2021.002
- Liu S., Zhou X., Yao Y., Shi K., Yu M., Ji F. Resection of the gastric submucosal tumor (G-SMT) originating from the muscularis propria layer: comparison of efficacy, patients’ tolerability, and clinical outcomes between endoscopic full-thickness resection and surgical resection. Surg. Endosc., 2020, № 34(9), pp. 4053-4064. https://doi.org/10.1007/s00464-019-07311-x
- Старков Ю.Г., Солодинина Е.Н., Джантуханова С.В., Выборный М.И. Классификация неэпителиальных опухолей верхних отделов желудочно-кишечного тракта для выбора способа оперативного вмешательства. Поволжский онкологический вестник, 2017. № 5(32). С. 45-50.
- Guo J.T., Zhang J. J., Wu Y. F., Liao Y., Wang Y. D., Zhang B. Zh., Wang Sh. , Sun S. Y. Endoscopic full-thickness resection using an overthe-scope device: A prospective study. World J Gastroenterol., 2021, № 27(8), pp. 725-736. https://doi.org/10.3748/wjg.v27.i8.725


