Выделение кислоты из отработанного травильного раствора методом диффузионного диализа с анионообменной мембраной
Автор: Козадерова О.А., Чернова В.Ю.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 3 (101) т.86, 2024 года.
Бесплатный доступ
При травлении стали образуются отходы - отработанные травильные растворы, содержащие свободные кислоты и соли металлов. Такие растворы необходимо перерабатывать или утилизировать. В статье показана возможность применения диализа для выделения соляной кислоты из такого раствора. Преимуществом этого мембранного метода являются компактность оборудования, возможность частичной регенерации компонентов сточной воды и организация замкнутого цикла потребления химических веществ на производстве, возможность комбинации с другими мембранными методами. Исследован процесс диффузионного диализа модельного раствора, содержащего соляную кислоту (1,5 моль/дм3) и хлорид железа (III) (0,25 моль/дм3). Эксперимент проведен в двухкамерном противоточном диализаторе с анионообменной мембраной МА-41 в режиме рецикла. Эффективность разделения компонентов раствора охарактеризована такими параметрами процесса, как потоки кислоты через мембрану, коэффициент разделения, коэффициент задержания соли. Процесс проведен в двух вариантах: при соотношениях объемов отдающего (питающего) и принимающего растворов равного 1:1 (первый вариант) и 2:1 (второй вариант). При диализе изучаемого модельного раствора получены следующие значения коэффициентов разделения соляная кислота/соль железа (III) для первого и второго вариантов соответственно: 27,2 и 19,2. Соотношение объемов отдающего и принимающего растворов, равное 2:1, позволяет получить раствор соляной кислоты заданной концентрации за меньшее время, чем при соотношении объемов отдающего и принимающего растворов, равном 1:1. Преимуществом первого варианта проведения эксперимента является возможность получения более чистого целевого продукта - раствора соляной кислоты (с меньшим содержанием соли железа (III)).
Соляная кислота, хлорид железа (iii), травильный раствор, диффузионный диализ, очистка
Короткий адрес: https://sciup.org/140308566
IDR: 140308566 | УДК: 66.081.62 | DOI: 10.20914/2310-1202-2024-3-217-222
Recovery of acid from spent pickling solution by diffusion dialysis with anion exchange membrane
When etching steel, waste products such as spent etching solutions containing free acids and metal salts are formed, and such solutions must be recycled or disposed of. The article shows the possibility of using dialysis to isolate hydrochloric acid from these solutions. The advantage of this membrane method is the compactness of the equipment, the possibility of partial regeneration of wastewater components and the organization of a closed cycle of chemical consumption in production, as well as the possibility of combination with other membrane methods. The process of diffusion dialysis of a model solution containing hydrochloric acid (1.5 mol/dm3) and iron (III) chloride (0.25 mol/dm3) has been studied. The experiment was carried out in a two-chamber countercurrent dialyzer with an anion exchange membrane MA-41 in the recycle mode. The efficiency of separation of the solution components is characterized by such process parameters as acid fluxes through the membrane, separation coefficient, and salt rejection coefficient. The process was carried out in two versions: with the volume ratios of the giving (feeding) and receiving solutions equal to 1:1 (first variant) and 2:1 (second variant). During dialysis of the studied model solution, the following values of the hydrochloric acid/iron (III) salt separation coefficients were obtained for the first and second variants, respectively: 27.2 and 19.2. The volume ratio of the giving and receiving solutions, equal to 2:1, allows us to obtain a hydrochloric acid solution of a given concentration in less time than with a volume ratio of giving and receiving solutions equal to 1:1. The advantage of the first variant of the experiment is the possibility of obtaining a cleaner target product, namely a solution of hydrochloric acid (with a lower content of iron (III) salt).
Текст научной статьи Выделение кислоты из отработанного травильного раствора методом диффузионного диализа с анионообменной мембраной
Травление стали в растворах кислоты относится к химическим способам очистки металлов. Такие способы применяются при серийном и массовом производстве изделий из нержавеющих сталей с целью восстановления утраченных под воздействием температуры антикоррозионных свойств. Кроме химической очистки применяются электрохимическое травление, механическая и лазерная обработка [1].
Травление стали проводят обычно в растворах соляной и серной кислот. Преимуществом соляной кислоты по сравнению с серной является высокая скорость травления, небольшая относительно массы удаляемой окалины масса шлама, низкая плотность этого шлама, что облегчает его последующее удаление с поверхности изделия [2].
This is an open access article distributed under the terms of the Creative Commons Attribution 4.0 International License
Кроме растворов соляной и серной кислот применяют травильные растворы других составов: раствор хлорида железа, плавиковая кислота – азотная кислота, бихромат калия – серная кислота, соляная кислота – уротропин, сульфат меди – серная кислота – желатин [3].
При травлении стали образуются отходы – отработанные травильные растворы, содержащие свободные кислоты и соли металлов. Тип и концентрация кислот и солей в таких отходах определяются применяемым травильным раствором, который выбирается в зависимости от вида обрабатываемой стали. Объем кислых сточных вод от промывки бунтов до и после операции травления в кислотном растворе, составляет более 3,5 м³ на одну тонну протравленного кислотой горячекатаного проката или проволоки [4].
Отработанный травильный раствор необходимо перерабатывать или утилизировать. Среди методов переработки травильных растворов выделяют ионообменную очистку, нейтрализацию, микробиологическую очистку, выпаривание, кристаллизацию, пирометаллургию, экстракцию и процессы мембранного разделения (диффузионный диализ, электродиализ, мембранную дистилляцию) [5–11].
Процесс ионообменной переработки отработанного травильного раствора состоит из двух этапов. Сначала через слой анионита пропускают отработанный травильный раствор (стадия удерживания кислоты), затем – разбавленный водный раствор кислоты (стадия вытеснения кислоты) [6]. Удерживание кислоты на анионите осуществляется за счет исключения сильно гидратированных ионных пар соли, которые в меньшей степени, чем молекулы или ионные пары кислоты, проникают в нанораз-мерные «поры» гелевого анионита. В работе [6] такой вариант разделения кислоты и соли на сильноосновном анионите АВ-17x8 в сульфатной форме продемонстрирован для реального отработанного травильного раствора промышленного предприятия черной металлургии (состав – более 200 г/дм3 сульфата железа и более 65 г/дм3 серной кислоты).
Пример комбинации метода нейтрализации и мембранного электролиза для конверсии отработанного кислого травильного раствора, образующегося в процессе травления изделий из титана соляной кислотой, описан в работе [7]. Процесс включает в себя нейтрализацию этого раствора щелочью, фильтрацию и сушку осадка гидроксида титана, а также электрохимическую переработку фильтрата, содержащего хлорид натрия, в электролизёре с ионообменными мембранами.
В последние годы проявляется интерес к микробиологической переработке сточных вод, содержащих тяжелые металлы. Обзор материала по этой теме можно найти в работе [8].
При диффузионном диализе с анионообменной мембраной ионы кислого отработанного раствора (питающего раствора) мигрируют через мембрану в приемную камеру, через которую прокачивается дистиллированная вода, под действием градиента концентрации. Фиксированные группы анионообменной мембраны заряжены положительно, в связи с этим анионы могут беспрепятственно мигрировать через мембрану, в то время как большинство катионов (коинов) отторгаются мембраной в силу Доннановского исключения. Однако, при диффузионном диализе миграция катионов через анионообменную мембрану из исходного раствора в принимающий необходима для поддержания электронейтральности растворов. Перенос катионов через анионообменную мембрану происходит в результате их увлечения анионами. Водородные ионы мигрируют через анионообменную мембрану легче, чем другие катионы, из-за небольшого размера, низкого заряда, высокой подвижности, особого механизма переноса в водных растворах. В результате при диффузионном диализе смешанного раствора «соль-кислота» можно получить пермеат, обогащенный кислотой, и ретентат, обогащенный солью.
Варианты применения диффузионного диализа можно найти как для разделения органических кислот/минеральных солей, так и для разделения неорганических кислот/минеральных солей [9–13]. В работе [11] рассмотрена возможность использования различных типов ионообменных мембран в диффузионном диализе для разделения серной кислоты и сульфата никеля. Изучен процесс диализного разделения реального раствора отходов гальванического производства следующего состава: 252,3 г/л серной кислоты, 20,9 г/л ионов никеля, небольшие количества ионов цинка, железа, меди.
Цель работы – оценка возможности выделения кислоты из раствора, содержащего соляную кислоту и соль – хлорид железа (III), методом диффузионного диализа с анионообменной мембраной МА-41 и получение основных характеристик этого процесса.
Материалы и методы
Объект исследования – раствор, моделирующий отработанный травильный раствор, следующего состава: соляная кислота 1,5 моль/дм3, хлорид железа (III) 0,25 моль/дм3. Железо способно к образованию хлоридных комплексов.
В изучаемом растворе большая доля Fе3+ (около 75%) представлена в виде [FеСl 2 ]+. Изучение диффузионного переноса соляной кислоты и соли железа (III) через анионообменную мембрану проводили с применением двухкамерного проточного диализатора (рисунок 1). Исследуемый раствор (питающий раствор, рисунок 1) подавали с помощью перистальтического насоса в режиме рецикла в одну из камер снизу вверх.
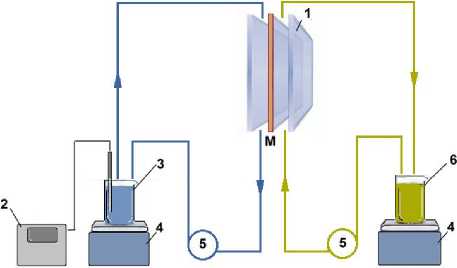
Рисунок 1. Схема установки для реализации периодического диализа: 1 – двухкамерная ячейка с анионообменной мембраной М; 2 – рН-метр; 3 – емкость с приемным раствором; 4 – магнитная мешалка; 5 – перистальтический насос; 6 – емкость с питающим раствором
Figure 1. Installation scheme for the implementation of periodic dialysis: 1 – two-chamber cell with an anion exchange membrane M; 2 – рН meter; 3 – container with a receiving solution; 4 – magnetic stirrer; 5 – peristaltic pump; 6 – container with a feeding solution
Через смежную камеру (приемную) в режиме рецикла подавали противотоком (сверху вниз) дистиллированную воду. Скорость потоков через камеры 20 см3/мин. Толщина камер 1 см. Рабочая площадь мембраны в ячейке 67 см2. С течением времени эксперимента в приемной камере происходило увеличение концентрации диффундирующих веществ. Рассматривали два варианта соотношения объемов отдающего (питающего) и принимающего растворов – 1:1 и 2:1. В первом случае максимально возможная концентрация соляной кислоты, которую теоретически можно получить в приемной камере, составляет 0,75 моль/дм3. Это соответствует степени извлечения кислоты 50%. Для второго варианта возможно получение кислоты более высокой концентрации. Однако в настоящей работе мы ограничились получением пермеата с одинаковой концентрацией по соляной кислоте для первого и второго вариантов.
Расчет критериев эффективности процесса – отношения концентраций Fе3+/Н+ в пермеате (r Fе3+/Н+ ), потоков кислоты (J i , моль·см-2/с), коэффициента задержания соли (R), а также коэффициента разделения (S) – проводили по формулам:
Камеры диализатора разделяла мембрана МА-41 [14]. Это гетерогенная сильноосновная анионообменная мембрана, представляющая собой композицию из полиэтилена и сополимера стирола и дивинилбензола с четвертичными аммониевыми группами. Толщина мембраны 0,046 см. Перед проведением экспериментов мембрану кондиционировали в соответствии с методикой [15], затем переводили в хлоридную ионную форму. После этого мембрану выдерживали в рабочем растворе не менее суток, после чего отмывали водой до отсутствия в промывных водах кислоты и железа.
Контроль изменения концентрации кислоты в пермеате осуществляли в течение эксперимента (метод прямой потенциометрии, измерение рН раствора), в пермеате и ретентате по окончании эксперимента (кислотно-основное титрование). Содержание железа (III) в пермеате и ретентате находили по окончании эксперимента (комплексонометрическое титрование: раствор Трилона Б в присутствии сульфосалициловой кислоты).
Результаты и обсуждение
На рисунке 2 приведены кинетические кривые изменения концентрации соляной кислоты в принимающем растворе.
И для первого, и для второго вариантов эксперимента сначала наблюдается линейная зависимость концентрации от времени, затем прирост концентрации кислоты замедляется.
Рисунок 3 показывает изменение потоков кислоты через мембрану. При достижении времени эксперимента 3,5–4 ч наблюдается снижение потоков. Это время соответствует началу отклонения от линейной зависимости функции концентрации от времени (рисунок 1). Данный эффект связан с заметным уменьшением движущей силы процесса (градиента концентраций), что наиболее сильно проявляется для первого варианта эксперимента (для соотношения объемов отдаю-щий/принимающий раствор равного 1:1).
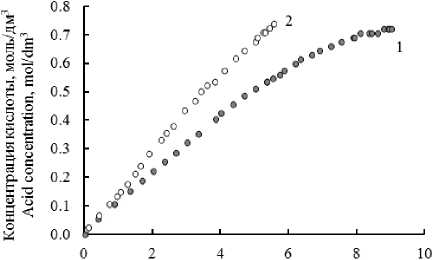
Время эксперимента, ч Experiment duration, h
Рисунок 2. Изменение концентрации соляной кислоты в камере пермеата для соотношения объемов отдающего и принимающего растворов 1:1 (кривая 1) и 2:1 (кривая 2) Figure 2. The change in the concentration of hydrochloric acid in the permeate chamber for different volume ratios of the giving and receiving solutions: 1:1 (curve 1) and 2:1 (curve 2)
Состав растворов до и после эксперимента приведен на рисунке 4. На основе их анализа найдены коэффициенты разделения кислота/соль и коэффициент задержания соли (таблица 1). Раствор кислоты, полученный при отношении объемов отдающего и принимающего растворов равного 1:1, содержит меньшее количество соли железа (III). Однако прирост концентрации кислоты в этом случае идет с меньшей скоростью (рисунок 1).
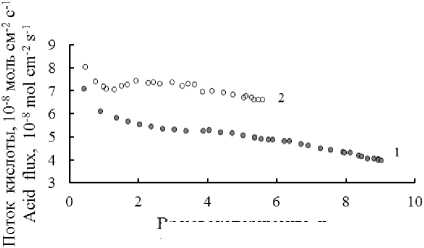
Время эксперимента, ч Experiment dura lion, h
Рисунок 3. Потоки кислоты через мембрану для соотношения объемов отдающего и принимающего растворов 1:1 (кривая 1) и 2:1 (кривая 2)
Figure 3. Acid fluxes through the membrane for different ratios of volumes of giving and receiving solutions: 1:1 (curve 1) and 2:1 (curve 2)
При соотношении объемов отдающего и принимающего растворов 2:1 можно получить раствор соляной кислоты заданной концентрации за время в 1,5 раз меньшее, чем при одинаковых объемах отдающего и принимающего растворов, но содержание соли железа (III) в этом растворе будет в 1,4 раза больше.
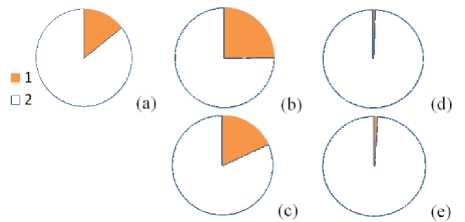
Рисунок 4. Мольное соотношение Fе3+ (1) и НСl (2) в исходном растворе (a), ретентате (b, c) и пермеате (d, e) при отношениях объемов отдающего и принимающего растворов 1:1 (b, d) и 2:1 (c, e) соответственно
Figure 4. Molar ratio of Fе3+ (1) and НСl (2) in the initial solution (a), retentate (b, c) and permeate (d, e) with volume ratios of giving and receiving solutions of 1:1 (b, d) and 2:1 (c, e), respectively
Сравнение полученных характеристик разделения кислоты и соли с характеристиками диализа, найденными для аналогичных систем [9, 16-19] показывает необходимость разработки усовершенствованных анионообменных мембран с более высокими коэффициентами разделения соляная кислота / хлорид железа (III). Это может быть достигнуто как путем изменения структурных свойств мембран, например, модифицированием объема или поверхности образцов, так и созданием более тонких ионообменных мембран, имеющих повышенную диффузионную проницаемость по кислоте. В свое время предприятие «Щекиноазот» выпускало опытную партию тонких гетерогенных ионообменных мембран, в том числе и МА-41 [20]. Привлекательным направлением применения этих мембран может быть именно вариант диализа, рассмотренный в настоящей статье.
Таблица 1.
Характеристики диализного разделения раствора, содержащего соляную кислоту (1,5 моль/дм3), хлорид железа (III) (0,25 моль/дм3) с анионообменной мембраной МА-41
Table 1.
Characteristics of dialysis separation of a solution containing hydrochloric acid (1.5 mol/dm3), iron (III) chloride (0.25 mol/dm3) with an anion exchange membrane MA-41
|
Показатели Раrаmеtеrs |
Отношение объемов отдающий раствор: принимающий раствор Volume ratio giving solution: receiving solution |
|
|
1:1 |
2:1 |
|
|
Отношение концентраций Fе3+/Н+ в пермеате (r Fе 3+ /Н +) Ratio of Fе3+/Н+ concentrations in permeate ( r f е 3 +/Н+) |
0,0061 |
0,0087 |
|
Коэффициент задержания соли, R, % Salt rejection coefficient, R, % |
98,2 |
97,4 |
|
Коэффициент разделения, S | Separation coefficient, S |
27,2 |
19,2 |
Заключение
Реализован диффузионный диализ модельного раствора, содержащего соляную кислоту (1,5 моль/дм3) и хлорид железа (III) (0,25 моль/дм3): режим рецикла, анионообменная мембрана МА-41. Проведена оценка характеристик диализа, позволяющих судить об эффективности процесса выделения кислоты из смешанного раствора (диффузионные потоки кислоты через мембрану, коэффициент задержания соли, коэффициент разделения кислота / соль, содержание соли в пермеате) и их зависимость от соотношения объемов отдающего и принимающего растворов (2:1 или 1:1 соответственно).
Применение отдающего раствора в объеме в два раза большим по сравнению с объемом принимающего раствора позволяет получить заданную концентрацию кислоты в приемной камере за меньшее время. Это связано с тем, что движущая сила процесса диализа (градиент концентраций) в данном случае падает гораздо медленнее. Однако содержание соли железа (III) в пермеате для такого варианта проведения процесса оказывается более высоким.
Дальнейшим развитием настоящего исследования может быть работа с более тонкими модифицированными образцами отечественных ионообменных мембран, которые позволят получить повышенные коэффициенты разделения минеральная кислота/соль.
Список литературы Выделение кислоты из отработанного травильного раствора методом диффузионного диализа с анионообменной мембраной
- Лаврентьев А.Ю., Какорин Д.Д., Дожделев А.М. Выбор способа очистки поверхности наплавленного металла в процессе аддитивного производства металлических изделий // Современные материалы, техника и технологии. 2023. № 3. С. 35-39.
- Михайловский И.А., Мумбаева А.А. Выбор способа удаления окалины с поверхности катанки при производстве углеродистой проволоки // Актуальные проблемы современной науки, техники и образования. 2017. Т. 2. С. 42-44.
- Астраумова В.Г., Пятанова П.А., Ложникова Т.В. Исследование скорости коррозии при химическом травлении стальных корпусов высокочастотных резонаторов // Техника радиосвязи 2023. № 1. С. 98-102.
- Филиппов А.А., Пачурин Г.В., Ребрушкин М.Н., Конюхова Н.С. Снижение комплексного воздействия опасных и вредных факторов в условиях производства стальной проволоки // XXI век. Техносферная безопасность. 2020. № 5(2) С. 222-232. https://doi.org/10.21285/2500-1582-2020-2-222-232
- Zhang C., Zhang W., Wang Y. Diffusion dialysis for acid recovery from acidic waste solutions: Anion exchange membranes and technology integration // Membranes. 2020. V. 10. №. 8. P. https://doi.org/doi:10.3390/membranes10080169
- Крачак А.Н., Груздева А.Н., Хамизов Р.Х., Долгоносов А.А. Переработка отработанного сульфатного травильного раствора методом удерживания кислоты на сильноосновном анионите // Сорбционные и хроматографические процессы. 2022. Т. 22. № 5. С. 684-693. https://doi.org/10.17308/sorpchrom.2022.22/10721
- Быковский Н.А., Кантор Е.А., Малкова М.А., Пучкова Л.Н., Фанакова Н.Н. Сточные воды производства изделий из титана - сырье для получения Ti(OH)4, NaOH и HCl // Экология и промышленность России. 2021. Т. 25. № 2. С. 8-11. https://doi.org/10.18412/1816-0395-2021-2-8-11
- Шипэй В., Лю T., Cяо С., Ло Ш. Достижения в области бактериальной ремедиации для очистки от тяжелых металлов: мини-обзор // Проблемы окружающей среды и природных ресурсов. 2022. № 11. С. 100-122.
- Jiuyang L., Junming H., Jing W., Junwei Y. et al. High-performance porous anion exchange membranes for efficient acid recovery from acidic wastewater by diffusion dialysis // Journal of Membrane Science. 2021. V. 624. P. 119116. https://doi.org/10.1016/j.memsci.2021.119116
- Ruiz-Aguirre A., Lopez J., Gueccia R., Randazzo S. et al. Diffusion dialysis for the treatment of H2 SO4-CuSO4 solutions from electroplating plants: Ions membrane transport characterization and modeling // Separation and Purification Technology. 2021. V. 266. P. 118215. https://doi.org/10.1016/j.seppur.2020.118215
- Loza S., Loza N., Kovalchuk N., Romanyuk N. et al. Comparative study of different ion-exchange membrane types in diffusion dialysis for the separation of sulfuric acid and nickel sulfate // Membranes. 2023. V. 13. №. 4. P. 396. https://doi.org/10.3390/membranes13040396
- Козадерова О.А., Калинина С.А., Моргачева Е.А., Нифталиев С.И. Cорбционные характеристики и диффузионная проницаемость анионообменной мембраны МА41 в растворах молочной кислоты // Сорбционные и хроматографические процессы. 2021. Т. 21. № 3. С. 317-325. https://doi.org/10.17308/sorpchrom.2021.21/3465
- Vasil'eva V., Goleva E., Pismenskaya N., Kozmai A. et al. Effect of surface profiling of a cation-exchange membrane on the phenylalanine and NaCl separation performances in diffusion dialysis // Separation and Purification Technology. 2019. V. 210. P. 48-59. https://doi.org/10.1016/j.seppur.2018.07.065
- ООО ИП «Щекиноазот». URL: http://azotom.ru/monopolyarnye-membrany
- Кононенко Н.А., Демина О.А., Лоза Н.А., Фалина И.В. и др. Мембранная электрохимия. Краснодар: Кубанский гос. ун-т, 2017. 290 с.
- Culcasi A., Gueccia R., Randazzo S., Cipollina A. et al. Design of a novel membrane-integrated waste acid recovery process from pickling solution // Journal of Cleaner Production. 2019. V. 236. P. 117623. https://doi.org/10.1016/j.jclepro.2019.117623
- Pal S., Mondal R., Guha S., Chatterjee U., Jewrajka S.K. Crosslinked terpolymer anion exchange membranes for selective ion separation and acid recovery // Journal of Membrane Science. 2020. V. 612. P. 118459. https://doi.org/10.1016/j.memsci.2020.118459
- Gueccia R., Randazzo S., Chillura Martino D., Cipollina A., Micale G. Experimental investigation and modeling of diffusion dialysis for HCl recovery from waste pickling solution // Journal of Environmental Management. 2019. V. 235. P. 202-212. https://doi.org/10.1016/j.jenvman.2019.01.028
- Irfan M., Bakangura E., Afsar N. Ul, Xu T. Augmenting acid recovery from different systems by novel Q-DAN anion exchange membranes via diffusion dialysis // Separation and Purification Technology. 2018. V. 201. P. 336-345. https://doi.org/10.1016/j.seppur.2018.02.042
- Гаршина Т.И., Козадёрова О.А., Шапошник В.А. физико-химические характеристики тонких ионообменных мембран // Сорбционные и хроматографические процессы. 2007. Т. 7. № 1. С. 148-151.


