Выживаемость несвязанных керамических эндопротезов лучезапястного сустава
Автор: Александров Т.И., Симонова Е.Н., Лукинов В.Л.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 5 т.29, 2023 года.
Бесплатный доступ
Введение. Выживаемость имплантатов является важным временным показателем улучшения качества жизни пациента. В зарубежной литературе разделу выживаемости имплантатов уделяется особое внимание.Цель. Оценка эффективности и выживаемости несвязанного керамического эндопротеза лучезапястного сустава.Материалы и методы. Анализу подвергнуто 83 отдаленных случая тотального эндопротезирования лучезапястного сустава несвязанным керамическим имплантатом. В Новосибирском НИИТО с 2011 по 2021 г. проведено тотальное эндопротезирование лучезапястного сустава 81 пациенту с тяжелыми изменениями кистевого сустава. У двоих пациентов оперативное вмешательство выполнялось на двух суставах. Проведено ретроспективное неконтролируемое когортное исследование, в ходе которого госпитализированные пациенты поделены на три группы, согласно этиологической причине возникновения заболевания. Использовались рентгенологические методы контроля состояния имплантата (рентгенография в двух проекциях и МСКТ кистевого сустава). Для бинарных показателей рассчитывалось количество, частоты и 95 % доверительный интервал частот по формуле Вильсона в группах. Сравнение проводилось точным двусторонним тестом Фишера. Корректировка ошибки p проводилась методом Бенджиамини - Хохберга. Для анализа выживаемости строились кривые Каплана - Мейера. Сравнение групп проводилось обобщенным критерием хи-квадрат.Результаты. Каждый случай повторного оперативного вмешательства оценивался с позиции выделенных групп. В зависимости от времени, прошедшего с момента операции до повторной хирургической помощи, были рассчитаны временные рамки общей и групповой выживаемости компонентов эндопротеза лучезапястного сустава. Представлены причины и объем оперативного вмешательства во время реоперации.Обсуждение. В доступной литературе отсутствуют данные о выживаемости несвязанных компонентов керамического эндопротеза лучезапястного сустава и о важных этапах послеоперационного периода у ортопедических больных. Представлены графические изображения с предложением деления ортопедического послеоперационного периода.Заключение. Промежуточные выводы тотального эндопротезирования несвязанным керамическим эндопротезом лучезапястного сустава вселяют оптимизм в получении стойкого положительного эффекта мобильности кистевого сустава, утраченной в результате дегенеративного процесса. Одиннадцатилетний срок наблюдения демонстрирует, что выживаемость несвязанного керамического эндопротеза лучезапястного сустава составляет 88 %.
Эндопротез, эндопротезирование, лучезапястный сустав, выживаемость имплантата, послеоперационный период
Короткий адрес: https://sciup.org/142239024
IDR: 142239024 | УДК: [616.727.43-089.227.844]-089.168.1 | DOI: 10.18019/1028-4427-2023-29-5-461-467
Survival of unconstrained ceramic wrist joint implants
Introduction Survival of implants is an important indicator of improvement in the patient's quality of life. In foreign literature, the issue of implant survival finds special attention.The aim of the work was to evaluate the efficacy and survival of an unconstrained ceramic wrist joint endoprosthesis.Materials and methods We analysed 83 cases of total wrist arthroplasty with an unconstrained ceramic implant at long-term follow-up. At the Novosibirsk RSITO, total wrist arthroplasty was performed in 81 patients with severe changes in the wrist joint from 2011 to 2021. Two patients underwent arthroplasty on two joints. A retrospective uncontrolled cohort study was conducted which divided the hospitalized patients into three groups according to the etiological cause of the disease. Radiological methods were used to control the state of the implant (radiography in two projections and CT-scans of the wrist joint). For binary indicators, the number, rates and 95 % confidence interval of frequencies were calculated according to the Wilson formula in the groups. Comparison was carried out by Fisher's exact two-sided test. The p-error was corrected using the Benjamini - Hochberg method. Kaplan - Meier curves were constructed for survival analysis. The groups were compared using a generalized chi-square test.Results Each case of repeated surgical intervention was evaluated from the standpoint of selected groups. Depending on the time elapsed from surgery to revision, we calculated the time frame for overall and group survival of the components of the wrist joint endoprosthesis. The causes and scope of surgical revision are presented.Discussion There are no data on the survival of unconstrained ceramic wrist joint implants in the foreign literature. Graphic images according to a proposal for the division of the orthopaedic postoperative period are presented. Conclusions 1. Intermediate conclusions in regard to total arthroplasty with an unconstrained ceramic endoprosthesis of the wrist joint inspire optimism in obtaining a stable positive effect of motion range lost due to the degenerative process in the wrist joint. 2. An 11-year follow-up period demonstrates that the survival rate of an unconstrained ceramic wrist endoprosthesis is 88 %.
Текст научной статьи Выживаемость несвязанных керамических эндопротезов лучезапястного сустава
Статистика раннего и позднего послеоперационного периода тотально замещённого несвязанным керамическим эндопротезом лучезапястного сустава представлена в предыдущей статье [1]. Выживаемость имплантатов является важным временным показателем улучшения качества жизни пациента [2].
В русскоязычной литературе статей, посвящённых результатам эндопротезирования лучезапястного сустава, ограниченное количество [3, 4]. И, как следствие, имеются пробелы в освещении проблемы, отсутствуют данные о выживаемости имплантатов. В иностранных журналах и научных книгах разделу
выживаемости имплантатов уделяется особое внима- Цель – оценка эффективности и выживаемости ние, однако отсутствуют данные использования кера- несвязанного керамического эндопротеза лучезапяст-мических имплантатов [6-15]. ного сустава.
МАТЕРИАЛЫ И МЕТОДЫ
В Новосибирском Научно-исследовательском институте травматологии и ортопедии имени Я.Л. Цивьяна выполнено на момент написания статьи более 120 оперативных вмешательств по замене лучезапястного сустава. Анализу подвергнуто 83 отдаленных случая хирургической помощи. Дата протокола заседания локального этического комитета ФГБУ ННИИТО им. Я.Л. Цивьяна от 17.01.2023 года, номер выписки 002/23, номер протокола заседания 001/23. Нами фиксированы все случаи повторных хирургических вмешательств, их причины и объем помощи. Мы оценивали время повторной госпитализации и результат ревизионной операции. Кривая Каплана – Мейера позволила нам оценить выживаемость компонентов эндопротеза (ЭП) лучезапястного сустава. В травматолого-ортопедическом отделении № 3 Новосибирского НИИТО с 2011 по 2021 год проведено тотальное эндопротезирование лучезапястного сустава 81 пациенту с тяжелыми дегенеративно-дистрофическими изменениями кистевого сустава, оформившему добровольное согласие на оперативное лечение и согласившемуся на предложенный план лечения. У двоих пациентов оперативное вмешательство выполнялось на двух суставах.
Проведено ретроспективное неконтролируемое когортное исследование, в ходе которого госпитализированные пациенты поделены на три группы, согласно этиологической причине возникновения заболевания.
В группу RA вошли пациенты с ревматическими заболеваниями кистевого сустава. В группу Travma вошли пациенты с последствиями травм и оперативных вмешательств. В малочисленную группу AVN вошли случаи дисплазии и остеохондропатии кистевого сустава.
Все пациенты проходили рентгенографическое исследование до операции, в конце оперативного вмеша- тельства и во время контрольных приемов. При возникновении жалоб на боли пациентам назначалась МСКТ оперированного сустава для оценки стабильности компонентов эндопротеза. После выявления причины повторного обращения нами определялся объем повторной хирургической операции.
Оценка выживаемости эндопротеза складывалась из двух точек: первая точка соответствовала первичному эндопротезированию лучезапястного сустава, второй точкой являлась дата повторного оперативного вмешательства. Все повторные хирургические оперативные вмешательства вносились в таблицу с указанием времени, прошедшего с момента первой операции. Результаты подвергались статистическому анализу. Пациенты, которые не обращались за повторной хирургической помощью, оценивались как продолжающееся наблюдение.
Статистические методы
Для бинарных показателей пола, вовлечения эндопротеза, артродеза, операций без протеза, положительной динамики рассчитывалось количество, частоты и 95 % доверительный интервал (95 % ДИ) частот по формуле Вильсона в группах. Для количественной оценки различий между группами вычислялось отношение шансов (ОШ) с 95 % ДИ. Сравнение проводилось точным двусторонним тестом Фишера. Корректировка ошибки множественных сравнений в достигнутых уровнях значимости p проводилась методом Бенджиамини – Хохберга (табл. 1). Для анализа свободы от реопераций строились кривые Каплана – Мейера. Составлялись таблицы выживаемости эндопротеза с оценками свобод и 95 % ДИ. Сравнение групп проводилось обобщенным критерием хи-квадрат.
РЕЗУЛЬТАТЫ
Причинами повторного обращения служили перипро-тезный перелом, дислокация компонента, вывих эндопротеза, артрофиброз тотально замещенного лучезапястного сустава, порочное положение кисти (сохранение и фиксация кисти в порочном положении соответственно исходному состоянию), асептическая нестабильность компонента. По объему ортопедической помощи мы разделили обращения на три подгруппы: переустановка ЭП, артродез и мягкотканные вмешательства.
Рентгенологические методы исследования позволяли нам оценивать клинические проявления, описываемые пациентами на контрольных осмотрах. Оценивалось положение компонентов эндопротеза, околоимплантный остеолиз, дефекты конструкции. В случае обнаружения проявлений нестабильности компонентов эндопротеза или нарушения целостности околоимплантой костной ткани (перипротезный перелом) объем оперативного вмешательства предполагал переустановку компонента эндопротеза (переустановка ЭП). В случае невозможности переустановить компонент эндопротеза нами выполнялось оперативное вмешательство – тотальный артродез кистевого суста- ва (артродез). Нами ни разу не было обнаружено механического разрушения компонентов эндопротеза. В тех случаях, где нестабильность компонентов эндопротеза выявлена не была, выполнялась хирургическая помощь с освобождением суставной поверхности эндопротеза от рубцовых тканей и перемещением сухожилий для достижения баланса положения кисти. Сравнительные показатели результатов повторного вмешательства, причины обращения и объем хирургической помощи с определением доли гендерного и возрастного деления представлены в таблице 1. Также в таблице 1 представлены количественные показатели каждой исследуемой группы, вошедшие в графические изображения представленной статьи.
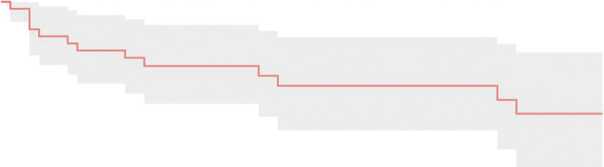
Для оценки времени активной функции ЭП каждая операция была обозначена на временной кривой, где исходная точка – это время операции (рис. 1). В зависимости от срока, прошедшего с момента первой операции до проведения повторной операции, были рассчитаны временные рамки. Исходя из того, что исходное состояние пациентов было различным, как и причина возникновения дегенеративного изменения кистевого сустава, результаты объединялись в определенную группу пациентов. Объединение результатов позволило определить групповую выживаемость эндопротеза (рис. 2, 3, 4).
Важным элементом удовлетворительного результата восстановления и сохранения мобильности кистевого сустава является взаимодействие на всех этапах ортопедического лечения со специалистами смежных направлений. Среди основных узких специалистов необходимо выделить реабилитологов, ревматологов и неврологов.
Помощь реабилитологов остро необходима на первом этапе послеоперационного периода. Значительное количество исследователей указывает на незаменимость участия реабилитологов в послеоперационном периоде. Подконтрольная разработка оперированного сустава позволяет исправить порочный стереотип движения, сформированный у пациентов за долгие годы болезни [16-20]. Привлечение ревматологов необходимо для подбора базовой терапии, принимая во внимание единый патологический механизм морфологических изменений сустава [6, 17, 21]. Привлечение неврологов позволяет корректировать афферентно-эфферентную связь верхней конечности, что позитивно сказывается на конечном результате.
Таблица 1
|
Показатели |
RA (n = 26) |
Travma (n = 48) |
AVN (n = 9) |
Сравнение |
|
|
n, % [95 % ДИ] |
n, % [95 % ДИ] |
n, % [95 % ДИ] |
ОШ [95 % ДИ] |
Двусторонний тест Фишера, p-уровень, коррекция |
|
|
Пол, мужской |
1, 4 % [1 %; 19 %] |
28, 58 % [44 %; 71 %] |
5, 56 % [27 %; 81 %] |
RA vs. Tavma: 33,5 [4,7; 1475] RA vs. AVN: 0 [0; 0,4] Travma vs. AVN: 1,1 [0,2; 5,9] |
RA vs. Tavma: < 0,001*, < 0,001* RA vs. AVN: 0,002*, 0,004* Travma vs. AVN: > 0,999, > 0,999 |
|
Переустановка ЭП |
1, 4 % [1 %; 19 %] |
6, 12 % [6 %; 25 %] |
1, 11 % [2 %; 43 %] |
RA vs. Tavma: 3,5 [0,4; 170,6] RA vs. AVN: 0,3 [0; 28,2] Travma vs. AVN: 1,1 [0,1; 59] |
RA vs. Tr.: 0,410, > 0,999 RA vs. AVN: 0,454, > 0,999 Travma vs. AVN: >0,999, > 0,999 |
|
Артродез |
0, 0 % [0 %; 13 %] |
3, 6 % [2 %; 17 %] |
0, 0 % [0 %; 30 %] |
– |
RA vs. Tr: 0,548, > 0,999 RA vs. AVN: > 0,999, > 0,999 Travma vs. AVN: > 0,999, > 0,999 |
|
Мягкотканные вмешательства |
2, 8 % [2 %; 24 %] |
9, 19 % [10 %; 32 %] |
2, 22 % [6 %; 55 %] |
RA vs. Tavma: 2.7 [0,5; 28,1] RA vs. AVN: 0,3 [0; 4,9] Travma vs. AVN: 0,8 [0,1; 9,3] |
RA vs. Tr.: 0,309, 0,803 RA vs. AVN: 0,268, 0,803 RA vs. Tr.: > 0,999, > 0,999 |
|
Положительная динамика |
26, 100 % [87 %; 100 %] |
45, 94 % [83 %; 98 %] |
9, 100 % [70 %; 100 %] |
– |
RA vs. Tavma: 0,548, > 0,999 RA vs. AVN: > 0,999, > 0,999 Travma vs. AVN: > 0,999, > 0,999 |
Сравнение показателей между группами RA, Travma, AVN
100.0%
— Все пациенты (на 60 мео.: 80%, 95% ДИ от 70% до 91 %)
g. 90.0%
° 80.0%
° 70.0%
0 12 24 36 48 60
Время (месяцы)
Число пациентов под риском (всего событий)
Рис. 1. Кривая Каплана – Мейера свободы от повторных операций у всех пациентов
— | 83(0)70(7)53(9)41 (11)35(11)27 (13)
0 12 24 36 48 60
Время (месяцы)
Рис. 2. Кривая Каплана – Мейера свободы от риска повторных операций у пациентов в группах
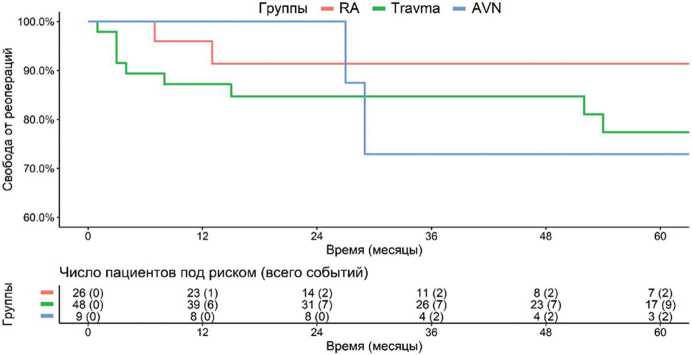
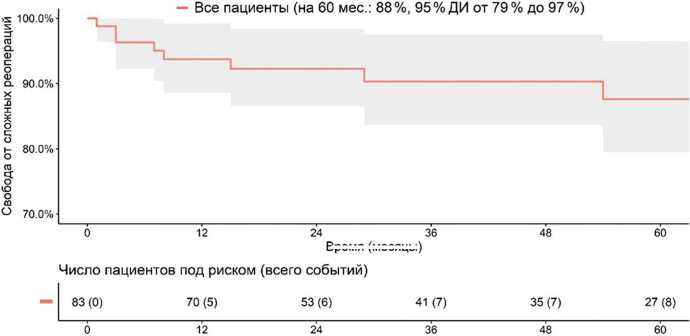
Время (месяцы)
Рис. 3. Кривая Каплана – Мейера свободы от риска повторных операция с переустановкой ЭП у всех пациентов
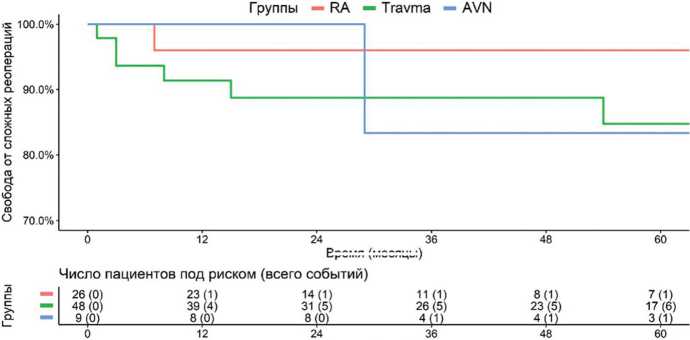
Время (месяцы)
Рис. 4. Кривая Каплана – Мейера свободы от риска повторных операция с переустановкой ЭП у пациентов в группах
Время (месяцы)
Время(месяцы)
Причиной повторного хирургического вмешательства в группе RA явился срыв компенсации основного заболевания. Клиническими проявлениями являлись реактивные тендовагиниты сухожилий сгибателей пальцев кисти. Длительно существующие реактивные тендовагиниты агрессивно влияют на общее самочувствие пациента и на стабильность компонентов ЭП. Подобное патологическое состояние требует тесного взаимодействия «ревматолог-пациент-травматолог». В начальной стадии клинических проявлений возможна консервативная коррекция патологического состояния. Первичное тотальное эндопротезирование лучезапястного сустава выполняется с тыльной стороны, и во время доступа осуществляется синовэктомия сухожилий разгибателей запястья и пальцев кисти. Именно по этой причине, при неэффективности консервативного лечения в течение месяца, необходим доступ к сухожилиям сгибателей. Необходима субтотальная синовэктомия сухожилий сгибателей запястья и пальцев кисти. При этом следует отметить, что изолированного вскрытия карпального канала с освобождением срединного нерва недостаточно. Рентгенологические признаки нестабильности компонентов эндопротеза являются основанием к переустановке компонентов с использованием костного цемента.
После тотального эндопротезирования лучезапястного сустава очень ценным является возвращение человека к социальной жизни с улучшенным качеством жизни. Были отмечены случаи, когда пациенты полностью переставали обращать внимание на опери- рованный сустав. Наряду с положительными характеристиками после эндопротезирования лучезапястного сустава наблюдались случаи с чрезмерной физической активностью оперированной руки. В ряде таких случаев выполнение тяжелого физического труда ограничивает функциональные возможности оперированного сустава при отсутствии рентгенологических признаков нестабильности компонентов эндопротеза. С этой точки зрения следует обращать внимание пациентов на то, что замещенный эндопротезом сустав является искусственным и следует ограничивать силовую нагрузку на оперированный сустав.
В группе пациентов с посттравматическими изменениями сустава встречались перипротезные переломы, вывихи и дислокации компонентов ЭП. Причиной обращения являлись эпизоды падения на оперированную руку. Несмотря на малые размеры головчатой кости, в ряде случаев требовалась переустановка дистального компонента методом Pressfit с последующей хорошей остеоинтеграцией ЭП. К сожалению, именно в этой группе были выявлены три случая, закончившиеся тотальным артродезом кистевого сустава (рис. 5).
Несмотря на малочисленность группы AVN, необходимо отметить, что наибольшие сложности возникли с пациентами, у которых была диагностирована дисплазия кистевого сустава. Длительно существующий стереотип движений во многом сводил к минимуму старания реабилитологов и травматологов. В этой группе отмечалась нестабильность проксимального компонента ЭП.
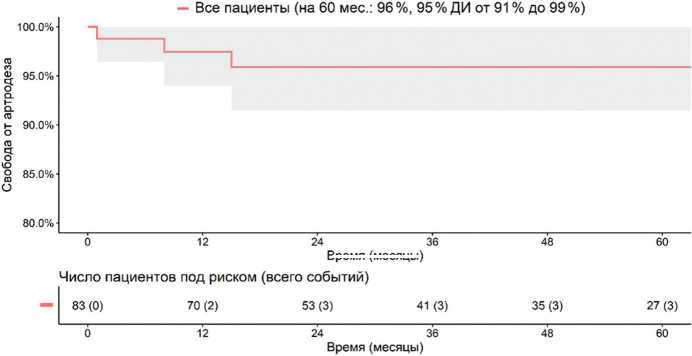
Время(месяцы
Рис. 5. Кривая Каплана – Мейера свободы от артродеза у всех пациентов
Во время ревизионной операции выполнялась переустановка индивидуальных компонентов с использованием костного цемента. Наряду с вмешательством на ЭП осуществлялась транспозиция сухожилий с коррекцией положения кисти. Транспозиции подвергаются сухожилия сгибателей и разгибателей запястья в зависимости от исходного состояния ки- сти. Этих мер было достаточно для стабилизации и длительного положительного эффекта от оперативного вмешательства.
Полученные данные позволяют отметить, что выживаемость тотального эндопротезирования несвязанного керамического эндопротеза лучезапястного сустава составила 88 %.
ОБСУЖДЕНИЕ
В классической литературе представление о послеоперационном периоде наблюдения разнообразны. Во многих источниках указываются одни и те же названия, однако подразумеваются разнообразные временные рамки. В научных публикациях указываются временные рамки без объяснения их значения. Указывается пяти- и десятилетняя оценка выживаемости эндопротезов [33-45]. Единственное определение послеоперационного периода нами обнаружено в большой медицинской энциклопедии.
Послеоперационный период сводится к двум последовательным этапам [5]. Ближайший послеоперационный период начинается с момента окончания операции и продолжается до выписки больного из лечебного учреждения. Отдаленный послеоперационный период протекает вне стационара и используется для окончательной ликвидации общих и местных расстройств, вызванных операционной травмой.
В российской литературе отсутствуют данные о выживаемости каких-либо эндопротезов лучезапястного сустава. В мировых публикациях существует информация об осложнениях тотального эндопротезирования лучезапястного сустава, достигающих 35 %. Menon сообщал о 33 % неудачных исходов эндопротезирования лучезапястного сустава протезами «Volz» через 40 месяцев после установки [6]. Частота неудачных исходов в исследовании Cooney et al. по использованию протезов «Meuli» составила 23 % после 5 лет наблюдения [6]. В исследовании Rademer et al. в 2003 г. по использованию эндопротеза «APH» было выявлено 80 % неудовлетворительных результатов через 52 месяца после установки [46].
Процент отрицательных результатов, описанных выше, прежде всего, связан с поиском оптимальной формы и материала для имплантата. Отказ от скомпрометированной формы эндопротеза привлекал конструкционные идеи для поиска новой модели. Отрицатель- ные эффекты трибологической пары трения вынуждал искать современные материалы для нового поколения эндопротезов. Спрос на улучшение качества жизни и сохранение мобильности утраченного сустава со стороны пациентов обязывает исследователей искать оптимальную форму и материал.
Показатель положительных результатов керамических эндопротезов в нашем исследовании составил 88 %. Аналогичных гомогенных по выбранному методу хирургического лечения статей, посвященных изучению выживаемости керамических эндопротезов лучезапястного сустава, нами в литературе найдено не было. Нами предпринята попытка интерпретации своих результатов в различные временные периоды.
В случае эндопротезирования установка в организм человека инородного тела планируется на продолжительный период времени. Рисками эндопротезирования сустава могут служить вывихи, нагноение, сохранение боли и ограничения функции, расшатывание компонентов эндопротеза [22-32]. Эти проявления могут отмечаться в разное время и по разным причинам. Эндопротезирование не влечет за собой выздоровления, а лишь длительное улучшение качества жизни.
На основании этого тезиса послеоперационный период является важным этапом наблюдения и анализа. Полученные нами результаты фактически и статистически представлены в таблице 1. Их значения использовались в графиках, что позволяет нам определить закономерности, которые мы предлагаем к обсуждению.
Анализируя литературные данные и результаты проведенного исследования, ортопедический послеоперационный период мы поделили на ближайший (период наблюдения в стационаре), ранний (до 2 лет), среднесрочный (от 2 до 8 лет) и отдаленный (более 8 лет).
Ближайший послеоперационный период наблюдения составляет 6-8 дней. Позволяет регулярно оцени- вать послеоперационный шов, положение кисти, рентгенологические признаки положения компонентов ЭП.
Ранний послеоперационный период необходимо выделить по причине выявления нарушений, которые возможно исправить. В этот временной отрезок формируется рубцовая ткань, изменяется стереотип движения в оперированном суставе.
В послеоперационном периоде наблюдения от 2 до 8 лет (среднесрочный) могут наблюдаться вторичные изменения со стороны компонентов эндопротеза. Наиболее частыми признаками является перепротезный остеолиз (асептическая нестабильность). В этот период времени уже завершена социальная адаптация пациентов, что позволяет пользоваться оперированной рукой без акцентирования внимания на искусственном суставе.
Отдаленный послеоперационный период служит одной цели – определение выживаемости ЭП.
Выделение этапов послеоперационного периода нам представляется оптимальным и обоснованным, объединяющим представление о функции имплантата. Подобное деление позволило нам оценить результаты применения хирургического метода.
ЗАКЛЮЧЕНИЕ
Представленные результаты проведенного исследования демонстрируют положительную динамику комплексной реабилитации пациентов после тотального эндопротезирования лучезапястного сустава.
Анализ данных, полученных в отдаленном периоде, позволяет заключить, что тотальное эндопротезирование несвязанным керамическим эндопротезом лучезапястного сустава приводит к стойкому положительному эффекту.
Одиннадцатилетний срок наблюдения демонстрирует, что выживаемость несвязанного керамического эндопротеза лучезапястного сустава составляет 88 %.
С учетом недостаточности представленных в литературе данных, посвященных этому аспекту, существует необходимость в проведении дальнейших исследований результатов тотального эндопротезирования лучезапястного сустава.
Список литературы Выживаемость несвязанных керамических эндопротезов лучезапястного сустава
- Александров Т.И., Прохоренко В.М. Симонова Е.Н. Результаты тотального эндопротезирования лучезапястного сустава керамическими имплантатами в среднесрочном и отдаленном периоде. Вопросы реконструктивной и пластической хирургии. 2022;25(4):66-76. doi: 10.52581/1814-1471/83/07
- Знаменский Н.Н. Имплантация искусственных зубов. Медицинское обозрение. 1891;35(3):261-275.
- Карпенко В.Ю., Бухаров А.В., Курильчик А.А. и др. Эндопротезирование при опухолевом поражении дистальных отделов конечностей. Онкология. Журнал им. П.А. Герцена. 2017;6(5): 31-36. doi: 10.17116/onkolog20176531-36
- Шайхлисламова А.Р., Анисеня И.И. Способ проектирования индивидуальных компонентов эндопротеза лучезапястного сустава для производства при помощи аддитивных технологий. Медицинская техника. 2022;1(331):25-27.
- Большая медицинская энциклопедия: [в 30 т.]. Т. 29. Дополнительный. Гл. ред. Б.В. Петровский. М.: Сов. энцикл.; 1988:544.
- Tome-Bermejoa, Lara-Escobarb F., Sanchez-Infantea J.L., et al. Total wrist arthroplasty in patients with rheumatoid arthritis. Evaluation of preliminary results. Rev esp cir ortop traumatol. 2008;52(4):199-205. doi: 10.1016/S1988-8856(08)70096-8
- Reigstad O. Wrist arthroplasty: bone fixation, clinical development and mid to long term results. Acta Orthop Suppl. 2014 Apr;85(354):1-53. doi: 10.3109/17453674.2014.900597
- Boeckstyns ME, Herzberg G, Merser S. Favorable results after total wrist arthroplasty: 65 wrists in 60 patients followed for 5-9 years. Acta Orthop. 2013;84(4):415-9. doi: 10.3109/17453674.2013.823588
- Reigstad O, Holm-Glad T, Korslund J, et al. 15-20 Year Follow-up After Wrist Arthroplasty Surgery - Revisiting the Development and Introduction of a New Prototype Concept for Total Wrist Arthroplasty. J Hand Surg Asian Pac Vol. 2022;27(6):945-951. doi: 10.1142/S242483552250093X
- Quigley RJ, Ambrose C, Adams BD. The Effect of Locking Screws on Distal Component Fixation in Total Wrist Arthroplasty Using a Cadaver Model. J Hand Surg Glob Online. 2022;4(6):348-354. doi: 10.1016/j.jhsg.2022.08.002
- Zijlker HJA, Ritt MJPF, Beumer A. Erratum to "Fourth-generation total wrist arthroplasty: a systematic review of clinical outcomes". J Wrist Surg. 2022;11(5):e1. doi: 10.1055/s-0042-1755184
- Zijlker HJA, Ritt MJPF, Beumer A. Fourth-generation total wrist arthroplasty: a systematic review of clinical outcomes. J Wrist Surg. 2021;11(5):456-464. doi: 10.1055/s-0041-1735840
- Holzbauer M, Mihalic JA, Pollak M, Froschauer SM. Total wrist arthroplasty for posttraumatic wrist osteoarthritis: a cohort study comparing three indications. Life (Basel). 2022;12(5):617. doi: 10.3390/life12050617
- Eschweiler J, Li J, Quack V, et al. Total wrist arthroplast - a systematic review of the outcome, and an Introduction of FreeMove - an approach to improve TWA. Life ^Basel). 2022;12(3):411. doi: 10.3390/life12030411
- Herren DB, Ishikawa H, Rizzo M, Ross M, Solomons M. Arthroplasty in the hand: what works and what doesn't? J Hand Surg Eur Vol. 2022;47(1):4-11. doi: 10.1177/17531934211017703
- Faudot B, Ballerini J, Ross M, et al. Mechanical performance comparison of two surgical constructs for wrist four-corner arthrodesis via dorsal and radial approaches. Clin Biomech (Bristol, Avon). 2021;82:105274. doi: 10.1016/j.clinbiomech.2021.105274
- Bajuri MN, Abdul Kadir MR, Murali MR, Kamarul T. Biomechanical analysis of the wrist arthroplasty in rheumatoid arthritis: a finite element analysis. Med Biol Eng Comput. 2013;51(1-2):175-86. doi: 10.1007/s11517-012-0982-9
- Zhang M, Li A, Liu H, Wang M. Coarse-to-Fine Hand-Object Pose Estimation with Interaction-Aware Graph Convolutional Network. Sensors (Basel). 2021;21(23):8092. doi: 10.3390/s21238092
- Ota M, Matsui Y, Kawamura D, et al. Correlation between carpal rotational alignment and postoperative wrist range of motion following total wrist arthroplasty. BMC Musculoskelet Disord. 2022;23(1):821. doi: 10.1186/s12891-022-05776-x
- Larsson S, Carlsson IK, Rosberg HE, et al. Patients' experiences before and after total wrist fusion or total wrist arthroplasty: A qualitative study of patients with wrist osteoarthritis. J Hand Ther. 2022;35(1):41-50. doi: 10.1016/j.jht.2020.10.004
- Lestienne V, Chaves C, Tanwin Y, et al. Results of interposition arthroplasty with the Amandys® pyrocarbon implant in rheumatoid wrist at a mean 5 years' follow-up. Hand Surg Rehabil. 2021;40(5):579-587. doi: 10.1016/j.hansur.2021.05.009
- Clavien PA, Barkun J, de Oliveira ML, et al. The Clavien-Dindo classification of surgical complications: five-year experience. Ann Surg. 2009;250(2):187-96. doi: 10.1097/SLA.0b013e3181b13ca2
- Wagner ER, Srnec JJ, Fort MW, et al. Outcomes of Revision Total Wrist Arthroplasty. J Am Acad Orthop Surg Glob Res Rev. 2021;5(3):e21.00035. doi: 10.5435/JAAOSGlobal-D-21-00035
- Cobb TK, Beckenbaugh RD. Biaxial long-stemmed multipronged distal components for revision/bone deficit total-wrist arthroplasty. J Hand Surg Am. 1996;21(5):764-70. doi: 10.1016/S0363-5023(96)80189-4
- Karjalainen T, Pamilo K, Reito A. Implant Failure After Motec Wrist Joint Prosthesis Due to Failure of Ball and Socket-Type Articulation-Two Patients With Adverse Reaction to Metal Debris and Polyether Ether Ketone. J Hand Surg Am. 2018;43(11):1044.e1-1044.e4. doi: 10.1016/j. jhsa.2018.03.010
- Holm-Glad T, R0kkum M, Rohrl SM, et al. A randomized controlled trial comparing two modern total wrist arthroplasties : improved function with stable implants, but high complication rates in non-rheumatoid wrists at two years. Bone Joint J. 2022;104-B(10):1132-1141. doi: 10.1302/0301-620X.104B10.BJJ-2022-0201.R2
- Martínez Villén G, Rodríguez Nogué L, García González E. Postoperative assessment and management of metallosis and periprosthetic osteolysis in patients treated with metal-on-polyethylene total wrist prostheses. J Hand Surg Eur Vol. 2022;47(9):952-958. doi: 10.1177/17531934221113723
- Curlewis K, Leung B, Sinclair L, et al. Systemic medical complications following joint replacement: a review of the evidence. Ann R Coll Surg Engl. 2023;105(3):191-195. doi: 10.1308/rcsann.2022.0012
- Zijlker HJA, Fakkert RK, Beumer A, et al. Comparative outcomes of total wrist arthrodesis for salvage of failed total wrist arthroplasty and primary wrist arthrodesis. J Hand Surg Eur Vol. 2022;47(3):302-307. doi: 10.1177/17531934211057389
- Rothe CJ, Sivakumar BS, Buchan CA, Graham DJ. Metal-on-Metal Disease in High-Motion Wrist Arthroplasty. Hand (N Y). 2022;17(2):NP11-NP16. doi: 10.1177/15589447211003178
- Pong TM, van Leeuwen WF, Oflazoglu K, et al. Unplanned Reoperation and Implant Revision After Total Wrist Arthroplasty. Hand (N Y). 2022;17(1):114-118. doi: 10.1177/1558944719898817
- Nunez FA Jr, Wright L, Kilpatrick SE, Seitz WH Jr. Revision Total Wrist Arthroplasty Due to Polyethylene Wear, Metallosis-Induced Carpal Tunnel Syndrome, Distal Ulnar Impingement, and Fourth Carpometacarpal Joint Pain: Case Report and Pitfalls to Avoid. Hand (N Y). 2020;15(1):NP1-NP6. doi: 10.1177/1558944718810863
- Cooney W, Manuel J, Froelich J, Rizzo M. Total wrist replacement: a retrospective comparative study. J Wrist Surg. 2012;1(2):165-72. doi: 10.1055/s-0032-1326728
- Martínez Villén G, Rodríguez Nogué L. Universal 2™ total wrist arthroplasty: A single-surgeon 6.5-year follow-up study of 22 prostheses. Hand Surg Rehabil. 2021;40(4):413-419. doi: 10.1016/j.hansur.2021.02.005
- Llopis E, Cerezal L, Auban R, et al. Postoperative Imaging of the Wrist and Hand. Magn Reson Imaging Clin N Am. 2022;30(4):645-671. doi: 10.1016/j.mric.2022.03.004
- Weiss AP, Akelman E. Total wrist replacement. Med Health R I. 2012;95(4):117-9.
- Nair R. Review article: Total wrist arthroplasty. J Orthop Surg (Hong Kong). 2014;22(3):399-405. doi: 10.1177/230949901402200326
- Adams BD. Total wrist arthroplasty. Tech Hand Up Extrem Surg. 2004;8(3):130-7. doi: 10.1097/01.bth.0000131199.39073.2a
- Boeckstyns ME. Wrist arthroplasty - a systematic review. Dan Med J. 2014;61(5):A4834.
- Morapudi SP, Marlow WJ, Withers D, et al. Total wrist arthroplasty using the Universal 2 prosthesis. J Orthop Surg (Hong Kong). 2012;20(3):365-8. doi: 10.1177/230949901202000321
- Levadoux M, Legré R. Total wrist arthroplasty with Destot prostheses in patients with posttraumatic arthritis. J Hand Surg Am. 2003;28(3):405-13. doi: 10.1053/jhsu.2003.50086
- Clough OT, Lee G, Hayter E, et al. Surgery with the Motec total wrist replacement: learning from earlier designs. J Surg Case Rep. 2021;2021(1):rjaa560. doi: 10.1093/jscr/rjaa560
- Rossello MI, Zotta I, Rossello C, et al. Total Wrist Arthroplasty with Integra Freedom® Implants: A Pilot Study with a New Evaluation System. Indian J Orthop. 2022;56(6):1040-1047. doi: 10.1007/s43465-022-00618-3
- Gvozdenovic R, Vadstrup LS. A high incidence of early failure after Amandys® wrist interposition arthroplasty among 13 cases. J Hand Surg Eur Vol. 2022;47(2):215-216. doi: 10.1177/17531934211025231
- Marie C, Aribert M, Bouyer M, et al. Clinical, functional, and radiological results of the Amandys® interposition arthroplasty in 13 cases of wrist osteoarthritis. Hand Surg Rehabil. 2021;40(4):420-426. doi: 10.1016/j.hansur.2021.03.001
- Radmer S, Andresen R, Sparmann M. Total wrist arthroplasty in patients with rheumatoid arthritis. J Hand Surg Am. 2003;28(5):789-94. doi: 10.1016/s0363-5023(03)00307-1


