Взаимодействие пентафенилсурьмы и пента(пара-толил)сурьмы с бифенил-2,2’-дикарбоновой кислотой. Реакция пентафенилсурьмы с бифенил-4,4’-дикарбоновой кислотой. Строение продуктов реакций
Автор: Пупкова Ю.О., Шарутина О.К., Шарутин В.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 3 т.17, 2025 года.
Бесплатный доступ
Взаимодействием пентафенилсурьмы и пента(пара-толил)сурьмы с бифенил-2,2'-дикарбоновой кислотой (мольн. соотношение 2:1) в толуоле и бензоле синтезированы биядерные производные Ph4SbOC(O)C6H4C6H4OC(O)SbPh4 (1) и Tol4SbOC(O)C6H4C6H4OC(O)SbTol4 ∙ 2PhH (2) с выходами 70 и 73 % соответственно. Реакция пентафенилсурьмы с бифенил-4,4-дикарбоновой кислотой в бензоле приводит к образованию Ph4SbOC(O)C6H4C6H4SbPh4 ∙ 3PhH (3). Кристаллографические характеристики комплекса: (1) [C62H48O4Sb2, M = 1100,50; моноклинная сингония, пр. гр. Pn; параметры ячейки: a = 9,889(5) Å, b = 25,446(14) Å, c = 10,321(5) Å; β = 105,85(2), V = 2498(2) Å3, Z = 2; выч = 1,463 г/см3; = 1,130 мм–1; F(000) = 1108,0; обл. сбора по 2: 5,98–53,82; всего отражений 25282; независимых отражений 9696 (Rint = 0,0706); GOOF = 1,190; R-фактор 0,0522]; (2) [C82H76O4Sb2, M = 5475,71; моноклинная сингония, пр. гр. С2/с; параметры ячейки: a = 12,009(7) Å, b = 30,69(2) Å, c = 19,374(11) Å; β = 93,57(2), V = 7126(8) Å3, Z = 1; выч = 1,276 г/см3; = 0,806 мм–1; F(000) = 2808,0; обл. сбора по 2: 5,72–54,34; всего отражений 69807; независимых отражений 7887 (Rint = 0,0708); GOOF = 1,048; R-фактор 0,0422; (3) C80H66O4Sb2, M = 1334,85; триклинная сингония, пр. гр. R-1; параметры ячейки: a = 10,676(8) Å, b = 13,404(8) Å, c = 13,917(9) Å; = 116,53(2), β = 104,21(3), = 97,60(2), V = 1658,7(19) Å3, Z = 2; выч = 1,336 г/см3; = 0,864 мм–1; F(000) = 680,0; обл. сбора по 2: 5,988–54,57; всего отражений 35142; независимых отражений 7353 (Rint = 0,0683); GOOF = 1,065; R-фактор 0,0419]]. Атомы сурьмы в комплексах имеют искаженную тригонально-бипирамидальную координацию с атомом кислорода карбоксильной группы в аксиальном положении.
Пентафенилсурьма, пента(пара-толил)сурьма, бифенил-2, 2-дикарбоновая кислота, бифенил-4, 4'-дикарбоновая кислота, деарилирование, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147251984
IDR: 147251984 | УДК: 546.865 +547.53.024+547.581.2+548.312.5+539.26 | DOI: 10.14529/chem250307
Interaction of pentaphenylantimony and penta(para-tolyl)antimony with biphenyl-2,2'-dicarboxylic acid. Reaction of pentaphenylantimony with biphenyl-4,4'-dicarboxylic acid. Structure of reaction products
The interaction of pentaphenylantimony and penta(para-tolyl)antimony with biphenyl-2,2'-dicarboxylic acid (molar ratio 2:1) in toluene and benzene, led to synthesis of binuclear derivatives 4-Ph4SbOC(O)C6H4C6H4OC(O)SbPh4 (1) and Tol4SbOC(O)C6H4C6H4SbTol4 ∙ 2PhH (2), yielding 70 % and 73 %, respectively. The reaction of pentaphenylantimony with biphenyl-4,4’-dicarboxylic acid in benzene produced Ph4SbOC(O)C6H4C6H4SbPh4 ∙ 3PhH (3) (81%). Crystallographic characteristics of the complex-es: (1) [C62H48O4Sb2, M = 1100.50; monoclinic syngony, space group Pn; cell parameters: a = 9.889(5) Å, b = 25.446(14) Å, c = 10.321(5) Å; β = 105.85(2), V = 2498(2) Å3, Z = 2; calc = 1.463 g/cm3; = 1.130 mm–1; F(000) = 1108.0; collection area by 2: 5.9853.82; total reflections 25282; independent reflections 9696 (Rint = 0.0706); GOOF = 1.190; R-factor 0.0522]; (2) [C82H76O4Sb2, M = 1368.93; monoclinic syngony, space group C2/c; cell parameters: a = 12.009(7) Å, b = 30.69(2) Å, c = 19.374(11) Å; β = 93.57(2), V = 7126(8) Å3, Z = 1; calc = 1.276 g/cm3; = 0.806 mm–1; F(000) = 2808.0; collection area by 2: 5.7254.34; total reflections 69807; independent reflections 7887 (Rint = 0.0708); GOOF = 1.048; R-factor 0.0422; (3) [C80H66O4Sb2, M = 1334.85; triclinic syngony, space group P-1; cell parameters: a = 10.676(8) Å, b = 13.404(8) Å, c = 13.917(9) Å; = 116.53(2), β = 104.21(3), = 97.60(2), V = 1658.7(19) Å3, Z = 2; calc = 1.336 g/cm3; = 0.864 mm–1; F(000) = 680.0; collection area by 2: 5.98854.57; total reflections 35142; independent reflections 7353 (Rint = 0.0683); GOOF = 1.065; R-factor 0.0419]. The antimony atoms in the complexes have a distorted trigonal-bipyramidal coordination with the oxygen atom of the carboxyl group in the axial position.
Текст научной статьи Взаимодействие пентафенилсурьмы и пента(пара-толил)сурьмы с бифенил-2,2’-дикарбоновой кислотой. Реакция пентафенилсурьмы с бифенил-4,4’-дикарбоновой кислотой. Строение продуктов реакций
В основной части публикаций, посвященных вопросам практического использования органических соединений сурьмы, изучаются различные аспекты их биологической активности [1–6]. Специфичность свойств конкретного соединения обусловлена природой лигандов у центрального атома металла, синтез же новых органических производных сурьмы позволяет увеличить разнообразие соединений с полезными свойствами.
Известно, что большинство органических ОН-кислот дефенилируют пентафенилсурьму, образуя производные Ph4SbX (X – остаток кислоты) [7–10]. Реакции пентаарилсурьмы с органическими соединениями, содержащими несколько реакционноспособных функциональных групп, представляют интерес, поскольку могут приводить к образованию комплексов сурьмы, в которых лиганд выполняет различные структурные функции. С другой стороны, для органических соединений, содержащих различные функциональные группы с подвижным атомом водорода, реакции с пентаарилсурьмой являются своеобразным показателем их активности в этих группах. Так, при взаимодействии пентафенилсурьмы с сульфосалициловой кислотой сначала происходит замещение атома водорода в сульфонатной группе, при избытке пентафенилсурьмы в реакцию вступает карбоксильная группа, а гидроксильная группа участия в реакции не принимает [11]. При взаимодействии пентафенилсурьмы с салициловой кислотой реагирует только карбоксильная группа [12], в то время как реакция пентафенилсурьмы с 4 - гидроксибензойной кислотой в толуоле в присутствии метоксида натрия протекает и по карбоксильной и по гидроксильной группам [13]. В реакции пентафенилсурьмы с 2,4-дигидроксибензойной кислотой независимо от соотношения реагентов участвуют карбоксильная и пара- гидроксильная группы, образуя биядерный комплекс - 2-гидрокси-4-тетрафенилстибоксибензоат тетрафенилсурьмы, в молекуле которого три-гонально-бипирамидальная координация двух атомов сурьмы искажена в разной степени [14].
Настоящая работа посвящена изучению реакций пентафенилсурьмы и пента( пара -толил)сурьмы с бифенил-2,2'-дикарбоновой кислотой и пентафенилсурьмы с бифенил-4,4 ' -дикарбоновой кислотой и установлению особенностей строения полученных продуктов.
Экспериментальная часть
В работе использовали дикарбоновые кислоты производства фирмы Alfa Aesar. Элементный анализ выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
Взаимодействие пентафенилсурьмы с бифенил-2,2'-дикарбоновой кислотой. Смесь 0,25 г (0,5 ммоль) пентафенилсурьмы и 0,06 г (0,25 ммоль) бифенил-2,2 ' -дикарбоновой кислоты в 3 мл толуола помещали в стеклянную ампулу, запаивали и выдерживали при 100 ° С 1 ч. После охлаждения и вскрытия ампулы прибавляли 1 мл октана, перемешивали и медленно концентрировали раствор до объема 1 мл. Образовавшиеся кристаллы фильтровали и сушили. Получили 0,19 г (70 %) бесцветных кристаллов 1 с т. пл. 242 °С. Найдено, %: С 67,48; H 4,50. Для C 62 H 48 O 4 Sb 2 вычислено, %: С 67,60; Н 4,36. ИК-спектр ( ν , см-1): 3049, 1637, 1584, 1554, 1479, 1435, 1184, 1061, 1022, 997, 853, 839, 762, 729, 690, 468, 454, 418.
Взаимодействие пента( пара -толил)сурьмы с бифенил-2,2'-дикарбоновой кислотой. Смесь 0,25 г (0,43 ммоль) пента-( пара -толил)сурьмы и 0,05 г (0,215 ммоль) бифенил-2,2 ‘ -дикарбоновой кислоты в 5 мл бензола помещали в стеклянную ампулу, запаивали и выдерживали при 100 ° С 1 ч. После охлаждения и вскрытия ампулы прибавляли 1 мл октана, перемешивали и медленно концентрировали раствор до объема 1 мл. Образовавшиеся кристаллы фильтровали и сушили. Получили 0,187 г (72 %) кристаллов 2 с т. пл. 195 °С (с разл.). Найдено, %: С 71,69; Н 5,68. Для C 82 H 76 O 4 Sb 2 вычислено, %: С 71,88; Н 5,55. ИК-спектр ( ν , см-1): 3053, 3032, 3017, 2954, 2920, 2864, 1630, 1611, 1591, 1560, 1493, 1477, 1435, 1393, 1335, 1271, 1211, 1188, 1142, 1117, 1101, 1059, 1036, 1015, 955, 878, 835, 797, 764, 750, 708, 679, 656, 582, 569, 544, 525, 486, 440.
Взаимодействие пентафенилсурьмы с бифенил-4,4'-дикарбоновой кислотой. Смесь 0,25 г (0,5 ммоль) пентафенилсурьмы и 0,06 г (0,25 ммоль) бифенил-4,4'-дикарбоновой кислоты в 3 мл бензола помещали в стеклянную ампулу, запаивали и выдерживали при 100 ° С 1 ч. После вскрытия ампулы прибавляли 1 мл октана, перемешивали и медленно концентрировали раствор до объема 1 мл. Образовавшиеся кристаллы фильтровали и сушили. Получили 0,27 г (81 %) бесцветных кристаллов 3 с т. пл. 242°С. Найдено, %: С 71,68; H 4,99. Для C62H48O4Sb2 вычислено, %: С 71,93; Н 4,94. ИК-спектр ( ν , см-1 ): 3049, 1637, 1584, 1554, 1479, 1435, 1184, 1061, 1022, 997, 853, 839, 762, 729, 690, 468, 454, 418.
ИК-спектры соединений записывали на ИК-спектрометре Shimadzu IRAffinity-1S в таблетках KBr в области 4000–400 см–1.
РСА кристаллов 1-3 проведен на дифрактометре D8 Quest фирмы Bruker (Mo K a-излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT- Plus [15]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [16] и OLEX2 [17]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Основные кристаллографические данные и результаты уточнения структур приведены в табл. 1, основные длины связей и валентные углы – в табл. 2.
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1975714 (1), № 2117977 (2), № 2119793 (3); или .
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1–3
|
Параметр |
1 |
2 |
3 |
|
Формула |
C 62 H 48 O 4 Sb 2 |
C 82 H 76 O 4 Sb 2 |
C 80 H 66 O 4 Sb 2 |
|
М |
1100,50 |
1368,93 |
1334,62 |
|
Сингония |
Моноклинная |
Моноклинная |
Триклинная |
|
Пр. группа |
Pn |
C2/ c |
Р–1 |
|
a , Å |
9,889(5) |
12,009(7) |
10,676(8) |
|
b , Å |
25,446(14) |
30,69(2) |
13,403(8) |
|
c, Å |
10,321(5) |
19,374(11) |
13,917(9) |
|
а, град |
90,00 |
90,00 |
116,53(2) |
|
β, град |
105,85(2) |
93,57(2) |
104,21(3) |
|
Y, град |
90,00 |
90,00 |
97,60(2) |
|
V , Å3 |
2498(2) |
7126(8) |
1658,7(19) |
|
Z |
2 |
1 |
2 |
|
Р выч, г/см |
1,463 |
1,276 |
1,336 |
Окончание табл. 1
|
Параметр |
1 |
2 |
3 |
|
-1 µ , мм |
1,130 |
0,806 |
0,864 |
|
F (000) |
1108,0 |
2808,0 |
680,0 |
|
Размер кристалла, мм |
0,33 × 0,14 × 0,03 |
0,38 × 0,21 × 0,11 |
0,42 × 0,18 × 0,16 |
|
Область сбора данных по 2 θ , град |
5,98–53,82 |
5,72–54,34 |
5,988–4,57 |
|
Интервалы индексов отражений |
–12 ≤ h ≤ 12, –31 ≤ k ≤ 32, –12 ≤ l ≤ 12 |
–15 ≤ h ≤ 15, –39 ≤ k ≤ 39, –24 ≤ l ≤ 24 |
–13 ≤ h ≤ 13, –17 ≤ k ≤ 17, –17 ≤ l ≤ 17 |
|
Измерено отражений |
25282 |
69807 |
35142 |
|
Независимых отражений |
9696 |
7887 |
7353 |
|
R int |
0,0706 |
0,0708 |
0,0683 |
|
Переменных уточнения |
613 |
396 |
377 |
|
GOOF |
1,190 |
1,048 |
1,065 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0522, w R 2 = 0,1083 |
R 1 = 0,0422, wR 2 = 0,1035 |
R 1 = 0,0419, wR 2 = 0,1061 |
|
R -факторы по всем отражениям |
R 1 = 0,0772, wR 2 = 0,1218 |
R 1 = 0,0706, wR 2 = 0,1183 |
R 1 = 0,0607, wR 2 = 0,1204 |
|
Остаточная электронная плотность (max/min), e/A3 |
1,03/–2,69 |
0,90/–0,48 |
1,61/–1,17 |
Таблица 2
Основные длины связей и валентные углы в соединениях 1–3
|
Связь |
d, Å |
Угол |
ω , град |
|
|
1 |
||||
|
Sb(1)–C(21) |
2,110(8) |
C(21)Sb(1)C(1) |
113,1(3) |
|
|
Sb(1)–C(1) |
2,119(8) |
C(21)Sb(1)С(11) |
131,6(3) |
|
|
Sb(1)–С(31) |
2,173(8) |
C(1)Sb(1)С(11) |
112,1(3) |
|
|
Sb(1)–O(1) |
2,260(5) |
C(31)Sb(1)O(1) |
177,4(3) |
|
|
Sb(1)–С(11) |
2,139(8) |
C(11)Sb(1)С(31) |
84,3(4) |
|
|
Sb(2)–O(3) |
2,246(5) |
C(21)Sb(1)С(31) |
97,4(3) |
|
|
Sb(2)–С(61) |
2,130(8) |
C(21)Sb(1)O(1) |
84,3(3) |
|
|
Sb(2)–С(71) |
2,111(8) |
C(1)Sb(1)С(31) |
96,1(3) |
|
|
Sb(2)–С(81) |
2,156(8) |
C(1)Sb(1)O(1) |
85,1(3) |
|
|
Sb(2)–С(91) |
2,213(9) |
С(21)Sb(1)С(31) |
97,4(3) |
|
|
О(1)–С(47) |
1,285(9) |
С(61)Sb(2)С(81) |
110,9(3) |
|
|
О(2)–С(47) |
1,228(10) |
С(71)Sb(2)С(61) |
108,4(4) |
|
|
О(3)–С(48) |
1,312(10) |
С(71)Sb(2)С(81) |
137,9(4) |
|
|
О(4)–С(48) |
1,242(10) |
С(91)Sb(2)O(3) |
175,2(3) |
|
|
Sb(1) ⋅⋅⋅ O(2) |
3,048(12) |
С(71)Sb(2)С(91) |
93,3(4) |
|
|
Sb(2) ⋅⋅⋅ O(4) |
2,920(11) |
С(81)Sb(2)O(3) |
86,4(3) |
|
|
2 |
||||
|
Sb(1)–О(1) |
2,240(2) |
C(21)Sb(1)O(1) |
178,52(13) |
|
|
Sb(1)–С(1) |
2,111(3) |
С(11)Sb(1)С(1) |
116,61(13) |
|
|
Sb(1)–С(11) |
2,110(4) |
С(31)Sb(1)С(1) |
128,20(15) |
|
|
Sb(1)–С(31) |
2,104(4) |
С(31)Sb(1)С(11) |
112,81(14) |
|
|
Sb(1)–С(21) |
2,184(4) |
C(1)Sb(1)O(1) |
84,92(12) |
|
|
O(1)–C(47) |
1,292(4) |
C(1)Sb(1)C(21) |
94,81(14) |
|
|
O(2)–C(47) |
1,219(4) |
C(11)Sb(1)O(1) |
82,37(12) |
|
|
Sb(1) ⋅⋅⋅ O(2) |
3,168(9) |
C(11)Sb(1)C(21) |
96,46(15) |
|
|
Преобразования симметрии: 11-x, +y, 1/2-z |
||||
|
3 |
||||
|
Sb(1)–C(11) |
2,118(4) |
C(11)Sb(1)C(21) |
120,78(14) |
|
|
Sb(1)–O(1) |
2,214(3) |
С(11)Sb(1)С(1) |
115,41(14) |
|
Окончание табл. 2
|
Связь |
d, А |
Угол |
ω , град |
|
Sb(1)–С(31) |
2,174(3) |
С(1)Sb(1)С(21) |
120,76(14) |
|
Sb(1)–С(21) |
2,130(4) |
С(31)Sb(1)O(1) |
174,83(11) |
|
Sb(1)–С(1) |
2,120(4) |
C(1)Sb(1)С(31) |
94,49(14) |
|
O(1)–C(47) |
1,290(4) |
С(11)Sb(1)O(1) |
83,59(12) |
|
O(2)–С(47) |
1,216(5) |
C(11)Sb(1)С(31) |
96,92(14) |
|
Sb(1) ⋅⋅⋅ O(2) |
3,443(10) |
C(21)Sb(1)C(31) |
96,04(15) |
|
Преобразования симметрии: 13-x, 2-y,2-z; 22-x, 2-y,1-z |
|||
Обсуждение результатов
Известно, что при взаимодействии пентаарилсурьмы с монокарбоновыми кислотами образуются карбоксилаты тетраарилсурьмы, то есть происходит замещение атома водорода в карбоксильной группе на фрагмент Ar4Sb [18]. Исследовано множество таких реакций и получено несколько десятков различных карбоксилатов тетраарилсурьмы.
Однако в настоящее время реакции пентаарилсурьмы с дикарбоновыми кислотами описаны только на нескольких примерах. Особенностью таких реакций является возможность замещения кислых атомов водорода на фрагмент Ar4Sb как в одной [19–21], так и в двух карбоксильных группах [22, 23].
Мы нашли, что пентафенилсурьма реагирует с бифенил-2,2 ′ -дикарбоновой кислотой (2:1 мольн.) в растворе толуола с образованием биядерного производного сурьмы 1 .
TolH
2 Ph 5 Sb + 2-HOC(O)C 6 H 4 –C 6 H 4 С(О)ОН-2 ′ → 2-Ph 4 SbOC(O)C 6 H 4 –C 6 H 4 С(О)ОSbPh 4 -2 ′ + 2 PhH
Показано, что взаимодействие пента( пара -толил)сурьмы с этой же кислотой в бензоле приводило к синтезу сольвата 2 с бензолом:
PhH
2 Tol 5 Sb + 2-HOC(O)C 6 H 4 –C 6 H 4 С(О)ОН-2 ′ → 2- Tol 4 SbOC(O)C 6 H 4 –C 6 H 4 С(О)ОSbTol 4 -2 ′ ∙ 2PhH
Мы показали, что единственным сурьмаорганическим продуктом реакции пентафенилсурь-мы с бифенил-4,4'-дикарбоновой кислотой в бензоле являлся сольват 3 .
PhH
2 Ph 5 Sb + 4-HOC(O)C 6 H 4 –C 6 H 4 С(О)ОН-4 ′ → 4-Ph 4 SbOC(O)C 6 H 4 –C 6 H 4 С(О)ОSbPh 4 -4 ′ ∙ 3PhH
После завершения реакций, ход которой контролировали методом ТСХ, в реакционную смесь прибавляли октан и медленно концентрировали, при этом на стенках ампулы кристаллизовались прозрачные кристаллы.
В ИК-спектрах полученных карбоксилатов бис (тетраарилсурьмы) 1, 2, 3 присутствуют интенсивные полосы поглощения, относящиеся к валентным колебаниям связи С=О: 1637, 1630, 1640 см–1 соответственно, при этом их положение смещено в область низкочастотных колебаний по сравнению со спектрами соответствующих кислот. Наличие фрагмента SbC 4 в полученных соединениях характеризуется присутствием в их ИК-спектрах полос поглощения при 454, 480, 460 см–1, а наличие связей Sb–O подтверждается полосами поглощения при 468, 486, 465 см–1, что соответствует литературным данным [24–26].
По данным РСА, атомы сурьмы в 1 – 3 характеризуются искаженной тригонально-бипирамидальной координацией (рис. 1–3).
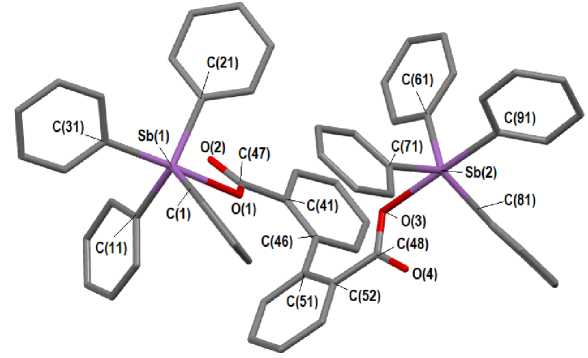
Рис. 1. Строение соединения 1
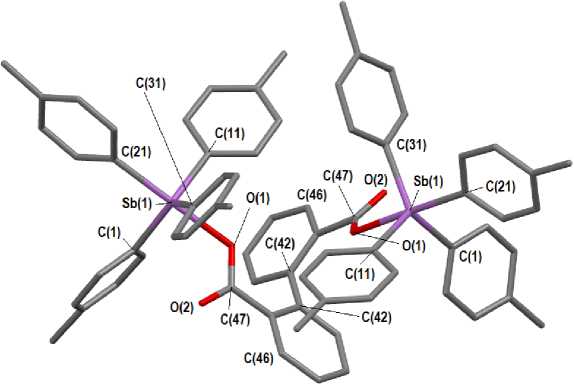
Рис. 2. Строение соединения 2 (сольватные молекулы бензола и атомы водорода не показаны)
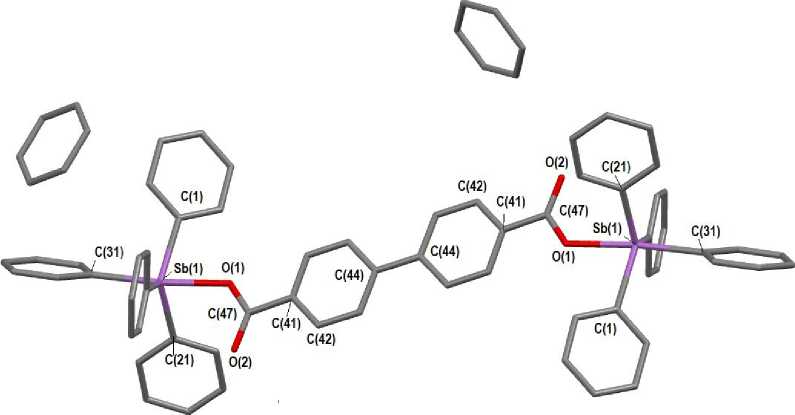
Рис. 3. Строение соединения 3 (атомы водорода не показаны)
Молекулы 2 и 3 имеют центр инверсии, который соответствует точке на середине связи C(42)-C(42 ‘ ) ( 2 ) или С(44)-С(44 ' ) ( 3 ). В молекуле 1 атомы Sb(1) и Sb(2) не эквивалентны. Аксиальные углы O(1)Sb(1)C(31), O(3)Sb(2)C(91) в 1 , O(1)Sb(1)C(21) в 2 и O(1)Sb(1)C(31) в 3 равны 177,4(3) ° , 175,2(3) ° ; 178,52(13) ° и 174,83(11) ° . Суммы экваториальных углов СSbС составляют 356,81(3) ° , 357,20(4) ° ; 357,62(15) ° и 356,95(14) ° в 1 - 3 соответственно. В 1 атомы Sb(1) и Sb(2) выходят из экваториальных плоскостей [С(1)С(11)С(21)] и [C(61)C(71)C(81)] соответственно на 0,219 и 0,198 Å, атом Sb(1) в 2 – из плоскости [С(1)С(11)С(21)] на 0,168 Å, в 3 – из плоскости [С(1)С(11)С(21)] на 0,215 Å, что приводит к искажению углов между экваториальными и аксиальными связями по сравнению с теоретическим значением 90 ° (в 1 углы O(1)Sb(1)C(1,11,21) равны 83,1(3) ° -85,1(3) ° , C(31)Sb(1)C(1,11,21) - 94,3(4) ° -97,4(3) ° ; O(3)Sb(2)C(61,71,81) - 82,6(3) ° -86,4(3) ° , C(91)Sb(1)C(61,71,81) - 93,3(4) ° -98,6(3) ° ; в 2 углы O(1)Sb(1)C(1,11,31) и
C(21)Sb(1)C(1,11,31) составляют 82,37(12) ° -87,06(13) ° и 94,24(15) ° -96,46(15) ° ), в 3 аналогичные углы равны 80,68(12) ° -88,08(13) ° и 94,49(14) ° -96,92(14) ° ). В 1 - 3 аксиальные связи Sb-C длиннее экваториальных. Так, в 1 связь Sb(1)–C(31) равна 2,173(8) Å, а экваториальные связи Sb(1)– C(1,11,21) – 2,119(8), 2,139(8), 2,110(8), в другом фрагменте молекулы при атоме Sb(2) аналогичные связи имеют значения 2,213(9) Å и 2,111(8), 2,130(8), 2,156(8) Å. В 2 и 3 длины аксиальных связей Sb–C (2,184(4) Å и 2,174(3) Å) также превышают длины экваториальных связей [2,104(4), 2,110(4), 2,111(3) Å и 2,118(4), 2,120(4), 2,130(4) Å). Расстояния Sb–O (2,260(5), 2,246(5) Å в 1 , 2,240(2) Å в 2 , 2,214(3) Å в 3 ) значительно длиннее, чем сумма ковалентных радиусов атомов (2,15 Å [27]). Бидентатность карбоксилатных лигандов проявляется слабо, поскольку имеет место значительная асимметрия координации: внутримолекулярные расстояния, обусловленные дополнительными взаимодействия Sb --- O=C с карбонильным атомом кислорода, составляют 3,046(8), 2,920(5) Å ( 1 ), 3,168(3) Å ( 2 ), 3,443(4) Å ( 3 ). Углы между плоскостями ароматических колец в остатке бифенил-2,2 ' -дикарбоновой кислоты составляют 66,63 ° и 71,80 ° (в 1 и 2 соответственно); в молекулах 3 кольца бифенил-4,4 ' -дикарбоновой кислоты лежат в одной плоскости, при этом плоскость карбоксильной группы отклоняется от нее на угол 6,13 ° .
Выводы
Установлено, что взаимодействие пентафенилсурьмы и пента( пара -толил)сурьмы с бифенил-2,2 ' -дикарбоновой кислотой (мольн. соотношение 2:1) в толуоле и бензоле приводит к образованию биядерных производных Ph 4 SbOC(O)C 6 H 4 C 6 H 4 OC(O)SbPh 4 ( 1 ) и Tol 4 SbOC(O)C 6 H 4 C 6 H 4 OC(O)SbTol 4 ∙ 2PhH ( 2 ) с выходами 70% и 73% соответственно. Реакция пентафенилсурьмы с бифенил-4,4 ' -дикарбоновой кислотой в бензоле приводит к образованию Ph 4 SbOC(O)C 6 H 4 C 6 H 4 SbPh 4 ∙ 3PhH ( 3 ). Атомы сурьмы в комплексах имеют искаженную тригонально-бипирамидальную координацию с атомом кислорода карбоксильной группы в аксиальном положении. С учетом внутримолекулярной координации атома металла с карбонильным атомом кислорода координационное число атома сурьмы составляет 6.


