Взаимосвязь показателей качества жизни и механической функции левого предсердия у пациентов после успешной радиочастотной изоляции легочных вен по поводу идиопатической пароксизмальной формы фибрилляции предсердий
Автор: Щербинина Диана Александровна, Мамчур Сергей Евгеньевич, Мамчур Ирина Николаевна, Хоменко Егор Александрович, Бохан Никита Сергеевич, Горшкова Татьяна Владимировна, Горбунова Елена Владимировна
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.30, 2015 года.
Бесплатный доступ
Цель: оценить взаимосвязь качества жизни (КЖ) и механической функции левого предсердия (ЛП) после успешной изоляции легочных вен (ЛВ). В исследование включено 120 пациентов после радиочастотной аблации (РЧА) по поводу фибрилляции предсердий (ФП), представленных двумя группами: в группе I фиксировалось нарушение механической функции ЛП, в группе Ii таких нарушений не выявлено. Были изучены внутрипредсердная гемодинамика с помощью инвазивной манометрии и эхокардиграфии и КЖ - при помощи опросника SF-36 через 3, 6 и 12 мес. Через 3 мес. выявлено снижение КЖ в группе I по сравнению с группой II, через 6 мес. КЖ в группе I улучшились, в то время как в группе II изменения не претерпели значимой динамики, через 12 мес. показатели КЖ между группами не различались. Аналогичная динамика наблюдалась для показателей механической функции ЛП. Вывод: снижение качества жизни у пациентов, перенесших успешную изоляцию ЛВ, ассоциируется с нарушением механической функции ЛП, сопутствующего массивному радиочастотному (РЧ) воздействию в области его антрумов.
Качество жизни, изоляция легочных вен, левое предсердие, механическая функция
Короткий адрес: https://sciup.org/14920004
IDR: 14920004 | УДК: 616.125.2
The relationship of quality of life and the mechanical function of the left atrium in patients after successful radiofrequency isolation of the pulmonary veins for idiopathic paroxysmal atrial fibrillation
The aim of the study was to estimate the relationship between quality of life (QoL) and left atrial (LA) mechanical function after successful pulmonary vein (PV) isolation. A total of 120 patients after the ablation for atrial fibrillation were enrolled in the study. Patients of group I had the LA mechanical function disorder; group II did not have this disorder. Intraatrial hemodynamics was studied by invasive manometry and echocardiography; QoL was evaluated by using the SF-36 questionnaire at 3, 6, and 12 months. In 3 months, QoL decrease was demonstrated in group I in comparison with group II. In 6 months, QoL in group I improved whereas it did not significantly change in group II. After 12 months, QoL did not differ between groups. A similar trend was observed for the characteristics of the LA mechanical function. Conclusion: The QoL deterioration in patients who underwent successful PV isolation was associated with the disorder of the LA mechanical function due to the massive radiofrequency exposure in the antral area.
Текст научной статьи Взаимосвязь показателей качества жизни и механической функции левого предсердия у пациентов после успешной радиочастотной изоляции легочных вен по поводу идиопатической пароксизмальной формы фибрилляции предсердий
ФП является самой распространенной аритмией сердца [1]. Наличие у пациентов ФП ассоциируется с двукратным увеличением смертности, в значительной степени обусловленной развитием инсульта и прогрессированием сердечной недостаточности (СН) [2–4]. Современные методы интервенционного лечения позволяют радикально устранить пароксизмальную форму ФП у 75–80% больных путем радиочастотной антральной изоляции ЛВ [5]. Более чем в 70% РЧА ЛВ приводит к значительному улучшению КЖ, снижению размеров ЛП и увеличению сократительной способности левого желудочка (ЛЖ) [6].
Однако исключение большой площади предсердного миокарда в области антрумов ЛП может привести к изменениям внутрисердечной гемодинамики в виде снижения сократимости ЛП или синдрома “жесткого предсердия” [7, 8]. Это ухудшение может быть следствием как известного механизма станнинга, так и других менее изученных, однако участвующих в нарушении предсердной сократимости механизмов [9].
Помимо выявления самого по себе факт нарушений сократительной функции предсердий крайне важен, однако до настоящего времени не изучен его вклад в клиническое течение заболевания, влияние на прогноз, КЖ и риск тромбообразования [9]. Вопрос о том, является ли нарушение механической функции ЛП предиктором или маркером неблагоприятного прогноза, для больных с ФП в постаблационном периоде, все еще остается открытым [10].
Цель исследования: оценить взаимосвязь показателей КЖ и механической функции ЛП у пациентов после проведения успешной радиочастотной изоляции ЛВ вен по поводу идиопатической пароксизмальной формы ФП.
Материал и методы
Исследование выполнено на базе НИИ комплексных проблем сердечно-сосудистых заболеваний (Кемерово) и МБУЗ “Кемеровский кардиологический диспансер”. Протокол исследования одобрен локальным этическим комитетом. Обязательным условием включения пациента в исследование явилось подписанное им информированное согласие на участие в исследовании.
В исследование включено 120 пациентов, подвергшихся успешной РЧА по поводу идиопатической пароксизмальной формы ФП. Под успешностью процедуры подразумевалось отсутствие любых предсердных тахиаритмий по данным опроса и трехсуточного мониторирования электрокардиограммы (ЭКГ) за время, прошедшее с окончания “слепого” периода (3 мес. после процедуры) до 1 года после катетерного вмешательства [11].
Критерии включения: наличие пароксизмальной формы ФП; катетерная РЧА в объеме антральной изоляции, дополненной или не дополненной любой методикой модификации субстрата (РЧА ганглионарных сплетений, комплексных фракционированных электрограмм, линейные РЧА в левом предсердии); переднезадний размер ЛП менее 5 см или объем ЛП менее 90 мл по данным эхокардиографии или 110 мл по данным компьютерной томографии; возраст пациентов моложе 70 лет.
Критерии исключения: ишемическая болезнь сердца (ИБС); врожденные пороки сердца (ВПС); гипертоническая болезнь (ГБ); структурные заболевания сердца, требующие открытой хирургической коррекции; тяжелая сопутствующая патология.
Респонденты были распределены на две группы: в группе I (n=72, 60%) у пациентов в ближайшем послеоперационном периоде фиксировалось нарушение механической функции левого предсердия (МФЛП), в группе II (n=48, 40%) подобных нарушений выявлено не было.
У всех пациентов интраоперационно были изучены показатели внутрипредсердной гемодинамики с помощью инвазивной манометрии в левых камерах сердца, внутрисердечной или чреспищеводной эхокардиграфии. В дооперационном, а также ближайшем и отдаленном
Таблица 1
Дооперационные клинические характеристики пациентов, включенных в исследование
(3, 6, 12 мес.) послеоперационном периодах внутрипред-сердная гемодинамика была изучена посредством трансторакальной и чреспищеводной эхокардиографии по расширенному протоколу, включавшему показатели сократительной и резервуарной функции ЛП и ЛВ. Помимо инструментальных показателей, были изучены показатели КЖ при помощи опросника SF-36.
Основная клинико-анамнестическая характеристика больных отражена в таблице 1.
Показатели КЖ анализировались при помощи опросника SF-36, включающего показатели физического и психологического компонентов здоровья, сгруппированные в 8 основных шкал:
-
1. Физический компонент здоровья (physical health – PH) включает следующие шкалы:
-
1.1. Физическое функционирование (PF), отражающее степень, в которой физическое состояние ограничивает выполнение физических нагрузок. Низкие показатели по этой шкале свидетельствуют о том, что физическая активность пациента значительно ограничивается состоянием его здоровья.
-
1.2. Ролевое функционирование, обусловленное физическим состоянием (RP) – влияние физического состояния на повседневную ролевую деятельность. Низкие показатели свидетельствуют о том, что повседневная деятельность значительно ограничена физическим состоянием пациента.
-
1.3. Интенсивность боли (BP) и ее влияние на способность заниматься повседневной деятельностью, включая работу по дому и вне дома. Низкие показатели по этой шкале свидетельствуют о том, что боль значительно ограничивает активность пациента.
-
1.4. Общее состояние здоровья (GH) – оценка больным своего состояния здоровья в настоящий момент и перспектив лечения. Чем ниже баллы по этой шкале, тем ниже оценка состояния здоровья.
-
-
2. Психологический компонент здоровья (mental health – MH) включает следующие шкалы:
-
2.1. Жизненная активность (VT) подразумевает ощущение себя полным сил и энергии или, напротив, обессиленным. Низкие баллы свидетельствуют об утомлении пациента, снижении жизненной активности.
-
2.2. Социальное функционирование (SF), определяется степенью, в которой физическое или эмоциональное состояние ограничивает социальную активность (общение). Низкие баллы свидетельствуют о значительном ограничении социальных контактов, снижении уровня общения в связи с ухудшением физического и эмоционального состояния.
-
2.3. Ролевое функционирование, обусловленное эмоциональным состоянием (RE), предполагает оценку степени, в которой эмоциональное состояние мешает выполнению работы или другой повседневной деятельности. Низкие показатели по этой шкале интерпретируются как ограничение в выполнении повседневной работы, обусловленное ухудшением эмоционального состояния.
-
2.4. Психическое здоровье (MH) характеризует настроение, наличие депрессии, тревоги, общий показатель положительных эмоций. Низкие показатели свидетельствуют о наличии депрессивных, тревожных переживаний, психическом неблагополучии.
-
Статистическая обработка результатов исследования осуществлялась с помощью программы STATISTICA версии 8.0.360.0 компании StatSoft, Inc. (США). Значения представлены для качественных величин в виде процентного соотношения, для количественных – в виде среднего значения и стандартного отклонения или медианы и квартильного размаха. Анализ различия показателей в двух независимых группах проводился при помощи критериев Манна–Уитни и чІ с поправкой Йетса. Различия в сравниваемых группах считались статистически значимыми при уровне ошибки первого рода (р) менее 0,05.
Результаты
Как следует из ретроспективного анализа КЖ (табл. 2), исходно ни по одному из показателей не было зарегистрировано статистически значимых различий между исследованными группами. При этом показатели всех шкал находились ниже границы нормы, что пациенты связывали с симптомностью аритмии (все пациенты до операции имели III–IV класс симптомности по EHRA, в среднем 3,3±0,3) [11].
По результатам анализа данных опросника SF-36, полученным в сроки 3 мес. после оперативного лечения ФП, выявлено снижение всех параметров КЖ у пациентов группы I по сравнению с группой II. По шкале PF отличие составило 16,18 баллов, ролевого физического функционирования (RF) – 26,51 балла, BP – 19,84 балла, GH – 26,33 балла, VT – 15,19 балла, SF – 10,38 балла, RE – 23,06 балла, MH – 4,59 балла (рис. 1).
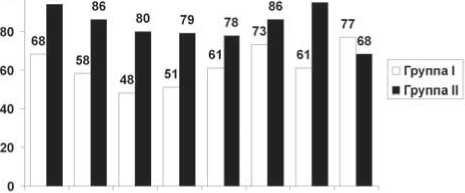
Через 6 мес. после проведения катетерной процедуры показатели КЖ в группе I улучшились, в то время как в группе II изменения не претерпели значимой динамики (рис. 2). Наиболее выраженными оказались изменения шкал ролевого RE и общей VT в группе I: показатели повысились на 9,87 и 17,63 балла соответственно (p<0,05).
По результатам анализа данных опросника SF-36, полученным в сроке 12 мес. после изоляции ЛВ, выявлено максимальное приближение показателей КЖ группы I к
Таблица 2
Данные опросника SF 36 у пациентов до проведения изоляции ЛВ
|
Показатели |
Группа I (n=72) |
Группа II (n=48) |
р |
|
PF |
69,6 (53,3–74,5) |
69,6 (51,8–77,2) |
0,75 |
|
RF |
49,3 (31,7–64,4) |
55,0 (32,9–69,1) |
0,28 |
|
BP |
58,2 (25,3–71,1) |
60,8 (27,4–73,2) |
0,51 |
|
GH |
47,2 (34,7–65,5) |
52,5 (38,1–66,8) |
0,37 |
|
VT |
56,6 (40,9–72,1) |
61,0 (48,2–76,6) |
0,66 |
|
SF |
68,5 (44,4–85,0) |
75,4 (49,9–87,1) |
0,82 |
|
RE |
65,7 (29,2–83,3) |
66,6 (28,4–82,1) |
0,91 |
|
MH |
66,3 (50,3–79,1) |
67,7 (52,2–77,1) |
0,69 |
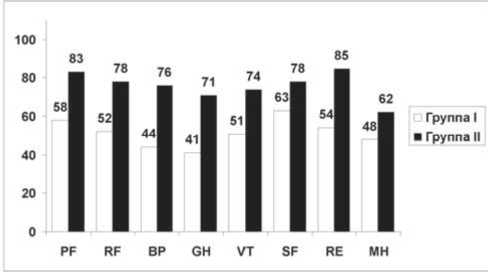
Рис. 1. Сравнение показателей КЖ по восьми шкалам у пациентов через 3 мес. после проведения изоляции ЛВ. p<0,05 во всех различиях
100 94 95
PF RF BP GH VT SF RE MH
Рис. 2. Сравнение показателей КЖ по восьми шкалам у пациентов через 6 мес. после проведения изоляции ЛВ. p<0,05 во всех различиях, кроме SF и MH
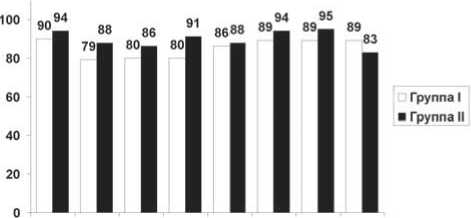
PF RF BP GH VT SF RE MH
Рис. 3. Сравнение показателей КЖ по восьми шкалам у пациентов через 12 мес. после проведения изоляции ЛВ. p>0,05 во всех различиях
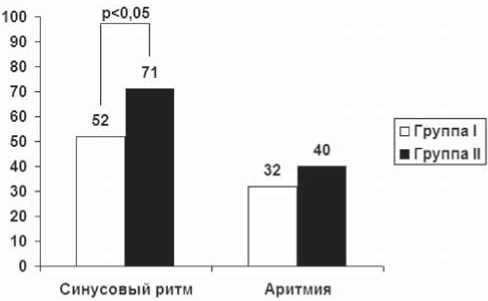
Рис. 4. Показатели КЖ в межприступный период и в период пароксизмов аритмий “слепого” периода
тем же показателям группы II с отсутствием статистически значимых различий между группами (рис. 3).
При этом абсолютные значения всех шкал в обеих группах по сравнению с дооперационными в течение всего периода наблюдения постепенно выросли и оказались в пределах нормальных значений, что пациенты связывали непосредственно с антиаритмическим эффектом вмешательства и элиминацией симптомных аритмий “слепого” периода – ими страдали 38 (32%) из всех обследованных пациентов.
Также стоит отметить, что к моменту проведения анкетирования в финальной точке (12 мес.) показатели механической функции ЛП у всех пациентов группы I вернулась к нормальным значениям. Поскольку симптом-ность аритмий “слепого” периода не различалась между группами (3,6±0,3 против 3,6±0,3 баллов по EHRA, р=0,916) [11], нами также было проведено сравнение показателей КЖ в обеих группах в межприступный период и период нарушения ритма.
Как следует из рисунка 4, различия в интегральном показателе КЖ между группами были отмечены лишь в межприступный период, что дает основания ассоциировать уровень КЖ именно с нарушенной сократительной функцией ЛП, сопутствующей массивному радиочастотному повреждению в области антрумов ЛП, а не с какими-либо иными факторами.
Обсуждение
Анализируя результаты данных опросника SF-36 до лечения, было выявлено снижение показателей уровня КЖ по всем шкалам у пациентов, страдающих ФП. Это свидетельствует о том, что пароксизмы ФП негативно влияют на жизнедеятельность человека, способность заниматься повседневной работой, а также на общее состояние здоровья и психологический статус. Этот факт подтверждается высоким классом симптомности аритмии по EHRA [11].
После проведения РЧ изоляции ЛВ отмечается улучшение показателей физического и психологического компонентов здоровья, по сравнению с этими же показателями в дооперационном периоде, которое достигает статистической значимости не ранее чем через 6 мес. после проведения процедуры. По нашему мнению, данный факт может быть обусловлен собственно антиарит-мическим эффектом РЧА, поскольку в пределах “слепого” периода симптоматичность предсердных тахиаритмий оказалась даже несколько выше (хотя и статистически незначимо), чем аритмий, по поводу которых проводилась процедура. В последующем пациенты отмечают выраженную положительную динамику КЖ за счет снижения частоты пароксизмов ФП посредством РЧ изоляции ЛВ. Однако даже по прошествии “слепого” периода у группы пациентов с выявленным нарушением механической функции ЛП показатели КЖ гораздо ниже таковых в группе без подобных нарушений.
Также была прослежена динамика изменения показателей КЖ по мере восстановления МФЛП, выявлена взаимосвязь между их ухудшением в относительно раннем послеоперационном периоде и нарушением механической функции ЛП. Наиболее наглядно это можно увидеть в сравнении показателей физического и психологического здоровья между группами I и II, особенно через 3 мес. после выполнения РЧ изоляции ЛВ. С этим фактом согласуется влияние частых пароксизмов послеоперационных тахикардий на КЖ пациентов обеих групп.
Таким образом, КЖ пациентов по окончании “слепого” периода после выполнения клинически эффективной изоляции ЛВ определяется нарушенной механической функцией ЛП, а не иными факторами.
Неспецифический опросник SF-36 для оценки КЖ может быть полезен в комплексном обследовании пациентов с различными формами ФП, а также для определения тактики лечения данной категории больных и контроля качества оказанной медицинской помощи. В дальнейшем следует направить усилия на научное обоснование и внедрение рутинных методов диагностики нарушения механической функции ЛП и их медикаментозной коррекции.
Выводы
Снижение КЖ у пациентов, перенесших успешную изоляцию ЛВ, ассоциируется с нарушением механической функции ЛП, сопутствующего массивному радиочастотному воздействию в области его антрумов.
Список литературы Взаимосвязь показателей качества жизни и механической функции левого предсердия у пациентов после успешной радиочастотной изоляции легочных вен по поводу идиопатической пароксизмальной формы фибрилляции предсердий
- Feinberg W.M., Blackshear J.L., Laupacis A. et al. Prevalence, age distribution, and gender of patients with atrial fibrillation: analysis and implications//Arch. Intern. Med. -1995. -Vol. 155. -P. 469-473.
- Wang T.J., Larson M.G., Levy D. et al. Temporal relations of atrial fibrillation and congestive heart failure and their joint influence on mortality: the Framingham Heart Study//Circulation. -2003. -Vol. 107. -P. 2920-2925.
- Benjamin E.J., Wolf P.A., D’Agostino R.B. et al. Impact of atrial fibrillation on the risk of death: the Framingham Heart study//Circulation. -1998. -Vol. 98. -P. 946-952.
- Stewart S., Hart C.L., Hole D.J. et al. A population-based study of the long-term risks associated with atrial fibrillation: 20-year follow-up of the Renfrew/Paisley study//Am. J. Med. -2002. -Vol. 113. -P. 359-364.
- Gallegoa A.M., Diaz-Infantea E., Garcia-Bolaoa E. Spanish Catheter Ablation Registry. 8th Official report of the Spanish Society of Cardiology Working Group on electrophysiology and arrhythmias (2008)//Rev. Esp. Cardiol. -2009. -Vol. 62(11). -P. 1276-1285.
- Earley M., Abrams D., Staniforth A. et al. Catheter ablation of permanent atrial fibrillation: medium term results//Heart. -2006. -Vol. 92. -P. 233-238.
- Мамчур С.Е., Мамчур И.Н., Хоменко Е.А. и др. Механическая функция левого предсердия и легочных вен до и после их антральной изоляции//Вестник аритмологии. -2013. -№ 71. -С. 5-11.
- Gibson D.N., Di Biase L., Mohanty P. et al. Stiff left atrial syndrome after catheter ablation for atrial fibrillation: clinical characterization, prevalence, and predictors//Heart Rhythm. -2011. -Vol. 8. -P. 1364-1371.
- Henein M. Left atrial function in health and disease. -Umea: Department of Public Health and Clinical Medicine, 2012. -118 p.
- Pagel P.S., Kehl F., Gare M. et al. Mechanical function of the left atrium//Anesthesiology. -2003. -Vol. 98. -P. 975-994.
- Calkins H., Kuck K.H., Cappato R. et al. 2012 HRS/EHRA/ECAS Expert Consensus Statement on Catheter and Surgical Ablation of Atrial Fibrillation: Recommendations for Patient Selection, Procedural Techniques, Patient Management and Follow-up, Definitions, Endpoints, and Research Trial Design//Europace. -2012. -Vol. 14. -P. 528-606.


