Зависимость карбоксилэстеразной активности почвенных грамотрицательных микроорганизмов от стадии роста и состава среды
Автор: Ремезовская Наталья Борисовна, Максимов Александр Юрьевич, Демаков Виталий Алексеевич
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 1, 2011 года.
Бесплатный доступ
Изучена зависимость роста и карбоксилэстеразной активности почвенных грамотрицательных бактерий рода Pseudomonas от концентрации источника углерода, азота и фосфора. Установлено, что карбоксилэстеразная активность исследуемых культур имеет высокий уровень конститутивного выражения. При высоких концентрациях глюкозы (более 1%) наблюдается угнетение роста и понижение эстеразной активности. Карбоксилэстеразная активность культур P. fluorescens в оптимальных условиях достигала 10 мкмоль/мг/мин.
Биотрансформация, карбоксилэстераза, сложные эфиры
Короткий адрес: https://sciup.org/147204535
IDR: 147204535 | УДК: 579.24+579.222.4
Dependence of carboxyl esterase activity in soil gram-negative microorganisms on growth phase and medium composition
Dependence of growth and carboxyl esterase activity in soil Gram-negative bacteria of genus Pseudomonas on concentration of carbon, nitrogen, and phosphorus sources was analyzed. It was determined that carboxyl esterase activity in cultures under study possessed high level of constitutive expression. Under high glucose concentrations (over 1%) growth suppression and lowering of the esterase activity was observed. It was found that carboxyl esterase activity in P. fluorescens cultures approached 10 mmol/mg/min under the optimal conditions.
Текст научной статьи Зависимость карбоксилэстеразной активности почвенных грамотрицательных микроорганизмов от стадии роста и состава среды
В настоящее время бактериальные эстеразы эффективно применяют в органическом синтезе оптически чистых компонентов. Кроме того, они активно используются в качестве биодеструкторов при деградации органических соединений в загрязненных природных объектах. Интерес к данной группе ферментов связан еще и с тем, что эстеразы не являются зависимыми от кофакторов, а также обычно стабильны и даже активны в органических растворах (Bornscheuer, 2002). Несмотря на значительные успехи в области селекции микроорганизмов – продуцентов ферментов, потребность промышленности в новых штаммах непрерывно возрастает (Коновалов, 2002; Мубараков, 2002). В связи с этим поиск новых эффективных микроорганизмов, содержащих высокоактивные карбоксилэстеразы с целью создания на их основе биокатализаторов, является актуальной задачей (Доронина и др., 2006). Основным источником для скрининга и селекции высокоактивных штаммов для биотрансформации и биодеградации органических соединений являются почвы естественной среды и техногенно-измененные грунты (Звягинцев, 1987; Bornscheuer, 2002, Демаков и др., 2007).
Ранее нами были селекционированы и идентифицированы культуры грамотрицательных почвенных микроорганизмов, аэробных протеобакте-рий, относящиеся главным образом к роду Pseudomonas , обладающие высокой карбоксилэстеразной активностью, определены минимальные ингибирующие концентрации эфиров спиртов в диапазоне С1–С10 и исследована эстеразная активность штаммов в отношении ряда ацетатных эфиров (Старкова, Ремезовская, 2007).
В данной работе исследуются зависимость роста и карбоксилэстеразной активности почвенных грамотрицательных бактерий рода Pseudomonas от соотношения концентраций источника углерода, азота и фосфора.
Объекты и методы исследования
Объектами исследования являются штаммы почвенных псевдомонад, выделенные из образцов подзолистой луговой и аллювиальной болотной почв, не несущих значительной антропогенной нагрузки, собранных в Нытвенском районе Пермского края с глубины 5 и 20 см от поверхности.
Для выращивания штаммов микроорганизмов, утилизирующих эфиры карбоновых кислот, была использована синтетическая среда N, имеющая следующий состав (г/л): KH 2 PO 4 – 1.0; K 2 HPO 4 × 3H 2 O – 1.6; NaCl – 0.5; MgSO 4 × 7H 2 O – 0.5; CaCl 2 – 0.005; CoCl 2 × 6H 2 O – 0.01; FeSO 4 × 7H 2 O – 0.005; pH 7.2 ± 0.2. (Максимов и др., 2003). В качестве источника азота использовали NH 4 Cl в концентрации 10 mM, источника углеводов – глюкозу в концентрации 0.1% или бутилацетат в концентрации 2–10 мМ. Ростовые субстраты асептически добавляли до конечной концентрации в автоклавированную и охлажденную до 25 ° С среду в соответствии с условиями эксперимента.
Количественное определение эстеразной активности по высвобождению р-нитрофенола из соответствующих его эфиров осуществляли с помощью фотоэлектроколориметра КФК–3 в кюветах с длиной оптического пути 0.5 см при Х =410 нм. В качестве субстрата использовали p-нитрофенил (NP)-ацетат.
25 мкл 10 мМ субстрата вносили в 2 мл среды, содержащей тестерную клеточную культуру. Реакцию проводили при температуре 22 ° С или 30 ° С (согласно условиям эксперимента) в течение 30 мин. Единица эстеразной активности (1ЕД) соответствует 1 мкмоль р-нитрофенола /мин /мг сухого веса клеток.
Результаты исследований
Зависимость роста и эстеразной активности бактерий от состава ростовой среды
Исследовали влияние сочетаний различных концентраций фосфатов и глюкозы на рост штаммов. Обнаружили, что для всех штаммов восьмикратное от 6.25 до 50 мМ изменение концентрации фосфатов (при стандартной концентрации в среде N– 25 мМ) приводит к незначительным изменениям в эффективности утилизации глюкозы в диапазоне от 0.05 до 0.5% (рис. 1). Во всех случаях плотность культуры увеличивалась пропорционально концентрации глюкозы (до 0.25%). При дальнейшем увеличении её содержания в среде накопление биомассы снижалось в разной степени в зависимости от индивидуальных биохимических характеристик изучаемых изолятов.
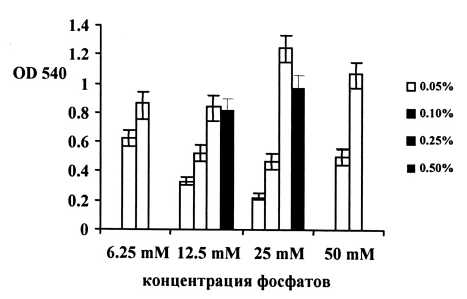
Рис. 1 . Зависимость роста штамма P. fluorescens ОН 5 от различных концентраций глюкозы и фосфатов
При изучении влияния различных сочетаний глюкозы и фосфатов в ростовой среде на эстеразную активность исследуемых культур обнаружили, что для большей их части зависимость активности от концентрации фосфатов детектируется только на низких концентрациях глюкозы (рис. 2).
Установлено, что в отличие от большинства штаммов специфическая активность штамма P. fluorescens ЛН 4 не зависит от изменения содержания глюкозы и фосфатов в широком диапазоне концентраций.
Определяли зависимость роста и активности выделенных штаммов от сочетания различных концентраций глюкозы и аммония в ростовой среде. Обнаружено, что количество вносимого источника азота незначительно оказывает влияние на плотность культуры при содержании глюкозы в среде 0.1%, притом утилизация псевдомонадами больших количеств глюкозы прямо зависела от увеличения концентрации аммония (рис. 3). При дальнейшем повышении концентрации изучаемых ростовых агентов наблюдалось снижение плотности культуры, в первую очередь, при повышении содержания глюкозы. Совместное внесение до высоких концентраций глюкозы и аммония приводило к ингибированию роста всех культур.
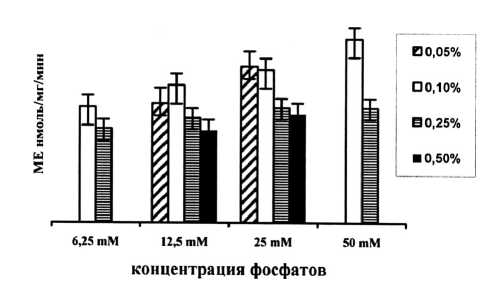
Рис. 2 . Карбоксилэстеразная активность штамма P. fluorescens ОН5 при различных концентрациях глюкозы и фосфатов
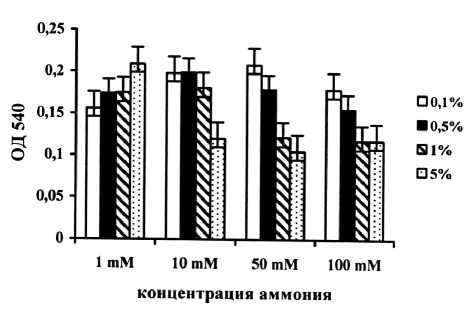
Рис. 3. Зависимость роста штамма Pseudomonas sp.ОН 1 от различных концентраций глюкозы и аммония
Показано, что эстеразная активность изучаемых штаммов не имеет линейной зависимости от концентрации источника азота в ростовой среде в широком диапазоне концентраций (рис. 4).
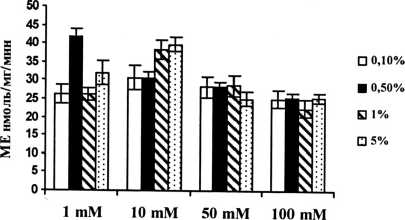
концентрация аммония
Рис. 4 . Зависимость активности штамма Pseudomonas sp. ОН 1 от различных концентраций глюкозы и аммония
Обнаружено также, что высокий уровень карбоксилэстеразной активности (более 4 мкмоль/мг/ мин), близкий к наблюдаемому на минеральной среде с глюкозой, достигается на полноценных питательных средах, таких как среда Luria-Bertani.
Полученные результаты изучения влияния источников азота, углеводов и энергии на рост и карбоксилэстеразную активность бактерий свидетельствуют о том, что синтез эстераз изучаемыми культурами имеет в большей степени конститутивный характер и не требует специфической индукции.
Зависимость роста и активности штаммов от фазы роста культуры
Для определения зависимости эстеразной активности культуры от фазы роста клетки исследуемых штаммов выращивали в течение 7 сут. на среде N разного состава (рис. 5). Измерения плотности и активности производились каждые 12 ч. Перед опытом штаммы длительно пассировали на жидкой среде LB.
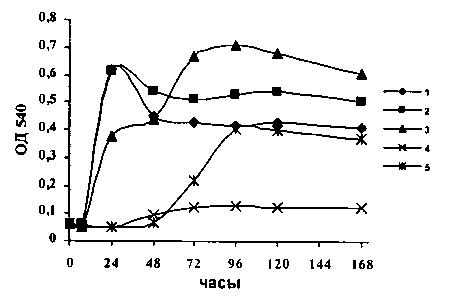
Рис. 5 . Рост штамма Ps. fluorescens ОН 6 на средах: 1 – 0.1% глюкоза; 2 – 0.1% глюкоза + 2мМ бутилацетат; 3 – 0.1% глюкоза + 10 мМ бутилацетат;
4 – бутилацетат 2 мМ; 5 – бутилацетат 10 мМ
Обнаружено, что при росте изолятов, выделенных из аллювиальной почвы, на средах, содержащих глюкозу в качестве единственного источника углерода или в сочетании с бутилацетатом, период адаптации составляет 6 ч., стадия логарифмического роста имеет протяженность не более 24 ч., и далее культура переходит в стационарную фазу. Показано, что в варианте с 10 мМ бутилацетатом лаг-фаза затягивается до 48 ч. Очевидно, что это связано с длительностью.
Как видно из представленного графика, период активного роста в варианте с 10 мМ бутилацетатом совпадает со второй зоной логарифмического роста в варианте с глюкозой и 10 мМ бутилацетатом, что свидетельствует о переключении ферментных систем с утилизации глюкозы на утилизацию бутилацетата. Бутилацетат как единственный источник углеводов не является оптимальным ростовым агентом, плотность культуры на среде с его концентрацией 2 мМ не превышает 15%, а при концентрации 10 мМ – 55–60% максимальной, детектируемой в варианте с двумя источниками углерода.
Среди штаммов, выделенных из луговой почвы, только ЛН 4 рос на средах, содержащих глюкозу. Как видно из представленных данных (рис.
6), сочетание глюкозы и бутилацетата в разных концентрациях оказывает стимулирующее влияние на ростовые процессы описываемого штамма, в то время как на средах с единственным ростовым источником наблюдается задержка стадии адаптации до 48 ч. К концу периода измерения максимальная плотность была зафиксирована в варианте с 10 мМ бутилацетатом.
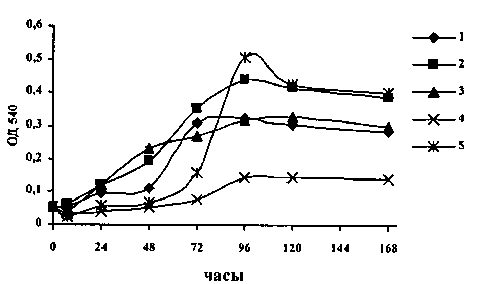
Рис. 6. Рост штамма Pseudomonas sp. ЛН 4 на средах различного состава:
1 – 0.1% глюкоза; 2 – 0.1% глюкоза + 2мМ бутилацетат; 3 – 0.1% глюкоза + 10 мМ бутилацетат;
4 – бутилацетат 2 мМ; 5 – бутилацетат 10 мМ
При изучении зависимости эстеразной активности штаммов от фазы роста культуры обнаружили, что в первые часы после переноса клеток с полной среды на минимальную наблюдается незначительное повышение активности фермента, связанное с адаптацией к новым ростовым условиям, после чего на всех штаммах во всех вариантах детектируется значительное снижение активности эстеразы.
Анализ динамики изменения ферментной активности штамма ОН 6 свидетельствует о том, что повышение активности на 48-м часу роста культуры связано, вероятно, с переходом от утилизации глюкозы к бутилацетату и экспрессией соответствующих генов. В конце периода измерения на стационарной стадии роста на всех вариантах наблюдалось повышение эстеразной активности культур, в ряде вариантов до 150% от исходного уровня, что может быть вызвано истощением ростовых агентов и активацией ферментных систем клетки в стрессовых условиях.
Сходная динамика изменения эстеразной активности наблюдается и при росте штамма ЛН 4, однако в этом случае повышение скорости конверсии маркерного субстрата детектируется только в варианте с 10 мМ бутилацетатом.
Заключение
Исходя из полученных данных о влиянии источников азота, фосфора, углеводов и энергии на рост и специфическую активность штаммов можно сделать вывод, что синтез эстераз изучаемыми культурами имеет в большей степени конститутивный характер и не требует специфической индукции. При этом увеличение концентрации глюкозы до 1%, фосфата в интервале 6.25–25 мМ и аммония в интервале 1–50 мМ стимулировало рост культуры, но приводило к лишь небольшому повышению уровня эстеразной активности. Этим изучаемые культуры отличаются от ранее исследованных продуцентов нитрилгидратаз, уровень активности которых был чувствителен к концентрации источников основных элементов (Максимов и др., 2003). Карбоксилэстеразная активность культур P. fluores-cens в оптимальных условиях достигала 10 мкмоль/мг/мин, что выше, чем у ранее описанных аналогов (Доронина и др., 2006).
Показано, что при высоких концентрациях глюкозы (5%) наблюдается угнетение роста бактерий и, у некоторых культур, понижение эстеразной активности. Таким образом, для получения высокого выхода активной биомассы могут быть использованы следующие концентрации источников углерода, азота и фосфора: глюкоза – 1%, аммоний – 50 мМ, фосфат – 25 мМ.
Работа поддержана ФЦП «Научные и научнопедагогические кадры инновационной России на 2009–2013 годы» (ГК№ 02.740.11.0078) и АВЦП «Развитие научного потенциала высшей школы (2009–2010 годы)», проект № 2.1.1.6252.
Список литературы Зависимость карбоксилэстеразной активности почвенных грамотрицательных микроорганизмов от стадии роста и состава среды
- Демаков В.А. и др. Биологическое разнообразие нитрилметаболизирующих бактерий антропогенно-измененных почв Пермского края//Экология. 2007. № 3. С. 1-6.
- Доронина Н.В. и др. Биодеградация метилацетата и этилацетата иммобилизованными клетками Pseudomonas esteropholus//Прикл. биохим. и микробиол. 2006. Т. 42, № 1. С. 52-54.
- Звягинцев Д.Г. Почва и микроорганизмы. М.: Изд-во МГУ, 1987. 256 с.
- Коновалов А.А. Разработка методов разделения рацемических эфиров с помощью гидролаз микроорганизмов: автореф. дис. канд. биол. наук. Уфа, 2002. 16 с.
- Максимов А.Ю и др. Влияние нитрилов и амидов на рост и нитрилгидратазную активность штамма Rhodococcus sp. gt1//Прикл. биохим. и микробиол. 2003. Т. 39, № 1. С. 63-68.
- Мубараков А.И. Разработка энантиоселективных биокатализаторов парциального ацилирования спиртов: автореф. дис. канд. биол. наук. Уфа, 2002. 18 с.
- Старкова М.К., Ремезовская Н.Б. Селекция грамотрицательных микроорганизмов, обладающих эстеразной активностью//Современные проблемы экологии, микробиологии и иммунологии. Екатеринбург-Пермь, 2007. С. 107-109.
- Bornscheuer U.T. Microbial carboxyl esterases: classification, properties and application in biocatalysis//FEMS Microbiology reviews. 2002. Vol. 26. P. 73-81.


