Значение полиморфизмов генов факторов VII и XIII системы свертываемости крови в патогенезе нетравматического асептического некроза головки бедренной кости
Автор: Панин Михаил Александрович, Загородний Николай Васильевич, Бойко Андрей Викторович, Самоходская Лариса Михайловна, Абакиров Медетбек Джумабекович, Волков Евгений Егорович
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.27, 2021 года.
Бесплатный доступ
Введение. Нетравматический асептический некроз головки бедренной кости - полиэтиологическое социально значимое заболевание, связанное с утратой трудоспособности в возрасте от 20 до 50 лет. Исследования в отношении выявления причин/предикторов некроза являются актуальными. Цель. Изучение вклада полиморфизмов генов факторов свертывания крови F7 и F13 в генез нетравматического асептического некроза головки бедренной кости. Материалы и методы. Изучены полиморфизмы генов системы свертывания крови F7 и F13; проведен сравнительный анализ частоты встречаемости значимых аллельных вариантов генов F7 (Arg353Gln) и F13 (Val134Leu) у пациентов с верифицированным диагнозом «асептический некроз» (основная группа) и у здоровых пациентов (контрольная группа). В основную группу вошел 41 больной (все - мужчины) с асептическим некрозом головки бедренной кости неясной этиологии. Результаты. Частота встречаемости аллелей гена Arg353Gln F7 в основной группе составила: GG - у 30 из 41 больного (73,2 %), GA - у 11 из 41 (26,8 %), причем полиморфный вариант АА не встретился ни у одного из 41 пациента. В контрольной группе частоты аллелей данного гена распределились следующим образом: GG - у 7 из 320 человек (2,2 %), GA - у 66 из 320 (20,6 %), AA - у 247 из 320 (77,2 %). Достоверные различия были выявлены нами в частотах встречаемости гомозиготных генотипов - АА (χ2 = 100,215, р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Нетравматический асептический некроз головки бедренной кости, полиморфизм генов факторов свертываемости крови, аваскулярный некроз, предикторы
Короткий адрес: https://sciup.org/142230151
IDR: 142230151 | УДК: 616.718.41-002.4-021.4:575.174.015.3 | DOI: 10.18019/1028-4427-2021-27-1-43-47
The significance of polymorphisms of gene coagulation factors VII and XIII in the pathogenesis of non-traumatic avascular necrosis of the femoral head
Introduction Non-traumatic avascular necrosis of the femoral head (ANFH) is a poly-etiologic and socially significant disease in the age of 20 to 50 years and is associated with disability. Research on the identification of necrosis causes/predictors is a relevant issue. Purpose To study the contribution of polymorphisms in the genes of coagulation factors F7 and F13 in the aetiology of non-traumatic avascular necrosis of the femoral head. Methods Polymorphisms of the genes of coagulation factors F7 and F13 were studied; comparative analysis of the frequency of important allelic variants of F7genes (Arg353Gln) and F13 (Val134Leu) in patients with a verified diagnosis of aseptic necrosis (study group) and in healthy patients (control group) was performed. The study group included 41 patients (all males) with aseptic necrosis of the femoral head of unknown etiology. Results The frequency of gene alleles in the F7 Arg353Gln in the study group were: GG in 30 out of 41 patients (73.2 %), GA in 11 out of 41 patients (26.8 %), and none of 41 patients had a polymorphic variant AA. The frequency of alleles of this type of gene in the control group was as follows: GG in 7 out of 320 subjects (2.2 %), GA in 66 out of 320 patients (20.6 %), AA in 247 out of 320 (77.2 %). Significant differences were identified in the frequencies of homozygous genotypes, AA (χ2 = 100.215, p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Значение полиморфизмов генов факторов VII и XIII системы свертываемости крови в патогенезе нетравматического асептического некроза головки бедренной кости
Нетравматический асептический некроз (НАН) головки бедренной кости – заболевание, характерное для мужчин в возрасте от 20 до 50 лет; утрата трудоспособности молодыми людьми выводит данное заболевание в разряд социально значимых [1, 2].
Среди причин НАН головки бедренной кости выделяют длительное применение кортикостероидов, злоупотребление алкоголем, системную красную волчанку, серповидноклеточную анемию, болезнь Legg-Calve-Perthes, ионизирующую радиацию, цитотоксические
агенты и др. [3, 4]. Однако известно, что некроз головки бедренной кости может наблюдаться и при отсутствии вышеупомянутых факторов - так называемый «идиопатический».
Согласно данным литературы, в основе развития НАН лежат три основных механизма: механическое препятствие току крови, тромботическая окклюзия сосудов, экстраваскулярная компрессия [5]. Правомочно придается значение взаимодействию между генетической предрасположенностью к нарушениям гемоциркуляции и внешними факторами. У многих пациентов с НАН головки бедренной кости наблюдается сочетание неблагоприятных внешних факторов риска с наследственными: гиперкоагуляция, гемоглобинопатии, нарушения ангиогенеза, оксидативный стресс [6].
Возможно предположить, что определенную роль в патогенезе НАН играют некоторые наследственные особенности (полиморфизмы) генов факторов свертываемости крови. Как известно, система гемостаза представляет собой совокупность процессов, обеспечивающих жидкое состояние крови, поддержание ее нормальной вязкости, предупреждение и остановку кровотечений. В нее входят факторы свертывающей, естественной противосвертывающей и фибринолитической систем крови. В норме все процессы находятся в определенном балансе и обеспечивают жидкое состояние крови. Смещение равновесия вследствие внутренних или внешних факторов может повышать риск кровотечений и тромбообразования.
Особое внимание при оценке риска тромбоэмболий и инфарктов уделяется генам коагуляционных (свертывающих) факторов крови VII и XIII (F7, F13), изменения в которых в большинстве случаев направлены на обеспечение защитного эффекта. Снижение активности данных факторов способствует уменьшению тром-бообразования [7, 8].
Ген F7 кодирует фактор свертывания крови VII – витамин-К-зависимый профермент, продуцирующийся в печени. Основной физиологической ролью F7 является активация фактора свертывания крови Х. После повреждения сосуда F7 связывается с тканевым фактором III и переходит в активную форму. Эта реакция является основным событием в процессе свертывания крови [9]. Изменения в гене F7 в большинстве случаев имеют протективный эффект относительно риска развития тромбоэмболии. Замена гуанина (G) на аденин (А) в позиции 10976 (генетический маркер G10976A) приводит к изменению биохимических свойств фактора VII. Снижение активности F7 в результате замены способствует уменьшению тромбообразования. Генотип АА является причиной снижения активности фермента F7 на 72 % по сравнению с диким (наиболее часто встречающимся в популяции) – генотип GG [10]. Маркер ассоциирован со снижением вероятности инфаркта миокарда, даже при наличии ангиографически задокументированного, тяжелого коронарного атеросклероза. Гетерозиготы (носители одной аллели А и одного G, генотип AG) имеют риск заболевания инфарктом миокарда в 2 раза меньший, чем носители двух аллелей G (генотип GG) [11].
Фактор XIII (F13) представляет собой плазматический гликопротеин, циркулирующий в плазме крови в комплексе с белком фибриногеном. При активации системы свертывания крови F13 подвергается расщеплению ферментом тромбином (фактором свертывания крови II). Кофактором в данной реакции являются ионы кальция. Активированный белок F13a катализирует "сшивание" мономеров фибрина, образуя связи между аминокислотами, что ведет к формированию фибрина-полимера. Фибрин – основа сгустка крови, он стабилизирует тромб, завершая процесс свертывания крови [12]. Изменения в гене F13 в большинстве случаев снижают риск развития патологий, связанных с повышенным тромбообразованием. Участок, в котором происходит замена нуклеотида гуанина (G) на тимин (Т) в позиции 103, обозначается как генетический маркер G103T. В результате замены преобразуются биохимические свойства белка F13, а именно, его способность "сшивать" фибриновые мономеры, вследствие чего фибриновые сгустки получаются более тонкими [13]. При анализе частотности аллелей (G103T) у пациентов, перенесших инфаркт миокарда, и у контрольной группы был доказан защитный эффект присутствия в генотипе аллели Т [14].
Целью настоящего исследования явилось изучение вклада полиморфизмов генов факторов свертывания крови F7 и F13 в генез нетравматического асептического некроза головки бедренной кости.
МАТЕРИАЛЫ И МЕТОДЫ
В основу исследования легло предположение о важности генетических факторов в развитии некроза головки бедренной кости. В связи с этим нами были изучены полиморфизмы генов системы свертывания крови F7 и F13, роль которых известна в генезе развития ишемических расстройств различной локализации.
В процессе исследования проведен сравнительный анализ частоты встречаемости значимых аллельных вариантов генов F7 (Arg353Gln) и F13 (Val134Leu) у пациентов с верифицированным диагнозом НАН (основная группа) и у здоровых пациентов (контрольная группа).
Нами был обследован 41 больной (все – мужчины) с НАН головки бедренной кости. В данную группу вошли пациенты с неясной причиной заболевания, которое клинически манифестировало в возрасте от 27 до 45 лет. Критериями исключения являлись алкоголизм, длительный прием кортикостероидов, системные заболевания соединительной ткани, заболевания крови и прочие известные этиологические факторы НАН [15].
Стаж заболевания варьировал от 1 до 20 лет. На момент обследования у 24 из 41 пациента основной группы 1–10 лет назад было проведено одно-, двустороннее тотальное эндопротезирование тазобедренного сустава в связи со вторичным артрозом на фоне НАН 3–4 ст. Пятнадцать пациентов с НАН головки бедренной кости 3 ст. готовятся к аналогичной операции. Два пациента (НАН 3 ст.) получают консервативное лечение в связи с отказом от хирургического вмешательства.
При анализе семейного анамнеза пациентов с НАН головки бедренной кости отмечена высокая частота сердечнососудистых заболеваний (инсульт, инфаркт, острый тромбоз) у ближайших родственников (мать/ отец) – у 61 % (25 из 41) пациентов основной группы.
Следует подчеркнуть, что у 13 больных сердечнососудистые заболевания имели место у обоих родителей, причем у 6 – с летальным исходом.
При анализе соматического статуса у 12 пациентов основной группы установлена артериальная гипертензия 1–3 ст., у 6 – варикозная болезнь вен нижних конечностей, у 3 в анамнезе – острый тромбофлебит, потребовавший хирургического вмешательства, у 3 – коагулопатии (гиперфибриногенемии), требующие перманентной медикаментозной коррекции.
В контрольную группу вошло 320 мужчин аналогичной возрастной категории (25–45 лет) – военнослужащих, обследованных при профилактических осмотрах [16]. Ни у одного из пациентов контрольной группы не было выявлено клинических проявлений заболеваний тазобедренных суставов.
В программу обследования было включено исследование полиморфизмов генов Arg353Gln F7 и Val134Leu F13 методом ПЦР. Для генетического ис- следования выполнялась экстракция геномной ДНК на сорбенте из лимфоцитов периферической цельной крови при помощи коммерческого набора «ДНК-сорб-В» («АмплиСенс», Москва).
Определение аллельных вариантов генов проводили методом ПЦР в реальном времени на амплифика-торе ДТ-96 (производитель ДНК Технология, Россия) тест-системами для ПЦР - анализа (производитель ДНК Технология, Россия) согласно рекомендациям фирмы производителя.
При статистической обработке полученных данных было проведено сравнение результатов в основной и контрольной группах. Достоверность значений определялась в программе STATISTIСА при подсчете значения р по критерию χ 2 Пирсона.
Все лица, включенные в исследование, дали письменное информированное согласие на участие в нем. Проведение исследования одобрено Этическим комитетом РУДН.
РЕЗУЛЬТАТЫ
Нами были проанализированы частоты встречаемости аллелей А и G (в гомо- и гетерозиготном состоянии) гена Arg353Gln F7 у больных НАН и у здоровых людей. Как следует из таблицы 1, наличие аллели А было выявлено у 26,8 % пациентов основной группы, что в 3,5 раза ниже, чем в контрольной (у 97,1 %), различия статистически достоверны. Присутствие в генотипе аллели G отмечено у 73,2 % пациентов с НАН и у 22,8 % человек из контрольной группы, различия также статистически достоверны (табл. 1).
Таблица 1
Наличие аллелей А и G гена Arg353Gln F7 у пациентов двух групп
|
Наличие аллели |
Основная группа (НАН, n = 41) |
Контрольная группа (n = 320) |
χ 2 |
р |
|
А (генотипы АА+GA) |
11/41 – 26,8 % |
311/320 – 97,1 % |
186,703 |
< 0,001 |
|
G (генотипы GG+GA) |
30/41 – 73,2 % |
73/320 – 22,8 % |
45,199 |
< 0,001 |
Частота встречаемости аллелей гена Arg353Gln F7 в основной группе составила: GG – у 30 из 41 больного (73,2 %), GA – у 11 из 41 (26,8 %), причем полиморфный вариант АА не встретился ни у одного из 41 пациента. В контрольной группе частоты аллелей данного гена распределились следующим образом: GG – у 7 из 320 человек (2,2) %, GA – у 66 из 320 (20,6 %, AA – у 247 из 320 (77,2 %).
Достоверные различия были выявлены нами в частотах встречаемости гомозиготных генотипов – АА ( χ 2 = 100,215, р < 0,001) и GG ( χ 2 = 205,770, р < 0,001) в основной и контрольной группах (рис. 1). В отношении гетерозиготного генотипа GA различия были не достоверны – χ 2 = 0,834, р = 0,362.
В дальнейшем нами были проанализированы частоты встречаемости различных аллельных вариантов гена Val134Leu F13.
Частота обнаружения аллели Т (генотипы TT+TG) у больных НАН составила 73,2 %, в контрольной группе – 90,0 %, различия статистически достоверны (р = 0,002). Различия в частоте встречаемости алле- ли G были еще более значимы: в основной группе – 90,2 %, в контрольной группе – 54,7 %; различия статистически достоверны – р < 0,001 (табл. 2).
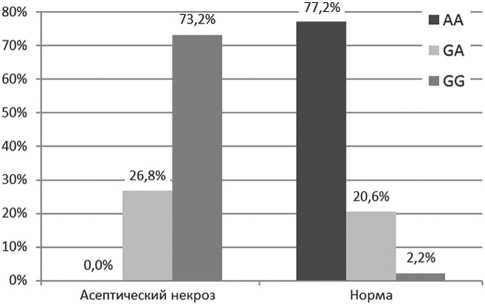
Рис. 1. Частота встречаемости аллелей гена Arg353Gln F7 у пациентов с НАН головки бедренной кости и контрольной группы
Таблица 2
Наличие аллелей Т и G гена Val134Leu F13 у пациентов двух групп
|
Наличие аллели |
Основная группа (НАН, n = 41) |
Контрольная группа (n = 320) |
χ 2 |
р |
|
Т (генотипы ТТ+ТG) |
30/41 – 73,2 % |
288/320 – 90,0 % |
9,810 |
0,002 |
|
G (генотипы GG+ТG) |
37/41 – 90,2 % |
175/320 – 54,7 % |
18,956 |
< 0,001 |
Анализ частот встречаемости различных аллельных вариантов гена Val134Leu F13 показал, что в основной группе наличие гомозиготного генотипа ТТ отмечено у 4 из 41 пациента (9,8 %), гетерозиготного генотипа GT – у 26 из 41 (63,4 %), гомозиготного генотипа GG – у 11 из 41 (26,8 %). В контрольной группе частоты встречаемости аналогичных генотипов составили соответственно: 45,3 % (у 145 из 320), 45,0 % (у 144 из 320) и 9,7 % (у 31 из 320) (рис. 2).
Генотип GG в 2,8 раза чаще отмечен у пациентов основной группы, различия статистически достоверны (26,8 % против 9,7 %, χ 2 = 10,388, р = 0,002).
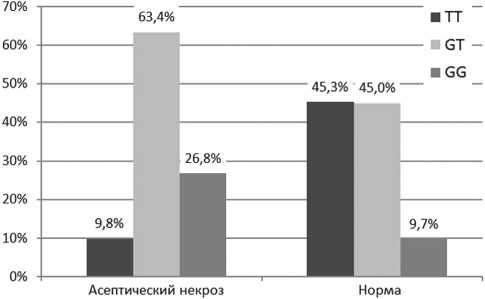
Рис. 2. Частоты встречаемости аллельных вариантов гена Val134Leu F13 у пациентов основной и контрольной групп
С учетом данных литературы о протективной роли аллели Т в развитии ишемических расстройств нами были проанализированы частоты встречаемости данной аллели в исследуемых группах.
Наличие генотипа ТТ гена Val134Leu F13 почти в 5 раз чаще ( χ 2 = 18,956, р < 0,001) выявлялось у здоровых людей (контрольная группа). Различия в частоте встречаемости аллели Т в гомо- и гетерозиготной комбинациях (ТТ и GT) в основной и контрольной группе оказались также статистически достоверными (72,7 % против 90,1 % соответственно, χ 2 = 4,946, р = 0,027). Учитывая разницу в степенях достоверности (р < 0,001 против р = 0,027), можно заключить, что ключевую про-тективную роль в развитии асептического некроза головки бедра играет только гомозиготный генотип ТТ.
ДИСКУССИЯ
В результате исследования установлены возможные причины так называемого идиопатического некроза головки бедренной кости. Показано, что риск развития НАН повышен при определенных полиморфизмах генов факторов свертываемости крови F7 и F13.
Полученные нами данные позволяют предположить, что наличие аллели G гена Arg353Gln F7 может рассматриваться как один из факторов риска развития асептического некроза головки бедренной кости. Повышенная более чем в 30 раз (по сравнению с контрольной группой) частота встречаемости гомозиготного генотипа GG гена Arg353Gln F7 у больных асептическим некрозом головки бедренной кости, вероятно, свидетельствует о высокой значимости нарушений системы свертывания крови в генезе данного заболевания.
На универсальный характер ишемических расстройств в организме человека указывают результаты исследования M. Ramzia с соавт., которые выявили двукратное повышение риска инфаркта миокарда у носителей гомозиготной аллели GG гена Arg353Gln F7 [17].
В то же время нами установлено, что наличие аллели А гена Arg353Gln F7 в 3,5 раза чаще выявлялось в контрольной группе. Это указывает на ее протективную роль в отношении развития НАН. Известно, что генотип АА является причиной снижения активности фермента F7 на 72 % и ассоциирован со снижением вероятности инфаркта миокарда даже при наличии тяжелого коронарного атеросклероза. [10]. В отношении генотипа АА гена Arg353Gln F7 важно отметить, что его наличие не выявлено нами ни у одного из пациентов основной группы. В литературе есть указания на протективную роль данной аллели в отношении инфаркта миокарда и ишемического инсульта [11], что указывает на сходные элементы патогенеза «больших сосудистых катастроф» и НАН.
При анализе полиморфизмов гена Val134Leu F13 нами установлено, что аллельный полиморфизм GG можно рассматривать в качестве одного из факторов риска НАН: частоты встречаемости данного полиморфизма были достоверно различны в основной и контрольной группах ( χ 2 = 10,388, р = 0,002). Литературных данных, указывающих на неблагоприятную прогностическую роль генотипа GG гена Val134Leu F13 в генезе ишемических расстройств, нами не обнаружено.
Генотип ТТ гена Val134Leu F13 почти в 5 раз чаще встречался у здоровых людей, чем у пациентов с НАН. Различия в частоте встречаемости аллели Т в гомо- и гетерозиготной комбинациях (ТТ и GT) в основной и контрольной группе оказались также статистически достоверными (72,7 % против 90,1 % соответственно, χ 2 = 4,946, р = 0,027). Учитывая разницу в степенях достоверности (р < 0,001 против р = 0,027), можно заключить, что ключевую протективную роль в развитии асептического некроза головки бедра играет гомозиготный генотип ТТ. На низкую частоту встречаемости аллели T гена Val134Leu F13 в группе пациентов с инфарктом миокарда по сравнению с контрольной группой указывают Kreutz R. с соавт. [18], что подтверждает “коагулопатический” генез так называемого идиопатического некроза головки бедренной кости.
Гомозиготный генотип GG гена Val134Leu F13 в 2,8 раза чаще встречался у больных с НАН (26,8 % в основной группе против 9,7 % в контрольной, р = 0,002). Возможны различные варианты трактовки полученных данных. В связи относительно низкой (менее одной трети) частотой встречаемости генотипа GG в основной группе трудно утверждать, что наличие генотипа GG – самостоятельный фактор риска НАН; возможно, имеет значение не наличие генотипа GG, а отсутствие аллели Т в генотипе.
ВЫВОДЫ
Таким образом, проведенное нами исследование показало, что полиморфизмы генов факторов свертывания крови F7 и F13 вно сят существенный вклад в генез нетравматического асептического некроза головки бедренной кости. Показано, что фак- тором риска развития НАН является гомозиготный генотип GG гена Arg353Gln F7. Низкая вероятность заболевания НАН обусловлена протективной ролью генотипа АА гена Arg353Gln F7 и генотипа ТТ гена Val134Leu F13.
При выполнении данной работы конфликта интересов не было. Финансирование из внешних источников не привлекалось.
Список литературы Значение полиморфизмов генов факторов VII и XIII системы свертываемости крови в патогенезе нетравматического асептического некроза головки бедренной кости
- Shannon B.D., Trousdale R.T. Femoral osteotomies for avascular necrosis of the femoral head // Clin. Orthop. Relat. Res. 2004. No 418. P. 34-40. DOI: 10.1097/00003086-200401000-00007.
- Expert Panel on Musculoskeletal Imaging. Avascular necrosis of the hip / A.A. DeSmet, M.K. Dalinka, N.P. Alazraki, R.H. Daffner, G.Y. El-Khoury, J.B. Kneeland et al. // American College of Radiology (ACR), Reston (VA), 2005. URL: http://www.guidelines.gov/summary/summary.aspx? doc_ id=8296&nbr=004628&string=avascular+AND+necrosis.
- Systematic analysis of classification systems for osteonecrosis of the femoral head / M.A. Mont, G.A. Marulanda, L.C. Jones, K.J. Saleh, N. Gordon, D.S. Hungerford, M.E. Steinberg // I. Bone Joint Surg. Am. 2006. Vol. 88, No 3. P. 16-26. DOI: 10.2106/JBJS.F.00457.
- Современный взгляд на патогенез нетравматического остеонекроза / М.А. Панин, Н.В. Загородний, Н.Н. Карчебный, И.А. Садков, А.С. Пе-тросян, А.Р. Закирова // Вестник травматологии и ортопедии имени Н.Н. Приорова. 2017. № 2. С. 69-75.
- Procoagulants and osteonecrosis / L.C. Jones, M.A. Mont, T.B. Le, M. Petri, D.S. Hungerford, P. Wang, C.J. Glueck // J. Rheumatol. 2003. Vol. 30, No 4. P. 783-791.
- Association between the T-786C eNOS polymorphism and idiopathic osteonecrosis of the head of the femur / C.J. Glueck, R.A. Freiberg, J. Oghene, R.N. Fontaine, P. Wang // J. Bone Joint Surg. Am. 2007. Vol. 89, No 11. P. 2460-2468. DOI: 10.2106/JBJS.F.01421.
- Di Minno G., Grandone E., Margaglione M. Clinical relevance of polymorphic markers of arterial thrombosis // Thromb. Haemost. 1997. Vol. 78, No 1. P. 462-466.
- Grant P.J. Polymorphisms of coagulation/fibrinolysis genes: gene environment interactions and vascular risk // Prostaglandins Leukot. Essent. Fatty Acids. 1997. Vol. 57, No 4-5. P. 473-477. DOI: 10.1016/s0952-3278(97)90431-2.
- Кузник Б.И. Система гемостаза // Физиология человека. 2000. № 1. С. 313-325.
- Golino P. The inhibitors of the tissue factor: factor VII pathway // Thromb. Res. 2002. Vol. 106, No 3. P. V257-V265. DOI: 10.1016/s0049-3848(02)00079-8.
- Polymorphisms of the coagulation factor VII gene and its plasma levels in relation to acute cerebral infarction differences in allelic frequencies between Chinese Han and European populations / W.Y. Kang, H.L. Wang, L.F. Xiong, X.F. Wang, H.Y. Chu, B. Qu, X.F. Liu, J. Yin, B.H. Duan, Z.Y. Wang // Chin. Med. J. (Engl). 2004. Vol. 117, No 1. P. 71-74.
- Komaromi I., Bagoly Z., Muszbek L. Factor XIII: novel structural and functional aspects // J. Thromb. Haemost. 2011. Vol. 9, No 1. P. 9-20. DOI: 10.1111/j.1538-7836.2010.04070.x.
- Muszbek L., Ariëns R.A., Ichinose A. ISTH SSC Subcommittee on Factor XIII. Factor XIII: recommended terms and abbreviation // J. Thromb. Haemost. 2007. Vol. 5, No 1. P. 181-183. DOI: 10.1111/j.1538-7836.2006.02182.x.
- Impact of FXIII-A Val34Leu polymorphism on coronary artery disease in Croatian patients / A. Bronic, G. Ferencak, R. Zadro, A. Stavljenic-Rukavina, R. Bernat // Mol. Biol. Rep. 2009. Vol. 36, No 1. P. 1-5. DOI: 10.1007/s11033-007-9144-9.
- Avascular Necrosis of Femoral Head: A Metabolomic, Biophysical, Biochemical, Electron Microscopic and Histopathological Characterization / A. Narayanan, P. Khanchandani, R.M. Borkar, C.R. Ambati, A. Roy, X. Han, R.N. Bhoskar, S. Ragampeta, F. Gannon, V. Mysorekar, B. Karanam, V. Sai Muthukumar, V. Sivaramakrishnan // Sci. Rep. 2017. Vol. 7, No 1. P. 10721. DOI: 10.1038/s41598-017-10817-w.
- Прогностическая значимость носительства аллельных вариантов генов, контролирующих систему гемостаза, и их сочетания с традиционными факторами риска в раннем развитии ишемической болезни сердца / Е.Ю. Андреенко, Л.М. Самоходская, А.В. Балацкий, П.И. Мака-ревич, С.А. Бойцов // Кардиоваскулярная терапия и профилактика. 2011. Т. 10, № 8. С. 32-39.
- Coagulation factor VII gene polymorphisms and cardiovascular diseases in Iranian population / M. Ramzi, N. Cohan, M. Yavarian, M.R. Jahromi // J. Indian College of Cardiology. 2013. Vol. 3, No 1. P. 6-8. DOI: 10.1016/j.jicc.2012.12.004.
- Factor XIII Val34Leu polymorphism and recurrent myocardial infarction in patients with coronary artery disease / R.P. Kreutz, A. Bitar, J. Owens, Z. Desta, J.A. Breall, E. von der Lohe, A. Sinha, M. Vatta, P. Nystrom, Y. Jin, D.A. Flockhart // J. Thromb. Thrombolysis. 2014. Vol. 38, No 3. P. 380-387. DOI: 10.1007/s11239-014-1059-4.


