Значение шкалы RIFLE в выборе программы экстракорпоральной детоксикации у больных с тяжелым острым панкреатитом
Автор: Подкорытова О.Л., Ветшева М.С., Вторенко В.И.
Журнал: Московский хирургический журнал @mossj
Статья в выпуске: 1 (35), 2014 года.
Бесплатный доступ
Острый панкреатит (ОП) остается одним из самых распространенных хирургических заболеваний. При развитии синдрома полиорганной недостаточности (СПОН) летальность при ОП достигает 25-80%, по данным разных авторов. Наиболее грозным осложнением в структуре СПОН является острая почечная недостаточность (ОПН), которая в разы утяжеляет состояние больного и прогноз заболевания. В последнее время для диагностики и оценки тяжести почечного повреждения используется шкала RIFLE, имеющая 4 стадии: риск (Risk), повреждение (Iinjury), недостаточность (Failure), потеря (Loss), стойкая потеря функции (End stage renal disease). Наиболее тяжелой является стадия - недостаточность (Failure), при которой отмечается повышение уровня креатинина в плазме крови в 3 раза по сравнению с исходным, что делает применение методов ЗПТ у данной категории больных обязательным. Данный метод лечения позволяет как замещать функцию почки, так и элиминировать провоспалительные цитокины, продукты метаболизма и различные биологически активные вещества. Применение методов зПТ в комплексной терапии ОП позволяет снизить летальность у данной группы больных.
Острый панкреатит, синдром системного воспалительного ответа, полиорганная недостаточность, острая почечная недостаточность, заместительная почечная терапия
Короткий адрес: https://sciup.org/142211132
IDR: 142211132 | УДК: 616.61;
Текст научной статьи Значение шкалы RIFLE в выборе программы экстракорпоральной детоксикации у больных с тяжелым острым панкреатитом
Несмотря на прогресс в хирургии за последнее десятилетие острый панкреатит (ОП) продолжает оставаться наиболее распространенным хирургическим заболеванием. Рост заболеваемости ОП может быть обусловлен, с одной стороны улучшением диагностических возможностей, однако не последнюю роль в развитии ОП играет увеличение провоцирующих факторов, таких как грубые нарушения диеты и употребление алкогольных напитков [1].
Наиболее тяжелой формой ОП является панкреоне-кроз, сопровождающийся развитием системного воспалительного ответа (ССВО) с синдромом полиорганной недостаточности (СПОН). Данная форма ОП рассматривается как тяжелый острый панкреатит (ТОП), смертность при котором, по данным различных авторов, достигает от 25 до 75 % [2–7]. Особое место в структуре СПОН занимает острая почечная недостаточность (ОПН), значительно ухудшающая состояние больного и прогноз. Основную роль в патогенезе ОПН при ТОП отводят развитию тяжелой ишемии на фоне гиповолемии и массивному выбросу медиаторов воспаления в ходе прогрессирования заболевания [8–10]. При возникновении у больного ОПН для дальнейшей тактики лечения важно определить степень поражения почек. Для этого, например, в интенсивной те- рапии пациентов нефрологического профиля активно используется шкала оценки функции почек RIFLE. Однако в отделениях общей реанимации эта шкала не столь активно применяется для оценки вклада ОПН в структуре СПОН. Шкала RIFLE образованна первыми буквами каждой из последовательно выделенных стадий острого почечного повреждения (ОПП): риск (Risk), повреждение (Iinjury), недостаточность (Failure), потеря (Loss), стойкая потеря функции (End stage renal disease) [11, 12]. Наиболее тяжелой является стадия – недостаточность (Failure), при которой отмечается повышение уровня креатинина в плазме крови в 3 раза по сравнению с исходным, снижение клубочковой фильтрации (КФ) больше чем на 75%, снижение диуреза ниже 0,35 мл/кг/ч в течение 24 часов, или развитие анурии в течение 12 часов.
Цель работы
Целью настоящей работы является: оценка эффекта экстракорпоральной детоксикации (ЭКД) в комплексном лечении ТОП, протекающего с синдромами системного воспалительного ответа и полиорганной недостаточности с острым почечным повреждением (ОПП) в стадии «недостаточность» по шкале RIFLE (RIFLE-F).
Материалы и методы
Выполнен ретроспективный анализ, проанализированы истории болезни 36 больных с ТОП, осложненным развитием ОПН с потерей функции почек по шкале RIFLE-Failure (RIFLE-F). В исследование вошли 7 женщин и 29 мужчин, в возрасте от 21 до 69 лет (в среднем 44,7±16,4), проходивших лечение в отделении реанимации и интенсивной терапии ГКБ № 52 за период 01.01.2000 по 31.12.2011 гг.
При поступлении в ОРИТ перед началом лечения, включающего в себя ЭКД – заместительную почечную терапию (ЗПТ) и в процессе самого лечения всем больным с ТОП проводилось комплексное клинико-лабораторное и инструментальное обследование и лапароскопическая диагностика, по совокупности полученных данных устанавливался диагноз ТОП. Данные о характере основного заболевания, вызвавшего сепсис/ССВО, осложнившегося СПОН с ОПН, представлены в табл. 1. Как видно из табл. 1, у всех больных был тяжелый острый панкреатит, причем преобладали пациенты с ТОП в фазе ферментативного перитонита с ССВО (73% от общего числа больных с панкреатитом). При выполнении санационно-диагностической лапароскопии всем пациентам проводилось дренирование брюшной полости (в 100% случаев). У 27% от общего числа больных развивались гнойно-септические осложнения: флегмона и/или абсцесс забрюшинной клетчатки, абсцесс сальниковой сумки, что потребовало проведения лапаротомии с санацией и дренированием очага инфекции. За время лечения в ОРИТ 8 больным из 10 с гнойно-септическими осложнениями была проведена санационная релапаротомия. Следует отметить, что выполнение лапаротомии и релапаротомии выполнено пациентам на фоне проведения ЗПТ.
-
60,7% пациентов имели сопутствующие заболевания, структура которых представлена в табл. 2. Из них у 30% – наблюдалось более двух сопутствующих заболеваний в той или иной степени тяжести, что вносило свой вклад в тана-тогенез ТОП (табл. 2).
В течение всего лечения в ОРИТ проводился ежедневный мониторинг клинико-лабораторных показателей и при необходимости инструментальные методы обследования. Для объективной оценки тяжести состояния пациентов и
Таблица 1
Распределение пациентов в зависимости от характера основного заболевания, вызвавшего СПОН и ССВО/сепсис
|
Диагноз основного заболевания |
Количество больных |
|
|
Абсолютное значение |
% |
|
|
ТОП, ферментативный перитонит |
26 |
73 |
|
ТОП, гнойно-септические осложнения |
10 |
27 |
|
ВСЕГО |
36 |
100 |
Таблица 2
Распределение больных по сопутствующей патологии
В таблице 3 представлены основные клинико-лабораторные показатели пациентов на момент начала ЗПТ. Как видно из табл. 3, у всех пациентов имелась полиорганная недостаточность с числом пораженных органов от 2 до 5, в среднем 3,7± 0,94. Отличительной особенностью данной
Таблица 3
Основные клинико-лабораторные характеристики у больных с ТОП, распределенных по шкале RIFLE-F
Синдром системного воспаления проявлялся лейкоцитозом от 17200 до 35000, либо лейкопенией – 3500, лихорадкой 38,0оС и выше, гипоальбуминемией 26 г/л и ниже, высоким уровенем С-реактивного белка (СРБ) – 96,4–129 нг/мл. У 55% больных в данной группе отмечено развитие острого респираторного дистресс-синдрома (ОРДС), в связи с чем они нуждались в респираторной поддержке. У 33,3% пациентов потребовалось проведение инотропной поддержки.
Всем больным проводилась ЭКД с использованием различных режимов. Длительность болезни к началу ЭКД находилась в диапазоне от 1 до 10 суток (4,2±2,7). Как следует из табл. 4, ЭКД применялась в виде постоянной заместительной почечной терапии (ПЗПТ) – низкопоточной веновенозной гемофильтации/гемодиафильтрации (ПВВГФ\ ПВВГДФ) – 26 больных (72,2%), а у 10 больных (27,7%), в виде интермиттирующей гемодиафильтрации (иГДФ).
Как известно, иГДФ основана на диффузионном и конвекционном способе массопереноса, с потоком диализата (300–500 мл/мин – высокопоточный), выполняется на аппарате «искусственная почка» (АИП) в любом временном интервале от 4-х до 6-ти часов. Имеющийся режим замещения (конвекция) осуществляется on line АИП и не требует специализированных растворов. Десяти пациентам процедура проводилась ежедневно на АИП «Fresenius 4008S» в режиме on line по 4–6 часов, при скорости кровотока 150–250 мл/мин и потока диализата 300–500 мл/мин, с объемами замещения за процедуру 10–26 л. Скорость замещения (доза диализа) составляла 20–70 мл/кг/ч. Процедуры
Распределение больных по видам ЗПТ
Таблица 4
Процедуры продленной низкопоточной ЗПТ (ПЗПТ) – продленная вено-венозная гемофильтрация (ПВВГ) и продленная вено-венозная гемодиафильтрация (ПВВГДФ) проводились 26 больным на аппаратах для острого диализа «Prisma» или «Аквариус».
Различие между использованными методами ЗПТ состояло в том, что при ПВВГ основным компонентом детоксикации является конвекция («доза диализа»), позволяющая удалять средне молекулярные вещества, различного рода цитокины, тогда как при ПВВГДФ к конвекционному компоненту добавляется диффузионная составляющая, направленная на удаление низкомолекулярных веществ, таких как мочевина, креатинин, фосфаты и выравнивание КОС плазмы крови в низкопоточном режиме (скорость потока диализата в разы меньше, чем при иЗПТ). При любом используемом методе ЗПТ проводилась коррекция гипергидратации (ультрафильтрация). При поведении процедуры были использованы современные расходные материалы и замещающие растворы.
В качестве антикоагулянта, как правило, использовался нефракционированный гепарин, вводимый линейно из расчета 5–10 Ед/кг/час. В некоторых случаях применялись низкомолекулярные гепарины. У пациентов с явлениями ДВС-синдрома или с высоким риском кровотечения процедуры проходили без применения гепарина, либо гепарин использовался только на промывание контура.
В качестве сосудистого доступа использовались 2–3ходовые центральные венозные катетеры диаметром 11,5– 12 Fr., установленные в центральную вену (внутренняя яремная, подключичная, бедренная).
У всех больных на всех этапах лечения проводился непрерывный мониторинг гемодинамики и газообмена, тяжесть состояния по шкалам APACHE II, Глазго, а также уровня в крови креатинина, билирубина, аминотрансфераз, амилазы, альбумина, С-реактивного белка (СРБ). Результаты лечения оценивались по выживаемости/летальности суммарно во всей группе больных, а также раздельно в подгруппах по характеру и режиму ЗПТ. При этом для оценки эффективности терапии показатели летальности сопоставляли с ожидаемой летальностью по шкале SAPS II и с учетом шкалы RIFLE.
Статистический метод
Данные представлены как среднее и стандартное отклонение для нормального распределения, для распределения, отличного от нормального. Значимость различий для количественных переменных между группами оценивалась по критерию Манна–Уитни и Краскела–Уоллиса, для кате- гориальных – по критерию χ2 или точному двустороннему критерию Фишера. Выживаемость оценивалась методом Каплана–Майера с оценкой достоверности различий по logrank тесту. Значимыми считались различия при р<0,05. Статистическая обработка выполнена с использованием пакета SPSS 13.0 (SPSS Inc., Chicago).
Результаты и обсуждение
Летальность в целом в группе больных с RIFLE-F составила 50% (18 из 36 больных), тогда как ожидаемая летальность, исходя из расчетного балла по шкале SAPS II, в прослеженной группе больных равнялась 63,5%, что на 13,5% ниже полученной у наших пациентов. Как видно из рис. 1, выживаемость к 28 суткам в подгруппах больных, разделенных по видам ЗПТ (интермиттирующая ЗПТ и продленная ЗПТ), составила также 50% в каждой подгруппе. Отсутствие разницы в исходах лечения у пациентов с RIFLE-F в зависимости от вида ЗПТ дало основание не разделять их по видам ЗПТ для дальнейшего анализа материала.
Выживаем ос і ь больных по Каплан-Майеру
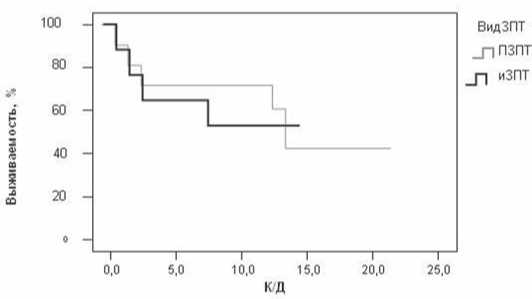
Рис. 1. Выживаемость в зависимости от вида ЗПТ у больных с ТОП и ОПП в стадии RIFLE-F по Каплан-Майеру
Данные литературы подтверждают полученные нами данные и выводы, что именно для пациентов с RIFLE-F вид ЗПТ не имеет доминирующего значения. В таблице 5 представлены основные клинические и лабораторные показатели пациентов на начало лечения, динамика в конце ЗПТ и их различие в группе умерших и выживших.
До начала ЗПТ в гр. 1 и гр. 2 существенных различий не выявлено (средний возраст выживших 43,0±17 года, умерших 46±15 лет).
Влияние на процент летальности оказывает начало проведение ЗПТ, так как у пациентов с ЗПТ с 3–4 суток отмечено некоторое снижение летальности в сравнении с пациентами, которым ЗПТ проводилось с 5-х суток. Несмотря на отсутствие статистической значимости полученных результатов, отмечена тенденция к уменьшению риска летального исхода в случае более раннего начала ЗПТ.
На момент начала ЗПТ так же не было больших различий в потребности инотропной поддержки и ИВЛ между выжившими и умершими – 28% и 22%, 33% и 28% соответственно. Однако имелась разница в показателях САД, умершие пациенты имели исходно более нестабильную гемодинамику (САД – 71,8±2,8 мм рт. ст.), в отличие от выживших (САД – 97,8±2,1 мм рт. ст.). В обеих подгруппах у больных отмечались высокие баллы по шкалам APACHE II (27,9±4,0 и 28,6±4,1), SAPS II (52,3±16 и 56±12) и низкие баллы по Глазго (10±2,0 и 10±3,3). Одинаково высокими были и показатели амилазы, в начале лечения – 958±863 (3-2456) у выживших и 535±690 (4–2190) у умерших. Также повышены и маркеры системного воспаления – снижен уровень альбумина и в десятки раз повышен СРБ.
В обеих подгруппах резко снижена функция почек – креатинин плазмы повышен до 710±150 с благополучным исходом и 670±148 мкмоль/л у умерших. У всех имел место сниженный темп диуреза – ниже 0,35 мл/кг/ч в течение суток или анурия в течение 12 часов.
Учитывая тяжелую степень повреждения почек – RIFLE-F, с момента поступления больных в ОРИТ, наряду с комплексным лечением панкреонекроза, начиналось проведение ЗПТ как по почечным, так и внепочечным показаниям – выраженный интоксикационный синдром, тяжелая токсическая энцефалопатия.
ЗПТ проводилось в различных режимах и с различной дозой диализа от 20 до 70 мл/кг/час, что имело случайный характер (ретроспективный анализ историй болезни).
Динамика основных мониторируемых показателей гомеостаза в группе умерших и выживших пациентов значительно отличалась. В ходе лечения с применением ЗПТ у выживших пациентов (гр. № 3) отмечено снижение тяжести состояния по шкалам APACHE II с 28 до 23,5 баллов и увеличение баллов по шкале Глазго с 10 до 13, также характерны изменения гемодинамических показателей, например повышение САД, снижалась потребность в инотропной поддержки (у 50% больных). В подгруппе №4 (умершие больные после ЗПТ) наоборот нарастала гемодинамическая нестабильность и отрицательная динамика со стороны ЦНС. В обеих группах больных (гр. № 3 и гр. № 4) отмечено значительно снижение уровня амилазы плазмы крови с 353 до 140 Ед/л и нормализация показателей билирубина плазмы крови. При этом на фоне ЗПТ отмечено снижение уровня воспалительных маркеров, таких как СРБ и повышение уровня альбумина в гр. № 3, повышение СРБ и снижение уровня альбумина в гр. № 4, что представлено на рис. 2, 3. Динамика ОПП на фоне комплексной терапии ТОП с использованием ЗПТ представлена на рис. 4. На рис. 4 представлены весьма интересные данные, полученные при анализе динамики показателей функции почек в ходе ЗПТ у пациентов 3 и 4 группы. На фоне комплексного лечения ТОП, включающего в себя ЗПТ, в группе № 3 отмечено полное восстановление функции почек к моменту перевода их из ОРИТ, у пациентов 4-ой группы в процессе
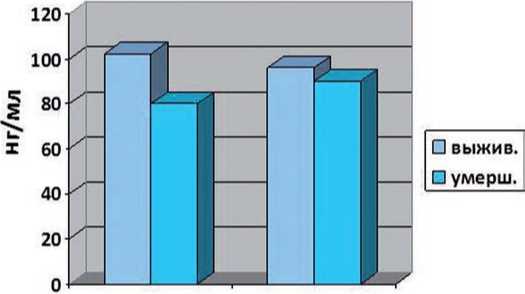
СРБ. До СРБ.после
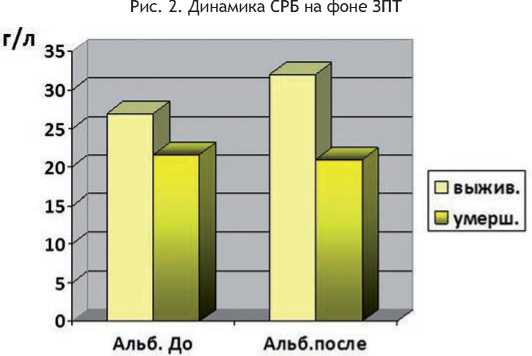
Рис. 3. Динамика альбумина на фоне ЗПТ
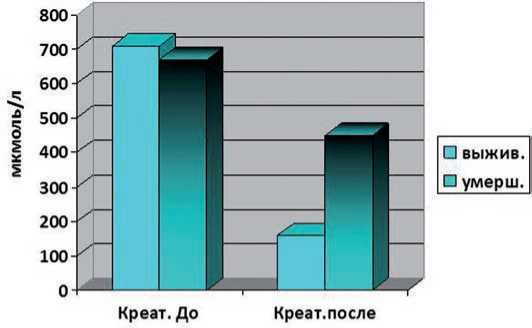
Рис. 4. Динамика ОПП на фоне ЗПТ лечения отмечено медленное и весьма умеренное снижение азотистых шлаков, без видимого улучшения КФ и уровня почасового диуреза (р≤0,05).
Поскольку при проведении ЗПТ использованы разные дозы диализа, проведен анализ летальности в зависимости от используемой дозы диализа. Многофакторный анализ продемонстрировал, что на прогноз ТОП оказывает влия- ние скорость объема замещения (доза конвекции) с пороговым уровнем 35 мл/кг/ч (р≤0,05), и он не зависит от других исследуемых факторов. Доминирующее значение выбора скорости объема замещения в исходе болезни приведены в таблице 5, в подгруппе выживших среднее значение этого показателя составляла 44,5±8,3, а в подгруппе умерших – 30,0±12,6 (р≤0,05). Летальность больных в зависимости от используемой дозы диализа также представлены на рис. 5. Как показано на рис. 5, у пациентов получавших ЗПТ со скоростью объема замещения 25 мл/кг/ч, летальность оказалась выше, чем у больных, которым использовалась скорость объема замещения >35 мл/кг/ч. В подгруппе больных с дозой конвекции 35мл/кг/ч умерло 6 из 24 больных, а в подгруппе больных, у которых она не превышала 25 мл/кг/ч, умерших оказалось 12 из 14 .
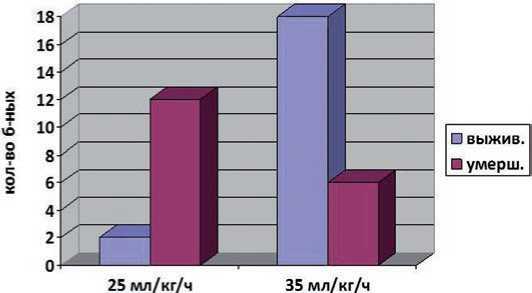
Рис. 5. Летальность в зависимости от дозы диализа
В настоящее время в зарубежной литературе опубликовано лишь небольшое число работ, посвященных применению ЗПТ при ТОП, все они относятся к периоду 2003– 2008 гг., многие из них носят экспериментальный характер [13–16]. Авторы данных работ полагают, что применение экстракорпоральной детоксикации может способствовать удалению медиаторов воспаления и провоспалительных цитокинов, массивный выброс которых в системную циркуляцию происходит при ТОП [9, 17, 18]. Однако имеются многочисленные работы по сравнению иЗПТ и ПЗПТ при лечении ОПН в рамках СПОН у больных, находящихся в критическом состоянии, результаты которых нельзя считать однозначными как в пользу иЗПТ, так и ПЗПТ [19–21]. Наше исследование также не выявило значительной разницы в видах ЗПТ, летальность/выживаемость в подгруппах иЗПТ и ПЗПТ.
Специального внимания заслуживают данные последних лет о значении дозы диализа, оцениваемой по скорости объема замещающего раствора в мл/кг массы тела/час [22, 23]. Ronco С. и соавторы еще в 2000 году продемонстрировали тесную связь между дозой диализа и выживаемостью больных с ОПН как при сепсисе (не было больных с ТОП), так и ОПН несептического генеза. При этом в случаях сеп-
Распределение больных по исходу заболевания
|
Показатели |
До начала ЗПТ |
после ЗПТ |
Р ≤ 0,05 |
||
|
Выжив. (Гр. №1) |
Умер. (Гр. №2) |
Выжив. (Гр. №3) |
Умер. (Гр. №4) |
||
|
n=18 |
n=18 |
||||
|
Возраст |
43±17 |
46±15 |
|||
|
Длит.б-ни до ЗПТ |
3,8±2,2 |
4,7±3,2 |
|||
|
APACHE II, б |
27,9±4 |
28,6±4,1 |
23,5±2,5 |
29,3±3,3 |
|
|
SAPS II,б |
52,3±16 |
56±12 |
47,5±7 |
58±8,3 |
|
|
GCS, б |
10±2 |
10±3,3 |
13±1,2 |
9±2,3 |
|
|
САД , мм.рт.ст |
97,8±2,1 |
71,8±2,8 |
105±2,5 |
80,4±2,6 |
|
|
ИВЛ |
22% |
28% |
17% |
28% |
|
|
Инотр.поддер. |
28% |
33% |
28% |
39% |
|
|
Бил., мкмоль/л |
46±7,8 |
69±10,2 |
24±5,6 |
53±7,7 |
* |
|
АМИЛАЗА, Ед/л |
958±863 (3–2456) |
535±690 (4–2190) |
169±105 (38–379) |
211±212 (13–540) |
* |
|
АЛЬБ., г/л |
27±5,2 |
21,6±3,5 |
32±3,3 |
21,0±2,1 |
* |
|
Креатинин, мколь/л |
710±150 |
670±148 |
160±70 |
450±150 |
** |
|
СРБ нг/мл |
102±21 |
80±32 |
96,4±15 |
90±25 |
|
|
Доза конвекции, мл/кг/час |
44,5±8,3 |
30,0±12,6 |
** |
||
сиса лучшая выживаемость выявлялась при скорости объема замещения 45 мл/кг/ч и более [24].
Наши наблюдения полностью согласуются с этими данными. Исход болезни и, соответственно, эффект от применения ЗПТ тесно коррелировал с дозой диализа. Пороговым значением, которой, по нашим данным, была доза конвекции не менее 35 мл/кг/час. Применение именно такого режима ЗПТ позволило добиться снижения летальности у наиболее тяжелой категории больных с ТОП, осложненной ОПН в стадии RIFLE-F. Причем показатели летальности и прогноза, рассчитанные по APACHE II и SAPS II у наших больных, оказались более высокими. В отличие от других авторов, в качестве ЗПТ в комплексном лечении ТОП мы использовали как ПЗПТ, так и иГДФ. При этом различий в эффективности обоих вариантов ЗПТ мы не выявили.
Заключение
Таким образом, на основании проведенного анализа историй болезни пациентов с ТОП, осложненным развитием ОПН в стадии RIFLE-F, потребовавшей применения в комплексной терапии ТОП методов ЗПТ, можно сделать следующие выводы:
-
1. Применение методов ЗПТ в комплексном лечении данной категории больных с ТОП являлось неотъемлемой составляющей терапии, при отсутствии которой летальность могла составить около 100% вследствие тяжелого повреждения почек.
-
3. Заместительная почечная терапия может быть с успехом применена в комплексном лечении тяжелого острого панкреатита, осложненного синдромом системного воспалительного ответа и полиорганной недостаточностью, при условии обеспечения дозы конвекции не менее 35 мл/кг/ч, ведущей к значительному снижению летальности у пациентов с ОПП-RIFLE-F.
-
4. Более ранняя ЗПТ в структуре комплексной терапии ТОП может привести к улучшению результатов лечения этой тяжелой категории больных.
Таблица 5 2. Выбор методов ЗПТ не оказывает существенного влияние на выживаемость пациентов в исследуемой группе больных (RIFLE-F).
Список литературы Значение шкалы RIFLE в выборе программы экстракорпоральной детоксикации у больных с тяжелым острым панкреатитом
- Andrew Kingsnorth. Acute pancreatitis//BMJ. 2006, May 6. Vol. 332(7549). P. 1072-1076.
- Савельев В. С., Филимонов М. И., Бурневич С. З. Панкреонекрозы. М.: ООО «Медицинское информационное агентство», 2008. 264 с.
- Гальперин Э.И., Дюжева Т.Г. Панкреонекроз: неиспользованные резервы лечения//Аналы хирургии и гепатологии. 2007. № 12(2). С. 46-50.
- Савельев В.С., Филимонов М.И., Гельфанд Б.Р., Бурневич С.З., Орлов Б.Б., Цыденжапов Е.Ц. Острый панкреатит как проблема ургентной хирургии и интенсивной терапии//Consilium Medicum. 2000. Т. 2, № 9.
- Working UK Party on Acute Pancreatitis. UK guidelines for the management of acute pancreatitis//Gut. 2005. Vol. 54 (suppl. 3).
- D.J. van Westerloo et al. New Insights into Pathophysiolog and Severity Assessmtnt of Acute Pancreatitis. Yearbook of Intesive Care and Emergency Medicine, 2003. P. 823-844.
- Dervenis C., Johnson C.D., Bassi C. et al. Diagnosis, objective assessment of severity, and management of acute pancreatitis. Santorini consensus statement//Int. J. Pancreatol. 1999. Vol. 25. P. 195-210.
- Zhang X.P., Wang L., Zhou Y.F. The pathogenic mechanism of severe acute pancreatitis complicated with renal injury: A review of current knowledge//Dig. Dis. Sci. 2008. Vol. 53. P. 297-306.
- Windsor J.A., Fearon K.C.H., Ross J.A. et al. Role of serum endotoxin and antiendotoxin core antibody levels in predicting the development of multiple organ failure in acute pancreatitis//Br. J. Surg. 1993. Vol. 80. P. 1042-1046.
- Bellomo R., Ronco C., Kellum J. A, Mehta R. L, Palevsky P. (the ADQI workgroup). Acute renal failure -definition, outcome measures, animal models, fluid therapy and information technology needs: the Second International Consensus Conference of the Acute Dialysis Quality Initiative (ADQI)//Crit. Care. 2004. Vol. 8. R. 204-212.
- Cruz D.N., Ricci Z., Ronco C. Clinical review: RIFLE and AKIN-time for reappraisal//Crit. Care. 2009. Vol. 13. P. 211.
- Schmidt J., Werner J. Acute pancreatitis: reliable and prospective conservative therapy//Langenbecks Arch. Chir. Suppl. Congressed 1998. Vol. 115. P. 434-438
- Yang Z. et al. Effect of early hemofiltration on pro-and antiinflammatory responses and multiple organ failure in severe acute pancreatitis//J. Huazhong. Univ. Sci. Technolog. Med. Sci. 2004. Vol. 24(5). P. 456-459.
- Yang Z. et al. Protective effect CVVH and organ damage in patients with severe acute pancreatitis//World J. Gastroenterology. 2004. Vol. 16(4). P. 232-234.
- Wang H. et al. Clinical effects continuous high volume hemofiltration on acute pancreatitis complicated with multiple organ dysfunction syndrome//World J. Gastroenterology. 2003. Vol. 9(9). P. 2096-2099.
- Hao Wang, Wei-Qin Li, Wei Zhou, Ning Li, Jie-Shou Li. Clinical effects of continuous high volume hemofiltration on severe acute pancreatitis complicated with multiple organ dysfunction syndrome//World J. Gastroenterology. 2003. Vol. 9(9). P. 2096-2099.
- En-Qiang Mao et al. Effect of time interval for hemofiltration on the prognosis of severe acute pancreatitis//World J. Gastroenterol. 2003. Vol. 9(2). P. 373-376.
- Saudan P., Niederberger M., De Seigneux S., Romand J., Pugin J., Perneger T., Martin P.Y. Adding a dialysis dose to continuous hemofiltration increases survival in patients with acute renal failure//Kidney Int. 2006. Vol. 70. P. 1312-1317.
- Palevsky P.M., Zhang J.H., O'Connor T.Z., Chertow G.M., Crowley S.T., Choudhury D., Finkel K., Kellum J.A., Paganini E., Schein R.M., Smith M.W., Swanson K.M., Thompson B.T., Vijayan A., Watnick S., Star R.A., Peduzzi P. Intensity of renal support in critically ill patients with acute kidney injury//N. Engl. J. Med. 2008. Vol. 359. P. 7-20.
- Vinsonneau C., Camus C., Combes A., Costa de Beauregard M.A., Klouche K., Boulain T., Pallot J.L., Chiche J.D., Taupin P., Landais P., Dhainaut J.F. Hemodiafe Study Group. Continuous venovenous haemodiafiltration versus intermittent haemodialysis for acute renal failure in patients with multiple-organ dysfunction syndrome: a multicentre randomised trial//Lancet. 2006. Vol. 368(9533). P. 379-85.
- Honore P.M., Matson J.R. Extracorporeal removal for sepsis: acting at the tissue level -the beginning of a new era for this treatment modality in septic shock//Crit. Care Med. 2004. Vol. 32. P. 896-897.
- Honore P.M., Joannes-Boyau O., Jacobs R., Solignac M. Blood purification in sepsis: fiction or fact for the clinician//Reanimation. 2010. Vol. 19. P. 7-12.
- Ronco C., Bellomo R., Homel P. et al. Effects of different doses in CVVH on outcomes of ARF: Aprospective randomized trial//Lancet. 2000. Vol. 355. P. 26-30.


