Агрессивная ангиомиксома тазовой области: клинико-морфологические особенности и оптимизация хирургического подхода
Автор: Садыхова Л.З., Исламов Ф.Э., Сисакян В.Г., Селюнина Н.А., Шифон С.А., Жданова Е.А.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 1 т.25, 2026 года.
Бесплатный доступ
Актуальность. Агрессивная ангиомиксома (АА) – редкое мезенхимальное новообразование, преимущественно поражающее область таза и промежности у женщин репродуктивного возраста. Описание клинического случая. Представлен клинический случай пациентки, 41 год, с гигантской агрессивной ангиомиксомой левой большой половой губы, размерами 300×160×60 мм. Первоначально дифференциальный диагноз проводился с кистой бартолиновой железы и паховой грыжей, однако комплексное обследование, включающее УЗИ, КТ и МРТ с контрастированием, выявило неоднородное образование с инфильтративным ростом в забрюшинное пространство. МРТ-картина демонстрировала характерные «слоистые» изменения, а гистологическое исследование подтвердило диагноз: диффузный рост опухолевых клеток в миксоматозной строме с экспрессией CD34, HMGA2 и рецепторов эстрогена/ прогестерона. Лечение включало двухэтапную операцию: наружную мобилизацию опухоли с последующей лапароскопической резекцией забрюшинного компонента новообразования и пластикой дефекта тазового дна. Гистологический анализ краев резекции и лимфатических узлов подтвердил отсутствие опухолевых клеток. Заключение. МРТ – «золотой стандарт» диагностики АА, позволяющий оценить связь опухоли с тазовым дном. В лечении АА остаются нерешенными дилеммы, такие как радикальность резекции опухоли, частота рецидивов при которой достигает 40–50 %, что обосновывает преимущество органосохраняющих подходов. Особое внимание уделяется гормональной терапии агонистами ГнРГ и ингибиторами ароматазы – направлению, перспективному как в отношении предоперационного уменьшения объема опухоли, так и профилактики последующих рецидивов. Однако данный подход ограничен временным эффектом и побочными эффектами, что подчеркивает необходимость дальнейших исследований для стандартизации лечения и уточнения прогностической роли маркеров экспрессии HMGA2 для оценки риска рецидивов.
Агрессивная ангиомиксома, тазовые опухоли, гормон-зависимые опухоли, хирургическое лечение, диагностика
Короткий адрес: https://sciup.org/140314358
IDR: 140314358 | УДК: 616.718.19-006-07-089 | DOI: 10.21294/1814-4861-2026-25-1-179-185
Aggressive pelvic angiomyxoma: clinical and morphological characteristics and optimization of the surgical approach
Background. Aggressive angiomyxoma (AA) is a rare mesenchymal neoplasm that predominantly involves the pelvic and perineal regions in women of reproductive age. Description of the clinical case. We report the case of a giant 300×160×60 mm AA on the left labia majora in a 41-year-old female patient. The initial differential diagnosis included Bartholin’s gland cyst and inguinal hernia; however, comprehensive examination involving ultrasound, CT, and contrast-enhanced MRI revealed a heterogeneous mass with infltrative growth into the retroperitoneal space. The MRI fndings demonstrated characteristic “layered” changes, and histological examination confrmed the diagnosis: diffuse proliferation of tumor cells within a myxoid stroma, expressing CD34, HMGA2, and estrogen/progesterone receptors. Treatment involved a two-stage surgical procedure: external mobilization of the tumor followed by laparoscopic resection of the retroperitoneal component and pelvic foor defect reconstruction. Histopathological analysis of the resection margins confrmed negative (tumor-free) margins. Lymph node examination revealed no metastases. Conclusion. MRI is the gold standard for diagnosis of aggressive angiomyxoma, allowing for the assessment of the tumor extent and its relationship with the pelvic foor. The management of aggressive angiomyxoma remains challenging. Radical tumor excision characterized by a high recurrence rate (40–50 %) is shifting toward organ-preserving approaches. Hormonal therapy, combining GnRH agonists with aromatase inhibitors, is an effective strategy to reduce tumor size and recurrence risk. However, this approach is limited by its temporary effect and associated side effects, underscoring the need for a multidisciplinary strategy and further research to standardize treatment and clarify the prognostic role of HMGA2 expression markers for assessing recurrence risks.
Текст научной статьи Агрессивная ангиомиксома тазовой области: клинико-морфологические особенности и оптимизация хирургического подхода
Агрессивная ангиомиксома (АА) – редкое новообразование мягких тканей, преимущественно поражает область таза и промежности [1]. У женщин она диагностируется чаще, чем у мужчин, в соотношении 6:1 [2, 3]. В ретроспективном обзоре 87 наблюдений сообщается о среднем возрасте больных АА – 37,97 года, при этом минимальный возраст составлял 2 года, а максимальный – 65 лет [3].
Ангиомиксомы подразделяются на два гистологических варианта: поверхностную (кожную) и глубокую (агрессивную) формы. Поверхностная ангиомиксома представляет собой доброкачественное неинвазивное новообразование дермальной локализации, впервые описанное в ассоциации с синдромом Карни – редким аутосомнодоминантным заболеванием, характеризующимся множественными неоплазиями эндокринной системы и мезенхимальными опухолями. В отличие от нее агрессивная ангиомиксома является локальноинвазивной мезенхимальной неоплазией мягких тканей [4], обладающей выраженной склонностью к локальному рецидивированию [3]. Согласно классификации ВОЗ (2020), АА относится к опухолям неопределенной дифференцировки [2, 3, 5].
Клинической особенностью ангиомиксом является бессимптомное течение [3]. Иммуногистохимический анализ демонстрирует экспрессию рецепторов эстрогена и прогестерона в опухолевой ткани, что, согласно ряду исследований, может объяснять тенденцию к прогрессированию неоплазии в период беременности, а также устойчивую регрессию опухоли в послеродовом периоде, что характерно для гормонозависимых опухолей [1, 3, 5, 6]. Хотя в большинстве наблюдений АА протекает латентно, часть пациентов предъявляют жалобы на дискомфорт в области опухолевого поражения, тупую боль, локальное чувство давления, дизурические явления, задержку мочеиспускания или диспареунию [2, 3, 7].
Этиопатогенез ангиомиксом остается недостаточно изученным. Описаны хромосомные аберрации, в частности в локусе 12q13-15, где локализован ген HMGА2 (High Mobility Group AT-hook 2) [8]. Данный ген кодирует ДНК-связы-вающие белки, участвующие в регуляции транскрипции [6]. Посредством цитогенетического анализа выявлены клональные аберрации и транслокации с участием хромосомы 12, в частности t(8;12)(p12;q15) [4]. Несмотря на то, что данные генетические перестройки не всегда выступают в роли драйверных мутаций, их выявление имеет важное значение для дифференциальной диагностики и оценки риска рецидивов.
Представляем клинический случай агрессивной ангиомиксомы.
Описание клинического случая
Пациентка С., 41 год, обратилась с жалобами на прогрессирующее увеличение левой большой половой губы, которое связывала с физической нагрузкой. При осмотре выявлено асимметричное увеличение левой половой губы до 250 мм (рис. 1). Первоначально дифференциальный диагноз проводился с кистой бартолиновой железы и паховой грыжей. Пациентка не была беременна и имела в анамнезе одно кесарево сечение.
При УЗИ мягких тканей промежности выявлено значительное увеличение левой большой половой губы, размерами более 200×70×100 мм. В проекции запирательного отверстия визуализировалась грыжевая ножка толщиной 35 мм, содержащая
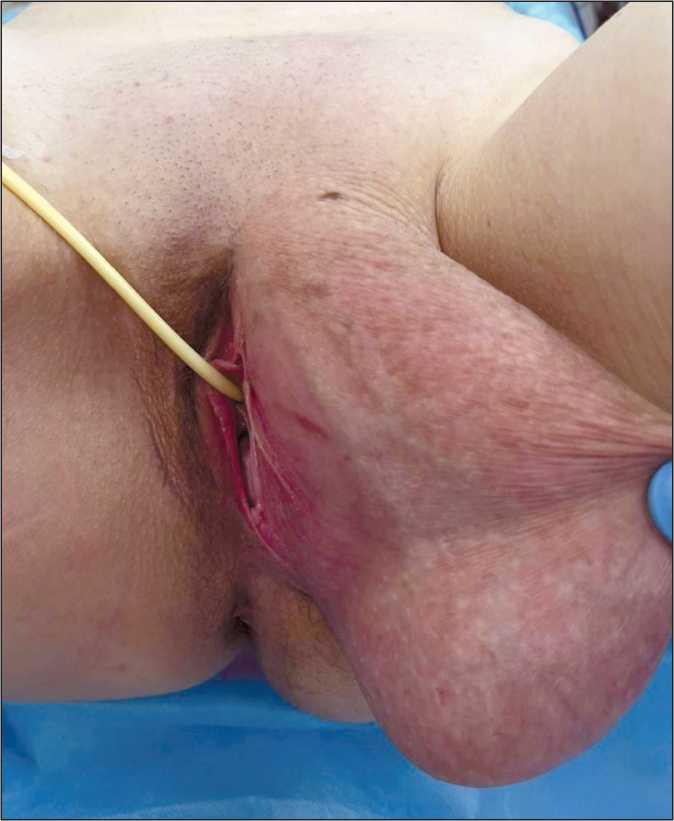
Рис. 1. Левая половая губа с патологическим образованием, размерами 200×70×100 мм.
Примечание: рисунок выполнен авторами
Fig. 1. A giant mass measuring 200×70×100 mm on the left labia.
Note: created by the authors
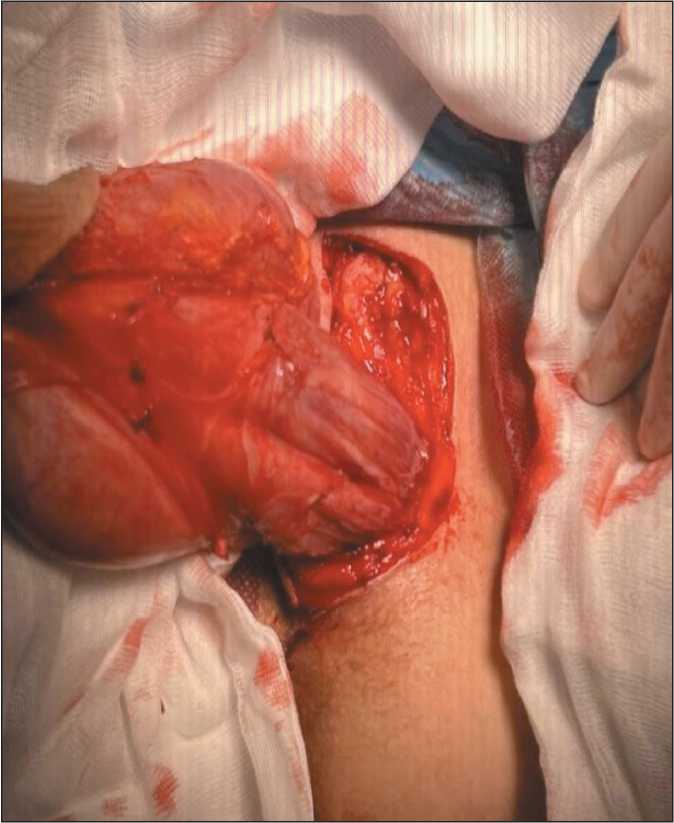
Рис. 2. Первый этап оперативного вмешательства. Примечание: рисунок выполнен авторами Fig. 2. The first stage of surgical treatment.
Note: created by the authors
жировую клетчатку, с грыжевым мешком в области половой губы. При этом ультразвуковая картина демонстрировала толстокапсульное ги-поэхогенное образование гетерогенной структуры с гипер- и анэхогенными компонентами и локальными участками васкуляризации по поверхности, без связи с брюшной полостью.
Компьютерная томография с контрастированием выявила крупное (до 252 мм в сагиттальной плоскости) неоднородное образование левой половины таза, распространяющееся в мягкие ткани промежности. Образование имело нечеткие контуры, плотность в диапазоне +20 – +35 HU, смещало матку, мочевой пузырь и прямую кишку. Органная принадлежность опухоли не определялась, признаков поражения брюшины и лимфаденопатии не отмечалось.
На основании комплексного обследования исключены грыжа запирательного отверстия и доброкачественные новообразования соединительной и других мягких тканей таза. Установлен предварительный диагноз – образование большой половой губы слева.
Большая часть новообразования располагалась в забрюшинном пространстве, меньшая часть локализовалась экстраперитонеально в области большой половой губы. В связи с особенностями анатомического расположения была выбрана комбинированная хирургическая тактика, включающая 2 этапа.
На первом этапе оперативного вмешательства произведена наружная мобилизация опухоли (рис. 2), имеющей конфигурацию «песочных часов». Второй этап выполнялся лапароскопическим доступом в объеме радикального иссечения забрюшинной части новообразования с последующей реконструкцией тазового дна. Наружная мобилизация позволила получить доступ к образованию, локализованному в глубоких слоях мягких тканей латерально от большой половой губы, с визуализацией костных структур таза. Выполнен разрез между влагалищем и большой половой губой для отделения опухоли от боковой стенки влагалища и мочевого пузыря с сохранением круглой маточной связки, кардинальной связки, мочеточника и запирательного нерва. Опухоль выделена до тазового дна с открытием доступа в забрюшинное пространство.
Одновременно установлены троакары, лапароскопический доступ осуществлен в брюшную полость с последующей мобилизацией париетальной брюшины и выделением левого забрюшинного пространства. Идентифицированы и выделены наружная и внутренняя подвздошные артерии и вены, бифуркация общей подвздошной артерии, мочеточник, запирательный нерв и подвздошно-
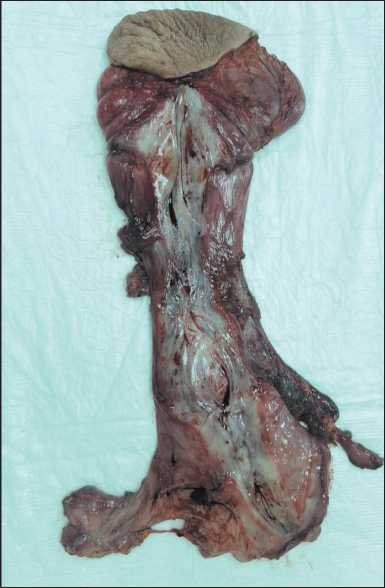
Рис. 3. Макропрепарат. Удаленная опухоль, размерами 300×160×60 мм. Примечание: рисунок выполнен авторами Fig. 3. Macroscopic examination of the surgical specimen measuring 300×160×60 mm. Note: created by the authors поясничная мышца. После радикального удаления новообразования образовался сквозной дефект между наружным хирургическим доступом и забрюшинным пространством, ограниченный тазовой костью и боковой стенкой влагалища. Для предотвращения пролапса тазовых органов и формирования грыжи дефект ушит нерассасы-вающимся шовным материалом. Края наружной раны соединены подкожным непрерывным швом. В ходе операции сохранены матка, придатки. Забрюшинное пространство перитонизировано, установлен дренаж.
Макропрепарат был представлен мягкотканой опухолью, размерами 300×160×60 мм, в тонкой капсуле с участками кровоизлияний (рис. 3). При гистологическом исследовании операционного материала выявлен диффузный опухолевый рост из округло-овальных клеток в миксоматозной строме с единичными сосудами. При исследовании краев резекции опухолевых клеток не обнаружено. В трех исследованных лимфоузлах метастазы отсутствовали. Окончательный гистологический диагноз: глубокая ангиомиксома (код ICD-O 8841/0).
Обсуждение
Диагностика агрессивной ангиомиксомы сопряжена со значительными трудностями, обусловленными редкостью данной патологии и неспецифичностью клинических проявлений. Дифференциально-диагностический ряд включает широкий спектр заболеваний [7]. В диагностическом алгоритме применяются методы медицинской визуализации: ультразвуковое исследование, компьютерная томография (КТ) и магнитно-резонансная томография (МРТ), причем последняя обладает наибольшей диагностической ценностью благодаря превосходной тканевой дифференцировке [9]. Однако окончательная верификация диагноза требует гистопатологического исследования с иммуногистохимическим подтверждением [7]. Ультразвуковое исследование брюшной полости – первоначальное визуальное диагностическое исследование AA, показывающее гипоэхогенное поражение с гетерогенной внутренней эхогенностью, фибриллярной внутренней структурой и возможностью обнаружения сигналов внутреннего кровотока. Однако УЗИ недостаточно для всесторонней оценки опухоли [5].
Магнитно-резонансная томография с контрастным усилением гадолинием является лучшим радиологическим вариантом для диагностики [5]. Магнитно-резонансная томография оценивает масштаб опухоли и ее связь с тазовой диафрагмой и окружающими органами. Агрессивная ангиомиксома имеет определенные МР-характеристики, такие как множественные скрученные полосчатые тени, показывающие «водоворотные» или «слоистые» изменения [10]. В отличие от УЗИ метод помогает определить границы опухоли [11].
На КТ ангиомиксомы имеют четко выраженный край с более слабым, чем у мышц, затуханием сигнала. Снижение интенсивности сигнала на КТ и высокая интенсивность сигнала МРТ, вероятно, обусловлены наличием свободной миксоидной матрицы и высоким содержанием воды в АА [6]. В то время как КТ-изображение обычно используется из-за ее широкой доступности, МРТ имеет присущее ей более высокое пространственное разрешение для лучшей характеристики мягких тканей и анатомических деталей. МРТ превосходит КТ для оценки промежностных и вульварных ангиомиксом, а также для оценки инвазии опухоли и ее связи с тазовым дном, что может помочь отличить поверхностную от агрессивной ангиомиксомы [12].
Гистологический анализ выявляет гладкую мышечную ткань, содержащую многочисленные сосуды, на фоне гипоклеточной фиброзной стромы [12]. Опухолевые клетки характеризуются аномальной ядерной атипией и митозами [9]. Имуногистохимическое исследование опухоли подтверждает диагноз АА при положительном ответе при окрашивании рецепторов для CD34, бета-катенина, HMGA2, эстрогена и прогестерона, отрицательном – для S100, SOX10, MUC4, STAT6, EMA, MyoD1, MDM2. Положительная экспрессия рецепторов эстрогена и прогестерона является важным отличием, которое стабильно выявляется при АА и отсутствует при поверхностной ангиомиксоме. Кроме того, для АА характерно наличие гипертрофии мышечной стенки [3, 12].
Учитывая выраженную экспрессию рецепторов эстрогена и прогестерона в большинстве ангиомиксом, значительный терапевтический потенциал демонстрируют гормональные препараты, включая агонисты гонадотропин-рилизинг гормона (ГнРГ), селективные модуляторы эстрогеновых рецепторов и ингибиторы ароматазы. Клинические наблюдения подтверждают их эффективность как в неоадъювантном режиме (для уменьшения объема опухоли перед операцией), так и при лечении рецидивов. Механизм действия агонистов ГнРГ основан на десенситизации рецепторов: после начальной стимуляции (в течение ~10 дней) происходят их интернализация и последующая down-регуляция, что приводит к выраженному снижению уровня половых гормонов. Этот эффект подтверждается клиническими случаями с полным клиническим ответом как при первичных, так и рецидивирующих опухолях. Некоторые исследователи рекомендуют включать агонисты ГнРГ в стандартные протоколы лечения, что может позволить избежать хирургических вмешательств у пациентов с гормон-рецептор-позитивными опухолями [13]. Продолжительность лечения варьируется от 3 мес до пожизненной терапии [1].
Перспективным направлением является применение ингибиторов ароматазы, механизм действия которых основан на блокировании продукции эстрогенных метаболитов. Клинические данные демонстрируют их способность индуцировать регресс опухоли, особенно при неоадъювантном использовании. Тем не менее оптимальная продолжительность гормональной терапии остается предметом дискуссий и требует дальнейших исследований для стандартизации лечения. В то же время следует учитывать, что эти препараты имеют побочные эффекты, включая проявления климактерического синдрома. Препараты стабилизируют, но не излечивают опухолевый процесс. Данный подход рассматривается как эффективная альтернатива хирургическому лечению для женщин в постменопаузе [13].
В настоящее время химиотерапия и лучевая терапия не имеют четко установленного положения в стандартных протоколах лечения ангиомиксомы [14]. Лучевая терапия является альтернативой хирургическому вмешательству и может быть использована при рецидивах опухоли. Однако следует учитывать, что эффективность лучевой терапии в монорежиме ограничена при низкой митотической активности опухоли [15]. В единичных клинических наблюдениях при тазовой локализации АА применялись предоперационное и интраоперационное облучение в комбинации с эмболизацией опухоли с целью снижения риска ре- цидива, однако долгосрочные результаты данного подхода неизвестны. Имеются немногочисленные сообщения об использовании лучевой терапии при рецидивирующих формах заболевания с интервалами между рецидивами, составляющими, по разным данным, 2–3 года. Однако отсутствие систематизированных данных и контролируемых исследований не позволяет сделать однозначных выводов об эффективности данного метода [14].
Хирургическое вмешательство является «золотым стандартом» лечения и подразумевает полное удаление новообразования [7]. При распространенных АА учитываются потенциальные функциональные нарушения смежных органов, а также косметические изменения. При опухолях большого размера с четкими границами локальная пересадка кожи может минимизировать постхирургическую деформацию [16]. Меньшие, более поверхностные опухоли вульвы или влагалища могут быть удалены путем широкого иссечения, но более крупные и/или глубоко расположенные опухоли таза могут потребовать обширной операции с резекцией тазовых органов. Хотя достижение радикального удаления опухоли является предпочтительным, в определенных клинических ситуациях допустима частичная резекция АА. Это актуально в случаях, когда сохранение органа с остаточной опухолевой тканью обеспечивает лучший функциональный исход по сравнению с радикальным вмешательством, сопряженным с высоким риском послеоперационных осложнений. Кроме того, ограниченная резекция может быть оправдана у пациенток репродуктивного возраста при необходимости сохранения фертильности [17].
Заключение
Несмотря на доброкачественную природу, АА отличается сложностью диагностики, необходимостью тщательной визуализации (предпочтительно МРТ) и мультидисциплинарного подхода к лечению. «Золотым стандартом» лечения остается хирургическое вмешательство, однако радикальность операции не всегда коррелирует с показателями безрецидивной выживаемости. Это позволяет рассматривать возможность применения органосохраняющих и функционально щадящих операций в клинически оправданных случаях, особенно у женщин репродуктивного возраста. Гормонотерапия (агонисты ГнРГ, ингибиторы ароматазы) демонстрирует высокую эффективность как в неоадъювантном режиме, так и при лечении рецидивов, однако метод требует дальнейшего изучения для оптимизации длительности лечения и оценки долгосрочных результатов. Необходимы дополнительные исследования для стандартизации подходов к лечению, особенно в отношении гормональной терапии, оценки молекулярных маркеров и потенциальных генетических мишеней.


