Активность супероксиддисмутазы в спермоплазме и качество спермы жеребцов
Автор: Романова А.И., Атрощенко М.М., Фролова Н.А., Широкова О.В.
Статья в выпуске: 2 т.258, 2024 года.
Бесплатный доступ
Целью настоящего исследования стало изучение активности антиоксидантного фермента - супероксиддисмутазы (СОД) в спермоплазме у жеребцов с высокой и низкой прогрессивной подвижностью (ПП) сперматозоидов. У жеребцов с высокой прогрессивной подвижностью сперматозоидов активность супероксиддисмутазы в спермоплазме была выше и достоверно отличалась от группы жеребцов с низкой прогрессивной подвижностью сперматозоидов (P
Жеребцы, сперма, спермоплазма, антиоксиданты, супероксиддисмутаза
Короткий адрес: https://sciup.org/142241644
IDR: 142241644 | УДК: 636.1.084.453.52:612.1 | DOI: 10.31588/2413_4201_1883_2_258_171
Superoxide dismutase activity in seminal plasma and semen quality of stallions
The aim of this study was to study the activity of the antioxidant enzyme superoxide dismutase (SOD) in the seminal plasma of stallions with high and low progressive motility (PP) of spermatozoa. In stallions with high progressive sperm motility the activity of superoxide dismutase in the seminal plasma was higher and significantly differed from the SOD activity in the group of stallions with low progressive sperm motility (P
Текст научной статьи Активность супероксиддисмутазы в спермоплазме и качество спермы жеребцов
В современном отечественном коневодстве большое значение уделяется устойчивости половых клеток к криоконсервации, так как искусственное осеменение обеспечивает высокие результаты только тогда, когда в работе используют здоровых жеребцов-производителей с высоким качеством и криоустойчивостью спермы [7].
Известно, что действие на организм неблагоприятных факторов химической и физической природы избыточно усиливает процессы свободнорадикального окисления (СРО) [2]. Антиоксидантная система организма регулирует уровень СРО и защищает клетки и ткани от накопления токсичных продуктов окисления и включает в себя: ферменты, неферментные белки и низкомолекулярные соединения [4, 5]. Активные формы кислорода (АФК) уравновешиваются антиоксидантной системой защиты, которая не допускает возникновения окислительного стресса (ОС) [1]. Антиоксиданты нейтрализуют цепную реакцию, ведущую к образованию ОС, тем самым защищая организм от негативного воздействия токсических соединений [1, 3].
Необходимо отметить, что при криоконсервации спермы жеребцов значительно возрастают показатели ОС и повреждения плазматических мембран сперматозоидов, которые в дальнейшем активируют несколько путей разрушения клеток, что в конечном итоге приводит к фрагментации их ДНК [9]. Добавление антиоксидантов в среду для криоконсервации снижает уровень структурных повреждений сперматозоидов и потерю их подвижности от перекисного окисления липидов (ПОЛ) [10, 11].
Семенная плазма, которая вырабатывается придаточными половыми железами, придатками семенников и семенниками, создает для сперматозоидов оптимальную среду и имеет большой запас антиоксидантов: ферментативных (каталаза, глутатионпероксидаза и супероксиддисмутаза) и неферментативных (множество соединений, поступающих в организм с кормом) [6, 8]. Самыми основными антиоксидантными ферментами в спермоплазме жеребцов являются: супероксиддисмутаза, каталаза и глутатионпероксидаза, способные катализировать анион супероксида, перекись водорода и перекись липидов [12, 14].
Целью настоящего исследования стало изучение активности антиоксидантного фермента – супероксиддисмутазы (СОД) в спермоплазме у жеребцов с высокой и низкой прогрессивной подвижностью (ПП) сперматозоидов.
Материал и методы исследований. Исследования проводили в 2021 году на базе АО «Терский племенной конный завод № 169» (Ставропольский край) на 16 жеребцах арабской чистокровной породы в возрасте от 5 до 15 лет (в среднем 8,5±4,5 лет). Сперму, предназначенную для исследований, получали в период случного сезона (март- апрель) согласно «Рекомендации по взятию, разбавлению и замораживанию спермы жеребцов» (2006). После получения спермы в каждом эякуляте определяли объем и концентрацию сперматозоидов (фотометр SDM1 Minitube GmbH, Tiefenbach, Германия). Далее эякулят делили на две части, одну часть разбавляли лактозо-хелато-цитратножелточной средой (ЛХЦЖ), в соотношении 1:3, определяли прогрессивную подвижность и выживаемость сперматозоидов при температуре 2-4 ˚С. Оценку прогрессивной подвижности (ПП) сперматозоидов проводили с использованием системы Argus CASA (ArgusSoft LTD., Санкт-Петербург, Россия) и микроскопа Motic BA 410 (Motic, Гонконг, Китай) в камере Маклера (Sefi-Medical Instruments Ltd., Израиль) при 37 ˚С. Для оценки выживаемости сперматозоидов (в часах) определяли их прогрессивную подвижность с интервалом 24 часа вплоть до снижения ПП до 5 %.
Другую часть эякулята сразу после получения центрифугировали при 3000 об/мин в течение 20 мин. После семенной плазмы, свободные от сперматозоидов, замораживали в пробирках типа Эппендорф (2,0 мл) и хранили при температуре -18 ˚С до проведения исследований. Исследование активности супероксиддисмутазы в спермоплазме проводили на иммунохимическом анализаторе Tecan Austria Sunrise (Bender Medsystems, Австрия).
Статистическую обработку проводили с использованием программ Statistica 13.3 (StatSoft, Россия) и Microsoft Office Exsel 2016. Достоверность различий определяли с помощью t-критерия Стьюдента. Результаты представлены в виде среднеарифметической (М) и ее стандартной ошибки (m), минимальных (Min) и максимальных (Max) значений. Отличия считали статистически значимыми при Р <0,05.
Исследования проводились при финансовой поддержке Российского научного фонда (проект № 20-16-00101-П).
Результат исследований. В таблице 1 приведены значения показателей спермы жеребцов, а также активности супероксиддисмутазы спермоплазмы.
микроскопии супернатанта аликвоты
Таблица 1 – Показатели спермы жеребцов, активность супероксиддисмутазы в спермоплазме, М±m, (Min, Max), (n=16)
|
Показатель, единицы измерения |
М±m |
Min |
Max |
|
Нативная сперма |
|||
|
Объем эякулята, мл |
30,5±5,6 |
12,0 |
41,0 |
|
Концентрация сперматозоидов в 1 мл, млн/мл |
259,9±21,9 |
177,0 |
399,0 |
|
Разбавленная сперма |
|||
|
Прогрессивная подвижность сперматозоидов, % |
56,7±5,1 |
25,0 |
80,0 |
|
Выживаемость сперматозоидов при температуре 2-4 ˚С, час |
219,6±23,5 |
48,0 |
456,0 |
|
Спермоплазма |
|||
|
Активность супероксиддисмутазы в спермоплазме, Ед/мл |
42,4±5,1 |
25,0 |
85,0 |
Наиболее точную оценку ПП сперматозоидов позволяет определить компьютерный анализ спермы (Рисунок 1). Компьютерная оценка учитывает количество сперматозоидов с прогрессивной и непрогрессивной подвижностью и количество неподвижных клеток в поле зрения.
Супероксиддисмутаза преобразует супероксидный радикал в перекись водорода, тем самым являясь ключевым фактором защиты клеток от окислительного стресса. В исследованиях Papas M. et al. (2019) установлено, что супероксиддисмутаза положительно влияет на общую и прогрессивную подвижность сперматозоидов в спермоплазме жеребцов. Сперма жеребцов с высоким содержанием супероксиддисмутазы в процессе криоконсервации выдерживает окислительный стресс благоприятнее, чем у жеребцов с низким содержанием этого фермента [12]. Partyka А. et al. (2013) установили, что при добавлении в разбавитель для спермы супероксиддисмутазы перекисное окисление липидов в плазматической мембране сперматозоидов петухов снижалось [13].
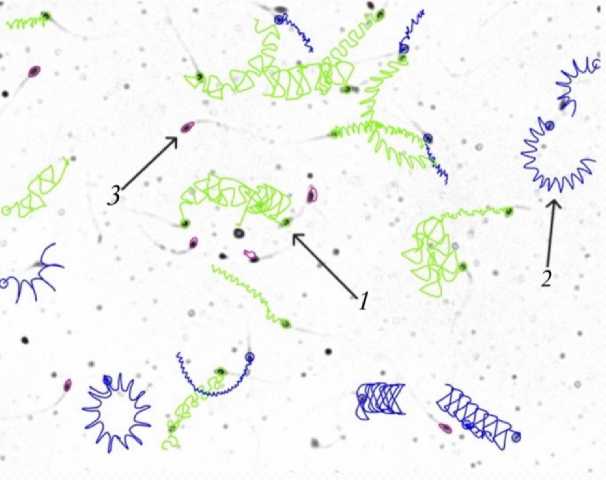
Рисунок 1 – Компьютерная оценка прогрессивной подвижности сперматозоидов с использованием системы Argus CASA, где 1 – сперматозоид с прогрессивной подвижностью, 2 – сперматозоид с непрогрессивной подвижностью, 3 – неподвижный сперматозоид
Таблица 2 – Показатели спермы и активности СОД в спермоплазме у жеребцов с высокой и низкой ПП сперматозоидов, М±m, (n=16)
|
Показатель |
Группа 1 |
Группа 2 |
|
ПП ниже 50 (n=6) |
ПП выше 50 (n=10) |
|
|
Прогрессивная подвижность сперматозоидов в нативной сперме, % |
33,2±2,7 |
62,4±6,1* |
|
Объем эякулята, мл |
23,2±4,1 |
32,4±4,4 |
|
Концентрация спермы в 1 мл, млн/мл |
307,7±40,8 |
266,1±22,1 |
|
Выживаемость сперматозоидов при температуре 2-4 °С, час |
179,3±29,5 |
254,0±28,8** |
|
Активность супероксиддисмутазы в спермоплазме, Ед/мл |
34,0±1,8 |
55,1±5,5* |
Примечание: * отмечены значения Р <0,05, ** отмечены значения Р <0,01
Для изучения взаимосвязи между активностью СОД в спермоплазме и качеством спермы жеребцов, всех исследуемых животных разделили на две группы в зависимости от показателя прогрессивной подвижности (ПП) сперматозоидов в нативной сперме (ГОСТ23681-79). В первую группу включили 6
жеребцов с ПП сперматозоидов в нативной сперме ниже 50 %. Во вторую группу включили 10 жеребцов с ПП сперматозоидов в нативной сперме выше 50 % (Таблица 2). По результатам исследования установили, что у жеребцов 2-ой группы (с высокой ПП сперматозоидов) активность СОД в спермоплазме была выше, чем у жеребцов 1-ой группы (P <0,05).
Заключение. Проведение исследования активности супероксиддисмутазы семенной плазмы позволило изучить взаимосвязь между этим антиоксидантным ферментом спермоплазмы и показателями спермы жеребцов.
Установили, что у жеребцов 2-ой группы (с высокой прогрессивной подвижностью сперматозоидов) активность супероксиддисмутазы в спермоплазме была выше и достоверно отличалась от жеребцов 1-ой группы (с низкой прогрессивной подвижностью сперматозоидов) (P <0,05).
Предполагаем, что активность супероксиддисмутазы в спермоплазме можно использовать в качестве биохимического маркера при отборе жеребцов с лучшими показателями качества спермы.
Список литературы Активность супероксиддисмутазы в спермоплазме и качество спермы жеребцов
- Никулин, В. Н. Влияние комплекса пробиотика на основе лактобактерий и селенита натрия на некоторые показатели антиоксидантной защиты макроорганизма / В. Н. Никулин, В. В. Герасименко, Т. В. Коткова [и др.] // Известия Оренбургского государственного аграрного университета. – 2013. – Т. 41. – № 3. – С. 254-257.
- Плосконос, М. В. Биохимические изменения в мембране сперматозоидов фертильных мужчин под воздействием индуктора оксидативного стресса и коррекция этих изменений / М. В. Плосконос // Проблемы репродукции. – 2015. – № 5. – С. 102-108.
- Жамсаранова, С. Д. Влияние характера питания на антиоксидантный статус организма обучающейся молодежи / С. Д. Жамсаранова, С. А. Чукаев, Л. Д. Дымшеева, С. Н. Лебедева // Science for EducationToday. – 2019. – Т. 9. – № 2. – С. 226-248.
- Чанчаева, Е. А. Современное представление об антиоксидантной системе организма человека / Е. А. Чанчаева, Р. И. Айзман, А. Д. Герасев // Экология человека. – 2013. – № 7. – С. 50-58.
- Янковский, О. Ю. Антиоксидантный статус организма человека и его коррекции / О. Ю. Янковский, С. И. Кузнецов // Вестник СПбГУ. – 2005. – № 2. – С. 40-52.
- Aitken, R. J. Use of xanthine oxidase free radical generating system to investigate the cytotoxic effects of reactive species on human spermatozoa / R. J. Aitken, D. Buckingham, D. Harkiss // Reproduction. – 1993. – Vol. 93. – P. 441-450.
- Atroshchenko, M. M. Reproductive characteristics of thawed stallion sperm / M. M. Atroshchenko, E. Arkhangelskaya, D. A. Isaev [et al.] // Animals. – 2019. – Vol. 9. – № 12. – P. 1099.
- Aurich, J. E. Effects of antioxidants on motility and membrane integrity of chilled-stored stallion semen / J. E. Aurich, U. Schönherr, H. Hoppe, C. Aurich // Theriogenology. – 1997. – Vol. 48. – P. 185-192.
- Contreras, M. J. Cryopreservation of stallion semen: Effect of adding antioxidants to the freezing medium on sperm physiology / M. J. Contreras, F. Treulen, M. E. Arias [et al.] // Reproduction in Domestic Animals. – 2020. – Vol. 55. – № 2. – P. 229-239.
- Memona, A. A. Effect of antioxidants on post thaw microscopic, oxidative stress parameter and fertility of Boer goat spermatozoa in Tris egg yolk glycerol extender / A. A. Memona, H. Wahida, Y. Rosninaa [et al.] // Animal Reproduction Science. – 2012. – Vol. 136. – № 1-2. – P. 55-60.
- Pagl, R. Anti-oxidative status and semen quality during cooled storage in stallions / R. Pagl, C. Aurich, M. Kankofer // Journal of Veterinary Internal Medicine. – 2006. – Vol. 53. – P. 486-489.
- Papas, M. Specific activity of superoxide dismutase in stallion seminal plasma is related to sperm cryotolerance / M. Papas, J. Catalán, B. Fernandez-Fuertes [et al.] // Antioxidants. – 2019. – Vol. 8. – P. 539.
- Partyka, A. The effect of cysteine and superoxide dismutase on the quality of post-thawed chicken sperm / A. Partyka, W. Niżański, J. Bajzert [et al.] // Cryobiology. – 2013. – Vol. 67. – № 2. – P. 132-136.
- Prete, C. D. Combined addition of superoxide dismutase, catalase and glutathione peroxidase improves quality of cooled stored stallion semen / C. D. Prete, T. Stout, S. Montagnaro [et al.] // Animal Reproduction Science. – 2019. – Vol. 210. – P. 106195.


