Алгоритм лучевой диагностики очаговых изменений скелета у пациентов с верифицированным злокачественным новообразованием
Автор: Сергеев Н.И., Котляров П.М., Солодкий В.А.
Журнал: Вестник Российского научного центра рентгенорадиологии Минздрава России @vestnik-rncrr
Рубрика: Лучевая диагностика
Статья в выпуске: 2 т.19, 2019 года.
Бесплатный доступ
Целью исследования является создание универсального алгоритма диагностики очаговых образований костных структур у больных с верифицированным злокачественным новообразованием. Проанализированы данные 80 больных с очаговыми изменениями в костях количеством 265 и минимальным размером очага 1 см. Методами обследования являлись мультипараметрическая магнитно-резонансная томография, выполненная с 86 применением модифицированного протокола сканирования, однофотонно-эмиссионная компьютерная томография, совмещённая с компьютерной томографией. Исследования проводились перед началом химио-лучевого лечения, через 1 месяц после начала терапии, далее через каждые 3 месяца сроком не менее 1 года. На основании анализа и статической обработки определены референсные значения и диагностическая информативность каждого метода. Сформулированы показания и противопоказания в зависимости от характера и локализации метастатического поражения. Предложенный алгоритм обследования может применяться в лечебных учреждениях онкологического и общего профиля, оснащенных необходимым оборудованием. Данный подход позволяет сэкономить ресурсы ЛПУ, повысить точность ранней диагностики костных метастазов за счет более эффективного использования имеющихся методов обследования.
Онкология, метастазы в кости, лучевая диагностика
Короткий адрес: https://sciup.org/149132100
IDR: 149132100
Algorithm of radiation diagnostics of focal lesions in the skeleton of patients with verified malignant neoplasm
The purpose of the study is to create a universal algorithm for diagnosing focal lesions of bone structures in patients with verified malignant neoplasm. The data of 80 patients with focal changes in the bones with the number of 265 and the minimal size of the focus of 1 cm were analyzed. Multiparameter magnetic resonance imaging, performed with the use of a modified scanning protocol, single-photon emission computed tomography, combined with computed tomography were used. The studies were carried out before the chemoradiation treatment, one month after the start of therapy, then every three months for at least one year. Based on the analysis and statistical evaluation, reference values and diagnostic information for each method were determined. Indications and contraindications are formulated depending on the nature and localization of metastatic lesions. The proposed survey algorithm can be used in medical institutions, which are equipped with the necessary instrumentation. This approach allows to save resources of medical institutions and to improve the accuracy of early diagnosis of bone metastases due to more effective use of existing survey methods.
Текст научной статьи Алгоритм лучевой диагностики очаговых изменений скелета у пациентов с верифицированным злокачественным новообразованием
Список сокращений
МРТ – магнитно-резонансная томография мпМРТ – мультипараметрическая магнитно-резонансная томография
МСКТ – мультиспиральная компьютерная томография
ОСГ – остеосцинтиграфия
ОФЭКТ/КТ – однофотонно-эмиссионная компьютерная томография, совмещенная с компьютерной томографией
Т1ВИ, Т2ВИ, STIR – основные импульсные последовательности, используемые при магнитно-резонансной томографии
ДКУ – динамическое контрастное усиление
ДВИ – диффузионно-взвешенные изображения
ИКД – измеряемый коэффициент диффузии
РФП – радиофармпрепарат
КДН – коэффициент дифференцированного накопления
Введение
Стремительное развитие медицинских технологий обусловливает совершенствование и модернизацию известных методов диагностической визуализации, появление новых. Так, перспективным направлением является развитие гибридных диагностических технологий, которые сочетают в себе данные о функциональном состоянии органов и тканей с привязкой к анатомическим изображениям [5]. В результате формируются большие блоки диагностических данных, что затрудняет их интерпретацию и применение на практике врачами клинических специальностей. Это обусловливает необходимость создания четких и универсальных алгоритмов обследования, объективно учитывающих диагностические возможности методов, их слабые и сильные стороны [11]. В равной степени это относится и к оценке результатов проводимого комбинированного или комплексного лечения онкологических больных с изменениями в костях, т. к. позволяет объективно оценить эффект и избежать проведения необоснованных или дублирующих исследований [7, 14]. Актуальность проблемы объясняется тем, что ранняя и точная диагностика костных изменений у пациентов с предполагаемым или верифицированным злокачественным новообразованием позволяет выработать оптимальную лечебную тактику, значительно повышая эффективность и результаты специализированного лечения [8, 13].
Цель исследования. Разработать универсальный алгоритм применения современных методов медицинской визуализации для достоверного определения характера костного поражения у пациентов с верифицированным злокачественным новообразованием.
Материалы и методы
В работу включены результаты обследования 80 больных с очаговым поражением скелета, с морфологически верифицированным первичным злокачественным новообразованием различной степенью дифференцировки, из которых рак молочной железы определялся у 36 больных, рак предстательной железы – у 21, рак легкого – у 12, рак почки – у 11.
Период наблюдения не менее 12 месяцев, в течение которого проводились субъективная и объективная оценки эффекта от консервативной терапии, позволил достоверно подтвердить характер наблюдаемых костных изменений у исследуемой группы больных. В результате наличие метастатического поражения было установлено у 64 больных, из которых у 17 больных определялись также и разноплановые неспецифические изменения. У 16 больных метастатическое поражение костно-суставной системы подтверждено не было.
Ввиду множественности поражения, в работе анализировались несколько очаговых изменений или очагов наблюдения (ОН) у каждого больного. Таким образом, общее количество (ОН) составило 265, из которых метастатические изменения составляли 219, а неметастатические – 46 ОН. Неспецифические изменения были представлены дегенеративно-дистрофическими изменениями (14 больных), посттравматическими изменениями (10 больных), гемангиомами (9 больных).
Всем больным выполнялась магнитно-резонансная томография на 1,5 Т аппарате, с использованием диффузионно-взвешенных изображений и модифицированного протокола «РНЦРР» (с) динамического контрастного усиления с введением 15-20 мл парамагнетика с помощью двух-колбового автоматического шприца. Проведение однофотонноэмиссионной компьютерной томографии подразумевает обязательное выполнение на первом этапе стандартной 2-х мерной остеосцтинграфии с использованием моно- и дифосфатов Тс-99м активностью 370-600 МБк. После этого, всем пациентам проводилась однофотонно-эмиссионная компьютерная томография, с выполнением компьютерной томографии на зону интереса.
Результаты
На основании сочетанного анализа данных обследования 64 больных (219 ОН), остеолитический тип с наличием деструктивных изменений определялся в 136 очагах наблюдения, остеобластический тип в 27 наблюдениях, а смешанный характер поражения в 56.
На основании полученных данных был произведен расчет диагностической информативности методов, полученные результаты представлены в таблице 1.
Таблица 1. Показатели операционных характеристик изучаемых методов исследования в оценке очаговых изменений костей
|
Чувствительность |
Специфичность |
Точность |
|
|
МРТ |
96,3% (211/219) |
97,8% (45/46) |
97,05% |
|
МСКТ |
92,2% (202/219) |
71,7% (33/46) |
81,95% |
|
ОСГ |
97,2% (213/219) |
63% (29/46) |
80,1% |
|
ОФЭКТ/КТ |
98,6% (216/219) |
84,8% (39/46) |
91,7% |
С учетом проведенного анализа причин ложно-положительных и ложноотрицательных результатов 80 больных с 265 изменениями в костях был сделан вывод о различной диагностической информативности методов в зависимости от характера и локализации поражения. На основании этого предложен алгоритм дифференцированного подхода к использованию лучевых методов при диагностике очаговых образований костных структур, в зависимости от характера течения патологического процесса. Были сформулированы основные показания к проведению исследований, которые могут быть представлены в следующем виде.
-
I. Мультипараметрическая МРТ наиболее эффективна:
-
1. При инфильтративно-диффузном поражении костного мозга, что обусловлено наилучшей визуализацией жидкость-содержащих объектов. При наличии межтрабекулярной инфильтрации без выраженного разрушения костных трабекул и реактивного усиления костного метаболизма МСКТ может давать ложноотрицательные результаты, ввиду перекрытия более высокой плотностью костной ткани менее плотных участков костного мозга.
-
2. При оценке экстраоссальных мягкотканых компонентов, т.к. МРТ обладает наилучшей способностью дифференцировать мягкие ткани, позволяет наиболее точно определить размеры внекостного поражения, оценить местную распространённость неопластического процесса, взаимоотношение с окружающими органами и тканями.
-
3. При остеолитическом и смешанном типе поражения черепа, позвоночного столба, костей таза, конечностей, что определяется наиболее четкой визуализацией на большинстве магнитно-резонансных томографов, не имеющих современных эффективных методик уменьшающих влияние динамической нерезкости на изображениях (например, DWIBS).
-
4. При отсутствии выраженного болевого синдрома (до 7–8/10 баллов), что обусловлено техническим регламентом проведения МР-исследования и необходимостью
соблюдать неподвижное положение больного в течение всего исследования. Данная проблема может быть решена проведением внутривенной премедикации с целью временного купирования болевого синдрома, однако это не всегда возможно по различным причинам.
-
II. Мультиспиральная компьютерная томография наиболее эффективна:
-
1. При предполагаемом остеобластическом или смешанном характере поражения мелких костей грудной клетки, верхнего плечевого пояса, осевого скелета (Микро-КТ). Физические основы метода позволяют хорошо дифференцировать мелкие костные структуры на фоне окружающих мягких тканей. В то же время на фоне системного остеопороза данные компьютерной томографии могут давать ложно-отрицательные результаты мелких остеолитических очагов.
-
2. При выраженном болевом синдроме (более 7–8/10 баллов), что объясняется быстрым временем выполнения КТ-исследования, отсутствием необходимости дополнительной седации пациента.
-
3. Является методом выбора при подозрении на наличие патологических переломов, позволяя достоверно визуализировать внутреннюю структуру кости, которая может быть скрыта выраженным отеком, затрудняющим оценку по данным магнитнорезонансной томографии.
-
4. МСКТ является методом контроля у больных с обширным остеолитическим поражением при проведении вертебропластики с использованием «костного цемента», позволяет наиболее достоверно оценить постоперационные результаты.
-
III. Остеосцинтиграфия наиболее целесообразна:
-
1. При опухолях с преимущественно остеобластическим поражением, что обусловлено физическими принципами метода, основанного на включении меченых фосфатов в метаболизм костной ткани. Таким образом, повышенная активность остеобластов вне зависимости от этиологии приводит к увеличению фиксации радиометки в сравнении с неизменным аналогичным участком, в то время как при остеолитических,
-
2. При безболевом течении метастатического процесса, т.к. позволяет обнаруживать очаги поражения на доклинической стадии на всем протяжении костно-суставной системы.
-
3. При подозрении на локализацию очагов в добавочном скелете (верхние и нижние конечности), т.к. эти локализации попадают в поле обзора других методов только при прицельных исследованиях.
деструктивных процессах с замедленной или не выраженной реакцией активность остеобластов снижена, что может приводить к ложно-отрицательным результатам.
-
IV. ОФЭКТ как метод диагностики оправдана:
-
1. При недостаточности данных планарной остеосцинтиграфии, т.к. за счет большего пространственного разрешения позволяет детализировать картину и более достоверно оценить характер фиксации радиометки.
-
2. При предполагаемой локализации поражения в костях таза, т.к. за счет трехмерной модели изображения позволяет снизить количество ложно-отрицательных результатов, обусловленных перекрытием «засветкой» мочевого пузыря в экскреторную фазу.
Представленные дифференцированные показания применения методов в первичной диагностике очаговых образований скелета позволяют наиболее эффективно определить первоначальное исследование. Так, например, при наличии локального болевого синдрома у пациентов с верифицированным ЗНО, в первую очередь, рекомендуется выполнение прицельной магнитно-резонансной томографии, а не остеосцинтиграфии. Это объясняется тем, что по данным ОСГ возможно получение пограничных значений уровня фиксации радиофармпрепарата, что будет являться недостаточным для достоверной постановки диагноза, и потребует дальнейшего выполнения ОФЭКТ/КТ или мпМРТ. В то же время при отсутствии болевого синдрома четких показаний для проведения прицельной МСКТ или МРТ нет, а выполнение этих методов в режиме «все тело» весьма затратно и не всегда возможно. При этом, безусловно, на практике встречаются наблюдения, когда данных одного любого метода может быть недостаточно – плохое качество изображений по тем или иным причинам, мелкие размеры образований, длительный хронический анамнез со стороны костносуставной системы и др. В подобных ситуациях целесообразно проведение дополнительных диагностических исследований с учетом разработанных критериев эффективности методов.
В качестве примера приводим наблюдение пациентки В, 1948 г.р. с диагнозом светлоклеточный рак почки. В связи с выраженным болевым синдром в поясничной области до 7 баллов по 10-бальной шкале больной выполнена остеосцинтиграфии. По данным ОСГ в левых отделах L5 позвонка определяется умеренно повышенный процент фиксации РФП (до 135%), однако достоверно поставить диагноз метастатического поражения представляется затруднительным. Также имеется очаг накопления в теле Th11 до 125%. Для уточнений выявленных изменений пациентке выполнена мультиспиральная компьютерная томография, при которой определяется значимая литическая деструкция тела L5 позвонка в связи с наличием патологического перелома и компрессией прилежащих структур, а также литический очаг в теле Th11 (Рис. 1).
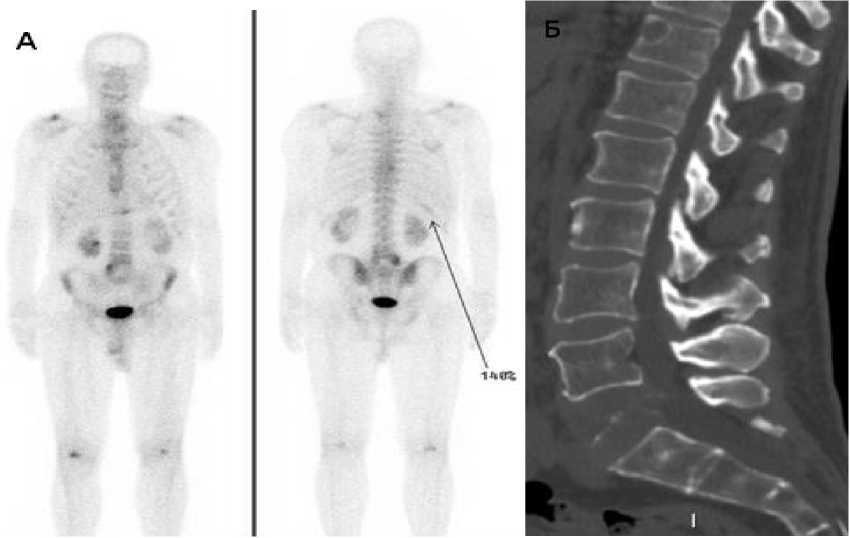
Рисунок 1. Пациентка В., 1948 г.р. с диагнозом светлоклеточный рак почки, метастатическое поражение костей. По данным остеосцинтиграфии (А) в проекции L5 отмечается участок сниженного накопления в центре с повышенной фиксацией РФП в правых отделах (КДН 135%). По данным МСКТ (Б) отмечается полная деструкция L5 с наличием мягкотканого компонента, литический очаг в передних отделах в Th11, также не видимый при ОСГ.
Приведённый клинический пример показывает возможность сокращения алгоритма обследования за счет выполнения компьютерной или магнитно-резонансной томографии в первую очередь на место болевого синдрома. Эти данные позволят выявить причину болевого синдрома и достоверно поставить диагноз «метастатическое поражение костей», после которых дополнительные исследования не требуются.
Обсуждение
Сформулированный подход позволяет максимально эффективно использовать арсенал имеющихся методов обследования в решении вопросов дифференциальной диагностики очаговых изменений скелета. Сокращение количества необоснованных и дублирующих обследований костно-суставной системы при подозрении на метастатическое поражение позволяет сэкономить ресурсы ЛПУ и уменьшить временной интервал в определении тактики лечения.
Список литературы Алгоритм лучевой диагностики очаговых изменений скелета у пациентов с верифицированным злокачественным новообразованием
- Асланиди И.П., Пурсанова Д.М., Мухортова О.В. и др. Диагностика рецидива рака предстательной железы по данным ПЭТ/КТ С 11С-ХОЛИНОМ у пациентов после радикальной простатэктомии. Медицинская радиология и радиационная безопасность. 2015. T. 60. № 5. С. 50-58.
- Долгушин М.Б., Котельникова Т.М., Пронин И.Н. и др. Исследование всего тела у больных с метастазами в головной мозг: МР-ДВИ, ПЭТ и ОФЭКТ/КТ. Вестник рентгенологии и радиологии. 2009. № 4-6. С. 58-64.
- Линденбратен Л.Д., Королюк И.П. Медицинская радиология (основы лучевой диагностики и терапии). Москва, «Медицина». 2000. 425 с.
- Петриев В.М., Тищенко В.К., Красикова Р.Н. 18-F-ФДГ и другие меченые производные глюкозы для использования в радионуклидной диагностике онкологических заболеваний (обзор). Химико-фармацевтический журнал. 2016. № 4. С. 3-14.
- Сергеев Н.И., Фомин Д.К., Котляров П.М., Солодкий В.А. Сравнительное исследование возможностей ОФЭКТ/КТ и магнитно-резонансной томографии всего тела в диагностике костных метастазов. Вестник РНЦРР. 2015. № 3. http://vestnik.rncrr.ru/vestnik/v15/papers/sergeev_v15-3.htm (дата доступа 19.06.2019).
- Сергеев Н.И., Нуднов Н.В. Дифференциальная диагностика доброкачественных и злокачественных поражений позвоночника по данным магнитно-резонансной томографии с использованием болюсного контрастного усиления. Вестник РНЦРР. 2012. № 12-4. http://vestnik.rncrr.ru/vestnik/v12/papers/sergeev_v12.htm (дата доступа 19.06.2019).
- Тепляков В.В. Шапошников А.А., Лазукин А.В. Частота востребованности хирургического компонента в комплексном лечении метастатического поражения костей. Саркомы костей, мягких тканей и опухоли кожи, 2016. № 1. С. 16-28.
- Andronis L., Goranitis I., Bayliss S., Duarte R. Cost-Effectiveness of Treatments for the Management of Bone Metastases: A Systematic Literature Review. Pharmacoeconomics. 2018. V. 36. No. 3. P. 301-322.
- DOI: 10.1007/s40273-017-0595-0
- Evangelista L., Bonavina M.G., Bombardieri E. Clinical results and economic considerations of 68Ga-PSMA and radiolabeled choline in prostate cancer. Nucl Med Biol. 2017. V. 50. P. 47-49.
- Giovacchini G., Giovannini E., Leoncini R., et al. PET and PET/CT with radiolabeled choline in prostate cancer: a critical reappraisal of 20 years of clinical studies. Eur J Nucl Med Mol Imaging. 2017. V. 44. No. 10. P. 1751-1776.
- Grimm L.J., Zhang J, Baker JA, et al. Relationships Between MRI Breast Imaging- Reporting and Data System (BI-RADS) Lexicon Descriptors and Breast Cancer Molecular Subtypes: Internal Enhancement is Associated with Luminal B Subtype. Breast J. 2017. V. 23. No. 5. P. 579-582.
- Lapa P., Marques M., Costa G., Lima J.P. The value of quantitative analysis in 18F-NaF PET/CT. Rev Esp Med Nucl Imagen Mol. 2017.V. 36. No. 2. P. 78-84.
- Klaff R., Berglund A., Varenhorst E., et al. Clinical characteristics and quality-of-life in patients surviving a decade of prostate cancer with bone metastases. BJU Int. 2015. V. 117. No. 6. P. 904-913.
- DOI: 10.1111/bju.13190
- Tatar Z., Soubrier M., Dillies A.F., et al. Assessment of the risk factors for impending fractures following radiotherapy for long bone metastases using CT scan-based virtual simulation: a retrospective study. Radiat Oncol. 2014. V. 9. P. 227. 10.1186/s13014- 014-0227-1.
- DOI: 10.1186/s13014-014-0227-1


