Анализ комбинированных сочетаний флуоксетина и психотропных лекарственных средств методом микроколоночной жидкостной хроматографии
Автор: Лазицкая А.М., Чмелевская Н.В., Илларионова Е.А., Давыдов А.К.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: В помощь практическому врачу
Статья в выпуске: 3 т.32, 2017 года.
Бесплатный доступ
Вопрос идентификации лекарственных средств в химико-токсикологических и судебно-химических исследованиях всегда является актуальным, а в психиатрии приобретает особенную остроту, так как люди с психическими болезнями часто злоупотребляют психотропными препаратами. Антидепрессанты нашли широкое применение в психиатрической практике. Флуоксетин - бициклический антидепрессант, производное фенилалкиламина, назначается индивидуально и в сочетании с другими сильнодействующими лекарственными средствами (ЛС). В данной статье предложены оптимальные условия анализа комбинированных сочетаний флуоксетина с тофизопамом, сульпиридом, рисперидоном, хлорпромазином, хлорпротиксеном, имипрамином, буспироном, бромдигидрохлор-фенилбензодиазепином. Представлены условия идентификации флуоксетина и психотропных ЛС из модельных смесей после извлечения их из мочи методом высокоэффективной жидкостной хроматографии (ВЭЖХ) на приборе «Милихром А-02».
Флуоксетин, тофизопам, хлорпромазин, буспирон, бромдигидрохлорфенилбензодиазепин, рисперидон, хлорпротиксен, сульпирид, имипрамин, высокоэффективная жидкостная хроматография, комбинированные сочетания, сhlorprotiхen
Короткий адрес: https://sciup.org/149125176
IDR: 149125176 | DOI: 10.29001/2073-8552-2017-32-3-83-87
Analysis of combinations of fluoxetine and psychotropic drugs by the method of microcolumn liquid chromatography
The question of identification of medicines in chemical-Toxicological forensic chemical and the research is always relevant, and in psychiatry is particularly important because people with mental illnesses are often abused with psychotropic drugs. Antidepressants found wide application in psychiatric practice. Fluoxetine a bicyclic antidepressant that is derived fenilalkilamina, prescribed individually or in combination with other potent drugs. In this article we propose the optimal conditions for the combined analysis of the combination of fluoxetine with tofizopama, sulpiride, risperidone, chlorpromazine, chlorprothixene, imipramine, buspirone, bromdihydrochlorphenylbenzodiazepin. The conditions of chromatographically proposed methodology in the identification of fluoxetine and psychotropic medicines from model compounds after their extraction from urine by high-performance liquid chromatography on device “Milichrom A-02” are presented.
Текст научной статьи Анализ комбинированных сочетаний флуоксетина и психотропных лекарственных средств методом микроколоночной жидкостной хроматографии
Психотропные средства используются при лечении больных с психическими патологиями, устойчивыми к традиционным методам терапии, а также при оказании паллиативной помощи, когда клиническая симптоматика больного представлена сложным психопатологическим синдромом [1, 2]. Психотропные средства применяются как самостоятельно, для купирования соответствующих психических расстройств, так и в качестве адъювантных (вспомогательных) средств в составе комплексного лечения хронического болевого синдрома различной этиологии [1–4]. В этом случае на первый план выступают анальгетические свойства некоторых психотропных средств. Эти эффекты способствуют увеличению диапазона терапевтического действия классических анальгетиков. Рациональные комбинации с психотропными средствами позволяют снижать дозировку основного обезболивающего препарата. Этим достигается лучший контроль над побочными действиями, присущими многим традиционным анальгетикам.
К основным группам психотропных средств, использующихся при оказании психиатрической и паллиативной помощи, относятся антидепрессанты, анксиолитики и нейролептики [2, 5]. Наиболее часто у терминальных больных наблюдаются такие психические отклонения, как бессонница, депрессия, делирий и тревожные расстройства. Медикаментозная коррекция нарушений сна проводится препаратами бензодиазепинового ряда (тофизопам, бромдигидрохлорфенилбензодиазепин, клоназепам); чистыми гипнотиками (золпидем, зопи-клон); антидепрессантами (флуоксетин, имипрамин). При тяжелых формах делирия у терминальных больных используются нейролептики (сульпирид, рисперидон, хлорпромазин, хлорпротиксен) [5]. Пациенты с психическими болезнями и болевым синдромом часто злоупотребляют психотропными препаратами, что может привести к соматическим осложнениям — интоксикации, абстинентному синдрому, смерти [6].
В судебно-химической практике встречаются случаи отравления флуоксетином [6, 7] непосредственно, а также в сочетании с психотропными препаратами, такими как тофизопам, бромдигидрохлорфенилбензодиазепин, хлорпромазин, рисперидон, хлорпротиксен, буспи-рон, сульпирид, имипрамин. Отравления препаратами этой группы занимают 3-е место среди отравлений ЛС, а в психиатрической практике их удельный вес составляет примерно 15% [8]. Кроме того, эти препараты включены в «Перечень наименований токсичных веществ, наиболее часто встречающихся при острых отравлениях» [9]. В литературе есть данные о химико-токсикологическом анализе производных фенилалкиламина, в том числе флуоксетина [7], однако сведения о химико-токсикологическом анализе флуоксетина в сочетании с другими психотропными лекарственными средствами отсутствуют.
В связи с расширением списка определяемых веществ и увеличением числа комбинированных отравлений возрастает важность вопроса о чувствительности методики идентификации лекарственных веществ и ее избирательности. Соответственно, разработка методики химико-токсикологического анализа, основанной на использовании современных инструментальных методов исследования, является актуальной проблемой.
В качестве объектов исследования в данной работе использовали трехкомпонентные сочетания флуоксетина с транквилизаторами (бромдигидрохлорфенилбен-зодиазепин, тофизопам, буспирон), нейролептиками (сульпирид, рисперидон, хлорпромазин, хлорпротиксен) и антидепрессантом (имипрамин).
Цель настоящего исследования: разработка методики обнаружения и идентификации флуоксетина в сочетании с другими психотропными веществами из модельных смесей с использованием метода микроколоночной ВЭЖХ.
Этот метод позволяет одновременно определять несколько соединений, отличается достаточной точностью и воспроизводимостью. Однако внедрение ВЭЖХ в практику ограничено из-за отсутствия унифицированных методик анализа. Это приводит к увеличению продолжительности всего анализа и существенно повышает стоимость анализа. Решение проблемы — разработка максимально унифицированных, экономичных и экспрессных методик для одновременного определения больших групп лекарственных веществ [10].
Материал и методы
В работе использовали микроколоночный жидкостный хроматограф «Милихром А-02» (ЗАО «ЭкоНова», Новосибирск, Россия), снабженный стальной колонкой размером 02х75 мм, заполненной сорбентом ProntoSIL-120-5-C18 AQ (Bischoff Anal. GmbH, Германия). Температура 40 °С.
Для приготовления элюентов и растворения образцов использовали: ацетонитрил «осч» (сорт 1) фирмы «Криохром» (Санкт-Петербург); лития перхлорат, спирт метиловый, воду очищенную, хлорную кислоту квалификации не ниже «хч».
Спирт метиловый перегоняли перед использованием. Вода дополнительно была очищена с помощью системы Norganic, Millipore Corporation (США).
В качестве стандартных веществ были использованы растворы субстанций флуоксетина, тофизопама, бром-дигидрохлорфенилбензодиазепина, хлорпромазина, рисперидона, хлорпротиксена, буспирона, сульпири-да, имипрамина в спирте метиловом с концентрацией 0,5 мг/мл.
Статистическую обработку результатов исследования проводили в соответствии с требованиями ГФ ХIII издания, том 1, ОФС 1.1.0013.15 «Статистическая обработка результатов химического эксперимента» [11]. Обработку полученных хроматограмм проводили с использованием программ «Милихром А-02» и «Альфахром» с базой данных БД-2003-500.
Исследования проводили на модельных смесях флуоксетина с психотропными препаратами.
Результаты и обсуждение
Нами, в судебно-химическом отделении Областного бюро судебно-медицинской экспертизы г. Иркутска, в качестве одного из методов идентификации и количественного определения лекарственных веществ в анализируемой пробе используется метод ВЭЖХ на микроко-лоночном жидкостном хроматографе «Милихром А-02» с УФ-детектором. Для анализа используется колонка с обращенно-фазным сорбентом ProntoSil-120-5-C18 AQ с термостатированием, размер 75х2 мм. В качестве подвижной фазы используется смесь перхлората лития, воды и ацетонитрила — А: [4M LiClO4 — 0,1M HClO4] — H2O (1:19); B: ацетонитрил; скорость потока элюента 100 мкл/ мин, температура 40,0 °C. Данные условия не позволяют достоверно разделить и идентифицировать флуоксетин в сочетании с другими психотропными ЛС. Поэтому для анализа таких комбинированных сочетаний был экспериментально подобран обращенно-фазный вариант хроматографии с градиентным элюированием, режим элюирования 3700 мкл от 5% Б до 70% Б в системе: элюент А: 0,2 M LiClO4 — 0,005 M HClO4 (рН 2,8); элюент Б — ацетонитрил. Объем пробы варьировался от 2 до 4 мкл.
На рисунке 1 приведена хроматограмма девятикомпонентной модельной смеси раствора флуоксетина с психотропными ЛС.
Пики исследуемых веществ в предложенном элюенте достаточно симметричны. Свидетельством этого являются значения коэффициентов асимметрии, рассчитанные на уровне 10% высоты пиков, которые близки к единице. Таким образом, данная хроматографическая система «сорбент-элюент» является оптимальной для анализа исследуемых лекарственных веществ.
Наглядно видно, что все исследуемые соединения отделяются друг от друга практически до базовой линии. Таким образом, показано, что предложенная форма градиента позволяет определять любые сочетания исследуемых соединений.
Детектирование исследуемых веществ осуществляли в интервале длин волн 190–360 нм с шагом 2 нм, базовая длина волны для нормирования спектра — 210 нм (длина волны максимального поглощения или близкая к ней).
Длины волн максимального и минимального поглощения исследуемых веществ представлены в таблице 1.
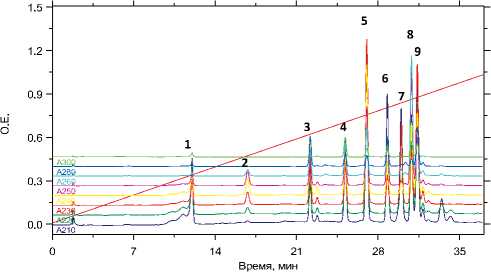
Рис. 1. Хроматограмма стандартного раствора смеси веществ в спирте метиловом
Примечание: Пики: 1 — сульпирид; 2 — рисперидон; 3 — бу-спирон; 4 — тофизопам; 5 — бромдигидрохлорфенилбензо-диазепин; 6 — имипрамин; 7 — флуоксетин; 8 — аминазин; 9 — хлорпротиксен.
Таблица 1
Длины волн максимального и минимального поглощения
|
Определяемое соединение |
λ мах, нм |
λ мin, нм |
|
Аминазин |
256 , 310 |
226, 280 |
|
Имипрамин |
252 |
плато 210, 232 |
|
Рисперидон |
238 , 274 |
222, 256 |
|
Буспирон |
212 , 238, 300 |
224, 264 |
|
Сульпирид |
212 , 294 |
плато 230, 268 |
|
Тофизопам |
208 |
плато 230, 280 |
|
Бромдигидрохлорфенилбензо-диазепин |
230 , 314 |
214, плато 292 |
|
Флуоксетин |
228 , 264 |
218, 248 |
|
Хлорпротиксен |
206 , 230, 270, 330 |
218, 254, 310 |
Идентификацию веществ проводили по временам удерживания и спектральным отношениям (табл. 2). Спектральные отношения для исследуемых соединений рассчитывали как отношение площадей пиков, зарегистрированных при длинах волн λх и λ210.
Таблица 2
Спектральные отношения для исследуемых соединений, растворитель: СН3CN – 0,2 М LiClO4 (pH 2,8)
|
№ |
Определяемое вещество |
Время удерживания, TR, мкл; n=10 |
Спектральное отношение, |
А( λ х)/А( λ 210) |
|||||
|
А220/А210 |
А230/А210 |
А240/А210 |
А250/А210 |
А260/А210 |
А280/А210 |
А300/А210 |
|||
|
1 |
Аминазин |
3121 |
0,635 |
0,523 |
0,676 |
1,111 |
1,125 |
0,062 |
0,148 |
|
2 |
Имипрамин |
2907 |
0,602 |
0,230 |
0,260 |
0,340 |
0,308 |
0,223 |
0,080 |
|
3 |
Рисперидон |
2226 |
0,506 |
0,772 |
0,938 |
0,579 |
0,474 |
0,541 |
0,032 |
|
4 |
Буспирон |
2298 |
0,867 |
1,083 |
1,383 |
0,520 |
0,042 |
0,072 |
0,156 |
|
5 |
Сульпирид |
1212 |
0,740 |
0,389 |
0,349 |
0,198 |
0,043 |
0,045 |
0,058 |
|
6 |
Тофизопам |
2568 |
0,677 |
0,474 |
0,454 |
0,451 |
0,404 |
0,145 |
0,243 |
|
7 |
Бромдигидрохлорфе-нилбензодиазепин |
2741 |
1,002 |
1,067 |
0,840 |
0,508 |
0,305 |
0,060 |
0,055 |
|
8 |
Флуоксетин |
3024 |
0,714 |
0,740 |
0,153 |
0,048 |
0,080 |
0,043 |
0,009 |
|
9 |
Хлорпротиксен |
3133 |
0,805 |
1,023 |
0,599 |
0,351 |
0,352 |
0,286 |
0,097 |
Проведена валидационная оценка разработанной методики. Условия пригодности хроматографической системы соблюдены. Предложенные нами условия хроматографирования использованы для разработки методики идентификации флуоксетина в сочетании с психотропными ЛС в извлечениях из мочи.
Методика идентификации комбинированных сочетаний флуоксетина и психотропных ЛС методом ВЭЖХ после извлечения их из мочи: в колбу вместимостью 100 мл вносят 50 мл мочи, содержащей смесь исследуемых веществ, настаивают в течение 2 ч при комнатной температуре, периодическом перемешивании и обработке на ультразвуковой бане RК 100 Bandelin electronic (Германия). Полученный раствор переносят в делительную воронку, добавляют 0,1 М раствор хлористоводородной кислоты до рН=4,0 и 20 мл хлороформа, затем проводят экстракцию двукратно в течение 20 мин. Хлороформные извлечения упаривают на водяной бане досуха, сухой остаток растворяют в 20 мл спирта метилового. Полученный раствор вводят в колонку в объеме 2 мкл. Хроматографируют анализируемый раствор в следующих условиях: градиентное элюирование 3700 мкл от 5% Б до 70% Б в системе: элюент А: 0,2 M LiClO4 – 0,005 M HClO4 (рН 2,8); элюент Б — ацетонитрил.
Результаты хроматографического анализа исследуемых соединений после извлечения их из мочи в предложенных условиях статистически обработаны и представлены в таблице 3.
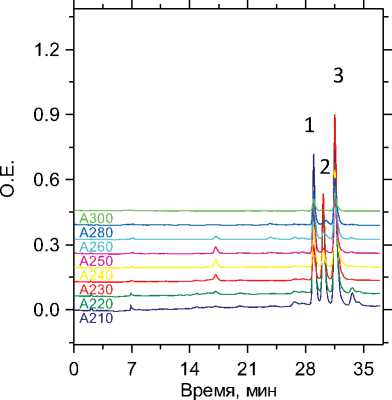
Рис. 2. Хроматограмма извлечения из мочи, пики: 1 — имипра-мин; 2 — флуоксетин; 3 — хлорпротиксен
Таблица 3
Время удерживания исследуемых соединений после извлечения их из мочи
|
Соединение |
Время удерживания, мин |
Метрологические характеристики (n=6) |
|
Аминазин |
31,21; 31,20; 31,22 31,22; 31,20; 31,23 |
X = 31,21; S X = 0,0052; ∆Х= 0,0133; Е = 0,04% |
|
Имипрамин |
29,07; 29,06; 29,08 29,06; 29,07; 29,06 |
X = 29,07; SX= 0,0037; ∆Х= 0,009; Е = 0,03% |
|
Рисперидон |
22,26; 22,27; 22,25 22,26; 22,24; 22,25 |
X = 22,26; SX= 0,0049; ∆Х= 0,0126; Е = 0,06% |
|
Буспирон |
22,98; 22,97; 22,98 |
X = 22,98; S X = 0,0047; |
|
22,96; 22,97; 22,99 |
∆Х= 0,012; Е = 0,05% |
|
|
Сульпирид |
12,12; 12,14; 12,13 |
X = 12,13; S X = 0,0061; |
|
12,12; 12,15; 12,11 |
∆Х= 0,0156; Е = 0,12% |
|
|
Тофизопам |
25,68; 25,67; 25,66 25,67; 25,66; 25,67 |
X = 25,67; S X = 0,0034; ∆Х= 0,0081; Е = 0,03% |
|
Бромдигидрохлорфе- |
27,41; 27,42; 27,40 |
X = 27,41; SX= 0,0036; |
|
нилбензодиазепин |
27,42; 27,41; 27,42 |
∆Х= 0,009; Е = 0,03% |
|
Флуоксетин |
30,24; 30,25; 30,23 |
X = 30,24; SX = 0,0038; |
|
30,24; 30,23; 30,25 |
∆Х= 0,008; Е = 0,04% |
|
|
Хлорпротиксен |
31,33; 31,32; 31,30 31,32; 31,33; 31,31 |
X = 31,32; S X = 0,0048; ∆Х= 0,0123; Е = 0,04% |
Примечание: X — среднее значение из n-определений; S X — стандартное отклонение среднего результата; DХ — абсолютная ошибка среднего арифметического; Е — относительная ошибка среднего результата.
На рисунках 2–6 приведены хроматограммы трехкомпонентных сочетаний флуоксетина с психотропными ЛС, полученные по разработанной методике. Видно, что все исследуемые вещества хорошо разделяются.
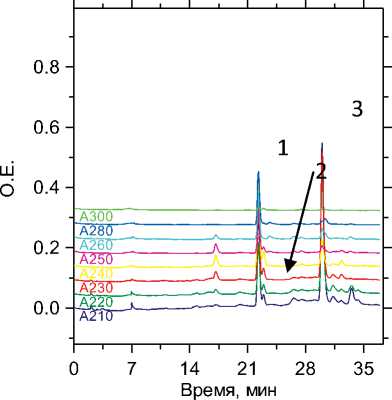
Рис. 3. Хроматограмма извлечения из мочи, пики: 1 — рисперидон, 2 — буспирон; 3 — флуоксетин
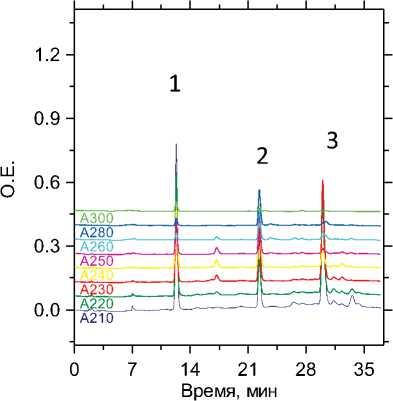
Рис. 4. Хроматограмма извлечения из мочи, пики: 1 — сульпи-рид; 2 — рисперидон; 3 — флуоксетин
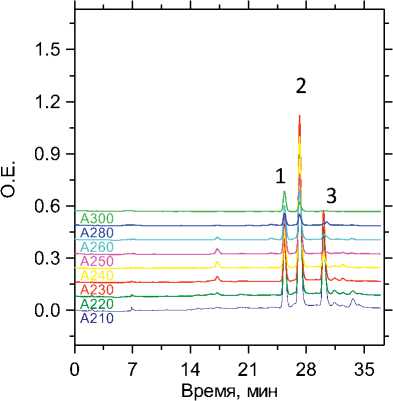
Рис. 5. Хроматограмма извлечения из мочи, пики: 1 — тофизопам; 2 — бромдигидрохлорфенилбензодиазепин; 3 — флуоксетин
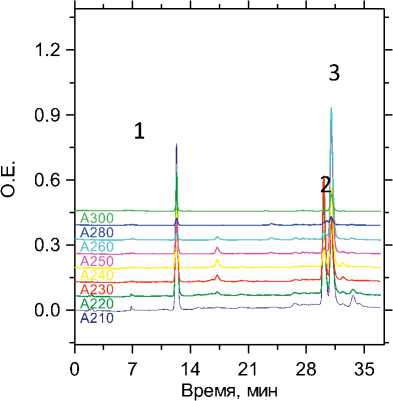
Рис. 6. Хроматограмма извлечения из мочи, пики: 1 — сульпи-рид; 2 флуоксетин; 3 — хлорпромазин
Выводы
На основании вышеизложенного можно сделать вывод, что предложенная методика позволяет идентифицировать флуоксетин в извлечениях из мочи как индивидуально, так и в сочетании с психотропными ЛС (тофизопамом, хлорпромазином, рисперидоном, хлорпротиксеном, буспироном, сульпиридом, имипра-мином, бромдигидрохлорфенилбензодиазепином). Следовательно, подобранные условия оптимальны, а методика унифицирована, что позволяет использовать метод ВЭЖХ для обнаружения флуоксетина и психотропных ЛС в комбинированных сочетаниях.
Список литературы Анализ комбинированных сочетаний флуоксетина и психотропных лекарственных средств методом микроколоночной жидкостной хроматографии
- Клинические рекомендации. Хронический болевой синдром (ХБС) у взрослых пациентов, нуждающихся в паллиативной медицинской помощи. Утверждены на II конференции с международным участием «Развитие паллиативной помощи взрослым и детям». - М., 2016. - С. 55-56.
- Контроль симптомов в паллиативной медицине / Под ред. проф. Г.А. Новикова. - М.: ГЭОТАР-Медиа, 2013. - 248 с.
- Данилов А.Б., Данилов Ал.Б. Управление болью. Биопсихосоциальный подход. - М.: «АММ ПРЕСС», 2014. - 592 с.
- Камчатнов П.Р. Нейропатическая боль: проблемы и решения // Журнал «Нейро News: психоневрология и нейропсихиатрия». - 2009. - № 4 (15). - С. 36-39.
- Машковский М.Д. Лекарственные средства, 15-е изд., перераб., испр. и доп. - М.: Новая Волна, 2005. - 1200 с.
- Малин Д.И. Побочное действие психотропных средств. - М.: Вузовская книга, 2000. - 207 с.
- Казарцев И.А., Воронкова Л.Г. Химико-токсикологическое исследование препарата флуоксетин // Суд.-мед. экспертиза. - 2008. - Т. 51, № 4. - С. 31-35.
- Скорнякова А.Б., Лазарян Д.С., Цыбулина М.Г. Химико-токсикологический анализ галоперидола в желчи методом высокоэффективной жидкостной хроматографии при комбинированных отравлениях // Вестник ВГУ. - 2006. - № 2. - С. 368-370.
- Приказ МЗ РФ от 29.12.2000 г. № 460 «Об утверждении учетной документации токсикологического мониторинга».
- Федорова Г.А., Кожанова Л.А. Применение микроколоночной высокоэффективной жидкостной хроматографии // Сборник трудов "Хроматография на благо России". - 2007. - С. 666-684.
- Государственная Фармакопея, 13-е изд. - 2015. - Т. 1. - 1470 с.


