Анализ референтных доз химических соединений, поступающих перорально с питьевой водой
Автор: Богданова В.Д., Аленицкая М.В., Сахарова О.Б.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Оценка риска в гигиене
Статья в выпуске: 3 (43), 2023 года.
Бесплатный доступ
На современном этапе многими исследователями отмечена статичность методологии оценки риска в отечественных нормативных документах как в отношении характера воздействия веществ, так и в отношении значений референтных доз для химических соединений, поступающих перорально с питьевой водой. Проанализированы референтные дозы химических соединений, поступающих перорально с питьевой водой. Объект исследования - основной перечень показателей, характеризующий безвредность воды по химическому составу. Сравнительный анализ референтных доз химических соединений и их доказательной базы проведен на основе нормативных документов, открытой электронной базы данных о воздействии на здоровье химических веществ в окружающей среде «Информационная система по оценке рисков» и основополагающих статей. Для обобщения и визуализации результатов оценки комбинированного воздействия химических веществ на здоровье человека использовался MS Excel и инструмент по работе с графами. Общий временной интервал последних пересмотров референтных доз для включенных в исследование веществ составил с 1987 по 2012 г. Не все эффекты для здоровья, предложенные в российском руководстве по оценке риска, лежат в основе расчета референтных доз химических соединений и могут быть согласованы на международном уровне на сегодняшний день, так как не представлены с опорой на основополагающие исследования. Изменения в референтных дозах коснулись хлорорганических соединений (бромдихлорметан, тетрахлорэтилен, тетрахлорметан, трихлорэтилен), лития, кадмия, кобальта, железа и меди. Выявлены ограничения в определении пероральной референтной дозы железа и аммиака, которые принято рассматривать со стороны органолептического восприятия. Также нет адекватных данных токсикологических исследований, которые обосновывают референтные дозы для меди, магния, аммиака, свинца, кремния, брома, хрома при пероральном поступлении с питьевой водой, в силу различных обстоятельств. Рекомендовано учитывать полученные сведения о референтных дозах при планировании исследований влияния качества питьевой воды на здоровье населения с использованием методологии оценки риска в условиях пероральной экспозиции химических веществ.
Анализ, риск, питьевая вода, пероральное поступление, референтная доза, неканцерогенный риск, обзор, безвредность
Короткий адрес: https://sciup.org/142239919
IDR: 142239919 | УДК: 614.7 | DOI: 10.21668/health.risk/2023.3.05
Analysis of reference doses of chemicals introduced with drinking water
At present, many researchers highlight that the risk assessment methodology is rather static in Russian regulatory documents. This goes for both the essence of chemical exposures and reference doses stipulated for chemicals introduced into the body with drinking water. In this study, we aimed to analyze reference doses of chemicals introduced into the body with drinking water. Our research object was represented by the basic list of indicators that describe drinking water safety as per its chemical structure. Comparative analysis of reference doses of chemicals and their evidence base relied on the valid regulatory documents, Information System for Risk Assessment open-access electronic database on effects of environmental chemicals on health, and background research articles. The results obtained by assessing combined effects of chemicals on human health were generalized and visualized in MS Excel and a tool for working with graphs. The overall time period when reference doses of the analyzed chemicals were last revised was between 1987 and 2012. Not all health effects suggested in the Russian Guide on risk assessment are used as a basis for calculating reference doses of chemicals; hence, not all of them can be agreed upon on the international level at present since they do not rely on background research. Changes in reference doses occurred for chlorinated organic compounds (bromdichloromethane, tetrachloroethylene, tetrachloromethane, and trichloroethylene), lithium, cadmium, cobalt, iron, and copper. We identified certain limitations in establishing an oral reference dose of iron and ammonia, which are conventionally considered from organoleptic perception. Due to various reasons, we did not find any adequate data obtained by toxicological studies that would substantiate reference doses for copper, magnesium, ammonia, lead, silicon, bromine, and chromium under oral introduction with drinking water. We recommend considering our research data on reference doses when planning a study with its focus on impacts exerted by drinking water quality on public health and employing the risk assessment methodology to analyze oral chemical exposure.
Текст научной статьи Анализ референтных доз химических соединений, поступающих перорально с питьевой водой
Оценка риска здоровью остается важнейшей методологией, использующейся при принятии управленческих решений для защиты здоровья населения под воздействием факторов окружающей среды [1–3]. На настоящий момент накоплено большое количество данных об опыте практического применения оценки риска как с использованием отечественного руководства1 [4, 5], так и на международном уровне по стандартной методике Агентства по охране окружающей среды США [6–8]. Следует подчеркнуть, что, несмотря на различие названий опорных документов, обе методологии основаны на единых принципах и связаны долгосрочным сотрудничеством стран [9].
Несмотря широкую заинтересованность в данной методологии, соотечественники подчеркивают статичность в отношении оценки риска в РФ и обращают внимание на альтернативные обновляющиеся легитимные онлайновые базы, такие как Федеральный регистр потенциально опасных химиче-
Аленицкая Марина Владимировна – доктор медицинских наук, профессор Департамента общественного здоровья и профилактической медицины (e-mail: ; тел.: 8 (423) 265-24-24; ORCID: .
Сахарова Ольга Борисовна – кандидат медицинских наук, доцент Департамента общественного здоровья и профилактической медицины (e-mail: ; тел.: 8 (423) 265-24-24; ORCID: .
1 Р 2.1.10.1920-04. Руководство по оценке риска для здоровья населения при воздействии химических веществ, загрязняющих окружающую среду. – М.: Информационно-издательский центр Минздрава России, 2005. – 161 с.
ских и биологических веществ [10]. В нем содержится часть информации, необходимая для оценки риска, а именно характер воздействия химических веществ. Однако отсутствуют референтные концентрации ингаляционного воздействия и референтные дозы ( RfD ) перорального воздействия, представляющие собой оценку с некоторой неопределенностью ежедневного воздействия на население, которое, вероятно, не будет сопровождаться заметным риском негативных последствий в течение жизни.
Оценка риска здоровью, обусловленного качеством питьевой воды, не менее актуальна, чем при воздействии других объектов окружающей среды [11–13]. Неканцерогенный риск при воздействии веществ, поступающих с питьевой водой, рассчитывается с помощью RfD , которая выражается в единицах мг/кг-сут. RfD учитывает нелинейный (пороговый) характер риска при пероральном воздействии веществ. Отсутствие на территории РФ системы обновляющихся референтных значений для химических веществ, несмотря на то что их значение должно отражать все имеющиеся современные научные данные, склоняет специалистов, выполняющих оценку риска здоровью населения, к анализу нескольких источников информации для сбора и обобщения данных о воздействии химических веществ на здоровье человека, в том числе зарубежных открытых баз данных [14, 15].
Таким образом, представляется актуальным собрать сведения о референтных дозах для химических соединений, поступающих перорально с питьевой водой, из различных источников данных, провести их сравнительный анализ и обобщить полученную информацию согласно современным представлениям.
Цель исследования – оценить референтные дозы химических соединений, поступающих перорально с питьевой водой.
Задачи исследования: 1) сбор сведений о референтных дозах химических соединений в объектах окружающей среды в соответствии с нормативными документами и электронными базами данных; 2) сравнительный анализ референтных доз химических соединений и характера их воздействий на здоровье на основании доказательной базы.
Материалы и методы: Выполнен сравнительный анализ пероральных референтных доз открытой электронной базы данных о воздействии на здоровье химических веществ в окружающей среде «Информационная система по оценке рисков» (The Risk Assessment Information System, далее – RAIS), обновляющейся регулярно, с представленными значениями в отечественном руководстве Р 2.1.10.1920-041 (далее – Руководство). В качестве обоснования референтных значений представлена информация первичных материалов, лежащих в основе разработанных референтных доз. Иерархичность источников представлена в следующем порядке:
-
1) «Объединенная информационная система о риске» (далее – IRIS), разработанная Агентством США по охране окружающей среды;
-
2) предварительные экспертные значения токсичности (Provisional Peer-Reviewed Toxicity Values, далее – PPRTV);
-
3) токсикологические профили веществ Агентства регистрации токсичных веществ и заболеваний (Agency for Toxic Substances and Disease Registry, далее – ATSDR);
-
4) сводные таблицы оценки воздействия на здоровье Агентства по охране окружающей среды (Environmental Protection Agency's Health Effects Assessment Summary Tables, далее – HEAST).
Уровень доверия к исследованиям представлен согласно вышеперечисленным источникам.
В основу представленного перечня химических веществ, по которому выполнен сравнительный анализ, легли показатели безвредности химического состава питьевой воды, контролируемые в рамках социально-гигиенического мониторинга в соответствии с МР 2.1.4.0176-202. К перечню были добавлены эссенциальные элементы кобальт и кремний, обсуждение референтной дозы которых также является актуальным при оценке качества питьевой воды [16]. Общее количество проанализированных веществ – 28. Дополнительно для анализа использовались данные СанПиН 1.2.3685-213 и сведения по некоторым веществам из Федерального регистра потенциально опасных химических и биологических веществ. Среди проанализированных веществ присутствуют микроэлементы, недостаток и избыток которых ведет к ухудшению здоровья, в связи с этим расставлены акценты на границах суточного потребления.
Для каждого вещества был рассмотрен порядок обоснования RfD , если она имеется. В распространенном варианте отправной точкой при установлении референтного уровня RfD является оперативный расчет уровня отсутствия наблюдаемого неблагоприятного воздействия (NOAEL – No-observed-adverse-effect level, из исследований на животных или эпидемиологических исследований) путем последовательного применения модифицирующих
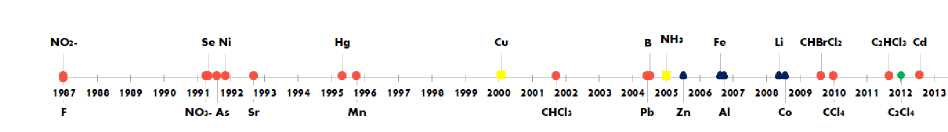
Рис. 1. Временная шкала пересмотра пероральных референтных значений: красным отмечены данные по IRIS; синим – PPRTV; зеленым – ATSDR; желтым – HEAST
факторов с учетом экспертной оценки по всем данным о рассматриваемом химическом веществе. Референтная доза получается путем деления дозы, используемой в эксперименте, либо определенной в эпидемиологическом исследовании, на совокупный модифицирующий фактор, который определяется качеством основополагающего исследования. Так, в частности, коэффициент «10» используется для экстраполяции с животных на человека, который десятикратно увеличивается для учета наиболее уязвимых групп населения и еще возрастает в 10 раз в случае, если исследование не учитывало хроническое воздействие.
Результаты и их обсуждение. К химическим соединениям, референтная доза которых не определяется ни одним из источников, относится кремний. В то же время соединения, по которым информация представлена в Руководстве, но отсутствует в RAIS, включают хром, бром и магний. Для большинства веществ наиболее актуальным источником остается IRIS (рис. 1). Общий временной интервал последних пересмотров референтных доз для включенных в исследование веществ составил период с 1987 по 2012 г.
Для некоторых химических соединений референтные дозы при пероральном употреблении с питьевой водой не были представлены в RAIS. К ним относятся бром, хром (суммарный), свинец, магний, кобальт и аммиак.
Референтная доза из RAIS ниже по следующим показателям в сравнении с Руководством: бромдихлорметан, тетрахлорэтилен, литий, кадмий, кобальт. Увеличенные референтные дозы по RAIS в сравнении с Руководством отмечены по тетрахлорметану, трихлорэтилену, железу и меди (рис. 2). Следует отметить, что за исключением тетрахлорметана (1-й класс опасности), остальные химические вещества, для которых референтная доза увеличена, относятся к 3-му и 4-му классам опасности, что характеризует их как умеренно опасные и малоопасные.
Проведенный анализ комбинированного воздействия химических соединений по Руководству позволил представить их влияние на органы-мишени в виде графа с учетом частоты встречаемости связей химических веществ и поражаемых органов (или систем органов) (рис. 3). Среди рассмотренных взаимосвязей отмечено, что наибольшему воздействию подвержены кровь, ЦНС, печень и почки. К химическим соединениям с широким спектром воздействия относятся хлорорганические соединения и тяжелые металлы.
Изолированным от остальных взаимосвязей является влияние фтора и стронция на костную систему, которое подтверждено эпидемиологическими исследованиями, рассмотренными далее.
Из проанализированных химических соединений к 1-му классу опасности относятся ртуть, мышьяк и хлорорганические соединения (тетрахлорметан, хлороформ, бромдихлорметан, тетрахлорэтилен и трихлорэтилен).
Оценивая неканцерогенный риск по суммарной концентрации всех растворимых форм ртути, в анализ преимущественно следует брать референтную дозу для неорганических форм, как указано в Руководстве. Неврологические последствия воздействия ртути были установлены у рабочих, которые подверглись ингаляционному воздействию ртути. Отмечалась невнятная речь, тремор, раздражительность, застенчивость, депрессия [17, 18]. Однако нет достоверных данных о воздействии элементарной ртути перорально. Референтная доза для хлорида ртути обосновывается влиянием на почки и подтверждается развитием аутоиммунного гломерулонефрита у крыс4. При хроническом воздействии неорганических соединений ртути с питьевой водой
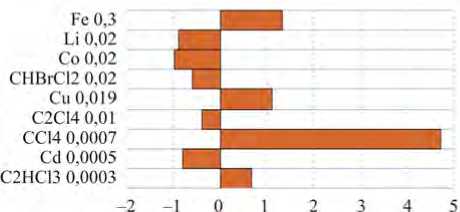
Рис. 2. Темп прироста (убыли) значений RfD по RAIS относительно Руководства: рядом с формулой вещества указана RfD (в мг/кг), принятая за 100 %
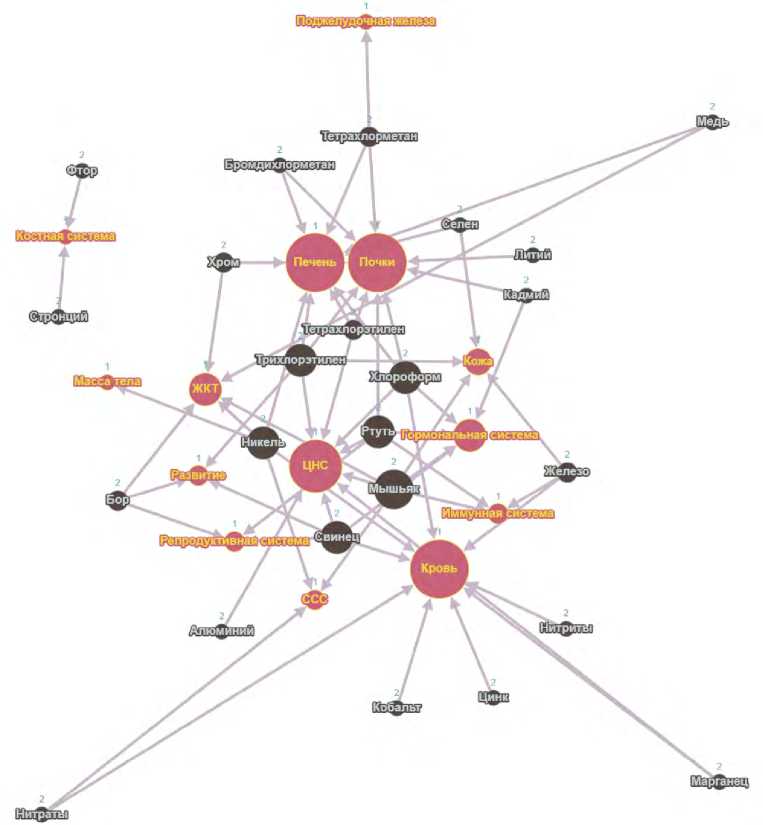
Рис. 3. Модель комбинированного воздействия химических веществ на здоровье человека согласно Руководству (цвет и нумерация отражают качественный признак: красный ( 1 ) – орган-мишень, черный ( 2 ) – химическое соединение; размер элементов – вес относительно количества взаимосвязей)
регистрировалось влияние на репродуктивную систему [19], снижение массы тела в экспериментах с крысами и аутоиммунный ответ в эксперименте с мышами [20]. Эпидемиологические исследования болезни Минамата [21], связанной с загрязнением рыбы метилртутью, и дальнейшие исследования беременных, а также экспериментальные данные [22] подтверждают серьезные последствия воздействия органических соединений ртути для нервной системы. Имеются эпидемиологические исследования воздействия метилртути на население с высоким содержанием рыбы в рационе питания. Доказано его влияние на сердечно-сосудистую и иммунную сис-темы5. В связи с этими данными, основанными на исследованиях с участием людей, модифицирую- щий коэффициент для органической ртути ниже в 100 раз, а референтная доза – в три раза.
Референтная доза мышьяка остается неизменной с 1991 г., так как на сегодняшний момент имеющиеся исследования обладают наиболее подробными сведениями об эффектах воздействия мышьяка на человека и являются основополагающими при определении референтной дозы, для которой модифицирующий коэффициент среди рассматриваемых соединений наименьший и равен трем. Отравление мышьяком выражается болезнью черных ног6, которая эндемична в районах Тайваня, и увеличением случаев гиперпигментации и кератоза с возрастом [23]. Характерные эффекты на сердечно-сосудистую систему при длительном воздействии мышьяка включают изменение деполяризации миокарда и сердечные аритмии [24]. В различных исследованиях также сообщалось о нарушениях работы дыхательной системы, неврологических расстройствах, диабетических эффектах, осложненной беременности и заболеваниях желудочно-кишечного тракта в результате употребления загрязненной мышьяком воды [25].
Среди рассмотренных хлорорганических продуктов обеззараживания воды, относящихся к 1-му классу опасности, наибольшее изменение референтной дозы отмечено для тетрахлорметана (или четыреххлористого углерода): увеличена референтная доза и соответственно уменьшена степень неканцерогенной опасности в 5,7 раза. Предыдущая референтная доза для четыреххлористого углерода перорального поступления (помещенная в базу данных IRIS в 1987 г.) составляла 0,0007 мг/кг в день, исходя из единственного 12-недельного исследования7, которое использовалось также для получения текущей референтной дозы. Максимальная недействующая доза была определена как 1 мг/кг (суточная доза – 0,7 мг/кг в день), а наименьший уровень воздействия, при котором наблюдается вредный эффект, – 10 мг/кг. Воздействие на здоровье выражено поражением печени, о чем свидетельствует вакуолизация гепатоцитов и значительное повышение активности сорбитолдегидрогеназы в сыворотке крови у крыс. Референтная доза 0,0007 мг/кг/день была рассчитана путем применения модифицирующего коэффициента, равного 1000, который учитывает межвидовую и внутривидовую изменчивости и экстраполяцию от субхронического к хроническому воздействию. В упомянутом исследовании отсутствуют данные о влиянии на почки и поджелудочную железу, как указано в Руководстве.
Основополагающими исследованиями для определения референтной дозы хлороформа при пероральном хроническом поступлении являются экспе- риментальные исследования на собаках8. Авторы отмечают повышение уровня АЛТ и обнаружение жировых кист в тканях печени, что связывают с ее повреждением. Известны нефротоксические эффекты при пероральном хроническом поступлении хлороформа [26].
Изменений референтных доз бромдихлормета-на по IRIS не проводилось с 1987 г. Отсутствуют эпидемиологические исследования воздействия исключительно бромдихлорметана, так как в основном продукты хлорирования представляют комбинацию хлорорганических соединений, в частности группы тригалогенметанов. Данные о референтной дозе бромдихлорметана получены из экспериментов на крысах и мышах9, в которых ведущим органом-мишенью определены почки. Хроническая референтная доза, согласно предварительным экспертным значениям токсичности для бромдихлорметана, была уменьшена с 0,02 до 0,008 мг/кг в отношении репродуктивной системы. Модифицирующий коэффициент равен 100, так как в нем не учитывалась экстраполяция с субхронического эксперимента на хронический благодаря исследованию, проводившемуся на двух поколениях животных10.
RfD для тетрахлорэтилена – 0,006 мг/кг в сутки – заменяет предыдущую RfD = 0,01 мг/кг в сутки, введенную в базу данных IRIS от 1988 г., которая основана на эксперименте с крысами11, данные о токсичности были обновлены по опубликованным исследованиям ингаляционного воздействия тетрахлорэтилена на животных и людей и усреднены по органам-мишеням, среди которых ведущую роль занимает центральная нервная система12, но также фигурируют почки, печень, иммунная система, процессы развития и репродуктивная система. Данные исследования первоначально ингаляционного воздействия стало возможным экстраполировать на пероральное благодаря математической модели, предложенной в 2011 г.13.
Референтная доза трихлорэтилена выше по RAIS в 1,7 раза в сравнении с данными Руководства и была рассчитана как усредненная величина по трем исследованиям, для каждого из которых определен свой модифицирующий коэффициент. Неблагоприятные неканцерогенные эффекты, связанные с пероральным воздействием трихлорэтилена, согласно экспериментальным исследованиям включают снижение массы тимуса14, задержку развития и пороки сердца плода крыс15.
Среди веществ второго класса опасности референтные дозы стронция, фтора, никеля, нитритов, бора, селена не претерпели изменений. Как отмечено выше, информация по RfD для суммарного брома полностью отсутствует в RAIS, так как оценка проводится в основном по бромсодержащим соединениям, присутствующим в воде [27]. Вместе с тем предлагается ориентироваться на значения RfD в Руководстве (1 мг/кг) по концентрации общего брома.
Фтор и стронций отмечены влиянием на костную систему. Основополагающие исследования для выведения RfD выявили рахитоподобные изменения в костях крыс при воздействии стронция16. В основе референтной дозы фтора лежит эпидемиологическое исследование17, в котором авторы отмечают пятнистость зубов у детей, характерную для флюороза.
Референтная доза никеля основана на экспериментальном исследовании с участием крыс18, в котором выраженным эффектом отмечено снижение массы тела. Выделена максимально недействующая доза – 5 мг/кг/день, с учетом модифицирующего фактора при ограничениях исследований референтная доза для человека принята 0,02 мг/кг. Следует отметить, что повреждения перечисленных органов и систем органов по Руководству представлены в исследованиях преимущественно с позиции низкого соотношения их веса с общей массой тела, что подчеркивает противоречивость других эффектов.
Вода, загрязненная нитратами уже на уровне более 20 мг/л, ассоциируется с младенческой метге-моглобинемией19. Референтная доза для нитратов как непосредственная причина метгемоглобинемии вычислена без модифицирующих факторов ввиду высокого уровня доверия к исследованиям и равна 1,6 мг/л. Нитриты, как и нитраты, способствуют развитию метгемоглобинемии, особенно в отношении младенцев, получавших смеси на основе загрязненной воды, что отмечено в эпидемиологическом исследовании20. Дети до года особенно восприимчивы к воздействию нитритов из-за высокого содержания в их кишечнике денитрифицирующих бактерий. Уровень доверия к исследованиям максимальный, и референтная доза нитритов 0,1 мг/кг была вычислена с учетом модифицирующего фактора, учитывающего чувствительность детей раннего возраста.
Референтная доза бора не отличается между представленной в RAIS и Руководстве, но в общем претерпела изменения – с 0,09 мг/кг, рассчитанной исходя из исследований на собаках21, до 0,02 мг/кг (доза, основанная на двух исследованиях на кры-сах22). Данные выявили статистически значимую тенденцию к снижению веса плода при увеличении дозы, что стало основополагающим действием при утверждении референтной дозы.
В эпидемиологических исследованиях, проведенных на территории Китая, где были отмечены высокие уровни селена в окружающей среде, ученые23 отмечали селеноз, включающий дисфункцию печени, выпадение волос, морфологические изменения ногтей, нарушения ЦНС (периферическая анестезия, акропа-рестезии и боли в конечностях). Исходя из данных регрессионного уравнения, составленного по зависимости между концентрацией селена и клиническими проявлениями, была рассчитана максимальная недействующая и референтная доза 0,005 мг/кг, не претерпевшая изменений впоследствии.
В отношении кобальта и лития IRIS сообщает о недостаточности данных для получения референтных доз при хроническом пероральном воздействии. В Руководстве приведена референтная доза 0,02 мг/кг для кобальта и лития.
У людей и животных кобальт стимулирует выработку эритроцитов за счет увеличения выработки гормона эритропоэтина [28], и его изучали для лечения анемии [29], но среди отрицательных эффектов воздействия отмечены снижение поглощения йода щитовидной железой24, дерматит у сенсибилизированных лиц и кардиомиопатия [30]. Основополагающим действием согласно предварительным экспертным значениям токсичности (PPRTV) для получения предварительных референтных значений при пероральном приеме кобальта выбрано поражение щитовидной железы. Однако доза 0,0003 мг/кг/день имеет низкую достоверность, так как экстраполирована с субхронической дозы.
Эффекты для здоровья при воздействии лития основаны на его использовании в качестве длительной поддерживающей терапии при лечении биполярных аффективных расстройств, в то же время отсутствуют эпидемиологические данные о воздействии лития из окружающей среды. Побочным эффектом при использовании лития для обозначенной выше терапии является нарушение концентрирующей функции почек, необратимые повреждения почек наступают при длительной литиевой терапии [31]. Предварительная референтная доза 2 мкг/кг для лития была экстраполирована с отмеченной минимально действующей терапевтической дозы с учетом модифицирующего фактора25.
В отношении свинца, несмотря на большой объем информации о его воздействии на здоровье, по результатам медицинских наблюдений и лабораторных исследований [32] негативные эффекты могут проявляться при столь низких уровнях свин- ца в крови, что практически не имеют порогового значения. Текущие знания о фармакокинетике свинца показывают, что значения риска, полученные с помощью стандартных процедур, не будут действительно указывать на потенциальный риск из-за сложности учета ранее поступившего в организм свинца и аккумулировавшегося, прежде всего, в скелете.
Кремний растворяется из минералов в воде с образованием биодоступной кремниевой кислоты. При рассмотрении данных об отслеживаемых или оцениваемых уровнях кремния в питьевой воде следует также отметить, что количество химического вещества, идентифицированное аналитически, не обязательно эквивалентно количеству, которое является биодоступным, в связи с этим для кремния референтная доза не определена ни одним из указанных источников26.
Для хрома референтная доза определена только Руководством как 0,005 мг/кг. Соединения хрома, которые являются побочным продуктом промышленной деятельности, смешиваются с поверхностными водами, а затем проникают в уровень подземных вод [33]. Было обнаружено, что шестивалентный хром может вызывать проблемы с кожей (раздражение, дерматит), респираторные проблемы (астма, аллергия), а также повреждать печень и почки [34].
К хроническим эффектам при воздействии кадмия относятся костные проявления, особенно остеомаляция и / или остеопороз и учащение переломов костей, названные болезнью итай-итай, которые впервые были зарегистрированы у японских женщин, живущих в районах с сильным загрязнением кадмием [35]. Токсикокинетическая модель для определения уровня хронического перорального воздействия кадмия на человека была рассчитана исходя из способности кадмия накапливаться в почечной ткани и снижать функцию почек27. Таким образом, была рассчитана референтная доза поглощенного с питьевой водой кадмия в сутки, равная 0,0005 мг/кг/день, которая представлена в Руководстве. Дальнейшие исследования и их обобщенный метаанализ позволили переоценить токсичность кадмия и рассчитать референтную дозу, поглощенную с водой, равную 0,0001 мг/кг/день28. Модифицирующий фактор для последней выбранной рефе- рентной дозы определен исходя из чувствительности людей, имеющих диабетическую нефропатию29.
Среди веществ 3-го и 4-го класса опасности присутствуют жизненно важные элементы, и получение значения оценки риска для таких химических веществ представляет собой особую проблему, поскольку кривая «доза – вредность» имеет «U-образную форму». Их значение риска должно защищать как от дефицита, так и от избытка. Для веществ 3-го класса опасности референтная доза осталась на прежнем уровне для цинка, алюминия, марганца и нитратов.
Цинк является важным микроэлементом для нормального функционирования организма. Его недостаток может привести к плохому заживлению ран, снижению работоспособности дыхательных мышц, иммунной дисфункции, анорексии, диарее, выпадению волос, дерматиту (энтеропатический акродерматит) и депрессии [36]. Оптимальная суточная доза потребления цинка варьируется в районе 12 мг в день (или 0,17 мг/кг), в то же время токсичность цинка вызывает снижение концентрации меди в эритроцитах и снижение активности Zn-су-пероксиддисмутазы, что установлено по клиническим исследованиям30 и взято в основу для расчета референтной дозы, равной 0,3 мг/кг.
Воздействие алюминия связывают с болезнью Альцгеймера, так как его обнаруживают в тканях мозга больных. Наиболее чувствительным показателем токсичности алюминия в экспериментах с грызунами отмечают нейроповеденческие расстрой-ства31, которые определяют предварительную референтную дозу для алюминия с низким уровнем доверия.
Так же, как и для алюминия, для железа отсутствуют данные о референтной дозе в IRIS в связи с недостаточностью данных для количественной оценки риска и определены предварительные значения согласно PPRTV. Хотя исследований хронического воздействия, сообщающих о токсичности для желудочно-кишечного тракта, не проводилось, клинический опыт применения добавок железа показывает, что желудочно-кишечные эффекты связаны с пероральной терапией железом, независимо от продолжительности лечения, и что интенсивность симптомов не меняется в течение курса лечения [37]. Этот эффект положен в основу рефе- рентной дозы и исследование, из которого рассчитана референтная доза 0,7 мг/кг, заключается в ежедневном приеме фумарата железа32. Данная RfD выше предложенной Руководством (0,3 мг/кг), при этом адекватное ежедневное потребление железа варьируется в зависимости от возраста и пола и колеблется от 0,15 до 0,27 мг/кг в сутки. Кроме того, также важно отметить, что индивидуальные потребности в железе, а также побочные реакции на него могут сильно различаться, подгруппы населения с наследственными нарушениями метаболизма железа или другими состояниями, влияющими на гомеостаз железа, не могут быть учтены. В связи с этим результаты оценки риска по железу следует рассматривать со стороны рефлекторноольфакторных эффектов, связанных с восприятием воды органами чувств потребителя.
Референтная доза для магния выделена только Руководством (11 мг/кг) без определения критических органов и является максимальной среди анализируемых веществ, так как небольшой избыток магния выводится с мочой, а токсическая гипермагние-мия наблюдается при десятикратном превышении дозы суточной потребности, равной около 350 мг для взрослых [38]. RAIS не предоставляет информации о количественной оценке риска по данному элементу.
Марганец необходим для нормального физиологического функционирования организма, поэтому, как и для железа, оценивают не только его избыток, но и недостаточность. Верхняя граница рекомендуемых доз перорального приема марганца не может являться границей токсичности. Эпидемиологическое исследование33, в котором показана неврологическая симптоматика у местного населения областей Греции с выявленным повышенным содержанием марганца в питьевой воде колодцев около 2 мг/л, вызывает некоторую обеспокоенность возможными неблагоприятными последствиями для здоровья.
Данные по RfD меди, несмотря на присутствие их в Руководстве, отсутствуют на первых четырех уровнях источников RAIS и предлагаются лишь в сводных таблицах HEAST по причине недостаточности данных для количественной оценки риска. В них референтная доза при отсутствии других данных рассчитывается исходя из стандартного предела при условии потребления 2 л/день воды и массы тела
Влияние, лежащее в основе референтной дозы, и уровень доверия к исследованиям по RAIS
|
Влияние |
Уровень доверия |
||
|
высокий |
средний |
низкий или отсутствует |
|
|
Нервная система |
Селен23 |
Тетрахлорэтилен11,12, марганец33 |
31 Алюминий |
|
Почки |
Ртуть4, бромдихлорметан9, кадмий27,29 |
- |
Литий25 |
|
Иммунная система |
Ртуть5, трихлорэтилен14 |
- |
|
|
ЖКК |
- |
- |
Железо32 |
|
Репро- и эмбриотоксичность |
Трихлорэтилен15, бор21,22 |
Бромдихлорметан10 |
- |
|
Кожа |
Селен23 |
Мышьяк6 |
- |
|
Кровь |
Нитриты20, нитраты19, селен23 |
Цинк30 |
- |
|
Печень |
- |
Тетрахлорметан7, хлороформ8 |
- |
|
Щитовидная железа |
- |
- |
Кобальт24 |
|
Снижение массы тела |
- |
Никель18 |
- |
|
Костная система и зубы |
Фтор17 |
Стронций16 |
- |
70 кг. Но так как для меди, например, в штате Нью-Джерси (США) предел содержания в питьевой воде равен 1,3 мг/л34, то рассчитанная RfD равна 0,04 мг/кг. Подвергнув тем же преобразованиям российский стандарт 1 мг/л, получим RfD , равную 0,03 мг/кг. Вместе с тем значение, представленное в Руководстве, – 0,019 мг/кг – выше, чем рассчитанные согласно стандартам. Хотя хроническая токсичность при длительном воздействии меди широко не изучалась, исследования пациентов с болезнью Вильсона – Коновалова, генетическим дефектом, приводящим к накоплению меди в тканях, дают информацию о хронической токсичности меди [39].
Единственное из проанализированных веществ 4-го класса опасности – аммиак. Референтная доза по аммиаку, несмотря на наличие в Руководстве как 0,98 мг/кг, отсутствует в сводных данных HEAST, который является последней инстанцией в иерархии источников данных. Комментарии в HEAST указывают, что 34 мг/л – это концентрация в питьевой воде, которая напрямую связана с органолептическим (вкусовым) порогом, и что безопасная концентрация аммиака может быть выше 34 мг/л, но данных недостаточно для того, чтобы оценить безопасный уровень. В СанПине приводятся две ПДК для аммиака: 1,5 и 2,0 мг/л. Наибольшая является актуальной для воды централизованных систем водоснабжения, хотя в предыдущем ГН 2.1.5.1315-0335 (недействующий с 2021 г.) была упомянута концентрация 1,5 мг/л. В результате не представляется возможным обосновать референтную дозу по аммиаку, данную в Руководстве с использованием упомянутых материалов.
Таким образом, влияния, лежащие в основе референтных доз, выведенных за период существования методологии оценки риска для наиболее распространенных химических загрязнителей питьевой воды, можно представить в виде сводной таблицы.
Выводы. Проведенный анализ референтных доз для химических соединений, поступающих перорально с питьевой водой, выявил следующие особенности, которые необходимо учитывать при проведении оценки риска:
-
1. За время существования методологии оценки риска только часть химических веществ претерпела изменения в отношении референтных доз при пероральном употреблении, которые не были учтены в отечественных нормативных документах.
-
2. Нет адекватных данных токсикологических исследований, которые обосновывают референтные дозы для меди, магния, аммиака, свинца, кремния, брома, хрома при пероральном поступлении с питьевой водой в силу различных обстоятельств.
-
3. Выявлены ограничения в определении пероральной референтной дозы ( RfD ) железа и аммиака, которые принято рассматривать со стороны органолептического восприятия.
-
4. На сегодняшний день не все эффекты для здоровья, предложенные в Руководстве, лежат в основе расчета референтных доз для химических соединений и могут быть согласованы на международном уровне.
-
5. Для вычисления коэффициента и индекса опасности предложено воспользоваться данными о критических органах и системах, референтными значениями, обновляющимися регулярно по данным эпидемиологических и экспериментальных исследований, вместе с тем дополнительно рекомендуется указывать, как их значение соотносится со значением из отечественных нормативных документов.
Финансирование. Исследование не имело финансовой поддержки.
Конфликт интересов. Авторы статьи заявляют об отсутствии конфликта интересов.
-
34 Health Effects Assessment Summary for Copper [Электронный ресурс] // EPA. – URL: https://rais.ornl.gov/ epa/heast/Copper.html#rc007440508 (дата обращения: 30.07.2023).
-
35 ГН 2.1.5.1315-03. Предельно допустимые концентрации (ПДК) химических веществ в воде водных объектов хозяйственно-питьевого и культурно-бытового водопользования: гигиенические нормативы / введ. в действие постановлением Главного государственного санитарного врача Российской Федерации от 30.04.2003 № 78. – М: Российский регистр потенциально опасных химических и биологических веществ Минздрава РФ, 2003. – 154 с. (утратило силу с 01.03.2021 на основании постановления Главного государственного санитарного врача РФ от 28.01.2021 № 2).
Список литературы Анализ референтных доз химических соединений, поступающих перорально с питьевой водой
- Развитие методологии анализа риска здоровью в задачах государственного управления санитарно-эпидемиологическим благополучием населения / Н.В. Зайцева, Г.Г. Онищенко, И.В. Май, П.З. Шур // Анализ риска здоровью. -2022. - № 3. - С. 4-20. DOI: 10.21668/health.risk/2022.3.01
- Барг А.О., Лебедева-Несевря Н.А., Корнилицына М.Д. Методические подходы к оценке субъективного восприятия риска населением при воздействии загрязнения атмосферного воздуха на здоровье // Анализ риска здоровью. -2022. - № 2. - С. 28-37. DOI: 10.21668/health.risk/2022.2.03
- Оценка риска здоровью городского населения с использованием фоновых долгопериодных средних концентраций вредных веществ в атмосферном воздухе / Д.С. Исаев, Н.А. Мозжухина, Г.Б. Еремин, Н.Н. Крутикова // Здоровье населения и среда обитания - ЗНиСО. - 2022. - Т. 30, № 5. - С. 23-31. DOI: 10.35627/2219-5238/2022-30-5-23-31
- Оценка риска для здоровья населения при употреблении питьевой воды города Латакунги и кантона Педро Ви-сенте Мальдонадо (Республика Эквадор) / К.А. Саласар Флорес, А.И. Курбатова, К.Ю. Михайличенко, А.С. Милутка // Гигиена и санитария. - 2022. - Т. 101, № 3. - С. 344-356. DOI: 10.47470/0016-9900-2022-101-3-344-356
- Оценка риска здоровью населения связанного с качеством питьевой воды (на примере нефтяных районов республики Башкортостан) / Л.Р. Рахматуллина, Р.А. Сулейманов, Т.К. Валеев, З.Б. Бактыбаева, Н.Р. Рахматуллин // Анализ риска здоровью. - 2021. - № 2. - С. 33-40. DOI: 10.21668/health.risk/2021.2.03
- Health risk assessment of total chromium in the qanat as historical drinking water supplying system / A. Kazemi, M. Es-maeilbeigi, Z. Sahebi, A. Ansari // Sci. Total Environ. - 2022. - Vol. 807, Pt 2. - P. 150795. DOI: 10.1016/j.scitotenv.2021.150795
- Health risk assessment and spatial distribution of nitrate, nitrite, fluoride, and coliform contaminants in drinking water resources of kazerun, Iran / M. Golaki, A. Azhdarpoor, A. Mohamadpour, Z. Derakhshan, G. Oliveri Conti // Environ. Res. -2022. - Vol. 203. - P. 111850. DOI: 10.1016/j.envres.2021.111850
- Spatial distribution, multivariate statistical analysis, and health risk assessment of some parameters controlling drinking water quality at selected primary schools located in the southwestern coastal region of Bangladesh / T. Kormoker, A.M. Idris, M.M. Khan, T.R. Tusher, R. Proshad, Md. S. Islam, S. Khadka, S. Rahman [et al.] // Toxin Reviews. - 2021. - Vol. 41, № 1. -P. 247-260. DOI: 10.1080/15569543.2020.1866012
- Броди М., Авалиани С.Л. Оценка риска для здоровья от факторов окружающей среды. 16 лет сотрудничества Агентства по охране окружающей среды США и гигиеническими и экологическими организациями Российской Федерации: результаты и размышления // Гигиена и санитария. - 2021. - Т. 100, № 12. - С. 1344-1349. DOI: 10.47470/00169900-2021-100-12-1344-1349
- Хамидулина Х.Х., Рабикова Д.Н. Разработка национального перечня канцерогенов, мутагенов и репроток-сикантов и его внедрение в регулирование обращения химических веществ на территории Российской Федерации и государств Евразийского экономического союза // Гигиена и санитария. - 2021. - Т. 100, № 9. - С. 897-902. DOI: 10.47470/0016-9900-2021-100-9-897-902
- Бабаян Г.Г., Сакоян А.Г. Тяжёлые металлы и мышьяк в питьевой воде и оценка риска здоровью населения региона с развитой горнодобывающей промышленностью // Гигиена и санитария. - 2020. - Т. 99, № 7. - С. 725-732. DOI: 10.33029/0016-9900-2020-99-7-725-732
- Seasonal Variation of Drinking Water Quality and Human Health Risk Assessment in Hancheng City of Guanzhong Plain, China / Y. Ji, J. Wu, Y. Wang, V. Elumalai, T. Subramani // Exposure and Health. - 2020. - Vol. 12, № 3. - P. 469-485. DOI: 10.1007/s12403-020-00357-6
- Potential toxic elements in groundwater and their health risk assessment in drinking water of Limpopo National Park, Gaza Province, Southern Mozambique / L. Ricolfi, M. Barbieri, P.V. Muteto, A. Nigro, G. Sappa, S. Vitale // Environ. Geochem. Health. - 2020. - Vol. 42, № 9. - P. 2733-2745. DOI: 10.1007/s10653-019-00507-z
- Вопрос выбора источника информации об уязвимых органах и системах в процедуре оценки риска. Выполнение сравнительных расчетов неканцерогенного риска / Д.С. Исаев, Г.Б. Еремин, Н.А. Мозжухина, Л.А. Леванчук // Анализ риска здоровью - 2022. Фундаментальные и прикладные аспекты обеспечения санитарно-эпидемиологического благополучия населения. Совместно с международной встречей по окружающей среде и здоровью RISE-2022: материалы XII Всероссийской научно-практической конференции с международным участием: в 2 т. - Пермь: Пермский национальный исследовательский политехнический университет, 2022. - Т. 1. - С. 29-36.
- Фомина С.Ф., Степанова Н.В. Оценка риска канцерогенных эффектов для детского населения г. Казани при многосредовом воздействии химических веществ окружающей среды // Анализ риска здоровью - 2020 совместно с международной встречей по окружающей среде и здоровью RISE-2020 и круглым столом по безопасности питания: материалы X Всероссийской научно-практической конференции с международным участием: в 2 т. - Пермь: Пермский национальный исследовательский политехнический университет, 2020. - Т. 1. - С. 199-206.
- Эссенциальные элементы и их нормирование в питьевой воде / О.О. Синицына, С.И. Плитман, Г.П. Амплеева, О.А. Гильденскиольд, Т.М. Ряшенцева // Анализ риска здоровью. - 2020. - № 3. - С. 30-38. DOI: 10.21668/health.iisk/2020.3.04
- Taux K., Kraus T., Kaifie A. Mercury Exposure and Its Health Effects in Workers in the Artisanal and Small-Scale Gold Mining (ASGM) Sector - A Systematic Review // Int. J. Environ. Res. Public Health. - 2022. - Vol. 19, № 4. - P. 2081. DOI: 10.3390/ijerph19042081
- Relating mercury occurrence in soil gases at establishments hosting children to historical mercury-using activities in Paris, France / P. Balon, G. Boissard, C. Cailleau, S. Belbeze, D. Hube, C. Vincq, J.-F. Brunet, F. Lion [et al.] // Sci. Total Environ. - 2022. - Vol. 814. - P. 152388. DOI: 10.1016/j.scitotenv.2021.152388
- Effects of Cadmium, Lead, and Mercury on the Structure and Function of Reproductive Organs / P. Massanyi, M. Massanyi, R. Madeddu, R. Stawarz, N. Lukac // Toxics. - 2020. - Vol. 8, № 4. - P. 94. DOI: 10.3390/toxics8040094
- Mercury-induced inflammation and autoimmunity / K.M. Pollard, D.M. Cauvi, C.B. Toomey, P. Hultman, D.H. Kono // Biochim. Biophys. Acta Gen. Subj. - 2019. - Vol. 1863, № 12. - P. 129299. DOI: 10.1016/j.bbagen.2019.02.001
- Murata K., Karita K. Minamata Disease // In book: Overcoming Environmental Risks to Achieve Sustainable Development Goals: Lessons from the Japanese Experience. Current Topics in Environmental Health and Preventive Medicine / ed. by T. Nakajima, K. Nakamura, K. Nohara, A. Kondoh. - Singapore: Springer, 2022. - P. 9-19. DOI: 10.1007/978-981-16-6249-2_2
- Continuous Exposure to Inorganic Mercury Affects Neurobehavioral and Physiological Parameters in Mice / H. Malqui, H. Anarghou, F.Z. Ouardi, N. Ouasmi, M. Najimi, F. Chigr // J. Mol. Neurosci. - 2018. - Vol. 66, № 2. - P. 291-305. DOI: 10.1007/s12031-018-1176-1
- Multidisciplinary approach to assess the toxicities of arsenic and barium in drinking water / M. Kato, N. Ohgami, S. Ohnuma, K. Hashimoto, A. Tazaki, H. Xu, L. Kondo-Ida, T. Yuan [et al.] // Environmental Health and Preventive Medicine. -2020. - Vol. 25, № 1. - P. 16. DOI: 10.1186/s12199-020-00855-8
- Environmental arsenic exposure and its contribution to human diseases, toxicity mechanism and management / Md S. Rahaman, Md M. Rahman, N. Mise, Md T. Sikder, G. Ichihara, Md K. Uddin, M. Kurasaki, S. Ichihara // Environ. Pollut. - 2021. - Vol. 289. - P. 117940. DOI: 10.1016/j.envpol.2021.117940
- Arsenic in groundwater of West Bengal, India: A review of human health risks and assessment of possible intervention options / S. Bhowmick, S. Pramanik, P. Singh, P. Mondal, D. Chatteijee, J. Nriagu // Sci. Total Environ. - 2018. - Vol. 612. -P. 148-169. DOI: 10.1016/j.scitotenv.2017.08.216
- Ewaid S.H., Abed S.A., Al-Ansari N. Acute toxicity of the water chlorination byproduct (chloroform) in male mice // AIP Conference Proceedings. - 2020. - Vol. 2290, № 1. DOI: 10.1063/5.0027353
- Bromine and iodine species in drinking water supply system along the Changjiang River in China: Occurrence and transformation / X. Yang, Q. Zheng, M. He, B. Chen, B. Hu // Water Res. - 2021. - Vol. 202. - P. 117401. DOI: 10.1016/j.watres.2021.117401
- Cobalt in athletes: hypoxia and doping - new crossroads / A.V. Skalny, I.P. Zaitseva, Y.G. Gluhcheva, A.A. Skalny, E.E. Achkasov, M.G. Skalnaya, A.A. Tinkov // J. Appl. Biomed. - 2019. - Vol. 17, № 1. - P. 28. DOI: 10.32725/jab.2018.003
- Cwiertnia A., Kozlowski M., Cymbaluk-Ploska A. The Role of Iron and Cobalt in Gynecological Diseases // Cells. -2023. - Vol. 12, № 1. - P. 117. DOI: 10.3390/cells12010117
- Long-Term Clinical and Toxicological Follow-up of Severe Cobalt and Chromium Intoxication - a Case Report / A.M. Pre-isser, L. Scheit, A. Kraft, O. Thieme, V. Harth // SN Compr. Clin. Med. - 2023. - Vol. 5. - P. 58. DOI: 10.1007/s42399-023-01393-4
- Relationship between serum lithium concentration and kidney damage in a preclinical model / G.P. Ossani, A.M. Uceda, N.R. Lago, D.J. Martino // Bipolar Disord. - 2020. - Vol. 22, № 3. - P. 281-285. DOI: 10.1111/bdi. 12854
- Toxic Effect of Acute Cadmium and Lead Exposure in Rat Blood, Liver, and Kidney / M. Andjelkovic, A. Buha Djord-jevic, E. Antonijevic, B. Antonijevic, M. Stanic, J. Kotur-Stevuljevic, V. Spasojevic-Kalimanovska, M. Jovanovic [et al.] // Int. J. Environ. Res. Public Health. - 2019. - Vol. 16, № 2. - P. 274. DOI: 10.3390/ijerph16020274
- Mani Tripathi S., Chaurasia S. Detection of Chromium in surface and groundwater and its bio-absorption using bio-wastes and vermiculite // Engineering Science and Technology, an International Journal. - 2020. - Vol. 23, № 5. - P. 1153-1161. DOI: 10.1016/jjestch.2019.12.002
- Hedberg Y.S. Chromium and leather: a review on the chemistry of relevance for allergic contact dermatitis to chromium // Journal of Leather Science and Engineering. - 2020. - Vol. 2, № 1. - P. 20. DOI: 10.1186/s42825-020-00027-y
- Imura J., Tsuneyama K., Ueda Y. Novel Pathological Study of Cadmium Nephropathy of Itai-itai Disease // In book: Cadmium Toxicity: New Aspects in Human Disease, Rice Contamination, and Cytotoxicity. Current Topics in Environmental Health and Preventive Medicine / ed. by S. Himeno, K. Aoshima. - Singapore: Springer, 2019. - P. 39-50. DOI: 10.1007/978-981-13-3630-0_3
- Gupta S., Brazier A.K.M., Lowe N.M. Zinc deficiency in low- and middle-income countries: prevalence and approaches for mitigation // J. Hum. Nutr. Diet. - 2020. - Vol. 33, № 5. - P. 624-643. DOI: 10.1111/jhn.12791
- The role of oral iron in the treatment of adults with iron deficiency / J.O. Lo, A.E. Benson, K.L. Martens, M.A. Hedges, H. Stowe McMurry, T. DeLoughery, J.E. Aslan, J.J. Shatzel // Eur. J. Haematol. - 2023. - Vol. 110, № 2. - P. 123-130. DOI: 10.1111/ejh.13892
- Magnesium: Biochemistry, Nutrition, Detection, and Social Impact of Diseases Linked to Its Deficiency / D. Fioren-tini, C. Cappadone, G. Farruggia, C. Prata // Nutrients. - 2021. - Vol. 13, № 4. - P. 1136. DOI: 10.3390/nu13041136
- Critical Review of Exposure and Effects: Implications for Setting Regulatory Health Criteria for Ingested Copper / A.A. Taylor, J.S. Tsuji, M.R. Garry, M.E. McArdle, W.L. Goodfellow Jr., W.J. Adams, C.A. Menzie // Environ. Manage. -2020. - Vol. 65, № 1. - P. 131-159. DOI: 10.1007/s00267-019-01234-y


