Аутоиммунный гепатит в сочетании с саркоидозом (клиническое наблюдение)
Автор: Семендяева Маргарита Ефимовна, Бакулина И.Ф., Лесняк Виктор Николаевич, Турусина Тамара Александровна, Степанов В.А., Уразова Ю.А.
Журнал: Клиническая практика @clinpractice
Рубрика: Cлучай из практики
Статья в выпуске: 1 (1), 2010 года.
Бесплатный доступ
Приводится описание клинического наблюдения, касающегося женщины 63 лет, у которой имеется сочетание двух заболеваний - аутоиммунного гепатита с перекрестным синдромом и системными проявлениями и саркоидоза с поражением легких и внелегочными проявлениями - гранулематозом печени.
Аутоиммунный гепатит, саркоидоз, гранулематоз печени
Короткий адрес: https://sciup.org/14338310
IDR: 14338310
Текст научной статьи Аутоиммунный гепатит в сочетании с саркоидозом (клиническое наблюдение)
АУТОИММУННЫЙ ГЕПАТИТ В СОЧЕТАНИИ ССАРКОИДОЗОМ (КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ)
Семендяева М. Е.(1), Бакулина И. Ф.(1), Лесняк В.Н.(1), Турусина Т. А.(1),
Степанов В. А.(1), Уразова Ю. А.(2)
1. Клиническая больница № 83 ФМБА России 2. Кафедра внутренних болезней ИПК ФМБА России
Приводится описание клинического наблюдения, касающегося женщины 63 лет, у которой имеется сочетание двух заболеваний — аутоиммунного гепатита с перекрестным синдромом и системными проявлениями и саркоидоза с поражением легких и внелегочными проявлениями — гранулематозом печени.
Больная С., 63 лет, в июне 2008г направлена в гастроэнтерологическое отделение Клинической больницы № 83 с целью уточнения диагноза с жалобами на слабость, диспептические явления, эпигастральные боли, метеоризм, запоры.
В анамнезе 2 операции (разрыв кисты яичника, аппендицит).
Страдает аутоиммунным тиреоидитом на протяжении нескольких лет. С 2006г при амбулаторном обследовании отмечено повышение щелочной фосфатазы до 600 ед/л (норма 80-258), ускорение СОЭ до 45 мм/час, неидентифицированные высыпания на коже. Весной 2008 г при рентгенологическом исследовании легких отмечено увеличение лимфоузлов средостения. Консультирована фтизиатром с заключением о наличии диффузного пневмосклероза.
Стационарное обследование в июне 2008г гепато-лиенального синдрома не выявило, в общем анализе крови ускорение СОЭ до 38 мм/час. Биохимическое исследование крови: общий белок 75 г/л, альбумины 42, глобулины — альфа1 3,3, альфа2 10,2, бета 15,1, гамма 28,4; холестерин — 5,3 ммоль/л, билирубин 22 мкмоль/л (связанный 5, свободный 17), АЛТ 31-49 ед/л, АСТ 29-61 ед/л, альфа-амилаза 54 ед/л, щелочная фосфатаза 508-724 ед/л, ГГТП 110-275 ед/л, глюкоза 5,6 ммоль/л, серомукоид 0,140 мг/л, тимоловая проба 3,3. Коагулограмма — гиперфибриногенемия, замедление фибринолиза. HBs-ag, a-HCV, РНК-ВГG — отрицательные; АNА — отрицательные, АМА — 29 (норма до 10).
При УЗИ органов брюшной полости выявлены диффузные изменения печени и поджелудочной железы, перетяжки в шейке и теле желчного пузыря с уплотнением его стенок; забрюшинные лимфоузлы не увеличены. Гепатохолесцинтиграфия с бромезидой функциональных изменений печени не выявила, отмечены умеренные нарушения наполнения желчного пузыря. Фракционное дуоденальное зондирование свидетельствовало о дискинезии желчного пузыря с желчезастойным синдромом. Эндоскопически отмечены признаки субатрофического гастродуоденита (рН-метрически – анацид-ное состояние желудочной секреции). Ирригоскопия выявила наличие дивертикулярной болезни; явления дивертикулита отсутствовали.
Выявленная у пациентки клинико-лабораторная симптоматика с наличием гиперглобулинемии, повышением гамма-глобулинов, ускорением СОЭ, сдвигами печеночных проб (главным образом повышением ферментов холестаза) дали основания предполагать диагноз «вероятного» аутоиммунного гепатита. Дополнительными критериями служили наличие высоких антимитохондриальных антител, аутоиммунного тиреоидита (табл. 1), при отрицательных маркерах вирусных гепатитов [1]. Это явилось основанием для начала терапии урсосаном в комбинации с гептралом и рифампицином и ГБО. В результате было отмечено снижение цифр щелочной фосфатазы и ГГТП (500 и 100 ед/л соответственно), с последующим подъемом после отмены лечения, о чем свидетельствовала повторная госпитализация (ноябрь 2008г).Последующее наблюдение за больной свидетельствует о сохраняющейся клинической симптоматике (март 2009г) и лабораторных сдвигах с нарастанием уровня холестерина (7 ммоль/л) и щелочной фосфатазы (>700 ед/л), изменением коагулограммы (снижение коагуляции), появлением гепатомегалии. Это дало основания для морфологического исследования ткани печении, полученной при пункционной биопсии печени; выявлены дистрофические изменения гепатоцитов, дисплазия I степени ядер гепатоцитов; имеющиеся в препарате портальные тракты не расширены, фиброз отсутствует. Следовательно, морфологических признаков аутоиммунного гепатита не обнаружено, что, как известно, не исключает этот диагноз [2], тем более что полученный биоптат может быть не информативным, если не содержит 10 и более трактов.
Итак, наблюдение за больной С. на протяжении почти одного года дало основания говорить о наличии у нее аутоиммунного гепатита (АИГ) I типа, частота которого составляет 85% всех случаев АИГ и который развивается в любом возрасте. В том числе в постменопаузальном периоде, как это имело место в данном наблюдении [3].
Клиническая картина начальной фазы АИГ скудная — астенический синдром, диспептические явления, боли в животе; кожный зуд не характерен, более того, его наличие дает основания усомниться в диагнозе [4]. Возможен вариант с внепеченочными проявлениями — кожные высыпания, аутоиммунный тиреоидит [5]. Характерные для I типа АNА (70-80% больных) у пациентки отсутствовали, но при первом обследовании выявлены АМА, что является диагностическим маркером первичного билиарного цирроза печени (ПБЦ) и отмечается у 88% больных [6,7], следовательно можно сделать заключение об особой форме АИГ, сочетающего
Таблица 1. Балльная система оценки для диагностики аутоиммунного гепатита
Патогенетическая цепь АИТ в настоящее время представляется следующим образом: генетическая предрасположенность (ослабление иммунологического надзора над аутореактивными клонами лимфоцитов) → воздействие неустановленного решающего фактора → повышенная экспрессия печеночных аутоантител и НLA II класса → активация аутоактивных клеток Т- и В-лимфоцитов → продукция медиаторов воспаления → повреждение ткани печени и развитие системного воспаления [2,9,10].
В отличие от заболеваний с известной этиологией причиной аутоиммунных процессов принято считать нарушение взаимодействия субпопуляций лимфоцитов, приводящее к развитию иммунного ответа на антигены собственных тканей. В то же время остается неясным, является ли данное нарушение первичным или вторичным, возникшим в результате изменения антигенных свойств тканей под влиянием неустановленного фактора. Исходя из этого понятно и характерное для АИГ наличие внепеченочных проявлений, наблюдающихся почти у половины больных, касающихся всех органов и систем: лихорадки, кожных васкулитов, лимфаденопатий, фиброзирующего альвеолита, тиреоидита и других. По данным клиники М. Е. Тареева [6], среди внепеченочных проявлений наиболее часто встречались синдром Шегрена (49,7%), фиброзирующий альвеолит (24,1%), аутоиммунный тиреоидит (18,6%).
Основываясь на патогенетической концепции АИГ, следует обсуждать и принципы его лечения.
Поскольку этиотропная терапия невозможна, на первый план выступает патогенетическая иммуносупрессивная терапия, основу которой составляют глюкокортикостероиды (ГКС) [11]. При этом необходимость лечения определяется выраженностью воспалительного синдрома, а не печеночной дисфункцией. Препараты выбора преднизолон с метилпрелнизолоном, нередко в сочетании с азатиоприном, метатрексатом. Цель лечения достижение клинической и биохимической ремиссии, которая наблюдается в среднем у 65%, однако показания можно разделить на абсолютные и относительные и, в то же время, выделить группу лиц с отсутствием показаний для этого вида терапии (табл. 2).
При выборе терапевтической тактики у данной больной мы руководствовались показаниями, сформулированными в этой таблице, и отказались от использования ГКС, сконцентрировав свое внимание на препаратах урсодезоксихолевой кислоты — УДХК (табл. 3).
Положительное влияние УДХК на циркуляцию желчных кислот, ее способность встраиваться в мембраны гепатоцитов и уменьшать продукцию на поверхности гепатоцитов антигенов НLA I класса и на эпителии желчных протоков антигенов HLA II класса, предотвращая тем самым развитие аутоиммунных реакций [12,13]. Тем не менее отчетливой положительной динамики в нашем случае отмечено не было.
В октябре 2009г. больная С. вновь была направлена в КБ№83, но уже в пульмонологическое отделение по поводу выявленного при очередной рентгенографии легких диссеминированного процесса в легких неясного генеза, подтвержденных КТ.
В крови в этот период по-прежнему определялась ускоренная до 35 мм/ч СОЭ, невысокая гиперамино-трансфераземия (АЛТ 43, АСТ 52 ед/л), повышение С-реактивного белка, щелочной фосфатазы до 665 ед/л, иммуноглобулинов класса М и G (3,77 г/л и 19,22 г/л соответственно).
Таблица 2. Показания к лечению аутоиммунного гепатита
|
Абсолютные |
Относительные |
Лечение не проводят |
|
Симптомы выражены |
||
|
Неуклонное |
||
|
прогрессирование |
Симптомы умеренно выражены или отсутствуют |
Бессимптомное течение с небольшими изменениями лабораторных показателей Непереносимость преднизо-лона и/или азатиоприна в анамнезе |
|
АсАТ >10 норм |
АсАТ 3-9 норм |
АсАТ <3 норм |
|
АсАТ >5 норм + -глобулины >2 норм |
АсАТ >5 норм + |
|
|
-глобулины <2 норм |
Выраженная цитопения |
|
|
Мостовидные некрозы Мультилобулярные некрозы |
Перипортальный гепатит |
Портальный гепатит |
|
Неактивный цирроз Декомпенсированный цирроз с кровотечением из вен пищевода в анамнезе |
Исследование функции внешнего дыхания с бронхолитиками выявило нарушение вентиляционной функции легких по обструктивному типу легкой степени тяжести, ограничение вентиляционного потока генерализованного характера; положительной реакции на вентолин не получено. Диффузионное исследование легких свидетельствовало о снижении диффузионной функции легких легкой степени за счет изменений альвеолярнокапиллярной мембраны. При бронхоскопии осмотрены бронхи с двух сторон до субсегментарных, просвет их широкий, свободный, слизистая розового цвета, гладкая, блестящая, рельеф не изменен, сосудистый рисунок дифференцируется, шпор бронхов не расширены. Взяты биопсии из нижней доли правого легкого и нижнедолевого и верхнедолевого бронхов. Заключение биопсии: получены крайне скудные фрагменты с единичными клетками плоского и цилиндрического эпителия.
Таблица 3. Лекарственные препараты, используемые при лечении первичного билиарного цирроза печени
|
Название препарата |
Эффективность |
Побочные действия |
|
Кортикостероиды |
Вероятна |
+ |
|
Азатиоприн |
Минимальна |
+/- |
|
Циклоспорин |
0 |
++ |
|
D-пеницилламин |
0 |
++ |
|
Метотрексат |
Исследуется |
+ |
|
Колхицин |
Минимальна |
0 |
|
Талидомид |
0 |
++ |
|
Урсодезоксихолевая |
||
|
кислота |
Доказана |
0 |
Пациентка переведена в гастроэнтерологическое отделение для продолжения обследования, где произведена статическая сцинциграфия, пункционная биопсия печени. При статической сцинциграфии отмечено достаточное накопление РФП в печени, распределение его неравномерное с участками гипофиксации в проекции S 2,3,4. Селезенка не увеличена, накопление в ней в пределах нормы, распределение неравномерное. Накопление РФП в РЭС скелета отсутствует. В биоптате печени выявлено наличие гранулем. Гранулематозные поражения печени встречаются при многих заболеваниях и свидетельствуют о генерализации патологического процесса. Они могу иметь место при инфекциях (туберкулез, бруцеллез), системных заболеваниях (саркоидоз, болезнь Крона) — см. табл. 4.
Гранулемы любого происхождения сходны по гистологической картине, локализуются всегда с портальными трактами и не нарушают архитектоники (табл. 5) [14].
В данном случае были обнаружены гранулемы с отсутствием казеоза, характерные для саркоидоза (рис.1).
Таблица 4. Этиология гранулематоза печени
|
Этиология |
Примеры |
|
Инфекции |
• Вирусные: |
|
- цитомегаловирус, |
|
|
- инфекционный мононуклеоз; |
|
|
• бактериальные: |
|
|
- бруцеллез, |
|
|
- туберкулез; |
|
|
• рикеттсиозные: |
|
|
- Ку-лихорадка; |
|
|
• спирохетозные: |
|
|
- бледная спирохета; |
|
|
• паразитарные: |
|
|
- шистосомоз |
|
|
Первичный бшшарный цирроз |
• Более часто на ранних стадиях |
|
• Инородное тело |
|
|
• Шовный материал |
|
|
• Тальк |
|
|
Системные заболевания |
• Саркоидоз |
|
• Болезнь Крона |
|
|
Лекарственные препараты |
* Аллопуринол |
|
• Сульфаниламиды |
|
|
• Антибиотики |
|
|
Опухоли |
• Неходжкинская лимфома |
|
* Лимфогранулематоз |
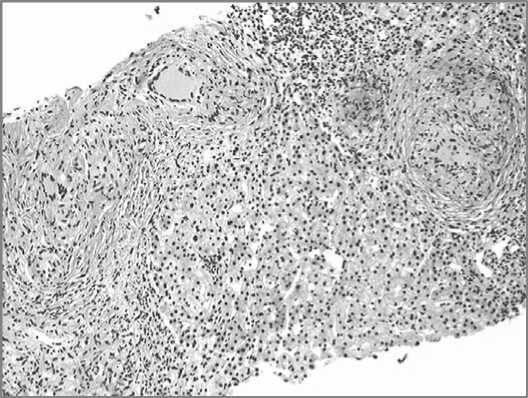
рисунок 1. Саркоидные гранулемы печени
Таким образом, у пациентки установлено второе заболевание — мультисистемный относительно доброкачественный гранулематоз неизвестной этиологии, характеризующийся скоплением активизированных Т-лимфоцитов (СD4+) и мононуклеарных фагоцитов, и образованием несекретирующих эпителиоидноклеточных гранулем в различных органах, т. е. саркоидоз [15].
Считается, что саркоидоз вызывается внешними агентами как триггерами иммунного ответа у генетически предрасположенных людей. Возникновение саркоидоза и его тяжесть связывают с генами гистосовместимости HLA, генами ответственными за выработку ангиотензинпревращающего фермента (АПФ), фактора некроза опухолей (ФНО- ) и др.
Как известно, главными мишенями саркоидоза являются легкие, лимфатическая система.
Клинические проявления варьируют от случайно выявленных на рентгенограмме изменений до хронической прогрессирующей дисфункции органов, церебральных и сердечно-сосудистых поражений.
При хроническом течении на первый план выступают слабость, утомляемость (в 90% случаев), кашель, боли в грудной клетке, суставах, одышка, сердцебиение. У наблюдавшейся пациентки можно говорить о клини-
Таблица 5. Характеристика гранулем
Фактически диагноз был документирован только благодаря биопсии ткани печени, т. е. путем выявления внелегочного саркоидоза, которому свойственно поражение практически всех органов и систем (табл. 6); но поражение печени занимает первое место (50-80%). При этом гранулемы в биоптатах находят довольно часто, тогда как гепатомегалию и лабораторные сдвиги — менее чем у 20% больных [15].
Итак, у пациентки наличествует аутоиммунный гепатит І типа с аутоиммунным перекрестом и системными проявлениями (тиреоидит, кожные стигмы) и саркоидоз 3 степени с поражением лимфоузлов средостения, легких и внелегочными проявлениями (гранулематоз печени).
Рисунок 2 (а, б). Компьютерные томограммы органов грудной клетки больной С. в аксиальной проекции. Изменения, характерные для саркоидоза.
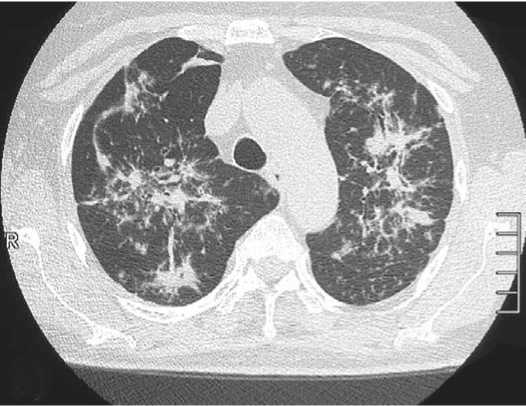
а) Срез на уровне дуги аорты, режим визуализации легочной ткани. Выявляются множественные мелкие очаги, сливающиеся в небольшие инфильтраты, большинство из которых прилежат к артериям и бронхам.
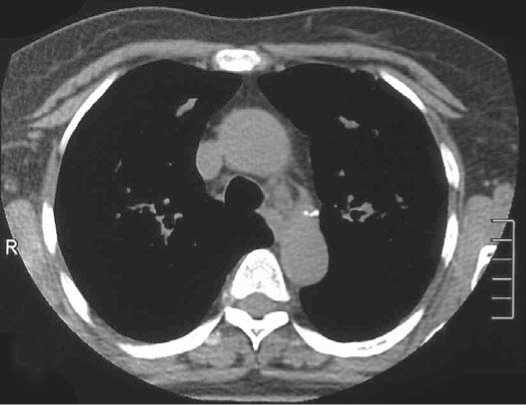
б) Срез на 1 см ниже дуги аорты, режим визуализации органов средостения. Увеличение лимфатических узлов парааортальной и паратрахеальной групп.
Таблица 6. Основные внелегочные проявления саркоидоза
|
Локализация |
Частота |
Проявления |
|
Печень |
50-80% |
Гранулемы в биоптате обнаруживают часто, но пальпируемые изменения и нарушения функции находят менее чем у 20% пациентов |
|
Глаза |
20-50% |
Увеит (передний и задний), снижение зрения. Узлы в коньюнктиее, увеличение слезных желез |
|
Селезенка |
10-40% |
Спленомегалия |
|
Суставы, кости |
25-39% |
Артралгия, острый и хронический артрит. Кистозные образования в костях (рис. 11-21) |
|
Периферические лимфатические узлы |
33% |
Наиболее часто пальпируются шейные (чаще заднего треугольника, чем переднего), аксиллярные, эпитрохлеарные и паховые лимфатические узлы. Увеличенные узлы дискретны, подвижны, безболезненны, без изъязвлений и дренирующихся карманов |
|
Кожа; узловатая эритема |
6-30% |
Глубокий васкулит кожи, наиболее частый клинико-патологический вариант панникулита (рис. 11-22, см. цв. вклейку). В биоптате нет гранулемы |
|
Кожа: другие поражения |
25% |
Макуло-папулярные изменения, подкожные узлы, lupus pernio, гипо- или гиперпигментация, келоид (рис. 11-23, 11-24, см. цв. вклейку) |
|
Кровь |
4-20% |
Поражения костного мозга |
|
ЛОР-органы |
1-15% |
Поражается нос, реже - носовые кости и околоносовые пазухи: хронический насморк с затруднением дыхания, сухой ринит с корками. Саркоидоз носоглотки напоминает аденоид. Саркоидоз небных миндали обычно выявляется после тонзилэктомии как гистологическая находка. Саркоидоз гортани обычно проявляется диффузной инфильтрацией наружного |
|
кольца, полипо- или опухолевидными инфильтратами, приводящими к стенозу, иногда требующему трахео-стомии. Поражение среднего уха, тугоухость, глухота, вестибулярные расстройства |
||
|
Нервная система |
10% |
Менингеальная инфильтрация и воспаление, энцефалопатия. Односторонний паралич лицевого нерва. Нейропатия мелких волокон |
|
Почки |
до 10% |
Нефролитиаз и его последствия. Редко интерстици-альный нефрит |
|
Эндокринные железы |
5-8% |
Несахарный диабет, гиперпролактинемия. Гипотиреоидизм, гипогонадизм, гипоадренализм и нарушения роста |
|
Околоушная слюнная железа |
6% |
Односторонний или двусторонний паротит, проявляющийся опуханием и болезненностью желез |
|
Сердце |
5% |
От доброкачественной аритмии или сердечных блокад разной степени до внезапной смерти |
|
Мужские половые органы |
<1% |
Плотные эластичные образования в эпидидимусе. Редкие случаи поражения простаты и полового члена |
|
Женские половые органы |
<1% |
Метроррагии. Бесплодие |
Едва ли можно сомневаться, что имеют место два сочетающихся заболевания. Достаточно обратиться к соответствующим литературным источникам (табл. 7) [17].
При подобном сочетании более чем одно системное проявление выявляется примерно у 80% больных, более чем два — у 40%.
Значение системных проявлений нельзя переоценить, поскольку они нередко являются дебютом болезни, либо приобретают ведущее значение в клинической картине заболевания (до20%) и могут определять прогноз.
Известно, что обнаруживаемые при АИГ аутоантитела, являясь главными доказательствами заболевания, не становятся патогенными и отдельные типы аутоантител не обязательно сочетаются с определенными заболеваниями. АИГ ІІ типа, например, является одним из компонентов аутоиммунного синдрома І типа (APECED) [16,18].
Высказывается предположение о возможности существования «малых» мутаций аутоиммунного регулятора І типа, могущих быть причиной развития одного или двух аутоиммунных заболеваний в течение жизни [19].
В заключении целесообразно обсудить прогноз у наблюдаемой нами пациентки.
Если говорить только об АИГ, то прогноз является относительно благоприятным; 10-летняя выживаемость составляет в среднем 93%. Длительное использование иммуносупрессантов позволяет достигнуть 10-20летней выживаемости у 20% больных.
Однако у нашей пациентки имеет место аутоиммунный перекрест, когда сочетаются биохимические и гистологические признаки АИГ и ПБЦ, что несомненно значимо для прогноза. Так, при бессимптомном течении болезни продолжительность жизни заметно больше. По данным различных авторов, средняя выживаемость больных с клиническими проявлениями болезни составляет 7,5-10 лет, при бессимптомном 10-16 лет. Клинические проявления у большинства больных с бессимптомным течением развиваются в течение 2-4 лет с момента выявления болезни; наличие и титр АМА не влияет на выживаемость.
Таким образом, можно было бы предполагать относительно благоприятное течение гепатита у больной С., однако сочетание в данном случае АИГ и саркоидоза с поражением печени отягощает прогноз, хотя возможны случаи спонтанной ремиссии саркоидоза, наступающей примерно у больных с бессимптомным течением болезни.
Таблица 7. Внепеченочные проявления и сочетающиеся заболевания при первичном билиарном циррозе
|
эндокринные |
Аутоиммунный тиреоидит Диффузный токсический зоб Сахарный диабет 1 типа Надпочечниковая недостаточность |
|
экзокринные |
Синдром Шегрена Недостаточность поджелудочной железы Аутоиммунная тромбоцитопепия |
|
гематологические |
Аутоиммунная гемолитическая анемия |
|
кожные |
Красный плоский лишай |
|
нейромышечные и суставные |
Артропатия (неэрозивная) Ревматоидный артрит Злокачественная миастения Миелит |
|
почечные |
Гломерулонефрит Почечный канальцевый ацидоз |
|
легочные |
Фиброзируюший альвеолит Саркоидоз |
|
кишечные |
Целиакия Язвенный колит Болезнь Крона |
|
ревматические |
Синдром Рейно Системная склеродермия CREST-синдром Системная красная волчанка Дерматомиозит Полимиозит Антифосфолипидный синдром |
КОММЕНТАРИЙ НАУЧНОГО РЕДАКТОРА
Приведенный выше случай сочетания двух достаточно редких заболеваний является одним из немногих примеров, описанных в медицинской литературе, не только в России, но и за рубежом. Однако, на наш взгляд, данная ситуация требует дополнительного обсуждения и не должна трактоваться однозначно. Дело в том, что саркоидное поражение печени может вызвать ряд симптомов, сходных с картиной аутоиммунного гепатита (АИГ) и цирроза печени – повышение уровня печеночных ферментов, гипергаммагло-булинемию, гепатомегалию, симптомы холестаза и даже портальную гипертензию [1]. В таком случае в основу диагноза АИГ должны быть положены результаты гистологического исследования ткани печени и доказательства аутоиммунной природы процесса, т.е присутствие аутоантител. В описанном примере биопсия печени выявила лишь саркоидные гранулемы без признаков воспаления паренхимы. Таким образом, главным аргументом в пользу АИГ стал высокий уровень антимитохондриальных антител (АМАТ). Необходимо заметить, что АМАТ являются важным биомаркером первичного билиарного цирроза печени (ПБЦ), в то время как при АИГ встречаются примерно в 20% случаев [2]. Кроме того, один из наиболее авторитетных исследователей проблемы гепатита Albert Czaja, на работы которого дважды ссылаются авторы обсуждаемого клинического разбора, предупреждает о возможности ложно-положительных титров АМАТ, доходящих при АИГ до 27% [3,4].
Интересно, что повышенный сыворточный уровень АМАТ описан при саркоидозе печени без ПБЦ [5,6]. В биопсийном материале 146 пациентов с признаками поражения печени и присутствием (методом иммуно-гистохими) АМАТ саркоидные гранулемы выявлены у одного больного [7].
Однако в целом .АМАТ при печеночном саркоидозе встречаются весьма редко и даже являются одним из дифференциальных критериев саркоидоза и ПБЦ [8,9]
Что касается аутоиммунного тиреоидита, то его комбинация саркоидозом, хотя и более редкая, чем с АИГ, но встречается у 9% пациентов [10]. Антитиреоидные антитела выявляются по данным разных исследований у более чем у 50% пациентов с саркоидозом [11,12].
Таким образом, несмотря на присутствие у больной клинико-лабораторных критериев АИГ, нельзя полностью исключить редкий вариант саркоидного поражения печени, мимикрирующий гепатит и ПБЦ. Дальнейшее наблюдение за пациенткой и повторное получение гистологического материала, вероятно, даст нам окончательный ответ о природе заболевания.
Список литературы Аутоиммунный гепатит в сочетании с саркоидозом (клиническое наблюдение)
- Karagiannidis A; Karavalaki M;Koulaouzidis A Hepatic sarcoidosis Annals of Hepatology 2006; 5(4): October-December: 251-256
- Kenny RP, Czaja AJ, Ludwig J, Dickson ER. Frequency and significance of antimitochondrial antibodies in severe chronic active hepatitis. Dig Dis Sci. 1986; 31:705-11
- Czaja AJ, Manns MP, Homburger HA. Frequency and significance of antibodies to liver/kidney microsome type 1 in adults with chronic active hepatitis. Gastroenterology. 1992; 103:1290-5
- Czaja AJ The Variant Forms of Autoimmune Hepatitis. Ann Int Med, 1996 vol. 125 no. 7 588-598
- Periera-Lima J, Schaffner F. Chronic cholestasis in hepatic sarcoidosis with clinical features resembling primary biliary cirrhosis:report of two cases. Am J Med 1987; 83: 144-148.
- Devaney K, Goodman ZD, Epstein MS, Zimmerman HJ, Ishak KG. Hepatic sarcoidosis: clinicopathologic features in 100 patients. Am J Surg Pathol 1993; 7: 272-280.
- Foschini MP, Macchia S, Losi L Identification of mitochondria in liver biopsies. A study by immunohistochemistry, immunogold and Western blot analysis Virchows Arch. 1998 Sep;433(3):267-73
- Eklund A, Stjernberg N, Uddenfeldt P, Danielsson A Kveim test and mitochondrial antibodies in the differential diagnosis between primary biliary cirrhosis and sarcoidosis Sarcoidosis. 1985 Mar;2(1):38-41.
- Valla D, Benhamou JP. Sarcoidosis and the liver. In: Gitlin N (ed): ThеLiver and Systemic Disease. New York, Churchill Livingstone, 1997.
- Papadopoulos KI, Hornblad Y, Liljebladh H, et al. High frequency of endocrine autoimmunity in patients with sarcoidosis. Eur J Endocrinol 1996; 134:331-336
- Hugues JN, Modigliani E, Battesti JP, et al. Thyroid disorders during sarcoidosis. Ann Med Interne (Paris) 1981; 132:367-371
- Antonelli A, Fazzi P, Fallahi P, Prevalence of Hypothyroidism and Graves Disease in Sarcoidosis Chest 2006;130;526-532


