Биоэлектрокаталитическое восстановление кислорода бактериальными лакказами на электродах, модифицированных многостенными углеродными нанотрубками
Автор: Алферов С. В., Федина В. В., Егоров К. А., Трубицина Л. И.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 2 (100) т.86, 2024 года.
Бесплатный доступ
В данной работе проведено исследование электрохимического поведения биоэлектродов на основе бактериальных лакказ Streptomyces carpinensis VKM Ac-1300, полученных с использованием различных способов иммобилизации. Биоэлектроды формировали путем закрепления фермента на поверхности электрода простой адсорбцией, методом адсорбции на предварительно модифицированном электроде многостенными углеродными нанотрубками и путем ковалентной сшивки фермента по карбоксильным группам с функционализированными многостенными углеродными нанотрубками. Оценка ориентации иммобилизованных ферментов лакказ и их способности к прямому и медиаторному электронному переносу проводилась методом прямой амперометрии при постоянном потенциале. Установлено, что в зависимости от метода иммобилизации правильную ориентацию и, как следствие, возможность прямого переноса электронов имеет от 5 до 10% иммобилизованного фермента. При этом ковалентное пришивание белка на поверхности модифицированных нанотрубками графитовых электродов приводит к более активному прямому переносу электронов, увеличению скорости восстановления кислорода и долговременной стабильности электродов. Таким образом, для бактериальных лакказ Streptomyces carpinensis VKM Ac-1300 показана возможность прямого переноса электронов при их иммобилизации путем ковалентного пришивания по карбоксильным группам многостенных углеродных нанотрубок, разработанные биоэлектроды могут быть использованы в качестве катодов в биотопливных элементах.
Лакказы, иммобилизация, перенос электронов, ковалентное связывание, углеродные нанотрубки
Короткий адрес: https://sciup.org/140306918
IDR: 140306918 | УДК: 640 | DOI: 10.20914/2310-1202-2024-2-126-131
Bioelectrocatalytic oxygen reduction by bacterial laccase on electrodes modified with multi-walled carbon nanotubes
In this work, the electrochemical behaviour of bioelectrodes based on bacterial laccase Streptomyces carpinensis VKM Ac-1300 obtained using different immobilization methods was investigated. The bioelectrodes were formed by fixing the enzyme on the electrode surface by simple adsorption, by adsorption on the modified electrode by multi-walled carbon nanotubes and by covalent bounding of the enzyme by carboxyl groups with functionalized multi-walled carbon nanotubes. The orientation of immobilized laccase enzymes and their ability to direct and mediated electron transfer were assessed by direct amperometry at constant potential. It was found that, depending on the method of immobilization, from 5 to 10% of immobilized enzyme has the correct orientation and, consequently, the ability to direct electron transfer. At the same time, covalent bounding of protein on the surface of graphite electrodes modified with nanotubes leads to a more active direct electron transfer, an increase in the rate of oxygen reduction and long-term electrode stability. Thus, for bacterial laccase Streptomyces carpinensis VKM Ac-1300 the possibility of direct electron transfer at their immobilization by covalent bounding with carboxyl groups of multi-walled carbon nanotubes was shown. The developed bioelectrodes can be used as cathodes in biofuel cells.
Текст научной статьи Биоэлектрокаталитическое восстановление кислорода бактериальными лакказами на электродах, модифицированных многостенными углеродными нанотрубками
Ферменты лакказы (benzenediol:oxygen oxidoreductase, EC 1.10.3.2) находят практическое применение в различных отраслях промышленности: пищевой, текстильной, целлюлознобумажной, косметической [1, 2]. Благодаря способности быстро восстанавливать кислород лакказы применяются при создании биокатодов в биотопливных элементах [3, 4]. Ключевым моментом при разработке биокатодов топливных элементов является выбор способа иммобилизации фермента, который обеспечивал бы надежность, технологичность, воспроизводимость и стабильность получаемых характеристик. Особенностью строения активного центра лакказ является наличие Т1 центра – первичного акцептора электронов, который передает электроны в медный кластер Т2/Т3, где происходит связывание и разрывание связей кислород-кислород. Для доставки электронов в этот каталитический центр возможны 2 механизма – опосредованный медиаторами и прямой перенос электронов (ППЭ).
Медиаторный перенос электронов предполагает использование редокс-соединений, которые облегчают перенос электронов от электрода к центру Т1. Однако с практической точки зрения, отсутствие медиаторов упрощает процесс изготовления биокатодов. Прямой перенос электрона между электродом и лакказой возможен только в том случае, если фермент правильно ориентирован на поверхности электрода, т. е. активный центр Т1 находится достаточно близко к электроду для осуществления прямого переноса электронов [1, 3, 4]. Для достижения оптимальной ориентации фермента при изготовлении биокатодов в БТЭ используют такие методы иммобилизации как адсорбция и ковалентное связывание. Так как метод адсорбции основан на случайном закреплении молекул белка на поверхности электрода, это может приводить к заметному снижению эффективности прямого транспорта электронов. Именно поэтому перед закреплением фермента проводят модификацию электродов с помощью наноструктурированных материалов. В частности, углеродные нанотрубки (УНТ) могут использоваться для улучшения электрохимического контакта электродов с окислительно-восстановительными центрами ферментов. УНТ могут находиться в непосредственной близости к активному центру и тем самым способствовать прямому переносу электронов между ферментом и электродом [5]. Однако наличие только УНТ бывает недостаточно, поэтому нанотрубки дополнительно модифицируются полициклическими ароматическими соединениями (ПАУ), которые являются аналогами субстрата лакказ (антрацен, антрахинон, нафталин), что способствуют правильной ориентации фермента [6, 7]. Другим подходом для иммобилизации лакказ
Цель работы – выбор метода иммобилизации бактериальных лакказ Streptomyces carpinensis для формирования стабильных биоэлектродов, которые потенциально могут быть использованы как биокатоды в БТЭ.
Материалы и методы
Все реактивы, использованные в работе, были квалификации ХЧ и ЧДА и приобретены в Sigma-Aldrich.
Адсорбция лакказы на графитовом электроде. Грифели («STABILO», HB, 2 мм) очищали мелкодисперсной наждачной бумагой (Р1200). Адсорбцию проводили путем погружения в раствор фермента лакказы Streptomyces carpinensis (3.0 ± 0.2 мг/мл, буфер 20 мМ Tris-HCI, рН 8.0, 0.2 5М NaCl, 0.3 M имидазол) на 24 часа.
Адсорбция лакказы на карбоксилированных нанотрубках. Грифели («STABILO», HB, 2 мм) промывали дистиллированной водой и обрабатывали ультразвуком в ацетоне в течении 5 мин. Обработанные электроды сушили при 90 °С в течение 2 ч для удаления растворителя. Кар-боксилированные многослойные нанотрубки (МУНТ-COOH) серии «Таунит-М» («Нано ТЦ», Томск) диспергировали в диметилсульоксиде ультразвуком в течение 2 мин. Электроды погружали в полученную суспензию нанотрубок на 5 мин, после чего помешали в ток горячего воздуха на 2 ч для удаления избытка растворителя. Процедуру повторяли 4 раза. Адсорбцию проводили путем погружения в раствор фермента лакказы Streptomyces carpinensis (3.0 ± 0.2 мг/мл, буфер 20 мМ Tris-HCI, рН 8.0, 0.25М NaCl, 0.3 M имидазол) на 24 часа.
Ковалентное связывание лакказы. Активацию карбоксильных групп на модифицированных МУНТ-COOH электродах проводили путем погружения в раствор 1-циклогексил-(2-морфолиноэтил) карбодиимид метоп-толу-олсульфоната (3 мг/мл в фосфатном буферном растворе (0.1 М, рН = 7)) на 2 ч. Ковалентную сшивку проводили путем погружения в раствор фермента лакказы Streptomyces carpinensis (3.0 ± 0.2 мг/мл, буфер 20 мМ Tris-HCI, рН 8.0, 0.25М NaCl, 0.3 M имидазол) на 24 часа.
Для удаления избытка несвязанного белка во всех случаях электроды промывали цитратным буферным раствором рН 4.5.
Электрохимические измерения проводили при помощи гальванопотенциостата «IPC-micro» («Kronas», Москва, Россия), интегрированного с ПК. Измерения проводили по двухэлектродной схеме (электрод сравнения Ag/AgCl) в цитратном буфере с рН 4.5, объем ячейки – 4 мл. Перед измерением буферный раствор дегазировали, ячейка продувалась аргоном до содержания кислорода 0 мг/мл, содержание кислорода контролировали с помощью кислородного электрода. Для насыщения буферного раствора кислорода включалась мешалка (скорость перемешивания 200 об/мин). Измеряемым параметром являлась амплитуда сигнала изменения силы тока рабочего электрода, определяемая как разность между начальным и конечным значениями токов в анаэробных и аэробных условиях. Измерения проводились при постоянном потенциале рабочего электрода 200 мВ [1]. Для определения лакказ, способных только к прямому переносу электронов оценку изменения силы тока проводили только в присутствии кислорода. Для определения лакказ, способных только к медиаторному переносу электронов в ячейку добавляли раствор субстрата АБТС (концентрация в ячейке 790 мкмоль).
Результаты
В работе были сформирована три типа электродов. Фермент закрепляли на поверхности электрода простой адсорбцией (электрод A), методом адсорбции на предварительно модифицированном электроде многостенными углеродными нанотрубками (электрод B) и путем ковалентной сшивки фермента по карбоксильным группам МУНТ-СООН, (электрод C). Типичный вид зависимости изменения силы тока от времени представлен на рисунке 1.
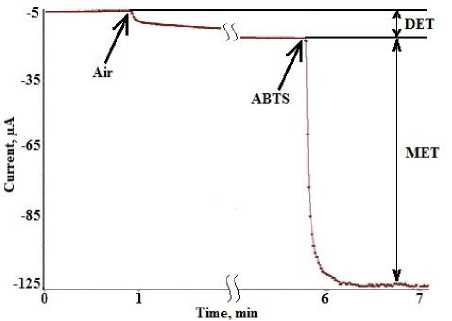
Рисунок 1. Зависимость изменения силы тока от времени для электрода A. DET – прямой перенос электронов, MET – перенос электронов с помощью медиатора
Figure 1. The dependence of the current on time for electrode A. DET - direct electron transfer, MET -mediated electron transfer
Начальное изменение силы тока при насыщении ячейки воздухом соответствует прямому переносу электронов от электрода на активный центр фермента и дальнейшему восстановлению кислорода. Изменение силы тока после добавления АБТС соответствует медиаторному переносу электронов на активный центр фермента и дальнейшему восстановлению кислорода.
Для каждого типа электродов была определена операционная стабильность. Результаты представлены в виде зависимости плотности тока от числа измерений (рисунок 2).
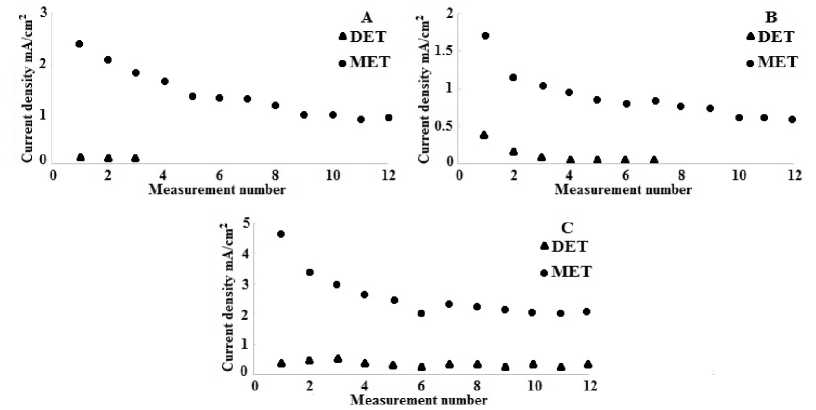
Рисунок 2. Эксплуатационная стабильность электродов с различными типами иммобилизации фермента лакказы. A - адсорбция на графитовом электроде, B - адсорбция на графитовом электроде, модифицированном МУНТ, C - ковалентное связывание с COOH-МУНТ на графитовом электроде
Figure 2. Operational stability of electrodes with different types of laccase enzyme immobilization. A - adsorption on graphite electrode, B - adsorption on graphite electrode modified with MWCNT, C - covalent bounding with MWCNT-COOH on graphite electrode
Для каждого типа электродов выполнена оценка максимальной скорости восстановления кислорода ферментом в режиме ППЭ. Параметр определялся как тангенс наклона прямой падения тока рабочего электрода. Скорости составили: для электрода A – 3,1 ± 0,3 мА • 10-3/мин, для электрода B – 7,7 ± 0,4 мА • 10-3/мин и для электрода C – 66 ± 4 мА • 10-3/мин.
Обсуждение
Применение метода амперометрии для оценки активности иммобилизованных ферментов лакказ ранее рассматривалось в работах [10, 11]. Данный метод позволяет оценить возможности иммобилизованного фермента к прямому переносу электронов, а значит судить о правильности ориентации активного центра фермента относительно поверхности электрода, и кроме того выполнить оценку максимальной скорости восстановления кислорода лакказами в режиме ППЭ. Полученные данные позволяют заключить, что наиболее перспективным методом закрепления является именно ковалентная сшивка фермента по карбоксильным группам с МУНТ-СООН на поверхности электрода. Данный метод позволяет на порядок увеличить скорость прямого ППЭ по сравнению с адсорбцией фермента на предварительно модифицированном электроде.
Оценка операционной стабильности электродов показывает, что для простой адсорбции эффект ППЭ исчезает уже после 3-го измерения, а для адсорбции на МУНТ после 7-го измерения, что свидетельствует о десорбции белка. Подобное поведение лакказ было ранее отмечено в работах [12, 13–20]. При использовании метода ковалентной сшивки сигнал биоэлектрода оставался стабильным, по крайней мере, в течение 12 измерений, что подтверждает правильность выбранного подхода закрепления фермента для его правильной ориентации и соответствует литературным данным [9].
Заключение
Для рекомбинантных бактериальных лакказ Streptomyces carpinensis показана возможность прямого переноса электронов на кислород при иммобилизации на поверхности графитового электрода. Наиболее перспективным методом иммобилизации является ковалентное связывание фермента с модифицированными углеродными нанотрубками. Данный метод способствует правильной ориентации фермента и как следствие, увеличению скорости восстановления кислорода и стабильности биоэлектрода во времени. Разработанные биоэлектроды могут быть использованы в качестве катодов в биотопливных элементах.
Работа выполнена при финансовой поддержке Министерства науки и высшего образования РФ в рамках государственного задания № FEWG-2024-0003 (Биокаталитические системы на основе клеток микроорганизмов, субклеточных структур и ферментов в сочетании с наноматериалами).
Список литературы Биоэлектрокаталитическое восстановление кислорода бактериальными лакказами на электродах, модифицированных многостенными углеродными нанотрубками
- Fernández-Fernández M., Sanromán M.Á., Moldes D. Recent developments and applications of immobilized laccase // Biotechnol. Adv. 2013. №31 (8). P. 1808-1825.
- By S., Arsenault A., Hassani T., Jones J. P., Cabana H. Laccase immobilization and insolubilization: From fundamentals to applications for the elimination of emerging contaminants in wastewater treatment // Crit. Rev. Biotechnol. 2013. №33 (4). P. 404-418.
- Le Goff A., Holzinger M., Cosnier S. Recent progress in oxygen-reducing laccase biocathodes for enzymatic biofuel cells Cell // Mol. Life Sci. 2015. №72. P. 941-952.
- Zhang Y. et al. Application of eukaryotic and prokaryotic laccases in biosensor and biofuel cells: recent advances and electrochemical aspects // Appl. Microbiol. Biotechnol. 2018. №102 (24). P. 10409-10423.
- Holzinger M., Le Goff A., Cosnier S. Carbon nanotube/enzyme biofuel cells // Electrochimica Acta. 2012. №82. P. 179-190.
- Stolarczyk K. et al. Hybrid biobattery based on arylated carbon nanotubes and laccase // Bioelectrochemistry. 2012. №87. P. 154-163.
- Giroud F. et al. Simplifying enzymatic biofuel cells: immobilized naphthoquinone as a biocathodic orientational moiety and bioanodic electron mediator // ACS Catalysis. 2015. №5 (2). P. 1240-1244.
- Bandapati M., Krishnamurthy B., Goel S. Fully assembled membraneless glucose biofuel cell with MWCNT modified pencil graphite leads as novel bioelectrodes // IEEE Transactions on Nanobioscience. 2019. №18 (2). P. 170-175.
- Gáspár S., Brinduse E., Vasilescu A. Electrochemical evaluation of laccase activity in must // Chemosensors. 2020. №8 (4). P. 126.
- Ruff A. et al. A fully protected hydrogenase/polymer-based bioanode for high-performance hydrogen/glucose biofuel cells // Nature communications. 2018. №9 (1). P. 3675.
- Olszewski B., Stolarczyk K. Laccase-catalyzed reduction of oxygen at electrodes modified by carbon nanotubes with adsorbed promazine or acetosyringone // Catalysts. 2018. №8 (10). P. 414.
- Wu F. et al. Role of organic solvents in immobilizing fungus laccase on single-walled carbon nanotubes for improved current response in direct bioelectrocatalysis // Journal of the American Chemical Society. 2017. №139 (4). P. 1565-1574.
- Gutiérrez-Sánchez C. et al. Enhanced direct electron transfer between laccase and hierarchical carbon microfibers/carbon nanotubes composite electrodes. Comparison of three enzyme immobilization methods // Electrochimica acta. 2012. №82. P. 218-223.
- Dey B., Dutta T. Laccases: Thriving the domain of bio-electrocatalysis // Bioelectrochemistry. 2022. V. 146. P. 108144.
- Lopes P., Koschorreck K., Nedergaard Pedersen J., Ferapontov A. et al. Bacillus Licheniformis CotA Laccase mutant: ElectrocatalyticReduction of O2 from 0.6 V (SHE) at pH 8 and in seawater // ChemElectroChem. 2019. V. 6. №. 7. P. 2043-2049.
- Han Z., Zhao L., Yu P., Chen J. et al. Comparative investigation of small laccase immobilized on carbon nanomaterials for direct bioelectrocatalysis of oxygen reduction // Electrochemistry Communications. 2019. V. 101. P. 82-87.
- Zhou Y., Umasankar Y., Ramasamy R.P. Laccase-TiO2 nanoconjugates as catalysts for oxygen reduction reaction in biocathodes // Journal of The Electrochemical Society. 2015. V. 162. №. 14. P. H911.
- Franco A., Cebrián-García S., Rodríguez-Padrón D., Puente-Santiago A.R. et al. Encapsulated laccases as effective electrocatalysts for oxygen reduction reactions // ACS sustainable chemistry & engineering. 2018. V. 6. №. 8. P. 11058-11062.
- Lalaoui N., David R., Jamet H., Holzinger M. et al. Hosting adamantane in the substrate pocket of laccase: direct bioelectrocatalytic reduction of O2 on functionalized carbon nanotubes // Acs Catalysis. 2016. V. 6. №. 7. P. 4259-4264.
- Zhang L., Cui H., Zou Z., Garakani T.M. et al. Directed evolution of a bacterial laccase (CueO) for enzymatic biofuel cells // Angewandte Chemie International Edition. 2019. V. 58. №. 14. P. 4562-4565.


