Динамика влияния NPY на амплитудно временные показатели изометрического сокращения миокарда предсердий
Автор: Искаков Н.Г., Зверев А.А., Искакова Е.В., Николаев Т.И., Аникина Т.А., Зефиров Т.Л.
Статья в выпуске: 4 т.260, 2024 года.
Бесплатный доступ
Цель исследования было изучение динамики влияния нейропептида Y (NPY) на частоту и амплитудно-временные параметры изометрического сокращения предсердного миокарда крыс в раннем постнатальном онтогенезе. В представленной работе изучали влияние неселективного агониста NPY на частоту спонтанной активности и сократимость предсердного миокарда крыс на разных этапах становления симпатической иннервации. NPY у 7-суточных животных вызывает разнонаправленный эффект на частоту спонтанной активности, а у 100-суточных животных достоверно уменьшает. Основные параметры изометрического сокращения при добавлении NPY уменьшаются в сравнении с контрольными значениями.
Нейропептид y, сердце, миокард, изометрическое сокращение, частота спонтанной активности
Короткий адрес: https://sciup.org/142243211
IDR: 142243211 | УДК: 612.17 | DOI: 10.31588/2413_4201_1883_4_260_105
Dynamics of the influence of NPY on amplitude-temporal indicators of isometric contraction of atrial myocardium
The purpose of the study was to study the dynamics of the influence of neuropeptide Y (NPY) on the frequency and amplitude-time parameters of isometric contraction of the atrial myocardium of rats in early postnatal ontogenesis. In this work, we studied the effect of a non-selective NPY agonist on the frequency of spontaneous activity and contractility of the rat atrial myocardium at different stages of the formation of sympathetic innervation. NPY in 7-day-old animals has a multidirectional effect on the frequency of spontaneous activity and significantly reduces it in 100-day-old animals. The main parameters of isometric reduction are reduced with the addition of NPY compared to control values.
Текст научной статьи Динамика влияния NPY на амплитудно временные показатели изометрического сокращения миокарда предсердий
Нейропептид Y (NPY) высококонсервативный пептид, состоящий из 36 аминокислот, который был впервые выделен из гипоталамуса свиньи в 1982 году Tatemoto [15]. NPY является классическим нейромедиатором, вырабатываемым в основном симпатическими нейронами [8]. Пептид является одним из наиболее распространенных в сердце и головном мозге млекопитающих [6]. На данный момент у позвоночных животных обнаружено восемь различных Y-рецепторов (R) (Y1-Y8) [7], из которых пять (Y1R, Y2R, Y4R, Y5R и Y6R)
клонированы у млекопитающих, а четыре (Y1R, Y2R, Y4R и Y5R) доказали свою функциональность в организме человека [10].
В центральной и периферической нервной системе Y(R) кодируются разными генами и имеют различное распределение в тканях, а также внутриклеточные сигнальные пути, это доказывает о том, что они участвуют в различных физиологических процессах. Y(R) представляют собой мономерные белки сопряжённые с G-белками. После активации с рецепторами изменяется положение субъединицы G-белка в результате чего происходят различные внутриклеточные механизмы, приводящие как к ингибированию, так и к активации различных сигнальных каскадов [3]. По литературным данным известно также, что в гладкомышечных клетках кроликов Y2R и Y4R могут связываться с Gq белком и способствовать выработке инозитолтрифосфата (IP3) путем активации фосфолипазы C (PLC) [4]. Показано, что в нейронах мозга крысы Y(R) могут регулировать K+ и Ca2+ каналы, а также связанные с G-белком калиевый ток внутреннего выпрямления. Связываясь с Y (R), NPY играет различные роли в биологических процессах, а иногда даже может функционировать совершенно по-разному.
Y(R) участвуют в физиологических процессах и в заболеваниях, такие как прием пищи, ожирение, гипертония, атеросклероз, эпилепсия, метаболические нарушения, заживление переломов [2]. NPY также регулирует аппетит, половое размножение, обучение и память. Кроме того, он обладает антидепрессивными свойствами [13] и значительно ингибирует обмен костной ткани в экспериментальных моделях [5].
В кровеносной системе NPY регулирует сосудистый тонус, взаимодействуя с симпатической нервной системой. Примечательно, что NPY является признанным регулятором нескольких гормональных систем и участвует в иммунной регуляции [14].
Было показано, что NPY не влияет на инотропию полосок предсердий человека [11]. Отрицательные инотропные эффекты были продемонстрированы в кардиомиоцитах взрослых крыс, а положительные инотропные эффекты были продемонстрированы в кардиомиоцитах взрослых морских свинок [12]. Показано, что NPY и его аналоги замедляют частоту спонтанной активности и влияет разнонаправлено на сократительную функцию миокарда предсердий в онтогенезе [1]. Однако изучение динамики активации нейропептидом Y YR в возрастном аспекте изучено недостаточно.
Материал и методы исследований. В экспериментальную группу входили 7- и 100-дневные белые беспородные крысы (n=34). В ходе эксперимента из сердец крыс в условиях in vitro изготавливались полоски миокарда правого предсердия с сохраненным синусовым узлом и спонтанной активностью. Полоски были погружены в ёмкость с рабочим раствором Тироде, который был обогащен карбогеном. Механическое изометрическое сокращение полосок миокарда проводили на установке "PowerLab" с датчиком силы "MLT 050/D" ("ADInstruments"). В момент «приработки» полоскам миокарда предсердий обеспечивалось максимальное натяжение, после чего оценивался уровень контроля первоначального значения изометрического сокращения. Полученные результаты фиксировались с помощью программного обеспечения «Chart 8.0». Исследование эффекта NPY изучалось в концентрации, варьирующей от 10-8до 106М с 1 по 20 минуту регистрации, так как известен тот факт, что эндогенное содержание NPY в сердечно-сосудистой системе варьирует от микромолярных до миллимолярных концентраций [9].
Эксперимент был проведен поэтапно: регистрация первоначального показателя изометрического сокращения, аппликация NPY и промывка. Длительность отдельно взятого этапа составляла 20 минут. После оценки эффектов NPY у каждой из концентраций препарат отмывали с помощью раствора Тироде, и в дальнейшем, стабилизируя амплитудно-временные параметры изометрического сокращения, фиксировали первоначальный результат для исследования очередной концентрации. Расчеты показателей изометрического сокращения полосок миокарда производились в программе «LabChart 8.0». Оценивались: частота спонтанного сокращения (количество пиков/мин), общая длительность сокращения (момент от начала сокращения до его завершения), амплитуда сокращения (от уровня изолинии до максимального пика сокращения). В экспериментах был использован фармакологический препарат неселективного агониста NPY производства «Sigma-Aldrich», USA. Исходные показатели изометрического сокращения миокарда предсердий принимали за 100 %, тогда как эффект влияния агониста рассчитывали в процентах от первоначальных значений. Статистическая обработка данных проводилась с использованием программ Microsoft Excel и Statistica 13. Достоверность различий рассчитывали по критерию Стьюдента. Статистические данные представлены в виде среднего арифметического и стандартной ошибки среднего (М±m). Исследуемые данные считали статистически значимыми при Р˂0,05, а n-количество использованных препаратов предсердного миокарда.
Результат исследований. В наших экспериментах частота спонтанной активности у 7-дневных крысят в контроле составлял 165 пиков/мин, у 100-суточных животных средний показатель в контроле составлял 85 пиков/мин. Достоверно большие показатели частоты спонтанной активности у новорожденных животных согласуются с литературными данными развития хронотропной функции у животных.
У 7-суточных животных при аппликации NPY в концентрации 10-8М не приводила к достоверным изменениям амплитудно-временных параметров изометрического сокращения предсердного миокарда с 1 по 20 минуту регистрации (n=8). При увеличении концентрации на один порядок наблюдали развитие двухфазного эффекта. Частота спонтанной активности (ЧСА) со 2 минуты регистрации увеличивалась на 15 % (P˂0,05), затем наблюдалось уменьшение к концу эксперимента до 6 % (P˂0,05) по сравнению с контрольными значениями. Уменьшение ЧСА сопровождалось уменьшением амплитуды сокращения на 10 % (P˂0,05; n=10). При концентрации
10-6 М мы также наблюдали наличие двухфазного эффекта. Частота спонтанной активности с 1 и 2 минуты регистрации увеличивалась на 10 % и 8 % (P˂0,05). С 17 по 20 минуты регистрации частота спонтанной активности уменьшалась на 4 % (P˂0,05) (рисунок 1А). Амплитуда сокращения с 1 и по 20 минуты регистрации уменьшалась (P˂0,05). Остальные исследуемые параметры достоверно не изменялись (n=9).
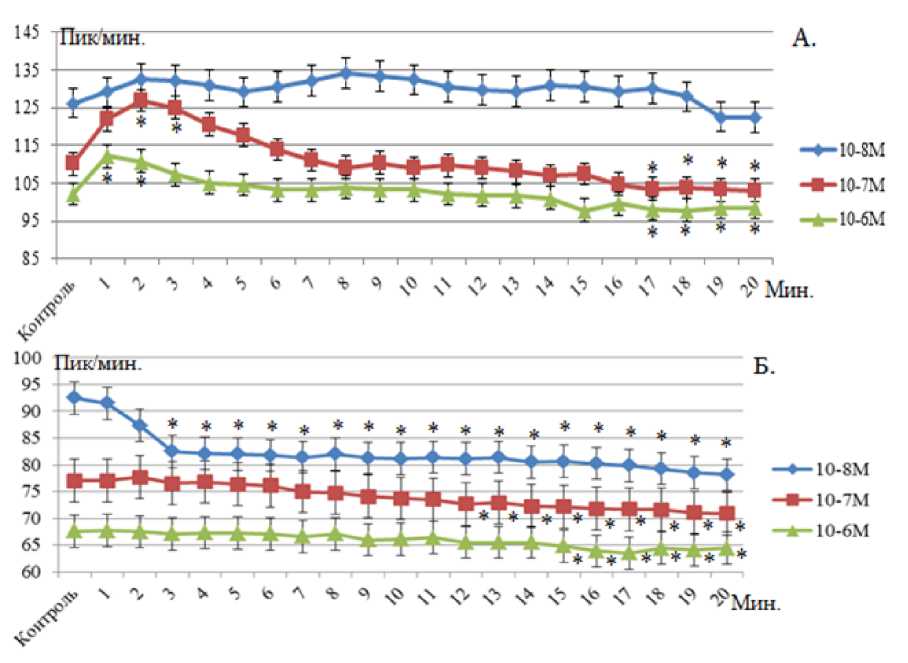
Рисунок 1 – Влияние NPY на частоту спонтанной активности с 1 по 20 минуту регистрации 7(А) - и 100 (Б) -суточных крысят
У 100-суточных животных при аппликации NPY 10-8 М ЧСА с 3 минуты регистрации уменьшалась на 10 % (P˂0,05) и к концу эксперимента уменьшилась на 15 % (P˂0,05) по сравнению с контрольным значением. Амплитуда сокращения и длительность сокращения достоверно не изменялись (n=10). В концентрации 10-7М ЧСА с 12 минуты регистрации уменьшилась на 5 % (P˂0,05). К 20 минуте регистрации ЧСА уменьшилась до 8 % (P˂0,05). Уменьшение ЧСА сопровождалось уменьшением амплитуды сокращения на 8 % (P˂0,05). К
20 минуте регистрации мы наблюдали уменьшение амплитуды сокращения на 12 % (P˂0,05; n=10). NPY в концентрации 10-6 М с 15 минуты регистрации уменьшала ЧСА на 4 % (P˂0,05). К 20 минуте регистрации ЧСА уменьшилась на 5 % (P˂0,05) по сравнению с исходным значением (рисунок 1Б). Уменьшение ЧСА сопровождалось уменьшением амплитуды сокращения на 6 % (P˂0,05) и к концу эксперимента уменьшилась на 8 % (P˂0,05; n=10) по сравнению с контрольным значением. Остальные исследуемые параметры не изменялись.
Заключение. Сердце сокращается под влиянием импульсов, возникающих в синусно-предсердном узле. ЧСА является важным физиологическим параметром не по которому оценивают работу сердца. Отклонения от нормы или наличия аритмий в работе синусного узла ведет к негативному влиянию на организм. Нейропептид Y выделяющийся из симпатических везикул совместно с АТФ и норадреналином способен регулировать работу через метаботропные рецепторы. Необходимо отметить, что пептид свои эффекты осуществляет последним, после норадреналина и АТФ. В наших экспериментах NPY оказывал эффекты у 7-суточных животных положительный на первых 3 минутах, что может быть связано с отсутствием сформированной симпатической иннервацией и NPY оказывает свои эффекты намного раньше. У 100-суточных животных при сформированной нервной регуляции NPY свои эффекты оказывает позже, что согласуется с данными.
Список литературы Динамика влияния NPY на амплитудно временные показатели изометрического сокращения миокарда предсердий
- Искаков, Н. Г. Роль NPY в изменениях параметров потенциала действия рабочих кардиомиоцитов, а также силы и частоты спонтанной активности правого предсердия взрослых крыс / Н. Г. Искаков, А. А. Зверев, Т. А. Аникина, А. С. Шалавина, Д. А. Ирдинкин, Т. Л. Зефиров // Российский кардиологический журнал. – 2021. – Т. 26. – № S5. – С. 37.
- Baldock, P. A. Hypothalamic Y2 receptors regulate bone formation / P. A. Baldock, A. Sainsbury, M. Couzens, R. F. Enriquez, G. P. Thomas, E. M. Gardiner, H. J. Herzog // Clin Invest. – 2002. – V. 109. – № 7. – P. 915-921.
- Colmers, F. Presynaptic inhibition by neuropeptide Y and baclofen in hippocampus: insensitivity to pertussis toxin treatment / F. Colmers // Brain Research. – 1989. – V. 498. – №. 1. – Р. 99-104.
- Heredia, D. P. Neuropeptide Y rapidly enhances [Ca2+] I transients and Ca2+ sparks in adult rat ventricular myocytes through Y1 receptor and Plc activation / D. P. Heredia, M. Delgado, C. Pereira, L. Perrier, R. Richard, S. Vassort // Mol. Cell. Cardiol. – 2005. – V.38. – P. 205-212.
- Diaz-delCastillo, M. Neuropeptide Y and Its Involvement in Chronic Pain / M. Diaz-delCastillo, D. P. D. Woldbye, A. M. Heegaard // Neuroscience. – 2018. – V. 387. – P. 162-169
- Dumont, Y. Neuropeptide, Y., and neuropeptide Y receptor subtypesin brain and peripheral tissues / Y. Dumont, J. C. Martel, A. Fournier, S. St-Pierre, R. Quirion, // Prog. Neurobiol. – 1992. – V. 38. – №. 2. – Р. 125-167.
- Larhammar, D. Ancient Grandeur of the Vertebrate Neuropeptide Y System Shown by the Coelacanth Latimeria chalumnae / D. Larhammar, C. A. Bergqvist // Front. Neurosci. – 2013. – V.8. – P. 7-27.
- Lundberg, J. O. The Nitrate-Nitrite-Nitric Oxide Pathway in Physiology and Therapeutics / J. O. Lundberg, E. Weitzberg, M. T. Gladwin // Nat. Rev. Drug Discov. – 2008. – V. 7. – №. 2. – P. 156-167.
- Maslyukov, P. M. NPY1 receptors are involved in rat myocardial contractility / P. M. Maslyukov, T. A. Anikina, A. A. Zverev, A. V. Krylova, K. Y. Moiseyev, T. L. Zefirov // Bulletin of experimental biology and medicine. – 2016. – V. 162. – №. 10. – P. 410-412.
- Matsumoto, S. Regulation of the phase and period of circadian rhythms restored by suprachiasmatic transplants / S. Matsumoto, J. Basil, A. E. Jetton, M. N. Lehman, E. L. Bittman // J. Biol. Rhythms. – 1996. – V. 11. – №. 2. – P. 145-162.
- Michel, M. C. XVI. International union of pharmacology recommendations for the nomenclature of neuropeptide Y peptide Yy, and pancreatic polypeptide receptors / M. C. Michel, A. Beck-Sickinger, H. Cox, H. N. Doods, H. Herzog, D. Larhammar, R. Quirion, T. Schwartz, T. Westfall // Pharmacol Rev. – 1998. – V. 50. – №. 1. – P. 143-150.
- Millar, B. C. Positive and negative contractile effects of neuropeptide-Y on ventricular cardiomyocytes / B. C. Millar, T. Weis, H. M.Piper, M. Weber, U. Borchard, B. J. Mcdermott, A Balasubramaniam // Am. J. Physiol. – 1991. – V. 6. – №. 2. – P. 1727-1733.
- Stogner, K. Neuropeptide-Y exerts antidepressant-like effects in the forced swim test in rats / K. Stogner, P. V. Holmes // Eur J Pharmacol. – 2000. – V. 387. – №. 2.(387). – P. 9-10.
- Straub, R. H. Neuropeptide Y cotransmission with norepinephrine in the sympathetic nerve-macrophage interplay / R. H. Straub, T. Schaller, L. E. Miller, S. Hörsten, D. S. Jessop, W. Falk, J. Schölmerich // J Neurochem. – 2000. – V. 75. – №. 6. – P. 2464-2471.
- Tatemoto, K. Neuropeptide Y—a novel brain peptide with structural similarities to peptide Yy and pancreatic polypeptide / K. Tatemoto, M. Carlquist, V. Mutt // Nature. – 1982. – V. 296. – P. 659-660.


