Физиолого-биохимические характеристики клеточной культуры Saussurea orgaadayi V. Khan. and Krasnob. при воздействии мета-хлорбензгидрилмочевины
Автор: Головацкая И.Ф., Резниченко А.Е., Лаптев Н.И.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Культуры in vitro
Статья в выпуске: 3 т.56, 2021 года.
Бесплатный доступ
Мета-хлорбензгидрилмочевина (МХБМ) - индуктор монооксигеназной системы человека, ключевые ферменты которой относятся к суперсемейству цитохромов Р-450 (CYP). В настоящее время отсутствуют сведения о роли МХБМ в регуляции жизнедеятельности растений, однако показано участие CYP в превращении вторичных метаболитов, например флавоноидов (Фл), и большинства фитогормонов. Горькуша оргадаай ( Saussurea orgaadayi V. Khan. and Krasnob.) - малоизученный вид растений. Ее клеточная культура, в соответствии с нашими данными, 2-кратно увеличивает суммарное количество эндогенных Фл при переходе от экспоненциального роста в стационарную фазу. В настоящем исследовании впервые показаны статистически значимые (p £ 0,05) различия в ответных ростовых реакциях каллусной культуры S. orgaadayi на действие МХБМ в разных концентрациях. Выявлено, что изменение ростового индекса по сырой и сухой массе обусловлено изменением объема и формы клеток, а также частоты встречаемости разных групп клеток. Впервые исследована динамика содержания флавоноидов, сопровождающая изменения роста культуры под влиянием МХБМ. Целью работы было определение роли мета-хлорбензгидрилмочевины в накоплении флавоноидов и изменчивости цитоморфологических характеристик (линейных размеров, объема и формы клеток, частоты встречаемости разных групп клеток, ростового индекса по сырой и сухой биомассе каллуса) каллусной культуры горькуши оргадаай. Каллусную культуру, полученную на основе семядольных эксплантов из стерильных проростков, многократно пассировали на модифицированной агаризованной питательной среде Мурасиге-Скуга (МС) с добавлением сахарозы, витаминов и регуляторов роста (0,8 мг/л 2,4-дихлорфеноксиуксусной кислоты и 0,5 мг/л 6-бензинаминопурина). Культуру выращивали в темноте при температуре 22-24 °С на среде МС с добавлением регуляторов роста и МХБМ (ООО «Синтегал», Россия) в концентрациях 0,01; 0,1; 1; 10; 100 мкМ. В контроле МХБМ не вносили. Продолжительность субкультивирования составила 30 сут, 2/3 растительного материала использовали для определения сырой и сухой биомассы с последующим выделением флавоноидов, 1/3 материала фиксировали в растворе Кларка в течение 2 сут. Для приготовления микропрепаратов каллусную культуру мацерировали в 3 н. растворе соляной кислоты при постоянном встряхивании до получения однородной суспензии клеток. Цитофотометрический анализ осуществляли с помощью световой микроскопии (видеокамера Moticam 2300, «Motic», Испания) с программным обеспечением. Определяли размеры 100 клеток для каждого варианта, оценивали их форму, вычисляли объем. Для расчета ростового индекса (РИ) определяли начальную (начало субкультивирования, М0) и конечную сырую или сухую массу каллусов (на 30-е сут субкультивирования, М30) и выражали в процентах к контролю: РИ = (М30 - М0)/М0. Количественное определение содержания суммы Фл в каллусной культуре осуществляли на основе их комплексообразования с хлоридом алюминия и последующего измерения оптической плотности окрашенных растворов (спектрофотометр UV-1650, «Shimadzu Corp.», Япония). В результате исследований установлено дозозависимое действие МХБМ на рост клеток за счет их деления (при 0,1 мкМ) и растяжения (1-100 мкМ), которое сопровождалось увеличением РИсыр и РИсух каллусной культуры соответственно в 2,1-3,5 и 1,5-2,9 раза (р сыр, отмеченное на среде с 1 мкМ МХБМ, происходило на фоне снижения суммы Фл на 83 %. Препарат МХБМ можно использовать в растительной биотехнологии в качестве модулятора роста клеток каллусных культур за счет снижения содержания ингибирующих рост метаболитов. Для активации клеточного деления наиболее предпочтительна доза 0,1 мкм МХБМ, тогда как для изменения содержания Фл, 2-кратно увеличивающих биомассу культуры, следует применять 100 мкМ МХБМ.
Saussurea orgaadayi, клеточная культура, мета-хлорбензгидрилмочевина, морфогенез, флавоноиды
Короткий адрес: https://sciup.org/142231373
IDR: 142231373 | УДК: 581.19:581.143.6 | DOI: 10.15389/agrobiology.2021.3.602rus
Influence of meta-chloro-benzhydryl urea on physiological and biochemical characteristics of Saussurea orgaadayi V. Khan. and Krasnob. cell culture
Meta-chloro-benzhydryl urea (m-СBU) is an inducer of the human monooxygenase system, its key enzymes belong to the cytochrome P-450 superfamily (CYP). Currently, there is no information about the role of m-СBU in the plant vital activity regulation; however, the participation of CYP in the metabolism of secondary metabolites, for example, flavonoids (Fl), and most phytohormones have been shown. Saussurea orgaadayi V. Khan. and Krasnob. is a poorly studied plant species. Its cell culture, in accordance with our data, doubles the total amount of endogenous Fl during the transition from exponential growth to the stationary phase. The present study, for the first time shows statistically significant (p
Текст научной статьи Физиолого-биохимические характеристики клеточной культуры Saussurea orgaadayi V. Khan. and Krasnob. при воздействии мета-хлорбензгидрилмочевины
Растения, в отличие от животных и человека, характеризуются способностью синтезировать вторичные метаболиты. Среди последних выделяют многочисленную группу флавоноидов (Фл), в которой изучено более 6900 представителей (1). Эти метаболиты синтезируются из п-кумароил-КоА последовательным воздействием различных ферментов, которые, как полагают, образуют слабо связанные с мембранами (например, с эндоплазматическим ретикулумом) упорядоченные макромолекулярные белковые комплексы — флавоноидные метаболоны (1, 2). При синтезе специфических Фл во время роста растений и в реакциях на стрессоры важную роль играет определенная локализация и продолжительность взаимодействий между специфическими белками (1, 3). Фл выполняют следующие физиологические функции: защиту от листогрызущих насекомых, патогенных микроорганизмов, ультрафиолетового излучения и света высокой интенсивности, привлечение насекомых-опылителей, ингибирование образования активных форм кислорода (АФК), участие в прорастании пыльцы, биологическую коммуникацию в ризосфере (нодуляция), повышение эффективности извлечения питательных веществ во время старения растения и его органов (3-6). Они способны к хелатированию металлов, что может служить механизмом in vivo для снижения токсичности (3). Кроме того, Фл выступают в качестве регуляторов развития, участвующих в изменении транспорта фитогормона индолил-3-уксусной кислоты (ИУК) и его метаболизма (7).
Так как Фл не синтезируются в организме животных и человека, эти соединения служат незаменимыми пищевыми компонентами. Природные Фл имеют низкую токсичность, поэтому их используют для профилактики и лечения различных патологий (8). Пищевые Фл с антиоксидантной активностью снижают частоту возникновения атеросклероза, сердечно-сосудистых заболеваний, диабета, тромбоза, воспаления при артрите, нейроде-генеративных заболеваний (болезни Альцгеймера и Паркинсона), ожирения, гиперлипидемии и гипертонии (4). Кверцетин проявляет антипроли-феративный эффект в отношении линий раковых клеток (9). Фл используют как сырье для промышленного производства фармакологических и косметических субстанций, в связи с чем возникает вопрос о контроле содержания Фл в растениях.
В качестве индукторов биосинтеза Фл рассматриваются не только негативные биотические и абиотические воздействия, но и эндогенные факторы, например гормональный баланс клеток, связанный с возрастом растения, его органов и клеточных культур (5, 10-12). Среди ферментов, участвующих в модификации Фл, выделяют цитохром-Р-450-зависимые монооксигеназы (CYP) — компоненты флавоноидных метаболонов (1, 2, 13). Индуктором цитохром-Р-450-зависимой монооксигеназной системы человека может служить мета-хлорбензгидрилмочевина (МХБМ) (14), однако сведения о роли МХБМ в регуляции жизнедеятельности растений отсутствуют.
Изучение молекулярных механизмов действия веществ в растительном организме затруднено вследствие присутствия многочисленных структурных элементов на клеточном, тканевом и органном уровнях, а также большого числа происходящих в них метаболических процессов. В связи с этим наиболее удачным модельным объектом могут служить гетеротрофные клеточные культуры, упрощенные по строению и не проявляющие фотосинтетической активности.
В настоящем исследовании впервые показаны статистически зна- чимые (p < 0,05) различия в ответных ростовых реакциях каллусной культуры горькуши оргадаай (Saussurea orgaadayi V. Khan. and Krasnob.) на действие МХБМ в разных концентрациях. Выявлено, что изменение ростового индекса по сырой и сухой массе обусловлено изменением объема и формы клеток, а также частоты встречаемости разных групп клеток. Впервые исследована динамика содержания флавоноидов, сопровождающая изменения роста культуры под влиянием МХБМ.
Целью работы было определение роли мета-хлорбензгидрилмоче-вины в накоплении флавоноидов и изменчивости цитоморфологических характеристик (линейных размеров, объема и формы клеток, частоты встречаемости разных групп клеток, ростового индекса по сырой и сухой биомассе каллуса) каллусной культуры горькуши оргадаай.
Методика. Производное мочевины — мета-хлорбензгидрилмочевина (галодиф, Galodif, CAS: 124057-07-4) было синтезировано в Томском политехническом университете (15), правообладатели препарата ООО «Синте-гал» и ООО «Наука, Техника, Медицина» (Россия). В работе использовали разведения матричного 100 мМ спиртового раствора МХБМ в концентрациях 0,01; 0,1; 1; 10; 100 мкМ.
Каллусную культуру многолетнего лекарственного растения горькуши оргадаай S. orgaadayi , полученную на основе семядольных эксплантов из стерильных проростков, многократно пассировали на модифицированной агаризованной питательной среде Мурасиге-Скуга (МС) с добавлением сахарозы, витаминов и регуляторов роста 0,8 мг/л 2,4-Д (2,4-дихлорфенок-сиуксусная кислота) и 0,5 мг/л 6-БАП (6-бензинаминопурин) (16). Культуру выращивали в темноте при температуре 22-24 ° С на среде МС с добавлением регуляторов роста и МХБМ, в контроле МХБМ не вносили.
Продолжительность субкультивирования составила 30 сут, 2/ з растительного материала использовали для определения сырой и сухой биомассы с последующим выделением флавоноидов, 1 / 3 материала фиксировали в растворе Кларка (96 % этиловый спирт:ледяная уксусная кислота в соотношении 3:1) в течение 2 сут. Затем материал отмывали от фиксатора 96 % раствором этилового спирта (3 раза по 30 мин) до исчезновения запаха уксусной кислоты и хранили в 70 % растворе этанола при 4 ° С (17). Для приготовления микропрепаратов каллусную культуру мацерировали в 3 н. растворе соляной кислоты при постоянном встряхивании до получения однородной суспензии клеток.
Цитофотометрический анализ осуществляли с помощью световой микроскопии (видеокамера Moticam 2300, «Motic», Испания) с программным обеспечением. Для каждого варианта измеряли размеры (L — длина, D — ширина) 100 клеток. По соотношению L/D оценивали форму клеток: 1,0 < L/D < 1,14 — округлые, 1,15 < L/D < 1,94 — овальные, L/D > 1,95 — вытянутые. Объем клеток вычисляли по формуле Ю.А. Цельникер (18) с учетом рассчитанного автором поправочного коэффициента (k), который зависит от L/D. При L/D > 2,5 для определения объема клеток (V, мкм3) применяли формулу цилиндра V = n (D/2)2Lk, при L/D < 2,5 — формулу эллипсоида вращения V = 4/3 n L/2(D/2)2. Для расчета ростового индекса (РИ) определяли начальную (начало субкультивирования, М е ) и конечную сырую или сухую массу каллусов (на 30-е сут субкультивирования, М 30 ) и выражали в процентах к контролю: РИ = (М 30 - М с )/М 0 .
Количественное определение содержания суммы Фл в каллусной культуре S. orgaadayi осуществляли на основе их комплексообразования с хлоридом алюминия и последующего измерения оптической плотности окрашенных растворов (спектрофотометр UV-1650, «Shimadzu Corp.», Япония) (19). Навеску сухого растительного сырья (1 г) трижды (по 60 мин) экстрагировали 70 % этиловым спиртом на кипящей водяной бане, экстракты объединяли. Аликвоту объединенного растительного экстракта выдерживали в течение 40 мин в присутствии хлористого алюминия и уксусной кислоты. Раствор сравнения, не содержащий хлористого алюминия, готовили для каждой пробы отдельно.
После взаимодействия веществ определяли оптическую плотность опытного раствора и стандартного раствора рутина при X = 415 нм. Вычисляли суммарное содержание Фл в пересчете на рутин и абсолютно сухое сырье (Х фл ):
Х фл = OD x • K x • т рут • 100 • 100 • СП рут - 1 • К рут - 1 • т х - 1 • (100 - W) - 1, где ОП х — оптическая плотность исследуемого раствора; ОП рут — оптическая плотность раствора рутина; т х — сырья масса, г; т рут — масса рутина, г; K x — коэффициент разбавления исследуемого раствора (1250); К рут — коэффициент разбавления раствора рутина (2500); W — потеря в массе при высушивании сырья, %.
При статистической обработке результатов в программе IBM SPSS Statistics («IBM Corporation», США) для Windows использовали параметрический t -критерий Стьюдента и непараметрический U-критерий Манна-Уитни для парного сравнения параметров групп. На рисунках представлены средние арифметические значения ( М) для ростовых ( n = 100) и биохимических ( n = 5) параметров с двухсторонними доверительными интервалами ( М ±1,96 SEM). Различия между значениями, отмеченные разными буквами, статистически значимы при р < 0,05.
Результаты. В проведенных экспериментах изучали зависимость морфогенеза и аккумуляции Фл у медленнорастущей каллусной культуры S. orgaadayi, полученной на основе семядолей, от концентрации МХБМ в питательной среде (рис. 1). На выбор культуры повлияли наши предварительные исследования (20), показавшие 3-кратное превышение содержания Фл (0,026±0,006 % к сухой массе) на 25-е сут в медленнорастущей культуре по сравнению с активно ростков S. orgaadayi.
растущей, полученной на основе гипокотилей про-
Б

Рис. 1. Формула мета-хлорбензгидрилмочевины (А) и каллусная культура клеток, полученная на основе семядольных эксплантов проростков горькуши оргадаай ( Saussurea orgaadayi V. Khan. and Krasnob.) (Б) .
А
При выборе времени субкультивирования каллуса руководствовались данными о приросте сырой массы у контрольной культуры. Рост каллус- ной культуры описывался S-образной кривой с несколькими фазами ростового цикла: лаг-фазой, или периодом медленного роста, в течение первых 10 сут, логарифмической фазой с длительностью 15 сут, 5-суточной фазой замедления и, начиная с 30-х сут, стационарной фазой (данные не приведены). На 25-е сут субкультивирования РИсыр культуры в контроле составил 2,32±0,70. Эксперимент проводили до 30-х сут с целью перехода культуры в стационарную фазу роста и увеличения выхода вторичных метаболитов Фл, что согласуется с данными других авторов (12).
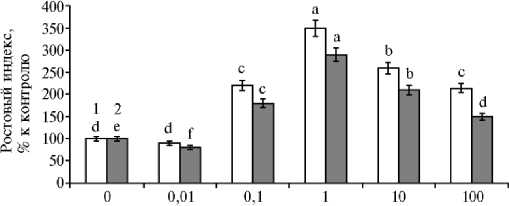
Добавление МХБМ в питательную среду в концентрациях 0,1100 мкМ увеличило прирост биомассы каллусной культуры. РИ сыр и РИ сух увеличивались соответственно в 2,1-3,5 и 1,5-2,9 раза (р < 0,05) относительно контроля (рис. 2). Действие 0,01 мкМ МХБМ не изменило РИ сыр , но снизило РИ сух на 20 % (р < 0,05). Наибольшие значения РИ сыр и РИ сух были отмечены при использовании 1 мкМ МХБМ. При этом в опыте каллусная культура отличалась от контрольной более светлой и рыхлой консистенцией.
Концентрация мета-хлорбензгидрилмочевины, мкМ
Рис. 2. Относительный прирост сырой (1) и сухой (2) биомассы каллусной культуры горькуши оргадаай ( Saussurea orgaadayi V. Khan. and Krasnob.) в зависимости от концентрации мета-хлор-бензгидрилмочевины. Различия между значениями каждого показателя, отмеченные разными буквами, статистически значимы при р < 0,05 ( М ±1,96 SEM).
Цитологический анализ выявил морфологическую гетерогенность популяции клеток культуры S. or-gaadayi (рис. 3, 4). Мы выделили группы клеток, которые различались по форме (округлые, овальные и вытянутые) и размеру (мелкие, средние и крупные). Мелкие клетки (9,0-35,7 тыс. мкм3) мы рассматривали как ме ристематические делящиеся, средние (35,75-75,94 тыс. мкм3) — как растущие, крупные (76,0323,2 тыс. мкм3) — как завершившие рост.
Контрольная каллусная культура на 30-е сут характеризовалась боль шей частотой встречаемости мелких клеток, чем средних и крупных соответственно в 1,6 и 3,4 раза (рис. 3, Б). Средний объем мелких клеток составлял 20,2±2,3 тыс. мкм3, тогда как средних и крупных — соответственно 51,5±1,4 и 112,1±2,6 тыс. мкм3 (рис. 3, А).
Результатом действия МХБМ на каллусную культуру было изменение роста клеток. При концентрации 0,1 мкМ количество мелких меристематических клеток увеличивалось на 16 % относительно контроля, что могло свидетельствовать об усилении клеточного деления (см. рис. 3, Б). Одновременно усредненный объем клеток крупных размеров уменьшался на 31 % по сравнению с контролем (см. рис. 3, А), что указывало на торможение процессов растяжения клеток. С повышением концентрации МХБМ увеличивалась частота встречаемости клеток среднего (на 55 и 30 % соответственно при 1 и 10 мкМ) и крупного (на 50 и 57 %, р < 0,05 при 1 и 100 мкМ) размеров (см. рис. 3, Б) и увеличивался объем крупных (на 61 %, р < 0,05 при 10 мкМ) и мелких (на 18 %, р < 0,05 при 100 мкМ) клеток относительно контроля. На этом фоне уменьшалось количество мелких клеток (на 49, 20 и 30 %, р < 0,05 соответственно при 1, 10 и 100 мкМ) и их объем (на 22 и 17 %, р < 0,05 при 1 и 10 мкМ) (см. рис. 3).
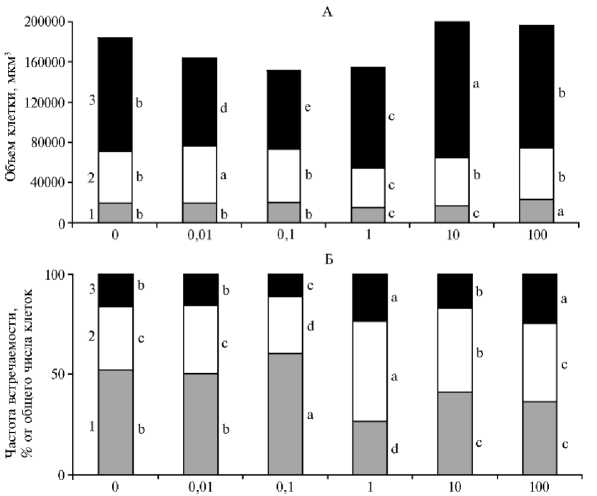
Концентрация мета-хлорбензгидрилмочевины, мкМ
Рис. 3. Объем клетки (А) и частота встречаемости клеток разного размера (Б) в каллусной культуре горькуши оргадаай ( Saussurea orgaadayi V. Khan. and Krasnob.) в зависимости от концентрации мета-хлорбензгидрилмочевины: 1 — мелкие, 2 — средние, 3 — крупные клетки. Различия между значениями каждого показателя, отмеченные разными буквами, статистически значимы при р < 0,05.
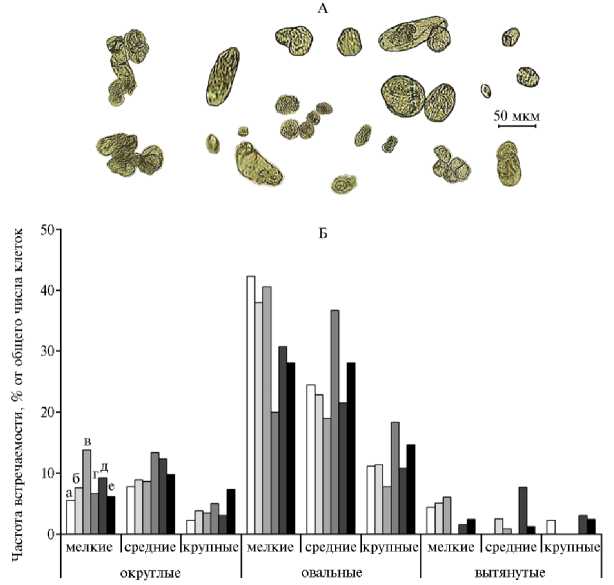
Рис. 4. Форма (А) и частота встречаемости (Б) клеток разной формы и размеров в каллусной культуре горькуши оргадаай ( Saussurea orgaadayi V. Khan. and Krasnob.) в зависимости от концентрации мета-хлорбензгидрилмочевины: а — 0 (контроль); б — 0,01 мкМ; в — 0,1 мкМ; г — 1 мкМ; д — 10 мкМ; е — 100 мкМ.
Под действием МХБМ увеличивалась доля округлых клеток всех размеров (рис. 4, Б). Наибольшие изменения наблюдали в частоте встречаемости мелких клеток (повышение в 2,5 раза, р < 0,05) при концентрации 0,1 мкМ МХБМ, средних и крупных клеток (рост соответственно в 1,7 и 2,3 раза, р < 0,05) — при 1 мкМ МХБМ. Наибольшая (увеличенная в 3,3 раза, р < 0,05) частота встречаемости крупных клеток округлой формы была отмечена при 100 мкМ МХБМ.
Изменение ростовых процессов в культуре могло свидетельствовать об изменении количества эндогенных веществ, осуществляющих регуляцию роста. Среди последних называют Фл, модулирующие гомеостаз раститель ных гормонов ауксинов (7). Мы установили, что суммарное содержание
Фл у контрольной культуры в процессе субкультивирования на стационарной стадии (30-е сут) составило 0,049±0,008 % к сухой массе, что на 50 % (р < 0,05) больше, чем на 25-е сут в точке перегиба логарифмического участка кривой роста. Эти данные свидетельствуют о замедлении роста на фоне повышения содержания эндогенных Фл.
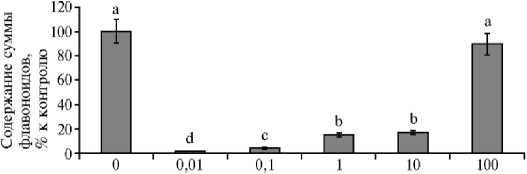
Концентрация мета-хлорбензгидрилмочевины. мкМ
Рис. 5. Содержание суммы флавоноидов в каллусной культуре горькуши оргадаай ( Saussurea orgaadayi V. Khan. and Krasnob.) в зависимости от концентрации мета-хлорбензгидрилмочевины. Различия между значениями, отмеченные разными буквами, статистически значимы при р < 0,05 ( М ±1,96 SEM).
При действии МХБМ происходило изменение суммарного содержания Фл по сравнению с контролем (рис. 5). Впервые показано, что уменьшение (на 80-95 %) суммарного количества эндогенных Фл под действием МХБМ сопровождалось активацией ростовых процессов в раститель ных клетках S. orgaadayi in vitro. Содержание суммы Фл максимально снижалось при низких концентрациях МХБМ и сохранялось на уровне контроля при 100 мкМ МХБМ. Максимальный (в 3,5 раза) прирост биомассы, отмеченный при 1 мкМ МХБМ, происходил на фоне снижения суммы Фл на 83 %.
Таким образом, в нашем исследовании было показано влияние МХБМ на рост каллусной культуры S. orgaadayi, что, вероятно, обусловлено его действием на растяжение и деление клеток. Дозозависимые изменения в накоплении биомассы культуры (см. рис. 2) сопровождались изменением частоты встречаемости клеток разных размеров и формы (см. рис. 3, 4). Действие МХБМ в самой низкой концентрации (0,01 мкМ) снижало РИсух, что могло определяться снижением объема крупных клеток на 23 % при равном контролю соотношении ранжированных по размеру групп клеток. Наибольшие РИсыр и РИсух культуры, отмеченные при действии 1 мкМ МХБМ, сопровождались повышенной частотой встречаемости средних и крупных клеток и снижением доли мелких клеток (см. рис. 3, Б). Концентрация 0,1 мкМ МХБМ оказывала меньший эффект, чем 1 мкМ МХБМ, что проявлялось в повышении частоты встречаемости мелких клеток и, соответственно, в снижении доли средних и крупных.
Наиболее активными концентрациями МХБМ в регуляции роста каллусной культуры горькуши оргадаай были 0,1-10 мкМ, под действием которых увеличивалось число меристематических округлых мелких клеток.
Ускорение роста сопровождалось изменением вторичного метаболизма, что выразилось в снижении суммарного количества Фл на 80-95 % (р < 0,05) относительно контроля (см. рис. 5). Действие МХБМ в высокой концентрации 100 мкМ достоверно увеличивало прирост биомассы культуры, существенно не меняя содержание Фл. Дозозависимая динамика роста и содержания Фл под действием МХБМ, вероятно, может свидетельствовать об изменении функционирования ферментов, участвующих в метаболизме Фл. На модификацию Фл в клеточной культуре указывают данные других авторов (21), изучавших комплексное воздействие экзогенных факторов (кадмия и глифосата) на суммарное содержание фенольных соединений, которое возрастало на фоне снижения количества фенилпропаноидов и флавоноидов.
На рост каллусной культуры могли оказывать действие Фл с разными свойствами. Наряду с антиоксидантными свойствами катехинов и кверцетина некоторые Фл в высоких дозах могут проявлять прооксидант-ную активность и повреждать клетки (8).
Показано влияние Фл на регуляцию клеточного цикла (22). В качестве возможных механизмов называют непосредственное взаимодействие Фл (например, кверцетина) с протеинкиназами Raf и MEK, обусловливающими проведение митотических сигналов, или их связывание с рецептором AhR и образование комплекса с ARNT, стимулирующего транскрипцию ингибитора клеточного цикла CDKNB1 (22, 23).
Кроме того, возможно и опосредованное действие Фл на рост, связанное с изменением транспорта ауксинов и их метаболизма. Известно, что пространственно-временное распределение ауксинов, обусловленное механизмами полярного транспорта, играет решающую роль в их физиологических эффектах (24). На примере мутантов tt4 показано, что дефицит Фл усиливает поток ИУК (25). Считается, что флавонолы непосредственно модулируют транспорт ИУК — процесс, который снижается в сверхаккумули-рующем кемпферол мутанте tt7 , дефектном по F39H (25). Негликозилиро-ванные кемпферол и кверцетин конкурируют с ингибитором транспорта ауксина l-N-нафтилфталаминовой кислотой за высокоаффинный сайт связывания комплекса, содержащего белки PGP1, PGP2 и MDR1/PGP19, которые принадлежат к АТФ-связывающим кассетным переносчикам. В то же время Фл выступают в качестве регуляторов ИУК-оксидазы, участвующей в деградации ИУК: Фл с о-гидроксилами в ядре В (кверцетин, мирицетин, лю-теолин) ингибируют активность фермента, тогда как Фл с п-гидроксилами (апигенин, нарингенин, нарингин) стимулируют его (26). В итоге первая группа Фл стимулирует рост, а вторая — ингибирует его.
В то же время неотъемлемым этапом нормального роста и развития растений считается окисление Фл, которое связано с деятельностью растительных пероксидаз или других ферментов (27, 28). В результате окисления Фл способны проявлять прооксидантное действие, которое выражается в повреждении биологических структур и общем снижении жизнеспособности клеток организма (28).
Исследуемый нами препарат МХБМ может регулировать активность гемсодержащих ферментов семейства цитохромов P-450 (CYP), принадлежащих к группе монооксигеназ у человека. Ферменты этой группы обнаружены во всех царствах и катализируют разнообразные химические реакции (13, 25). Изменения роста клеток культуры S. orgaadayi под действием МХБМ, сопровождавшиеся изменением содержания Фл, вероятно, также можно объяснить регуляцией функционирования CYP, участвующих в метаболизме Фл (2). Показано, что CYP82D кодирует флавон-6-гидрокси-лазу и 7-деметилазу и отвечает за биосинтез Фл в сладком базилике, тогда как CYP75 регулирует экспрессию флавоноид-3‘-гидроксилазы и флаво-ноид-3‘,5‘-гидроксилазы, которые участвуют в синтезе большинства антоцианов, в красном винограде (13). CYP93G1, ближайший гомолог CYP93G2 в рисе, — это флавон-синтаза II (FNSII), которая катализирует прямое превращение флаванонов в флавоны (30).
Другими эндогенными факторами роста клеток культуры горькуши могли выступать фитогормоны, в регуляции метаболизма которых также участвуют CYP. Например, CYP79B2/B3 ответствен за превращение L-триптофана (L-Trp) в индол-3-ацетальдоксим в альтернативном L-Trp-зависи-мом пути биосинтеза ауксинов (13), цитокинин-гидроксилазы CYP735A1 и CYP735A2 катализируют биосинтез транс-зеатинов, а CYP72C1 инактивирует брассиностероиды у Arabidopsis thaliana (13, 25).
Возможны и мембранные механизмы действия МХБМ на растительные клетки по аналогии с клетками человека. Такие механизмы могут быть связаны с блокадой быстрых натриевых каналов нейронов, ограничивающей распространение электрического потенциала. В результате МХБМ за счет регулирования водно-электролитного баланса стабилизирует концентрационный градиент ионов, а также препятствует изменению мембранной проницаемости и трансмембранного потенциала клетки. Наряду с этим МХБМ усиливает процессы микросомального окисления, проявляя детоксицирующее действие в клетках.
В соответствии с полученными нами данными, высокое содержание Фл на 30-е сут субкультивирования обусловливало завершение активного роста клеток каллуса у S. orgaadayi в контрольном варианте, что согласуется с данными по увеличению аккумуляции Фл на стационарной стадии клеточной культуры (11, 12) и в завершивших рост листьях растений Lactuca sativa L. (5). Также показано (12, 29), что в процессе длительного культивирования клеток суспензионной культуры повышается окислительный статус (накопление АФК) и происходит активация антиоксидантных ферментов и вторичных метаболитов. В связи с этим следует ожидать, что действие МХБМ увеличивает биомассу культуры, вероятно, за счет снижения количества Фл и, соответственно, увеличения продолжительности ростовой активности клеток.
На основе наших результатов и данных других авторов (2, 12, 25, 2830), полученных при исследовании растений и их клеточных культур, можно предполагать влияние МХБМ на активность ферментов, регулирующих содержание Фл и фитогормонов, а также ферментативных антиоксидантов.
Итак, используемая в эксперименте медленнорастущая каллусная культура горькуши оргаадай, полученная из семядольного экспланта, продуцировала флавоноиды. Введение экзогенной мета-хлорбензгидрилмоче-вины (МХБМ) в питательную среду в концентрации от 0,01 до 10 мкМ обусловливало снижение содержания вторичных метаболитов в каллусной культуре. Уменьшение суммарного содержания флавоноидов приводило к активации ростовых процессов. Происходило накопление биомассы каллуса и повышение ростового индекса культуры с максимумом при 1 мкМ МХБМ. Дальнейшее увеличение концентрации МХБМ снижало темпы прироста биомассы. Рост биомассы культуры сопровождался изменением частоты встречаемости разных типов клеток и размеров. При действии 0,1 мкм МХБМ увеличивалось число мелких меристематических клеток, а начиная с 1 мкМ МХБМ, возрастала частота встречаемости округлых и овальных клеток среднего и крупного размера при уменьшении встречаемости мелких клеток. При этом клетки достигали наибольших размеров при концентрации 10 мкМ, а максимальное число крупных клеток отмечали при 100 мкМ МХБМ. Такая динамика указывала на увеличение скорости деления клеток при низких концентрациях и растяжения клеток — при средних и высоких концентрациях МХБМ. Полученные данные свидетельствуют о дозозависимом действии МХБМ на рост клеток через изменение содержания флавоноидов.
Список литературы Физиолого-биохимические характеристики клеточной культуры Saussurea orgaadayi V. Khan. and Krasnob. при воздействии мета-хлорбензгидрилмочевины
- Nakayama T., Takahashi S., Waki T. Formation of flavonoid metabolons: functional significance of protein-protein interactions and impact on flavonoid chemodiversity. Frontiers in Plant Science, 2019, 10: 821 (doi: 10.3389/fpls.2019.00821).
- Ayabe S., Akashi T. Cytochrome P450s in flavonoid metabolism. Phytochemistry Reviews, 2006, 5: 271-282 (doi: 10.1007/s11101-006-9007-3).
- Falcone-Ferreyra M.L., Rius S.P., Casati P. Flavonoids: biosynthesis, biological functions, and biotechnological applications. Frontiers in Plant Science, 2012, 3: 222 (doi: 10.3389/fpls.2012.00222).
- Mouradov A., Spangenberg G. Flavonoids: a metabolic network mediating plants adaptation to their real estate. Frontiers in Plant Science, 2014, 5: 620 (doi: 10.3389/fpls.2014.00620).
- Головацкая И.Ф., Бойко Е.В., Видершпан А.Н., Лаптев Н.И. Возрастные морфофизиологические и биохимические изменения у растений Lactuca sativa L. под влиянием селена и света разной интенсивности. Сельскохозяйственная биология, 2018, 53(5): 1025-1036 (doi: 10.15389/agrobiology.2018.5.1025rus).
- Kumar V., Suman U., Rubal, Yadav S.K. Flavonoid secondary metabolite: biosynthesis and role in growth and development in plants. In: Recent trends and techniques in plant metabolic engineering /S. Yadav, V. Kumar, S. Singh (eds.). Springer, Singapore, 2018: 19-45 (doi: 10.1007/978-981-13-2251-8_2).
- Kuhn B.M., Errafi S., Bucher R., Dobrev P., Geisler M., Bigler L., Zažímalová E., Ringli C. 7-rhamnosylated flavonols modulate homeostasis of the plant hormone auxin and affect plant development. The Journal of Biological Chemistry, 2016, 291(10): 5385-5395 (doi: 10.1074/jbc.M115.701565).
- Белицкий Г.А., Кирсанов К.И., Лесовая Е.А., Якубовская М.Г. Механизмы антиканцерогенного действия флавоноидов. Успехи молекулярной онкологии, 2014, 1(1): 56-68.
- Ionkova I. Optimization of flavonoid production in cell cultures of Astragalus missouriensis Nutt. (Fabaceae). Pharmacognosy Magazine, 2009, 5(18): 92-97.
- Indu S., Vijaya L., Meeta B., Jossy V., Naresh C. Production of flavonoids in callus culture of Anthocephalus indicus A. Rich. Asian Journal of Plant Sciences, 2013, 12(1): 40-45 (doi: 10.3923/ajps.2013.40.45).
- Березина Е.В., Брилкина А.А., Щурова А.В., Веселов А.П. Накопление биомассы и фенольных соединений каллусами Oxycoccus palustris Pers. и O. macrocarpus (Ait.) Pers. в присутствии разных цитокининов. Физиология растений, 2019, 66(1): 35-45 (doi: 10.1134/S0015330318050032).
- Wang J., Qian J., Yao L., Lu Y. Enhanced production of flavonoids by methyl jasmonate elicitation in cell suspension culture of Hypericum perforatum. Bioresources and Bioprocessing, 2015, 2: 5 (doi: 10.1186/s40643-014-0033-5).
- Xu J., Wang X., Guo W. The cytochrome P450 superfamily: key players in plant development and defense. Journal of Integrative Agriculture, 2015, 14(9): 1673-1686 (doi: 10.1016/s2095-3119(14)60980-1).
- Новожеева Т.П., Чурсина И.Э., Новожеева А.В., Саратиков А.С. Влияние бензонала, галонала и галодифа на систему микросомального окисления гепатоцитов в онтогенезе. Химико-фармацевтический журнал, 2004, 38(2): 7-9.
- Штрыкова В.В., Куксёнок В.Ю., Филимонов В.Д., Галанов А.И. Способ получения мета-хлорбензгидрилмочевины (галодифа) с использованием магнитных наночастиц, модифицированных сульфогруппами. А.с. 2569684 (РФ). МПК С07С 275/24, С07С 273/18. ФГАО УВО ТПУ (РФ). № 2014154126/06. Заявл. 29.12.2014. Опубл. 27.11.2015. Бюл. № 33.
- Карначук Р.А., Лихачева А.В. Питательная среда для культивирования клеточной культуры SaussureaorgaadayiV. Khan. EtKrasnov. А.с. 2428472 (РФ). МПК C12N 005/02, C12N 005/04. ГОУ ВПО ТГУ (РФ). № 2010118803.Заявл. 05.11.2010.Опубл. 09.10. 2011. Бюл. № 25.
- Барыкина Р.П., Веселова Т.Д., Девятов А.Г, Джалилова X.X., Ильина Г.М., Чубатова Н.В. Основы микротехнических исследований в ботанике. Справочное руководство. М., 2000.
- Цельникер Ю.Л. Физиологические основы теневыносливости древесных растений. М., 1978.
- Государственная фармакопея СССР: Вып. 2. Общие методы анализа. Лекарственное растительное сырье. 11-е изд. М., 1989.
- Головацкая И.Ф., Бойко Е.В., Резниченко А.Е., Плюснин И.Н. Мелатонин и селен регулируют рост и окислительный статус клеточных культур Saussurea orgaadayi in vitro, полученных от разных эксплантов. Физиология растений, 2020, 67(6): 625-635 (doi: 10.31857/S001533032005005X).
- Гончарук Е.А., Николаева Т.Н., Назаренко Л.В., Калашникова Е.А., Загоскина Н.В. Ответная реакция культивируемых in vitro клеток Linumgrandiflorum Desf. на действие кадмия и глифосата. Сельскохозяйственная биология, 2018, 53(5): 938-946 (doi: 10.15389/agrobiology.2018.5.938rus).
- Galati G., Sabzevari O., Wilson J.X., O'Brien P.J. Prooxidant activity and cellular effects of the phenoxyl radicals of dietary flavonoids and other polyphenolics. Toxicology, 2002, 177(1): 91-104 (doi: 10.1016/s0300-483x(02)00198-1).
- Brunetti C., Di Ferdinando M., Fini A., Pollastri S., Tattini M. Flavonoids as antioxidants and developmental regulators: relative significance in plants and humans. International Journal of Molecular Sciences, 2013, 14(2): 3540-3555 (doi: 10.3390/ijms14023540).
- Pařízková B., Pernisová M., Novák O. What has been seen cannot be unseen-detecting auxin in vivo. International Journal of Molecular Sciences, 2017, 18(12): 2736 (doi: 10.3390/ijms18122736).
- Sotelo-Silveira M., Cucinotta M., Chauvin A.-L., Chávez Montes R.A., Colombo L., Marsch-Martínez N., de Folter S. Cytochrome P450 CYP78A9 is involved in Arabidopsis reproductive development. Plant Physiology, 2013, 162(2): 779-799 (doi: 10.1104/pp.113.218214).
- Макаренко О.А., Левицкий А.П. Физиологические функции флавоноидов в растениях. Физиология и биохимия культурных растений, 2013, 45(2): 108-112.
- Pourcel L., Routaboul J., Cheynier V., Lepiniec L., Debeaujon I. Flavonoid oxidation in plants: from biochemical properties to physiological functions. Trends in Plant Science, 2007, 12(1): 29-36 (doi: 10.1016/j.tplants.2006.11.006).
- Червяковский Е.М., Курченко В.П., Костюк В.А. Роль флавоноидов в биологических реакциях с переносом электронов. Труды Белорусского Государственного Университета. Серия: Физиологические, биохимические и молекулярные основы функционирования биосистем, 2009, 1: 9-26.
- Kim Y.-H., Kim Y., Cho E., Kwak S., Kwon S., Bae J., Lee B., Meen B., Huh G.-H. Alterations in intracellular and extracellular activities of antioxidant enzymes during suspension culture of sweetpotato. Phytochemistry, 2004, 65(17): 2471-2476 (doi: 10.1016/j.phytochem.2004.08.001).
- Lam P.Y., Zhu F.-Y., Chan W.L., Liu H., Lo C. Cytochrome P450 93G1 is a flavone synthase II that channels flavanones to the biosynthesis of tricin o-linked conjugates in rice. Physiology, 2014, 165(3): 1315-1327 (doi: 10.1104/pp.114.239723).


