Формирование цветности карамельных составов на основе аскорбиновой кислоты
Автор: Черепанов Игорь Сергеевич
Рубрика: Биохимический и пищевой инжиниринг
Статья в выпуске: 1 т.11, 2023 года.
Бесплатный доступ
В настоящее время особый интерес в пищевой технологии приобретают двухкомпонентные системы на основе L-аскорбиновой кислоты, применяемые в качестве источников биологически активных пищевых добавок. Представлены результаты исследований по изучению механизмов и динамики формирования цветности в процессах карамелизации в среде 40 %-ного этанола; объектами изучения являлись L-аскорбиновая кислота (Asc) и ее эквимолярная смесь с D-глюкозой (Glc). Образование окрашенных веществ в обеих системах идентифицировалось методами молекулярной спектроскопии по окончании термостатирования растворов (50 °С, 1,5 ч) и их последующего выдерживания (25 °С) в течение 30 суток. Расчет индексов окрашивания водно-этанольных систем Asc и Asc + Glc показал усиление интенсивности цветности при карамелизации L-аскорбиновой кислоты в присутствии D-глюкозы, указывая на формирование более протяженной и стабильной хромофорной системы в двойной системе, что подтверждается характером электронных спектров. Сравнительный анализ колебательных спектров исследуемых растворов показывает наличие полос, характерных для сопряженных С=О+ С=С-сочетаний, вторые производные полос в области валентных колебаний кратных связей идентифицируют в спектре двойной системы интенсивный сигнал 1654 см-1, относимый к О=С-С(OH)=С-фрагментам. Последнее свидетельствует о большей устойчивости хромофорных составляющих структуры, формирующейся в результате совместной карамелизации компонентов двойной системы. Конденсация продуктов трансформации Asc и Glc приводит, вероятно, к ряду окрашенных продуктов, одним из которых является замещенный δ-лактон, включающий гидрокси-α,β-еноновые фрагменты. Предполагается, что последние стабилизируются R-замещением, обеспечивая большую в сравнении с продуктами карамелизации аскорбиновой кислоты протяжённость и устойчивость формирующей цветность хромофорной системы. Дальнейшее изучение свойств карамельных составов на основе аскорбиновой кислоты (светостойкости, токсичности, антиокислительных свойств) позволит разработать доступные и экологичные полифункциональные пигменты для промышленного применения.
L-аскорбиновая кислота, цветность, d-глюкоза, механизм, водно-этанольные среды, молекулярная спектроскопия, полосы поглощения, хромофоры, индексы цветности, окрашенные продукты
Короткий адрес: https://sciup.org/147240302
IDR: 147240302 | УДК: 664.1:543.4 | DOI: 10.14529/food230108
Color formation during caramelization in ascorbic acid based systems
Currently, two-component systems based on L-ascorbic acid, used as sources of biologically active food additives, are of particular interest in food technology. The investigation presents the results of research on the mechanisms and dynamics of chromophores formation in caramelization processes in 40 % ethanol medium; the subjects of study were L-ascorbic acid (Asc) and its equimolar mixture with D-glucose (Glc). The formation of colored substances in both systems was identified by molecular spectroscopy at the end of thermostatting the solutions (50 °С, 1.5 h) and their subsequent aging (25 °С) for 30 days. The calculation of the color indexes of the water-ethanol systems Asc and Asc + Glc showed an increase in the intensity of chrominance during caramelization of L-ascorbic acid in the presence of D-glucose, indicating the formation of a longer and more stable chromophore system in the double system, which is confirmed by the nature of the electronic spectra. Comparative analysis of the vibrational spectra of the test solutions shows the presence of bands characteristic of conjugated C=O + C=C-combinations, second derivatives of bands in the region of multiple bonds stretching vibrations identify in the spectrum of the double system an intense signal of 1654 cm-1 related to O=C-C(OH)=C-fragments. The latter indicates greater stability of the chromophore components of the structure formed by the co-caramelization of the double system components. Condensation of Asc and Glc transformation products leads probably to a number of colored products, one of which is substituted δ-lactone, which includes hydroxy-α,β-enone fragments. It is assumed that the latter are stabilized by R-substitution, providing a greater length and stability of the chromophore system that forms color in comparison with the products of caramelization of ascorbic acid. Further study of the properties of caramel compositions based on ascorbic acid (light resistance, toxicity, antioxidant properties) will allow the development of affordable and environmentally friendly polyfunctional pigments.
Текст научной статьи Формирование цветности карамельных составов на основе аскорбиновой кислоты
Одной из основных качественных характеристик продуктов питания является их цвет, отчасти теряющийся в процессе переработки и хранения. Для восстановления или повышения интенсивности окраски продуктов питания широко применяются пищевые красители. На смену натуральным пигментам, выработка которых в настоящее время ограничена, в широком ассортименте пришли синтетические красители, применение которых, в свою очередь, часто вызывает опасение в токсикологическом аспекте. Карамельные составы на основе углеводов и родственных соединений являются перспективными экологичными материалами с широкой функциональностью [1], важным показателем которых является цветность, обусловленная образованием в ходе карамелизации различных групп окрашенных веществ. Последние представлены непредельными гидроксикарбонильными и карбоксильными циклическими либо ациклическими соединениями различной молекулярной массы, содержащими в качестве структурных элементов протяженные системы сопряженных связей, обуславливающих окраску. Известно, что различные по природе хромофорные структуры поглощают в разных областях ультрафиолетовой и видимой частей спектра, что может быть охарактеризовано различными спектрофотометрическими индексами [1], являющимися при этом лишь интегральными параметрами, и не позволяющими в полной мере описать структурные особенности продуктов карамелизации. Детализация функционально-группового состава карамелей мо- жет быть реализована с применением совокупности методов исследования, что позволит прогнозировать ключевые свойства карамельных составов и направленно управлять процессами их получения.
В настоящее время особый интерес в пищевой технологии приобретают двухкомпонентные системы на основе L -аскорбиновой кислоты, применяемые в качестве источников биологически активных пищевых добавок [2]. Последние обладают рядом полезных свойств, при этом разработка и подбор подобных составов активно не проводится, а закономерности их получения и выделения мало изучены, в связи с чем актуальным представляется изучение закономерностей формирования продуктов совместной карамелизации L -аскорбиновой кислоты с лабильными биологически активными веществами. С другой стороны, определенный интерес представляет влияние аскорбиновой кислоты на цветовые параметры углеводных карамелей, что актуально при разработке составов полифункциональных пищевых колеров [3].
L -аскорбиновая кислота в условиях термостатирования претерпевает трансформацию по различным направлениям [4–6], которая может контролироваться введением активных компонентов, таких как углеводы [7–11]. В частности, авторы [9] изучали поведение аскорбиновой кислоты в водных растворах в присутствии добавок различной природы (углеводы, полиолы, соли) и пришли к выводу об их влиянии на процессы термодеструкции, в том числе посредством изменения активности воды. В работе [10] исследована стабильность аскорбиновой кислоты в гетерогенных системах на основе пектиновых пленок. С другой стороны, среди продуктов деструкции аскорбиновой кислоты присутствуют потенциально биоактивные компоненты, в частности замещенные α-пироны [12].
Существенное влияние на динамику образования и строение продуктов взаимодействия компонентов пищевых систем оказывает природа растворителя, в связи с чем ряд исследований выполнен в этанольных и смешанных водно-этанольных средах [7, 8, 11]. Нами ранее показано, что продукты совместной карамелизации аскорбиновой кислоты и углеводов, полученные в среде осушенного этанола, сохраняют структурные фрагменты исходных веществ, проявляя антиокислительные свойства [7], тогда как увеличение содержания воды в растворителе (от 4 % и выше) интенсифицирует реакции неферментативного окрашивания, что приводит к образованию полукеталей де-гидроаскорбиновой кислоты [8] в качестве первичных продуктов. Подобные производные, являясь достаточно термодинамически стабильными, тем не менее склонны к реверсии с последующим развитием процессов усложнения структуры посредством конденсации. Описанные процессы ответственны за формирования цветности образующихся продуктов, при этом показано [13], что образование последних в системах углевод – аскорбиновая кислота является достаточно длительным процессом. В связи с чем целью настоящей работы являлось изучение механизмов образования и функционально-группового состава продуктов неферментативного окрашивания, обуславливающих формирование цветности в процессах карамелизации аскорбиновой кислоты и ее смеси с D-глюкозой.
Объекты и методы исследований
Целевые процессы были реализованы термостатированием водно-этанольных (40 % EtOH, «Merck») растворов, содержащих эквимолярные количества (0,002 моль) L-аскорбиновой кислоты (Asc) и D-глюкозы (Glc) («ч.д.а.») в колбах с обратным холодильником при 50 °С в течение 90 минут [8]. Растворы выдерживали при 25 °С до стабилизации окраски [6, 13], после чего отбирали пробы, часть которых наносили в виде капли на солевые подложки CaF2, которую высушивали струей воздуха до образования равномерной тонкой пленки. Для сравнения аналогичным образом проводили деструкцию L-аскорбиновой кислоты без введения углевода. Колебательные спектры полученных пленок регистрировались на ИК-Фурье спектрометре ФСМ-2201 (ООО «Инфраспек», СПб, Россия) в интервале волновых чисел 4000–860 см–1 с разрешением 2 см–1 относительно чистых CaF2-подложек. Спектры вторых производных получены в результате численного дифференцирования с использованием сглаживания полиномом 4-го порядка в окнах до 15 точек, отнесение проводили по экстремумам выше нулевой линии, интенсивности сигналов оценивали по разности амплитуд соседних экстремумов. Итоговые спектры обрабатывались в программе FSpec 4.3.0.9. Дополнительно отобранные пробы (1 мл) разбавляли растворителем в соотношении 1:5 и регистрировали электронные спектры растворов на спектро- фотометре СФ-2000 (ОКБ «Спектр», СПб, Россия) в кварцевых кюветах (l = 1 см) в интервале длин волн 200–500 нм с шагом 5 нм. Для расчета индексов окрашивания регистрировались спектры без разбавления в интервале длин волн 450–750 нм, расчет проводился по формулам [1]. Спектры обрабатывались в программе Excel.
Результаты и их обсуждение
Визуальная сравнительная оценка интенсивности окраски карамелизованных систем (рис. 1) показывает более насыщенный цвет растворов двойной системы.

Рис. 1. Водно-этанольные растворы карамелизованных систем: Asc + Glc (слева) и Asc (справа)
Электронные спектры реакционных систем представлены на рис. 2.
Анализ спектральных профилей показывает наличие полос 295 нм, относимых к поглощению производных дегидроаскорбиновой кислоты, его уширение в спектре 2 может свидетельствовать о присутствии фрагментов полимеризованных углеводов [14]; кроме того, спектр 2 дополнительно содержит слабо-выраженный пик при 245 нм, обусловленный π–π*-переходом электронов С=С-фрагментов [8]. Поглощение при 420 нм, характеризующее степень протекания неферментативного окрашивания, для обеих систем регистрируется примерно на одном уровне значений оптической плотности.
Математическая обработка электронных спектров в области 450–750 нм позволяет количественно оценить параметры цветности по значениям индексов окрашивания (см. таблицу), первый из которых – “ColorIndex” (CIEBCunit) характеризует общую глубину окраски, два других – “RedIndex”, “YellowIndex” (RI, YI) – красную и желтую составляющие цветности соответственно.
Анализ данных таблицы показывает близкие значения частных индексов RI и YI, показатель общей интенсивности окраски существенно выше для двойной системы, что
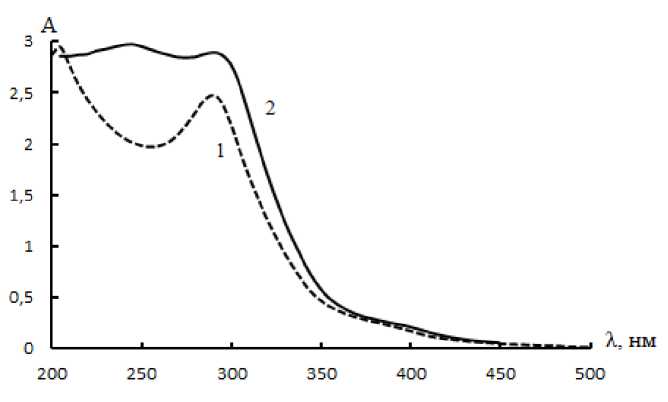
Рис. 2. Электронные спектры водно-этанольных растворов: 1 – Asc; 2 – Asc + Glc
Индексы окрашивания исследуемых систем
Более детальная информация может быть получена из анализа колебательных спектров (рис. 3). Спектры конденсированных фаз реакционных систем содержат характеристические полосы колебаний в области кратных связей, в частности 1638, 1642 и 1733, 1728 см–1. Сигналы 1730 (±3) см–1 в изучаемых системах можно отнести к колебаниям ν С=О , тогда как полосы 1640 (±2) см–1 характеризуют наличие в составе продуктов сопряженных С=С-фрагментов (ν С=С ). В спектре 2 наблюдается также слабое поглощение в области 2650–2550 см–1, относимое к колебаниям водородно-связанных карбоксильных групп. При этом полосы ν С=О и ν С=С , характерные для аскорбиновой кислоты (1755 и 1672 см–1 [15]), в спектрах не регистрируются, что указывает на трансформацию ее хромофорных фрагментов в ходе процессов.
Сигналы в области «фингерпринта» в обоих спектрах могут быть отнесены к колебаниям углеродных цепей и σ-функций, в частности 1370 (δ CH2 ), 1215, 1078 (ν СО , δ С–ОН+С–ОС ), 1034 (ν ring +ν С–ОН ) см–1, в спектре 2
дополнительно регистрируются несколько полос в интервале 1150–1050 см–1, относимых, вероятно, к скелетным колебаниям фрагментов D -глюкозы (ν СС , ν СО , δ СО , ν ССН ), представленным в структуре в незначительном количестве [7].
Дальнейшая детализация природы обуславливающих цветность непредельных функций возможна посредством анализа производных ИК-Фурье спектров в области кратных связей (рис. 4). В спектре 1 регистрируются четыре сигнала приблизительно равной интенсивности: 1620 (ν С=С ), 1645 (ν О=С–С=С ), 1703 (ν С=О ), 1720 (ν С=О ) см–1, несколько менее интенсивны сигналы 1654 и 1685 см–1, относимые к валентным колебаниям карбонильной группы в О=С–С(OH)=С-фрагментах [12; 16], тогда как в спектре 2 наиболее интенсивной является именно полоса 1654 см–1, отмеченные выше сигналы также проявляются достаточно существенно.
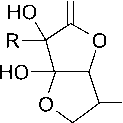
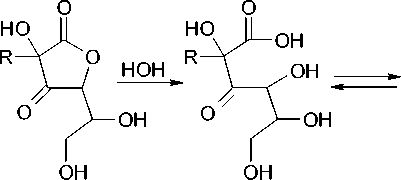
Можно предположить, что формирование цветности связано с включением α-гидрокси-α,β-еноновых фрагментов в структуру продуктов карамелизации [17], формирование которых в изученных системах может быть представлено следующим образом:
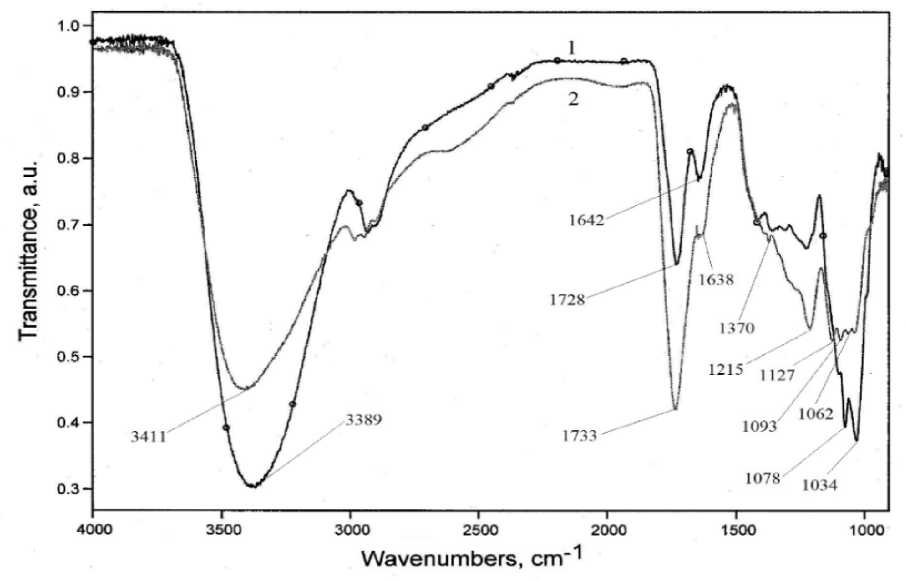
Рис. 3. ИК-Фурье спектры реакционных систем: 1– Asc; 2 – Asc + Glc
O
OH
OO
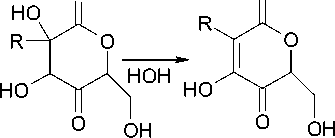
Полукетали (1), образующиеся на начальных стадиях протекания процессов (термостатирование при 50 °С) [8], при дальнейшем их развитии претерпевают рециклизацию с последующей гидратацией, продукт которой находится в равновесии с лактоном (2) [6], дегидратация которого формирует производное (3) с а-гидрокси-а,в-еноновым фрагментом в структуре [4]. В случае Asc-системы (R= OH) образуется 2,3,6-тригидрокси-4-оксо-2-гексен-5-олид, тогда как для двойной системы (R - остаток трансформированного углевода, включающий изолированные и сопряженные С=О и С=С-связи [8]) хромофорная составляющая лактона (3) обладает большей протяженностью, что подтверждается более высоким поглощением в области 300– 350 нм (см. рис. 1). Кроме того, замена в структуре (3) ОН на R, вероятно, в значительной степени повышает ее устойчивость и, как следствие, стабильность достаточно интен- сивной окраски системы Asc + Glc [4].
Относительно других продуктов можно предположить образование 3-гидрокси-2-пиронов при трансформации аскорбиновой кислоты (полосы 1685 см-1), изолированные (полосы 1620, 1720 см-1) и сопряженные (1645, 1703 см-1) С=С и С=О функции являются фрагментами трансформированного углевода. При этом интенсивных сигналов в области 1500-1600 см-1 не наблюдается (см. рис. 3, 4), что указывает на отсутствие в структуре продуктов карамелизации ароматических фрагментов, формирующихся обычно при глубокой кислотной деструкции углеводов.
Изученные механизмы формирования цветности имеют практическое приложение в технологии производства напитков. Соотношение исходных компонентов в реакционной системе влияет на пропорции их фрагментов в конечной структуре формирующих цветность веществ. Последнее, в свою очередь, опреде-
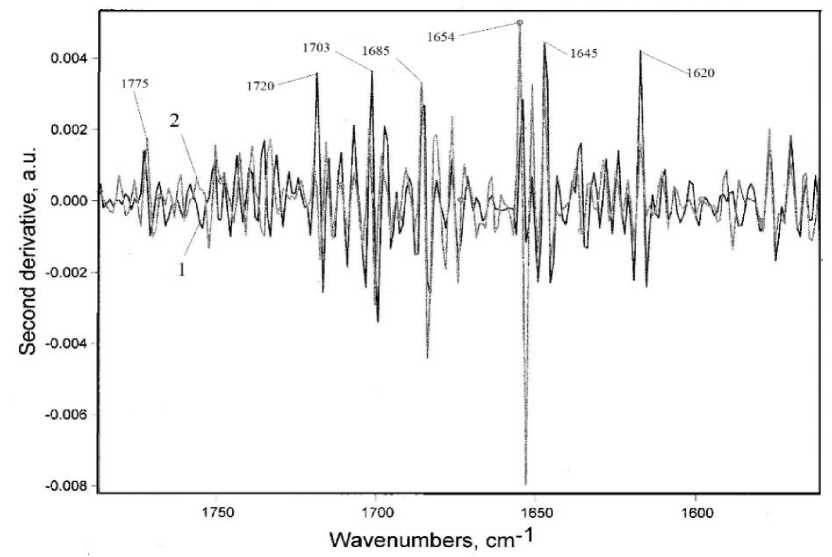
Рис. 4. Вторые производные ИК-Фурье спектров реакционных систем: 1– Asc; 2 – Asc + Glc
ляет строение и протяженность их хромофорных систем, и, как следствие, чистоту и яркость окраски растворов, что в настоящее время исследуется нами в рамках научной тематики по разработке рецептур коньячных колеров.
Заключение
На основании результатов исследования установлен функционально-групповой состав продуктов карамелизации в системах L-аскорбиновая кислота и L-аскорбиновая кислота – D-глюкоза в водно-этанольной (40 % EtOH) среде. Показано, что образующиеся в обеих системах на ранних стадиях полукетали L-гулоно-γ-лактонов со временем претерпевают гидратационную рециклизацию с последующей дегидратацией и образованием 2,3,5-замещенных 4-оксо-δ-лактонов, содержащих гидрокси-α,β-еноновые фрагменты. В случае двойной системы Asc + Glc последние стаби- лизируются замещением в положении 2 фрагментом трансформированного углевода, что повышает устойчивость хромофорной системы и интенсивность окраски раствора, что подтверждается расчетом индексов окрашивания. Продукты более глубокой деструкции (поглощение 400–420 нм), представляющие собой, вероятно, ациклические полисопряжен-ные системы, образуются в меньшем количестве. Дальнейшее изучение свойств карамельных составов на основе аскорбиновой кислоты (светостойкости, токсичности, антиокисли-тельных свойств) позволит разработать доступные и экологичные полифункциональные пигменты для промышленного применения.
Список литературы Формирование цветности карамельных составов на основе аскорбиновой кислоты
- Geng Y., Ning Y., Shao Q., Lu. Y. Wei X., Dai Y., Jia S., Zhong C., Man S., Zhang L., Zhang X. Preparation and Characterization of Acylcaramel // Journal of Agricultural and Food Chemistry, 2019. Vol. 67, no. 19. P. 5614-5620. DOI: 10.1021/asc.jafc.8b07148
- Spizzirri U., Garullo G., De Cicco L., Crispini A., Scarpelli F., Restuccia D., Aiello F. Synthesis and Characterization of a (+)-Catechin and L(+)-Ascorbic Acid Cocrystal as a New Functional Ingredient for Tea Drink // Heliyon. 2019. Vol. 5, no. 8.Article number: e02291. DOI: 10.1016/j .heliyon.2019.e02291.
- Chen H., Gu Z. Effect of Ascorbic Acid on the Properties of Ammonia Caramel Colorant Additives and Acrylamide Formation // Journal of Food Science. 2014. Vol. 79, no. 9. P. 1678-1682. DOI: 10.1111/1750-3841.12560.
- Tanaka H., Kimoto E. Preparation and Characterization of a 345 nm Absorbing Reductant Derived from Dehydro-L-ascorbic acid // Bulletin of Chemical Society of Japan. 1990. Vol. 63, no. 9. P. 2569-2572. DOI: 10.1246/bcsj.63.2569.
- Shinoda Y., Komura H., Homma S., Murata M. Browning of Model Orange Juice Solution: Factors Affecting the Formation of Decomposition Products //Bioscience Biotechnology Biochemistry. 2005. Vol. 69, no. 11. P. 2129-2137. DOI: 10.1271/bbb.69.2129.
- Otsuka M., Kurata T., Arakawa N. Isolation and characterization of an intermediate product in the degradation of 2,3-diketo-L-gulonic acid // Agricultural and Biological Chemistry. 1986. Vol. 50, no. 2. P. 531-533. DOI: 10.1271/bbb.1961.50.531.
- Черепанов И.С. Карамелизация L-арабинозы в присутствии L-аскорбиновой кислоты в этанольной среде // Научный журнал НИУ ИТМО. Процессы и аппараты пищевых производств. 2021. Т. 49, № 3. С. 23-29. DOI: 10.17586/2310-1164-2021-14-3-23-29
- Черепанов И.С., Мухдарова Э.Ш. Изучение влияния D-глюкозы на процессы деструкции L-аскорбиновой кислоты в водно-этанольных средах // Вестник МГТУ. 2022. Т. 25, № 3. С. 248258. DOI: 10.21443/1560-9278-2022-25-3-248-258
- Rojas A., Gerschenson L. Ascorbic Acid Destruction in Aqueous Model Systems: an Additional Discussion // Journal of Science Food and Agriculture. 2001. Vol. 81, no. 15. P. 1433-1439. DOI: 10.1002/jsfa.961.
- Chuang P.-T., Shen S.-C., Wu J. S.-B. Browning in Ethanolic Solutions of Ascorbic Acid and Catechin // Journal of Agricultural and Food Chemistry. 2011. Vol. 59, no. 14. P. 7818-7824. DOI: 10.1021/jf200817e.
- Perez C., Fessore E., Gerschenson L., Cameron R., Rojas A. Hydrolytic and Oxidative Stability of L(+)-Ascorbic Acid Supp orted in Pectin Films: Influence of Macromolecular Structure and Calcium Presence // Journal of Agricultural and Food Chemistry. 2012. Vol. 60, no. 21. P. 5414-5422. DOI: 10.1021/jf205132m
- Leonardi G., Truscello A., Mondrone G., Sebastiano R. A Facile Synthesis in Aqueous Medium of 3-Hydroxy-2-pyrone From Aldaric Acids or Their Derivatives // Results in Chemistry. 2022. Vol. 4, article Number: 100280. DOI: 10.1016/j.rechem.2021.100280
- Winanti D., Darmawati E., Syarief R. Minimally Processed for Cassava Browning Inhibition by Ascorbic Acid and Oxygen Absorbent // IOP Conference Series: Earth and Environmental Sciences. 2019. Vol. 309, Article Number: 012013. DOI: 10.1088/1755-1315/309/1/012013
- Li T.-X., Luo C., Geng Z.-Z., Jiang Z.-R., Ji L.-B., Shentu H.-Q. Type I Caramel Products of Maltose and Sucrose with Water and Their Antioxidant Activity // Food of Science and Technology (Campinas). 2020. Vol. 42. P. 1-6. DOI: 10.1590/fst.58520.
- Yadav R.A., Rani P., Kumar M., Singh R., Singh P., Singh P. Experimental IR and Raman Spectra and Quantum Chemical Studies of Molecular Structures, Conformers and Vibrational Characteristics of L-ascorbic Acid and its Anion and Cation // Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy. 2011. Vol. 84, no. 1. P. 6-21. DOI: 10.1016/j.saa.2011.07.043
- Lievens C., Mourant D., He M.; Gunawan R., Li X., Li C.-Z. An FT-IR Spectroscopic Study of Carbonyl Functionalities in Bio-oil // Fuel. 2011. Vol. 90, no. 11. P. 3417-3423. DOI: 10.1016/j .fuel.2011.06.001.
- Barril S., Clark A., Prenzler P., Karuso P., Scollary G. Formation of Pigment Precursor (+)-1"-Methylene-6"-hydroxy-2H-furan-5"-one Catechin Isomers from (+)-Catechin and a Degradation Products of Ascorbic Acid in a Model Wine System // Journal of Agricultural and Food Chemistry. 2009. Vol. 57, no. 20. P. 9539-9546. DOI: 10.1021/jf902198e


