Генетический маркер коллагена ITGA2 в оценке эффективности антиагрегантного эффектапрепаратов ацетилсалициловой кислоты
Автор: Рузов В.И., Алтынбаева Э.Н., Комарова Л.Г., Низамова Л.Т., Кулакова Ж.В., Васильева И.В.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 1, 2016 года.
Бесплатный доступ
Цель. Изучить эффективность препаратов ацетилсалициловой кислоты у пациентов с поли- морфизмом гена рецептора коллагена ITGA2.Материалы и методы. Обследовано 88 пациентов с ИБС и сопутствующей АГ, получающих ас- пирин и кардиомагнил на фоне базисной терапии β-адреноблокаторами, иАПФ и статинами.Проводилась оценка агрегационной активности тромбоцитов методом световой агрегометрии при помощи двухканального лазерного анализатора 230LA (BIOLA Ltd, Россия). Полиморфизм ге- на ITGA2 определяли с использованием реагентов «ДНК-Экспресс («Литех», Россия). Использован ампфликатор с флуоресцентной детекцией в режиме реального времени (Bio-Rad, США).Результаты и обсуждение. Оценка распределения аллельного полиморфизма гена ITGA2 показала преобладание Т-аллели. Так, среди больных было выявлено 30,7 % гомозигот по 1-й аллели (С/С), 22,7 % гомозигот по 2-й аллели (Т/Т) и 46,6 % гетерозигот (С/Т). Среди здоровых - 80 % гомози- гот по 1-й аллели (С/С), 20 % гетерозигот (С/Т); гомозигот по 2-й аллели (Т/Т) выявлено не было. Таким образом, у большинства (77,3 %) больных была обнаружена нуклеотидная замена в гене ITGA2 хотя бы в одной из хромосом. В контрольной группе, напротив, не наблюдалось наличия гомозигот по Т-аллели и преобладали гомозиготы по аллели С. Распределение типа агрегации тромбоцитов по полиморфизму ITGA2 показало преобладание среди пациентов с повышенной остаточной агрегацией тромбоцитов генотипов С/Т и Т/Т. Пациенты с гипоагрегацией ха- рактеризовались практически равномерным распределением генотипов С/С и Т/Т. Нормаль- ные параметры агрегации тромбоцитов были выявлены преимущественно у пациентов с С/С-генотипом.Выводы. Полученные результаты исследования свидетельствуют о преобладании аллели Т у па- циентов с повышенной агрегацией тромбоцитов.
Агрегация, генотип, полиморфизм гена itga2
Короткий адрес: https://sciup.org/14113136
IDR: 14113136 | УДК: 615.276:616-074:575.113
Genetic markers of collagen ITGA2 to evaluate the effectiveness of antiplatelet effect of the drug acetylsalicylic acid
Objective. To study the effectiveness of aspirin in patients with drug polymorphism ITGA2 collagen receptor gene.Materials and methods. We examined 88 patients with coronary artery disease and arterial hypertension, receiving aspirin and cardiomagnil on basic therapy β-blockers, ACE inhibitors and statins.The estimation of platelet aggregation activity by light aggregometry using a two-channel laser analyzer 230LA (BIOLA Ltd, Russia). ITGA2 gene polymorphism was determined using the reagents of DNA- Express ( «Liteh», Russia). Used thermocycler with fluorescence detection in real time (Bio-Rad, USA). Results and discussion. Assessment of the distribution of allelic polymorphism ITGA2 showed the predominance of T-allele. For example, among patients it revealed 30,7 % homozygous 1st alleles (C/C), 22,7 % homozygous 2nd allele (T/T) and 46,6 % heterozygous (C/T). Among healthy - 80 % for homozygotes 1st alleles (C/C), 20 % heterozygous (C/T); homozygotes for the 2nd allele (T/T) have been identified. Thus, the majority (77,3 %) patients in the nucleotide substitution ITGA2 gene has been detected in at least one of the chromosomes. In the control group, in contrast, was not observed by the presence of homozygous T allele and homozygous for the alleles dominated C. Distribution of platelet aggregation type polymorphism showed ITGA2 prevalence among patients with high residual platelet aggregation genotype C/T and T/T. Patients with hypo-aggregation substantially uniform distribution of genotypes C/C and T/T. Normal platelet aggregation parameters were found predominantly in patients with the C/C genotype.Conclusions. These results suggest the prevalence of T allele in patients with increased platelet aggregation
Текст научной статьи Генетический маркер коллагена ITGA2 в оценке эффективности антиагрегантного эффектапрепаратов ацетилсалициловой кислоты
Введение. Один из эффективных подходов к изучению роли генетических механизмов нарушения агрегации тромбоцитов связан с выделением генов с потенциально наибольшим вкладом в патогенез заболевания. Изучение генетических аспектов тромбоза свидетельствует о преобладании последнего у людей с «неблагоприятными» аллелями белков-участников гемостатического каскада [1–3].
Известно, что аллель T полиморфного маркера C807T гена ITGA2 ассоциирована с повышенной экспрессией GPIa-рецепторов тромбоцитов и повышенной адгезией тромбоцитов к коллагену. При этом повышенная экспрессия рецепторов GPIa/IIa обнаружена на поверхности тромбоцитов у гомозигот по аллели Т (генотип Т/Т), в то время как у гомозигот по аллели С (генотип С/С) наблюдается снижение экспрессии. Наличие Т-аллели ассоциируется с увеличением скорости адгезии тромбоцитов, а следовательно, и с повышением риска развития инфаркта миокарда, ишемического инсульта, тромбоэмболии [4–7] и может быть использовано, по мнению авторов, для оценки риска развития тромбозов после ангиопластики и стентирования коронарных артерий.
Исследование HAPI по изучению реактивности тромбоцитов у женщин и мужчин после терапии аспирином подтверждает роль наследственных факторов в формировании изменчивости функции тромбоцитов до и после терапии аспирином [8, 9]. Авторы считают невозможным предусмотреть развитие резистентности, а у женщин с сердечно-сосудистыми заболеваниями резистентность к аспирину способствует более высокому риску развития острых коронарных синдромов.
Согласно меморандуму рабочей группы по изучению резистентности к аспирину Международного общества по тромбозу и гемостазу [10], среди возможных механизмов неэффективности терапии аспирином рассматривается генетический полиморфизм рецепторов GPIIb/IIIa. Неоднозначная интерпретация генетических маркеров развития тромбоза, неизученность связи последних с функциональным состоянием тромбоцитов определили актуальность выбранной темы исследования.
Цель исследования. Изучить эффективность препаратов ацетилсалициловой кислоты у пациентов с полиморфизмом гена рецептора коллагена ITGA2.
Материалы и методы. Материалом для исследования служила ДНК, выделенная из цельной крови пациентов с использованием набора «ДНК-Экспресс» («Литех», Россия). Полиморфизм гена определяли с использованием реагентов фирмы «Литех» методом ПЦР в реальном времени. Амплификацию и плавление ее продуктов проводили на ам-плификаторе с флуоресцентной детекцией в режиме реального времени CFX96Real-Time PCR Detection System (Bio-Rad, США).
Агрегацию тромбоцитов определяли при помощи 2-канального лазерного анализатора 230LA (BIOLA Ltd, Россия) методом световой агрегометрии. Исследовалась спонтанная и индуцированная агрегация тромбоцитов. В качестве индуктора агрегации использовался аденозиндифосфат (АДФ) в концентрациях 0,1; 1,0 и 5,0 мкмоль. Степень спонтанной агрегации и агрегации, индуцированной 0,1 и 1,0 мкмоль АДФ, определяя-ли как максимальное значение среднего размера агрегатов и измеряли в относительных единицах. Степень агрегации, индуцированной АДФ в концентрации 5,0 мкмоль, опре- деляли как максимальное приращение свето-пропускания после добавления индуктора и измеряли в процентах. Нормальными принимались значения: для спонтанной агрегации – 1,0–1,5 отн. ед., для индуцированной 0,1 мкмоль АДФ – 1,0–2,0 отн. ед., для индуцированной 1,0 мкмоль АДФ – 1,5–5,5 отн. ед., для индуцированной 5,0 мкмоль АДФ – 25–70 %.
Результаты и обсуждение. В исследование были включены 88 пациентов с ИБС и сопутствующей АГ (возраст больных – от 41 до 91 года; средний возраст – 69,9±12,3 года). Средний возраст группы здоровых лиц – 47,60±8,11 года. Мужчины составили 42 %, а женщины – 58 % обследованных. Все пациенты получали базисную терапию ИБС и АГ (β-адреноблокаторы, ИАПФ, статины) и препараты ацетилсалициловой кислоты (аспирин – 100 мг/сут, кардиомагнил – 75 мг/сут).
Оценка распределения аллельного полиморфизма гена ITGA2 показала преобладание Т-аллели. Так, среди больных было выявлено 30,7 % гомозигот по 1-й аллели (С/С), 22,7 % гомозигот по 2-й аллели (Т/Т) и 46,6 % гетерозигот (С/Т). Среди здоровых – 80 % гомозигот по 1-й аллели (С/С), 20 % гетерозигот (С/Т); гомозигот по 2-й аллели (Т/Т) выявлено не было. Таким образом, у большинства (77,3 %) больных была обнаружена нуклеотидная замена в гене ITGA2 хотя бы в одной из хромосом. В контрольной группе, напротив, не наблюдалось наличия гомозигот по Т-аллели и преобладали гомозиготы по аллели С.
Распределение типа агрегации тромбоцитов по полиморфизму ITGA2 (табл. 1) показало преобладание среди пациентов с повышенной остаточной агрегацией тромбоцитов генотипов С/Т и Т/Т. Пациенты с гипоагрегацией характеризовались практически равномерным распределением генотипов С/С и Т/Т. Нормальные параметры агрегации тромбоцитов были выявлены преимущественно у пациентов с С/С-генотипом.
Распределение типов агрегации между различными генотипами было проверено парным t-тестом. Различия в распределении типов агрегации оказались статистически незначимыми (С/С и С/Т: p=0,1; C/C и T/T: p=0,05; C/C и T/T: p=0,4).
Таблица 1
|
Тип агрегации |
Итого |
||||
|
Гиперагрегация |
Гипоагрегация |
Норма |
|||
|
Генотип |
С/С |
11 (35,5 %) |
7 (22,6 %) |
13 (41,9 %) |
31 |
|
С/Т |
24 (57,1 %) |
8 (19,1 %) |
10 (24,8 %) |
42 |
|
|
Т/Т |
13 (68,4 %) |
3 (15,8 %) |
3 (15,8 %) |
19 |
|
|
Итого |
48 |
18 |
26 |
92 |
|
Распределение типа агрегации по полиморфизму ITGA2
Оценка спонтанной и АДФ-индуциро-ванной агрегации тромбоцитов не выявила значимых различий в распределении типов агрегации между различными генотипами (χ2=0,17) (табл. 2).
Распределение показателей агрегации у пациентов с полиморфизмом ITGA2 было проверено на нормальность методом Колмогорова–Смирнова. Данные имели ненормаль- ное распределение, поэтому для выявления достоверности различий в показателях агрегации тромбоцитов был использован тест Крускала–Уоллиса. Тест показал статистически значимые различия в показателях спонтанной агрегации тромбоцитов (p=0,01) и отсутствие различий при индукции агрегации тромбоцитов АДФ.
Таблица 2
Распределение показателей агрегации тромбоцитов по полиморфизму ITGA2
|
Генотип |
Спонтанная агрегация |
АДФ 0,1 мкмоль |
АДФ 1 мкмоль |
АДФ 5 мкмоль |
|
|
С/С, n=31 |
Среднее |
1,5468 |
2,2787 |
3,1552 |
40 % |
|
Станд. отклонение |
0,64019 |
1,32059 |
1,76522 |
15,3 % |
|
|
Медиана |
1,4 |
1,85 |
3,30 |
42 % |
|
|
С/Т, n=42 |
Среднее |
1,6752 |
2,5290 |
3,3452 |
38,9 % |
|
Станд. отклонение |
0,77846 |
1,19747 |
1,57775 |
15,5 % |
|
|
Медиана |
1,45 |
2,45 |
3,05 |
40,45 % |
|
|
Т/Т, n=19 |
Среднее |
2,5721 |
2,6716 |
3,6642 |
44,2 % |
|
Станд. отклонение |
1,39672 |
1,00877 |
1,58407 |
24 % |
|
|
Медиана |
2,15 |
2,70 |
4,10 |
38 % |
|
|
Итого |
Среднее |
1,8172 |
2,4741 |
3,3471 |
40,4 % |
|
Станд. отклонение |
0,97326 |
1,20201 |
1,63667 |
17,4 % |
|
|
Медиана |
1,50 |
2,30 |
3,35 |
40,65 % |
|
Известно, что степень АДФ-индуциро-ванной агрегации зависит от количества АДФ-рецепторов [11].
Для выявления достоверности различий в спонтанной агрегации тромбоцитов был ис- пользован однофакторный дисперсионный анализ, парный t-тест (с поправкой Бонфер-рони, различия считались статистически значимыми при p<0,17 (0,05/3)) и тест Тьюки. Выявлено (рис. 1) наличие статистически значимых различий в показателях спонтанной агрегации тромбоцитов (p<0,001). По данным парного t-теста, между генотипами С/С и С/Т статистически значимых различий выявлено не было (p=0,55), генотип Т/Т статистически значимо отличался как от генотипа С/С (p<0,001), так и от генотипа С/Т (p=0,001). Тест Тьюки (рис. 2) также под- твердил значимые отличия в спонтанной агрегации тромбоцитов для носителей генотипа Т/Т по сравнению с носителями генотипов С/Т и С/С. Разница в среднем размере агрегата составила 1,0253311 (95 % ДИ (0,4; 1,65)) для С/С и Т/Т и 0,9 (95 % ДИ (0,30; 1,49)) для С/T и Т/Т.
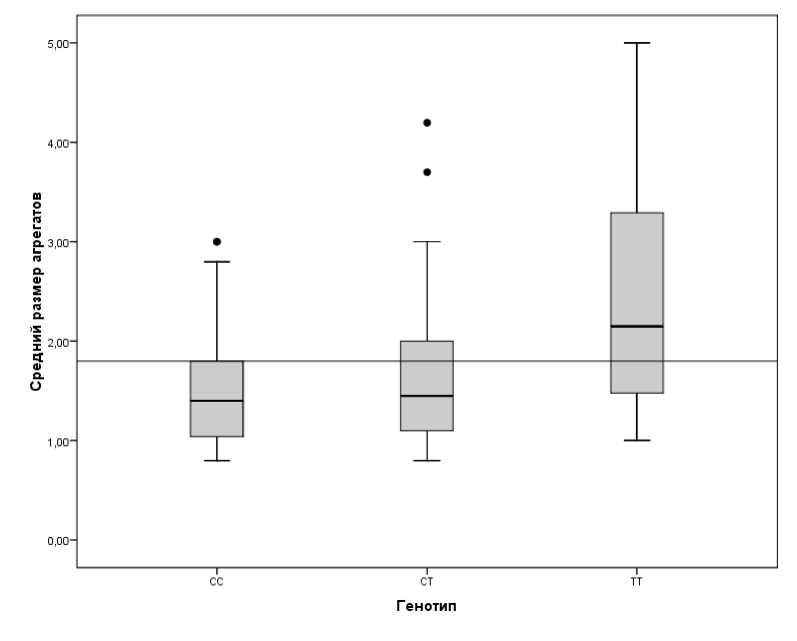
Рис. 1. Средний размер агрегатов (спонтанная агрегация тромбоцитов)
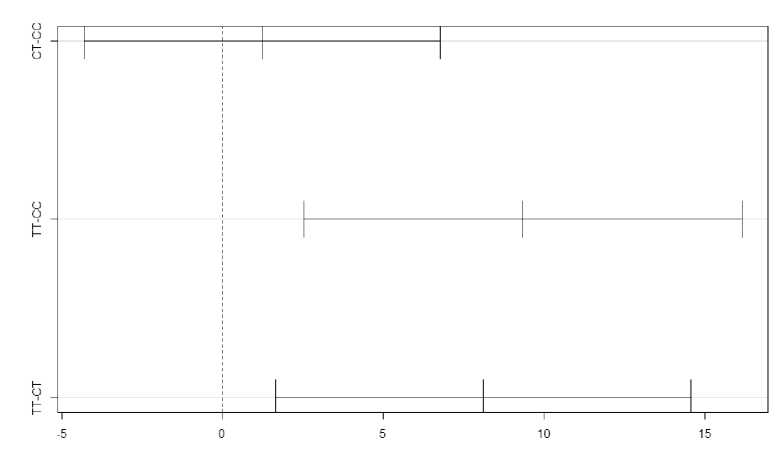
Рис. 2. Тест Тьюки (спонтанная агрегация тромбоцитов)
Данные литературы о связи различных полиморфных маркеров генов-кандидатов с эффективностью терапии основными классами антитромбоцитарных препаратов немногочисленны.
В последние годы активно обсуждается проблема недостаточной активности (аспи-ринорезистентности) терапии препаратами ацетилсалициловой кислотой [12–15]. Есть основания полагать, что резистентность к терапии может быть связана с полиморфизмом гена, кодирующегогликопротеиновыерецеп-торы тромбоцитов [16, 17].
Известно, что ген ITGA2 кодирует ин-тегрин альфа-2, известный также как GPIa – мембранный гликопротеин, экспрессирующийся на мембранах различных клеток, включая мегакариоциты, фибробласты и тромбоциты, и образующий комплексы с тканевыми белками [18]. Одновременно с этим комплекс GPIa и GPIIa служит одним из главных рецепторов коллагена, расположенных на клеточной мембране тромбоцитов иявляющихся активатором агрегации тромбоцитов [19].
Установление ведущей роли тромбоцитарного звена гемостаза в патогенезе атерот-ромбоза способствовало разработке большого количества лекарственных препаратов, показавших в крупных многоцентровых исследованиях свою эффективность у больных с острыми коронарными синдромами и хроническими формами ИБС, в т.ч. при чрескожных реваскуляризационных процедурах [20, 21].
Одной из возможных причинрезистент-ности к аспирину у пациентовна фоне антиагрегантной терапии является преобладание среди них лиц с повышенной экспрессиейре-цепторов GPIa/IIa.
Известно, что индуцируемые реакции тромбоцитов пропорциональны количеству формирующихся комплексов «агонист-рецептор». Ответ на антиагрегантные лекарственные препараты будет зависеть от плотности соответствующих рецепторов на мембране тромбоцитов. Исследования антагони- стов GPIIb-IIIa-рецепторов показали, что интенсивность тромбоцитарной агрегации строго коррелирует с количеством свободных рецепторов на поверхности клеток [22]. Для проверки гипотезы о связи повышенной агрегации тромбоцитов с геном, кодирующим ин-тегрин альфа-2, мы провели изучение связи агрегации тромбоцитов у принимающих препараты ацетилсалициловой кислоты с аллельным полиморфизмом гена ITGA2. Полученные результаты исследования свидетельствуют о преобладании аллели Т у пациентов с повышенной агрегацией тромбоцитов. Однако, возможно, недостаточный объем выборки предопределил отсутствие значимых различий в распределении типов агрегаций между различными генотипами, что предполагает дальнейшее изучение данной проблемы с расширением контингента обследуемых. В связи с тем, что в настоящее время не представляется возможным выделить генетические предикторы эффективности применения того или иного антиагреганта, требуется проведение дальнейших исследований, а наличие выявленной «неблагоприятной» полиморфной аллели (Т-аллели) является только вероятностным показателем, значение которого нельзя переоценивать.
Заключение. Таким образом, продолжение исследований по генотипированию в сочетании с тестированием функциональной активности тромбоцитов может помочь врачам выбрать оптимальную тактику анти-тромбоцитарной терапии. Требуется проведение рандомизованных исследований, демонстрирующих преимущество индивидуализированной терапии антиагрегантами, основанных на результатах генетических и функциональных тестов. Одновременно с этим для определения маркера высокой остаточной агрегации тромбоцитовна фоне антиагрегантной терапии, которая может иметь прогностическое значение для оценки эффективности конкретного антиагреганта, необходимы и дальнейшие фармакогенетические исследования.
Список литературы Генетический маркер коллагена ITGA2 в оценке эффективности антиагрегантного эффектапрепаратов ацетилсалициловой кислоты
- Сироткина О.В., Баженова Е.А., Беркович О.А., Пчелина С.Н. Сочетанное носительство аллельных вариантов генов системы тромбообразования как фактор риска развития инфаркта миокарда у мужчин молодого возраста. Российская кардиология: от центра к регионам: материалы Российского национального конгресса кардиологов. Томск; 2004. Кардиоваскулярная терапия и профилактика. 2004; 4: 447-448
- Podgoreanu M.V., White W.D., Morris R.W., Mathew J.P., Stafford-Smith M., Welsby I.J., Gro-cott H.P., Milano C.A., Newman M.F., Schwinn D.A. Inflammatory Gene Polymorphisms and Risk of Postoperative Myocardial Infarction After Cardiac Surgery. Circulation. 2006; 114 (suppl. 1): 275-281
- Torshin I.Yu. Bioinformatics in the post-genomic era: physiology and medicine. NY: Nova Biomedical Books; 2007. 35-67
- Furihata K., Nugent D.J., Kunicki T.J. Influence of platelet collagen receptor polymorphisms on risk for arterial thrombosis. Arch. Pathol. Lab. Med. 2002; 126: 305-309
- Lu J.X., Lu Z.Q. Zhang S.L., Zhi J., Chen Z.P., Wang W.X. Polymorphism in Integrin ITGA2 is Associated with Ischemic Stroke and Altered Serum Cholesterol in Chinese Individuals. Balkan Med J. 2014; 31 (1): 55-59
- Kunicki T.J., Kritzik M., Annis D.S., Nugent D.J. Hereditary variation in platelet integrin alpha 2 beta 1 density is associated with two silent polymorphisms in the alpha 2 gene coding sequence. Blood. 1997; 89 (6): 1939-1943
- Grundmann K., Jaschonek K., Kleine B., Dichgans J., Topka H. Aspirin non-responder status in patients with recurrent cerebral ischemic attacks. J Neurol. 2003; 250 (1): 63-66
- Shen H., Herzog W., Drolet M.A., Pakyz R., Newcomer S., Sack P., Karon H., Ryan K.A., Zhao Y., Shi X., Mitchell B.D., Shuldiner A.R. Aspirin Resistance in Healthy Drug-Naïve Men versus Women (From the Heredity and Phenotype Intervention Heart Study). Am. J. Cardiol. 2009; 104 (4): 606-612
- Gum P.A., Kottke-Marchant K., Poggio E.D., Gurm H., Welsh P.A., Brooks L., Sapp S.K., Topol E.J. Profile and prevalence of aspirin resistance in patients with cardiovascular disease. Am. J. Cardiol. 2001; 88 (3): 230-235
- Michelson A.D., Cattaneo M., Eikelboom J.W., Gurbel P., Kottke-Marchant K., Kunicki T J., Pulci-nelli F.M., Cerletti C., Rao A.K. Aspirin resistance: position paper of the Working Group on Aspirin Resistance. J. Thromb. Haemost. 2005; 3 (6): 1309-1311
- Сироткина О.В., Боганькова Н.А., Тараскина А.Е., Железняк Е.Л., Болдуева С.А., Вавилова Т.В. Молекулярно-генетический анализ АДФ-рецепторов тромбоцитов у здоровых лиц и пациентов, принимающих клопидогрел. Технологии живых систем. 2009; 8: 46-52
- Губский Л.В. Резистентность к дезагрегантам -причины, клиническая значимость, методы диагностики и коррекции. Тер. архив. 2008; 80 (12): 89-95
- Ушкалова Е.А. Новые пептидные ингибиторы агрегации тромбоцитов: компьютерное моделирование и синтез. Молекулярная медицина. 2012; 2: 21-26
- Шилов А.М. Ацетилсалициловая кислота -антиагрегант для профилактики и лечения сердечно-сосудистых заболеваний. Трудный пациент. 2013; 4: 3-8
- Hart R.G., Pearce L.A., Aguilar M.I. Meta-analysis: antithrombotic therapy to prevent stroke in patients who have nonvalvular atrial fibrillation. Ann. Intern. Med. 2007; 146 (12): 857-867
- Гарькина С.В., Дупляков Д.В., Павлова Т.В. Проблемы применения антитромбоцитарной терапии в кардиологии. Эффективная фармакотерапия. 2012; 1: 24-27
- Тупицына Т.В. Антиагрегантная терапия при ИБС. Некоторые проблемы и решения. Кардиология. 2010; 50 (6): 4-21
- Rivera J., Lozano M.L., Navarro-Núñez L., Vicente V. Platelet receptors and signaling in the dynamics of thrombus formation Haematologica. 2009; 94 (5): 700-711
- Kunicki T.J. The Influence of Platelet Collagen Receptor Polymorphisms in Hemostasis and Thrombotic Disease. Arterioscler. Thromb. Vasc. Biol. 2002; 22: 14-20
- Верткин А.Л., Зайратьянц О.В., Вовк Е.И., Колобов С.В. Лечение и профилактика желудочно-кишечных кровотечений при обострении ишемической болезни сердца. Фарматека. 2007; 15: 54-60
- Павлова Т.В., Поляков В.П., Дупляков Д.В., Хохлунов С.М., Кириллов В.И., Шавкунов С.А. Распределение полиморфизмов генов некоторых компонентов системы гемостаза у больных ИБС. Кардиология. 2009; 4: 9-12
- Мазуров А.В. Физиология и патофизиология тромбоцитов. М.: ГЭОТАР-Медиа; 2011. 480


