Химиолучевая терапия пациента с бластной плазмоцитоидной дендритноклеточной неоплазией. Клиническое наблюдение
Автор: Виноградова Ю.Н., Белоусова И.Э., Самородова И.А., Медведева Н.В., Бутримова А.С., Долбов А.Л., Пахомов А.Ю., Ильин Н.В., Артемов М.В., Одинцова М.В., Потапенко В.Г.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Клинический случай
Статья в выпуске: 1 т.22, 2026 года.
Бесплатный доступ
Бластная плазмоцитоидная дендритная клеточная неоплазия (БПДКН) – это клинически агрессивное гематологическое злокачественное заболевание, развивающееся из плазмоцитоидных дендритных клеток. Обычно проявляется кожными поражениями. Диагноз ставится на основании биопсии пораженного участка и, как правило, на основе идентификации бластных клеток, демонстрирующих классические иммунофенотипы CD123, CD4 и CD56 в дополнение к специфическим маркерам pDC. Медиана общей выживаемости составляет 18–24 месяца. К потенциальным факторам риска сокращения выживаемости относятся пожилой возраст, явное поражение костного мозга и генетические аномалии. На сегодняшний день не существует стандартного протокола лечения БПДК. Традиционно лечение проводится аналогично острому лейкозу или лимфоме, однако прогноз остается неблагоприятным. Обязательны оценка и лечение центральной нервной системы, а также тщательное наблюдение за состоянием кожи в сочетании с дерматологическим обследованием. Лучевая терапия применяется при изолированных поражениях кожи, у пациентов, которым не показана химиотерапия из-за возраста или сопутствующих заболеваний, а также при рецидиве заболевания после химиотерапии. Однако имеется очень мало данных о лучевой терапии БПДК.
Рак, злокачественные опухоли, бластная плазмоцитоидная дендритно-клеточная неоплазия, химиотерапия, лучевая терапия, ПЭТ/КТ с 18F-ФДГ
Короткий адрес: https://sciup.org/170211666
IDR: 170211666
Chemoradiotherapy of the patient with blast plasmacytoid dendritic cell neoplasm. A clinical case
Blast plasmocytoid dendritic cell neoplasm (BPDCN) is a clinically aggressive hematological malignant disease that develops from plasmocytoid dendritic cells. Skin lesions usually manifest it. The diagnosis is based on a biopsy of the affected area and, as a rule, on the identification of blastoid cells demonstrating the classical CD123, CD4 and CD56 immunophenotypes in addition to specific pDC markers. The median overall survival is 18-24 months. Potential risk factors for reduced survival include old age, apparent bone marrow damage, and genetic abnormalities. To date, there is no standard protocol for the treatment of BPDCN. Traditionally, treatment is similar to acute leukemia or lymphoma, but the prognosis remains unfavorable. Assessment and treatment of the central nervous system are mandatory, as well as careful monitoring of the skin condition in combination with a dermatological examination. Radiation therapy is used for isolated skin lesions, in patients who are not indicated for chemotherapy due to age or concomitant diseases, as well as in case of recurrence of the disease after chemotherapy. However, there is very little data on radiation therapy for BPDCN.
Текст научной статьи Химиолучевая терапия пациента с бластной плазмоцитоидной дендритноклеточной неоплазией. Клиническое наблюдение
агрессивный лейкоз из натуральных киллеров , одна ко в 2008 году Всемирная Организация Здравоохра нения изменила название опухоли на БПДКН [3, 4].
Заболевание часто дебютирует с одиночных или множественных узелковых и иногда язвенных поражений кожи, с быстрой генерализацией и вовлечением центральной нервной системы, внутренних органов, костного мозга и серозных оболочек [5-7]. В случае поражения кожи при гистологическом исследовании наблюдается инфильтрация дермы и подкожного слоя незрелыми бластоидными неопластическими клетками. В 10–20% случаев оно связано с другими гематологическими заболеваниями, чаще миелоидной направленности [8-10]. Дифференциальный диагноз БПДКН проводится в первую очередь с Т-лимфобластыми лимфомами/лейкозами и острым миелоидным лейкозом/саркомой. Схожими чертами обладают периферические и NK/T лимфо-мы/лейкозы, а также Т-пролимфоцитарные лейкозы [11-13].
Пациентов с БПДКН лечат по программам для острых лейкозов . С разной степенью эффективности применяют высокодозный метотрексат , цитарабин и аспарагиназу . Однако для заболевания типично быстрое развитие химиорезистентности и медиана общей выживаемости до появления таргетной и раз вития клеточной терапии составляла менее года [14, 15]. В последние годы с появлением новых лекарств и технологий прогноз пациентов улучшился [1619]. В связи с тем , что БПДКН чаще всего протекает в виде диссеминированного процесса , лучевая тера пия применяется крайне редко .
В статье представлен опыт успешного лечения БПДКН с помощью дистанционной конформной лу чевой терапии .
Клиническое наблюдение
Пациентка А ., 1986 г . р ., в январе 2022 года обра тила внимание на появление участка уплотнения на внутренней поверхности левого бедра , по внешним признакам похожего на липому . В марте 2022 года образование было удалено , гистологическое иссле дование послеоперационного материала утеряно . Послеоперационная рана заживала вторичным на тяжением .
В октябре 2022 года появились жалобы на утреннюю профузную потливость и вечерние подъемы температуры тела до 38С0. В связи с плохим заживлением раны, уплотнением её краев заподозрено злокачественное новообразованием и в ноябре 2022 года была выполнена инцизионная биопсия с гистологическим и иммуногистохимическим исследованием биоптата. В дольках подкожно-жировой клетчатки обнаружены крупные инфильтраты лимфоцитов мелких и средних размеров с умеренно выраженным плеоморфизмом ядер и экспрессией СD4, CD56, CD123 и CD68 и индексом пролиферативной активности – 30%. Выполнена стадирующая компьютерная томография (КТ) грудной клетки, брюшной полости и малого таза. Выявлена спленомегалия до 40×113×125 мм (селезёночный индекс 565 см3, норма до 450 см3) и абдоминальная лимфаденопатия: увеличение лимфоузлов по ходу брюшного отдела аорты до 11×13 мм, по ходу подвздошных артерий до 11×26 мм и паховых до 10×28 мм с перинодальным отёком. В гемограмме отмечались нормоцитарная анемия 113 г/л, лейкопения 2,7 тыс/мкл с лимфопенией 0,44 тыс/мкл и нейтропенией 1,7 тыс/мкл. Опухолевого поражения костного мозга по данным миелогистограммы не было. Анализы крови на антитела к гепатиту С и вирусу иммунодефицита человека отрицательны.
Поставлен диагноз « Неоплазия из бластных плаз - моцитоидных дендритных клеток с поражением абдоминальных лимфоузлов , селезёнки , кожи и под кожной клетчатки левого бедра »
В декабре 2022 года начата химиотерапия первой линии по программе «AMD». Проведено два курса в стандартных дозах : метотрексат 3 гр / м 2 в первый день курса , Л - аспарагиназа 6000 МЕ / м 2 во второй , четвертый , шестой и восьмой дни курса , дексамета зон 40 мг с первого по четвертый дни курса . На фоне химиотерапии В - симптоматика , рост образования и увеличение зоны некроза сохранялись . В качестве терапии второй линии в феврале и марте 2023 года проведено два курса по программе «AzaVen» в стан дартных дозах : азацитидин 75 мг / м 2, с первого по седьмой день 28- дневного курса , венетоклакс по 400 мг / сут постоянно . Эффекта не было .
С 13.04.23. В течение месяца проведено сдержи вающее лечение по программе « РЕР - С ». Все препа раты принимались перорально в стандартных дозах ( этопозид 50 мг / сутки , преднизолон 20 мг / сут , ци - клофосфан 50 мг / сут , прокарбазин 50 мг / сут ). Еже недельно проводился клинический анализ крови с коррекцией доз по необходимости . Вопреки химио терапии заболевание продолжало прогрессировать ( Рисунок 1). Принято решение о проведении палли ативного курса лучевой терапии .
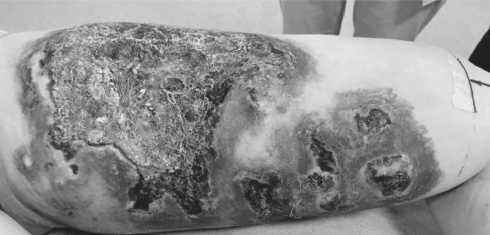
Рисунок 1. Поражение кожи внутренней поверхности левого бедра. Определяется выраженный отек мягких тканей левого бедра с наличием множественных разнокалиберных участков изъявления кожи и зонами некроза. Края дефектов обработаны раствором бриллиантового зелёного.
С целью оценки распространённости заболева ния пациентке было выполнено ПЭТ / КТ всего тела с 18F- ФДГ , по результатам которого , в мягких тканях по медиальной поверхности левого бедра определялся крупный участок неравномерного уплотнения кожи и подкожной жировой клетчатки неправильной фор -
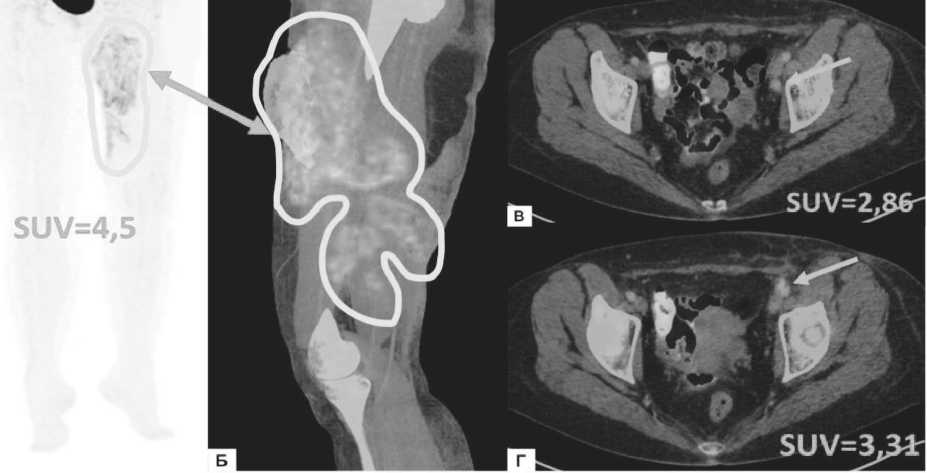
Рисунок 2. ПЭТ/КТ с ISF-ФДГ ПЭТ-изображение, фронтальная проекция (А), совмещенное ПЭТ/КТ-изображение, сагиттальная проекция в режиме многослойного изображения (Б), совмещенные ПЭТ/ КТ-изображения, аксиальные проекции (В, Г). Массивное метаболически активное образование кожи медиальной поверхности левого бедра (обведено белым цветом и отмечено стрелкой), единичные наружные подвздошные лимфоузлы слева с повышенным уровнем гликолитической активности (отмечены белыми стрелками)
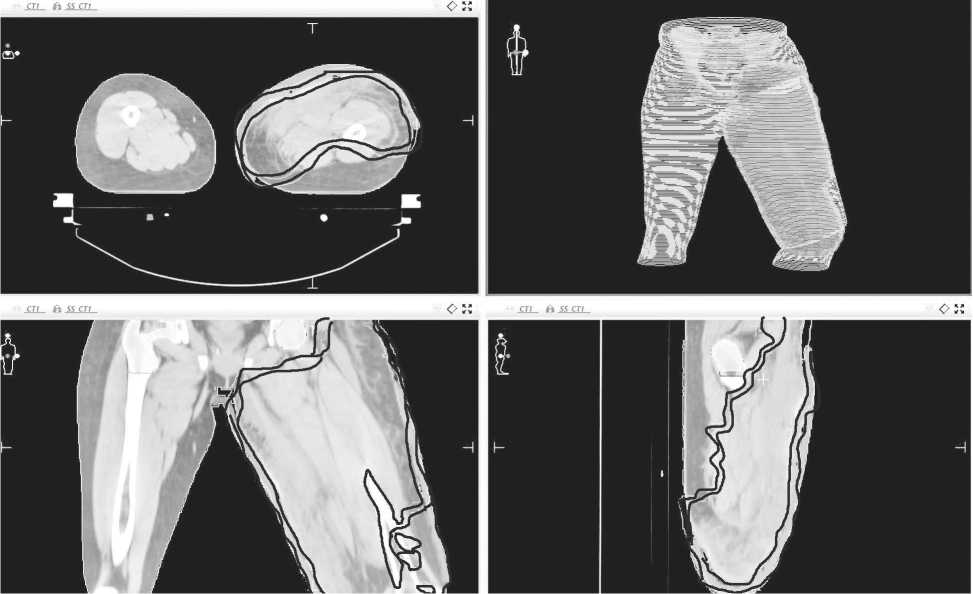
Рисунок. 3. Этап подготовки к дозиметрическому планированию лучевой терапии, оконтуривание
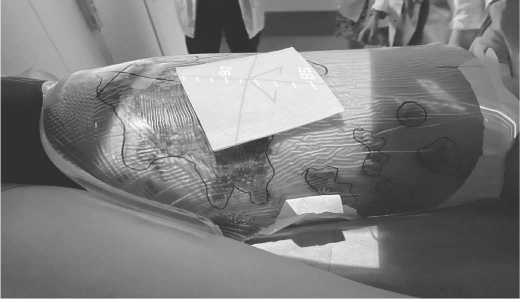
Рисунок 4. Укладка пациента на линейном ускорителе с применением тканеэквивалентного болюса - толщиной 1 см
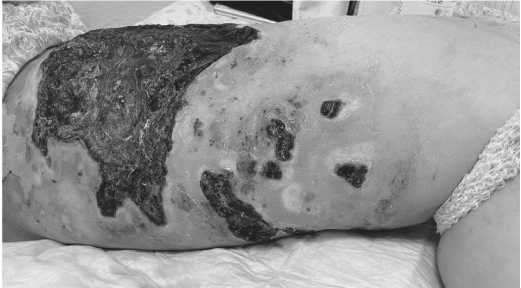
Рисунок 5. Область первичного очага на момент завершения лучевой терапии. Сохраняется отек мягких тканей левого бедра с обширными участками изъявления кожи и зонами некроза
мы приблизительными размерами 289×117×146 мм , с накоплением радиофармпрепарата по периферии зоны поражения SUV=12,6. При этом в центральных отделах дефекта кожного покрова ( в верхней трети левого бедра ) определялась зона аметаболизма , обу словленная некрозом тканей . Также были выявлены единичные метаболически активные парааорталь - ные , тазовые и паховые лимфоузлы слева (SUV=3,4), референсные значения SUV в пуле крови – 1,6, в пече ни - 2,6. ( Рисунок 2).
Учитывая отсутствие ответа на проводимое ле карственное лечение , объём поражения , болевой синдром , было принято решение о проведения пал лиативного курса 3D- конформной лучевой тера пии . Лечение проводили на линейном ускорителе электронов «Elektra Precise» тормозным излучением энергией 6 МэВ с применением тканеэквивалентно го болюса толщиной 1 см ( Рисунок 3 и 4) на область зоны поражения левого бедра , РОД 2 Гр до СОД 44 Гр с применением индивидуальных фиксирующих и формирующих устройств .
Пациентка перенесла лечение удовлетворитель но ( функциональный статус по шкале ECOG – 1. По окончании лучевой терапии отмечались ранние лу чевые реакции в виде лучевого эпителиита 2 сте пени по классификации шкалы оценки острых ос ложнений лучевой терапии RTOG (Radiation Therapy Oncology Group). В течении трех недель после начала облучения достигнуто стойкое разрешение лихорад ки . В дальнейшем отмечена редукция зоны пораже ния в виде уменьшения выраженности отёка мягких тканей , уплощение и уменьшение размеров очагов . Оценка динамики первичного очага в области пора жения мягких тканей левого бедра представлена на рисунках 5-8.
По результатам промежуточного контрольного ПЭТ/КТ исследования с 18F-ФДГ, был выявлен регресс большинства метаболический активных тазовых лимфатических лимфоузлов (до 3б по Deauville) и очагов, а также определялось уменьшение объема поражения кожи левого бедра (Рисунок 9). Полный местный ответ после проведенной лучевой терапии сохранялся в течение 2 лет.
Обсуждение . Бластная плазмоцитоидная ден дритная клеточная неоплазия ( БПДКН ) представ ляет собой редкое и агрессивное гематологическое заболевание . У взрослых больных существует два возрастных пика заболеваемости – 20 и 60 лет [20, 21], поэтому возраст дебюта заболевания был нети пичен для БПДКН .
Пожилой возраст и сниженный общесоматиче ский статус по результатам некоторых исследова ний имеют негативное прогностическое значение при БПДКН . Так в работе Garnache-Ottou F и соавт . проанализированы истории болезни 86 пациентов . Несмотря на , как правило , распространённый про цесс , только 15% больных имели снижение функ ционального статуса , что наряду с пожилым возрас том ассоциировалось с худшим прогнозом [22, 23]. У
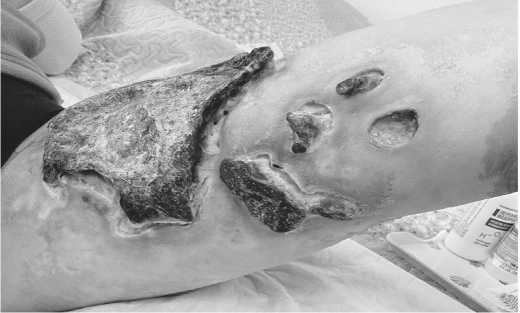
Рисунок 6. Область первичного очага с проявлением ранних лучевых реакций через 3 месяца после проведенной лучевой реакции. Отмечается уменьшение отека мягких тканей левого бедра и резорбция некротических очагов поражения
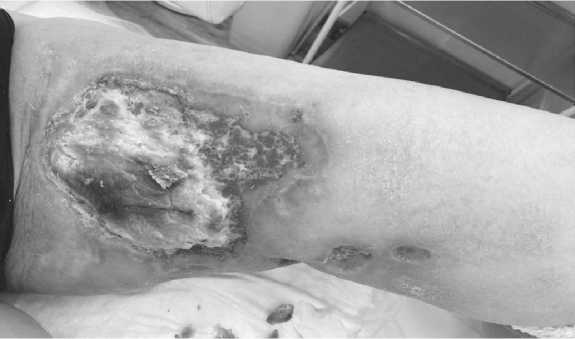
Рисунок 7. Область первичного очага через 6 месяцев после проведенной лучевой терапии. Определяется уменьшение участков поражения, отторжение некротических масс, грануляция тканей в области первичного очага левого бедра, а также регресс отека мягких тканей
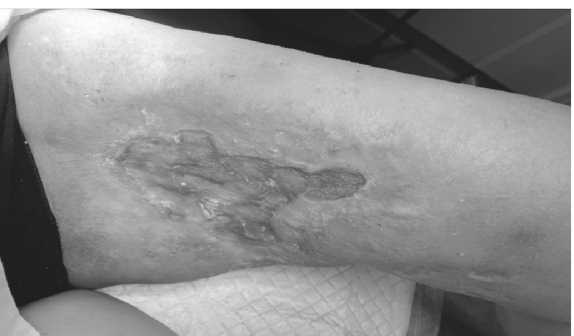
Рисунок 8. Состояние через 12 месяцев после проведения лучевой терапии. Определяется значительное уменьшение зоны поражения кожи левого бедра, за счет заполнения полости раны грануляционной тканью с последующим рубцеванием
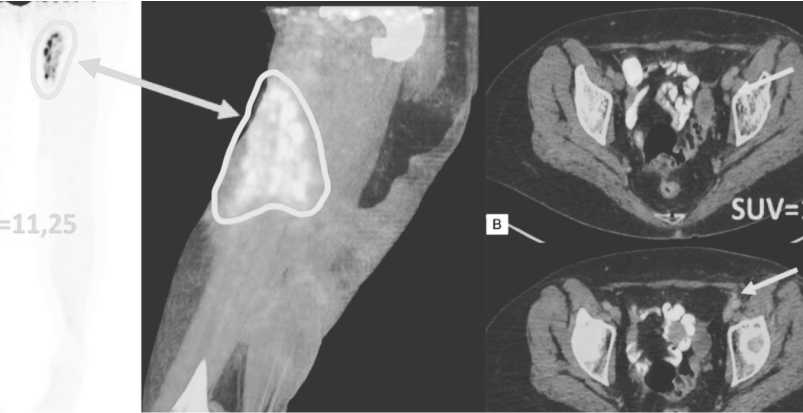
Рисунок 9. ПЭТ/КТ с 18F-ФДГ после проведения конформной лучевой терапии. ПЭТ-изображение, фронтальная проекция (А), совмещенное ПЭТ/КТ–изображение, сагиттальная проекция в режиме многослойного изображения (Б), совмещенные ПЭТ/КТ–изображения, сагиттальные проекции (В, Г). В динамике определяется уменьшение зоны поражения кожи (обведено белым цветом и отмечено стрелкой),, а также снижение уровня накопления 18F-ФДГ в наружных подвздошных лимфоузлах слева до фоновых значений (отмечены белыми стрелками) / При сравнении с предыдущим ПЭТ/КТ исследованием определяется увеличение накопления 18F-ФДГ в зоне первичного очага, обусловленное постлучевыми воспалительными изменениями
представленной пациентки , напротив , интенсивная терапия , в том числе таргетная , оказалась малоэф фективна , что может быть связано с биологически ми особенностями опухоли .
Большинство пациентов с БПДКН получает системную химиотерапию. Для молодых больных без значимой коморбидности используют протоколы для лечения острых лейкозов, в том числе таргет-ную терапию. Так в работе Gilis L и соавт. проанализированы результаты лечения высокодозным метотрексатом и аспарагиназой 6 пациентов с БПДКН. У всех получен ответ на лечение [24]. В связи с гипе- рэкспрессией bcl-2 и эпигенетическим нарушением регуляции онкогенов патогенетически обосновано применение азацитидина и венетоклакса [25, 26]. Крупные исследования пока не завершены, однако клинические наблюдения показывают эффективность комбинаций венетоклакса с гипометилирующими препаратами [27, 28]. Представленная пациентка получала разнообразные протоколы лечения, однако стойкого ответа не достигнуто. С другой стороны, перед началом облучения по результатам ПЭТ обнаружена метаболическая активность преимущественно в тканях бедра, в абдоминальных и тазовых
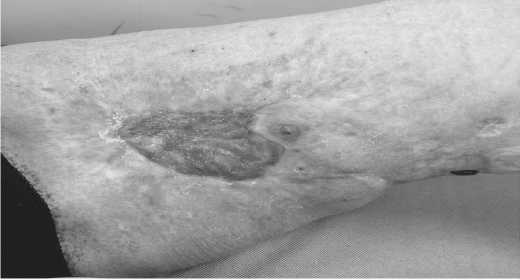
Рисунок 10. Состояние через 24 месяца после проведения лучевой терапии. Определяется положительная динамика в виде уменьшение зоны поражения кожи левого бедра, рана активно гранулирует с формированием рубца, отек и гиперемия отсутствуют.
лимфоузлах она была минимальна , а в селезёнке активности не было . Поэтому , вероятнее всего , ци тостатические препараты не проникали в крупные опухолевые очаги в коже и подкожной клетчатке , но были эффективны в остальных локусах .
Опубликованных литературных данных по применению лучевой терапии при БПДКН недостаточно. Лишь в нескольких сообщениях подробно описываются режимы лучевой терапии. Облучение применялось в том числе в качестве терапии первой линии у пациентов с кожными поражениями БПДКН [29, 30]. Наиболее подробная публикация с описанием дозы и методики лучевой терапии принадлежит Ishibashi и соавт. Проведена лучевая терапия электронным излучением в дозе 30 Гр за 10 фракций на область изолированного поражения. Достигнут хороший ответ, однако вне полей облучения отмечался рост новых очагов [31]. Из немногих публикаций, подробно описывающих протоколы облучения, сообщалось о суммарной дозе 27 Гр (разовая доза 3,0 Гр) с полным непосредственным ответом на проводимое лечение, но возникшим рецидивом через 2 месяца после лучевой терапии. В описании случая Fontaine et al. пациент получил 40 Гр в сочетании с метотрексатом и L-аспарагиназой, что привело к полному ответу, и пациент оставался жив через 30 месяцев после завершения лечения [32]. В трёх публикациях описаны более высокие суммарные дозы – 50,0-51,0 Гр [33, 34]. Во всех этих случаях был достигнут полный ответ. Однако только в одном случае, о котором сообщили Higgins et al., лучевая терапия как единственный метод лечения привела к долгосрочной ремиссии заболевания [29]. У двух других пациентов смерть от системного прогрессирования произошла через 9 и 25 месяцев соответственно после лучевой терапии. В целом, локальная лучевая терапия приводила к частичному или полному местному ответу, но у большинства пациентов наблюдалось прогрессирование в сроки от 2 до 31 месяца. Даже на ранней стадии заболевания, когда обнаруживается только поражение кожи, более высокие дозы при воздействии на одиночные или единичные очаги не всегда приводили к длительной ремиссии [35]. Можно предположить, что сочетание локальной лучевой терапии и химиотерапии может привести к более длительному ответу [36], что возможно и наблюдается у представленной больной. Выраженная положительная динамика в течение 12 месяцев после окончания облучения, удовлетворительное качество жизни подтверждает обоснованность выбранной тактики.
Заключение . Данные литературы и результаты лечения представленной пациентки подтвержда ют агрессивность и в целом низкую эффективность химиолучевой терапии БПДКН . Однако сочетание обоих методов лечения , по аналогии с другими гемо бластозами , может быть более эффективным , если проводить консолидирующее облучение крупных очагов .


