Имплантация in vitro первого отечественного транскатетерного протеза в нативный митральный клапан
Автор: Богачев-прокофьев А.В., Журавлева И.Ю., Шарифулин Равиль Махарамович, Железнев С.И., Демидов Д.П., Кливер Е.Э., Караськов А.М.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Приобретенные пороки сердца
Статья в выпуске: 1 т.22, 2018 года.
Бесплатный доступ
Цель Оценка in vitro опытного образца первого отечественного транскатетерного биопротеза для протезирования митрального клапана. Методы В эксперименте in vitro проведено испытание опытного образца транскатетерного митрального биопротеза на самораскрывающемся нитиноловом каркасе «Солертис» при имплантации в позицию нативного митрального клапана изолированного свиного сердца с использованием трансатриального доступа. Результаты Выявлены адекватная ориентация предсердных и желудочковых элементов биопротеза, надежный круговой охват и прилегание аннулярной части каркаса, обеспечивающие стабильную фиксацию протеза в позиции нативного митрального клапана без обструкции выходного отдела левого желудочка, полноценное функционирование створок, отсутствие парапротезной регургитации. Заключение Опытный образец первого отечественного транскатетерного митрального биопротеза в эксперименте in vitro продемонстрировал эффективность при имплантации в позицию нативного митрального клапана. Результаты исследования позволяют перейти к следующему этапу доклинических испытаний протеза - эксперименту in vivo.
Митральный клапан, биологический протез, транскатетерное протезирование митрального клапана
Короткий адрес: https://sciup.org/142230645
IDR: 142230645 | DOI: 10.21688/1681-3472-2018-1-22-28
In vitro implantation of a new transcatheter prosthesis in mitral valve position
Aim. The study was designed to focus on the evaluation of in vitro implantation of a new transcatheter mitral bioprosthesis. Methods. A prototype of the first domestic self-expanding transcatheter bioprosthesis “Solertis” was tested by implanting it in the position of a native mitral valve of isolated pig heart by using transatrial access. Results. A correct orientation of the atrial and ventricular elements of the bioprosthesis and reliable circular coverage/adaptation of the annular part of the stent, which provide stable fixation of the prosthesis in a mitral position without left ventricular outflow tract obstruction, were determined. The function of the prosthesis during saline load test was adequate and without paraprosthetic regurgitation. Conclusion. The prototype of “Solertis” self-expanding transcatheter bioprosthesis demonstrated its efficiency for the native mitral valve replacement in vitro. The study results allow for proceeding to the next stage of predinical testing-in vivo investigation.
Текст научной статьи Имплантация in vitro первого отечественного транскатетерного протеза в нативный митральный клапан
Пороки митрального клапана являются одной из наиболее распространенных форм патологии сердечно-сосудистой системы. В России в последние годы отмечается прибавление хирургических вмешательств при клапанных пороках сердца [1]. Основной прирост количества операций происходит за счет пороков дегенеративной и ишемической этиологии у пожилых пациентов, что объясняется тенденцией к увеличению продолжительности жизни населения. Традиционными методами лечения пороков митрального клапана являются протезирование и пластика клапана в усло- виях искусственного кровообращения [2]. Старение населения закономерно сопровождается наращением доли пациентов с тяжелым коморбидным состоянием, которой стандартная «открытая» операция протезирования митрального клапана не может быть выполнена в связи с высоким риском периоперационной летальности и жизнеугрожающих осложнений. По данным литературы, доля таких пациентов может достигать 50% [3]. Для аналогичной категории пациентов, страдающих пороками аортального клапана, была предложена и успешно применяется методика транскатетерной имплантации аортального протеза. Накопленный к настоящему времени опыт транскатетерной имплантации
@ (D
Статья доступна по лицензии Creative Commons Attribution 4.0.
ORIGINAL ARTICLES
ОО аортального протеза не только сделал ее методом выбора у пациентов высокого и крайне высокого риска [4], но и позволил применять методику у пациентов с умеренным операционным риском. Несмотря на достижения в миниинвазивной хирургии аортального клапана, развитие технологии эндоваскулярного протезирования митрального клапана значительно отстает. Это обусловлено более сложной функциональной анатомией митрального клапана в сравнении с аортальным. В настоящее время в клиническую практику внедрена методика транскатетерной имплантации клапана в биологический протез в митральной позиции при дисфункции последнего (методика «клапан-в-протез») и в кольцо после пластики митрального клапана (методика «клапан-в-кольцо»). При этом используются биопротезы, изначально предназначенные для транскатетерной имплантации аортального протеза [5]. Разработка устройств для транскатетерного протезирования нативного митрального клапана у пациентов с митральной недостаточностью развивается только в последние несколько лет и является наиболее перспективной в кардиохирургии. Все описанные в литературе протезы для эндоваскулярного протезирования митрального клапана находятся на этапе доклинических либо клинических испытаний.
Цель исследования — оценка in vitro опытного образца первого отечественного транскатетерного митрального биопротеза при имплантации в позицию нативного митрального клапана.
Методы
На базе лаборатории биопротезирования центра новых хирургических технологий ФГБУ «НМИЦ им. ак. Е.Н. Мешалкина» Минздрава России коллектив ученых разработал концепт самораскрывающегося нитинолово-го каркаса транскатетерного митрального биопротеза.
Каркасы опытных образцов были изготовлены компанией ООО «Ангиолайн интервеншионал девайс» (Новосибирск, Россия) с использованием метода лазерной резки (установка A-1 Laser International PRECICUT, Ченнаи, Индия) и электрохимической полировки из трубы внешнего диаметра 7,00 мм с толщиной стенки 0,50 мм. Придание конечного диаметра и закрепление цилиндрической формы осуществлялось термической обработкой в соляной ванне.
С учетом конструкции каркаса были разработаны лекала для выкраивания створок протеза. Раскрой биологического материала (свиной перикард, обработанный диглицидиловым эфиром этиленгликоля) выполняли с помощью лазерного аппаратного комплекса «МЕЛАЗ-Кардио» (Институт лазерной физики СО РАН, Новосибирск). Створчатый аппарат монтировали на каркасе вручную с использованием шовного материала. Облицовку корпуса каркаса и манжеты протеза так же выполняли из ксеноперикарда. Изготовленный протез получил название «Солертис» (рис. 1).
Клапан «Солертис» представляет собой биопротез на основе самораскрывающегося каркаса из сверхэластичного нитинола со створчатым аппаратом и об-

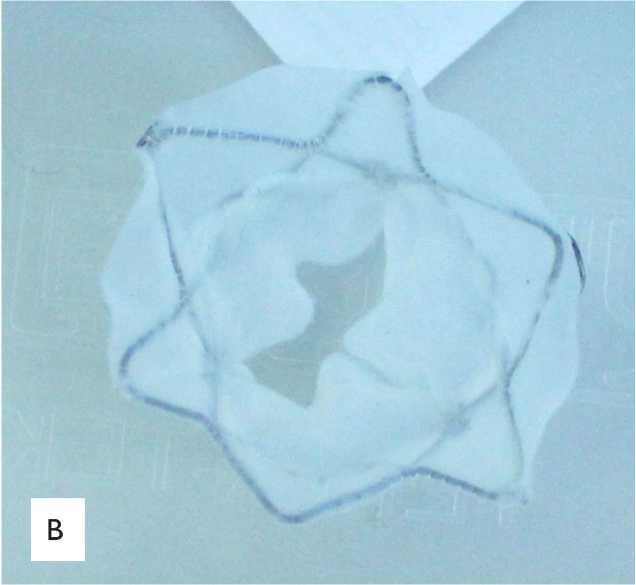
Fig. 1. “Solertis” bioprosthesis: A , side view; B , top view
Рис. 1. Внешний вид биопротеза «Солертис»: A — вид сбоку; B — вид сверху
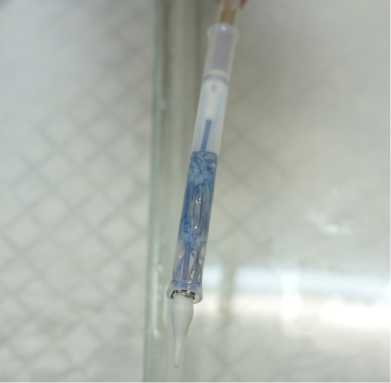
Рис. 2. Биопротез «Солертис», монтированный в систему доставки 18 Fr
Fig. 2. “Solertis” bioprosthesis built in 18 Fr delivery system
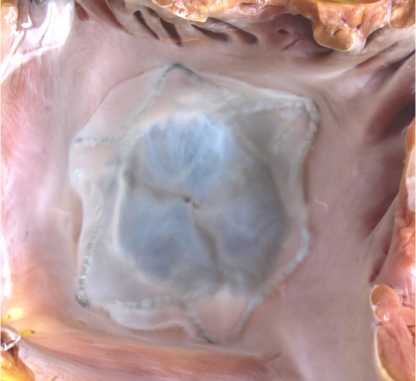
Рис. 3. Биопротез «Солертис» в митральной позиции, вид со стороны левого предсердия. Отсутствие сброса при гидравлической пробе
Fig. 3. “Solertis” bioprosthesis in a mitral valve position as seen from the left atrium. No shunt when tested hydraulically лицовкой из свиного перикарда. Каркас клапана имеет осесимметричную округлую форму аннулярной части, которая за счет радиальных распирающих сил должна закрепляться в позиции фиброзного кольца митрального клапана. Предсердная часть (манжета) в зоне митрально-аортального контакта отклонена от плоскости фиброзного кольца под углом 70 °C. Желудочковая часть протеза представлена двумя крючками, которые выполняют «якорную» функцию, отводя и фиксируя заднюю створку митрального клапана, препятствуя дислокации протеза в левое предсердие во время систолы. Конструкция клапана предусматривает возможность имплантации трансапикальным либо трансатриальным торакоскопическим доступом с использованием доста-вочной системы диаметром 18 Fr.
В эксперименте in vitro проведено испытание прототипа транскатетерного митрального биопротеза «Со-лертис». В качестве модели для имплантации выбрано сердце домашней свиньи. С целью прочной фиксации протеза в зоне имплантации и предотвращения па-рапротезных фистул использовали протез на 5–6 мм больше диаметра фиброзного кольца митрального клапана. В данном эксперименте для протезирования митрального клапана, имеющего фиброзное кольцо 22 мм, был использован биопротез 28 мм.
Перед имплантацией транскатетерный протез охлаждали в физиологическом растворе до 2 °С и колла- бировали до рабочего диаметра с последующим монтажом в прототип устройства доставки (рис. 2).
Через трансатриальный доступ доставочную систему с протезом позиционировали и ориентировали в проекции фиброзного кольца митрального клапана. Далее выполняли постепенное высвобождение транскатетерного клапана из доставочного устройства под визуальным контролем, сначала желудочковой части, затем корпуса протеза и предсердной части до полного расправления всех элементов. Дополнительной фиксации протеза не производили.
Результаты
При использовании прототипа транскатетерного митрального биопротеза достигнута его прочная фиксация в позиции нативного митрального клапана. Контрольная гидравлическая проба, выполненная при окклюзированной аорте, продемонстрировала удовлетворительную замыкательную функцию, отсутствие па-рапротезной регургитации (рис. 3).
С целью макроскопической оценки ориентации и фиксации желудочковых элементов каркаса биопротеза выполнена вентрикулотомия. Выявлено, что крючки каркаса адекватно раскрыты и фиксируют заднюю створку митрального клапана. Передняя створка фиксирована в открытом состоянии корпусом протеза, при этом подклапанный аппарат митрального клапана
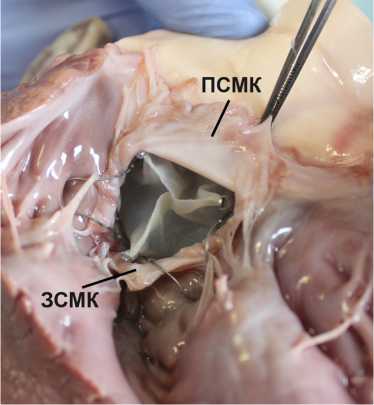
Рис. 4. Биопротез «Солертис» в митральной позиции, вид со стороны левого желудочка
Примечание. ПСМК — передняя створка митрального клапана; ЗСМК — задняя створка митрального клапана
Fig. 4. “Solertis” bioprosthesis in a mitral valve position as seen from the left ventricle
ПСМК, anterior mitral valve leaflet; ЗСМК, posterior mitral valve leaflet и элементы каркаса протеза не создают препятствия в выходном отделе левого желудочка (рис. 4).
Не было выявлено признаков травматического повреждения структур сердца, компрометации коронарного русла.
Обсуждение
Транскатетерное протезирование митрального клапана является перспективным методом лечения митральной недостаточности у пациентов с высоким риском стандартного хирургического лечения с использованием искусственного кровообращения [6]. В связи со сложной анатомо-функциональной организацией митрального клапана, конструкция транскатетерного клапана для протезирования нативного митрального клапана должна соответствовать целому ряду требований. Протез должен надежно фиксироваться в позиции митрального клапана, предотвращая дислокации как в левый желудочек, так и левое предсердие; выдерживать непрерывную циклическую нагрузку со стороны миокарда базальной части левого желудочка (ЛЖ); обеспечивать однонаправленный поток крови с исключением паравальвулярной регургитации; протез не должен создавать обструкцию выходного тракта
ЛЖ, компрометировать проводящую систему сердца и коронарное русло.
К настоящему времени известно о 6 моделях биопротезов для эндоваскулярного протезирования митрального клапана, проходящих клинические испытания: Tiara, Fortis, CardiAQ, Navigate, HighLife и Tendyne [7–17]. Еще несколько моделей находятся на этапе доклинической разработки [7–9, 18, 19]. Каркас большинства описанных биопротезов изготовлен из ни-тинола, что предполагает спонтанное раскрытие при освобождении клапана из системы доставки в зоне имплантации. Подобные биопротезы имеют 3 створки, изготовленные из свиного или бычьего перикарда, обработанного глутаровым альдегидом. Основное различие между протезами заключается в способе фиксации в митральной позиции. В большинстве моделей фиксация со стороны предсердия обеспечивается манжетой, которая «ложится» на предсердную поверхность митрального кольца. Такой манжеты в условиях низкого давления крови в предсердии достаточно, чтобы предотвратить миграцию клапана в ЛЖ. Модели, содержащие в конструкции манжету (Fortis, Tiara, Interpid, Gorman), со стороны ЛЖ имеют специальные фиксаторы (как правило, в виде крючков), обхватывающие створки нативного клапана и удерживающие биопротез от дислокации в левое предсердие. Недостаток подобной конструкции связан с риском обструкции выводного тракта ЛЖ передней створкой митрального клапана, заблокированной фиксатором при некоторых нестандартных анатомических или патологических вариантах митрального клапана либо в результате технических особенностей вмешательства. Другим вариантом фиксации со стороны ЛЖ является конструкция выводной зоны клапана в форме зонтика или парашюта, использованная в моделях CardiaQ, CardioValve, HighLife и DoubleCrown. При этом 3 последние конструкции напоминают катушку, верхняя плоская часть которой представлена левопредсердной манжетой, а нижняя — фиксатором, примыкающим к стенке ЛЖ. Корпус клапана, содержащий створчатый аппарат, является наиболее узкой частью катушки. Кроме того, биопротезы CardioValve, CardiaQ, Endovalve, Interpid и NaviGate содержат довольно острые зубцы во внешней части каркаса, непокрытой облицовкой и соприкасающейся с тканями реципиента, которые выполняют функцию дополнительного «якоря». Однако при использовании данной конструкции существует риск повреждения анатомических структур сердца, в частности коронарного синуса [8]. Поиск оптимальной конструкции транскатетерного митрального протеза, удовлетворяющей всем требованиям, не завершен.
Разработанный в ФГБУ «НМИЦ им. ак. Е.Н. Мешал-кина» Минздрава России протез для транскатетерного протезирования митрального клапана «Солертис» также смонтирован на нитиноловом каркасе. Протез имеет три области фиксации: атриальную — за счет манжеты, конфигурация которой учитывает анатомию левого предсердия и прилежащего корня аорты; аннулярную — за счет радиальных распирающих сил каркаса; желудочковую — за счет зубцов, фиксирующихся за створки митрального клапана. В отличии от описанных в литературе конструкций, створки представленного протеза изготовлены из свиного перикарда, консервированного эпоксидными соединениями.
В настоящем эксперименте in vitro выполнена имплантация прототипа первого отечественного транскатетерного биологического протеза в позицию нативного митрального клапана с использованием трансатриального доступа.
Результаты исследования продемонстрировали, что биопротез «Солертис» легко высвобождается из системы доставки и позиционируется в области нативного митрального клапана, все три зоны его крепления занимают предусмотренное конструкцией положение и выполняют фиксирующую функцию. Ранее мы представили результаты испытания in vitro транскатетерного биологического протеза для имплантации в протез митрального клапана [20]. Данный протез имеет 3 «желудочковых» крючка, каждый из которых фиксируется за створку ранее имплантированного биопротеза. При имплантации данной конструкции in vitro в позицию нативного митрального клапана был выявлен существенный недостаток: в условиях сохраненных створок и подклапанного аппарата митрального клапана крючок, проецирующийся на переднюю створку митрального клапана, вызывал обструкцию выходного тракта ЛЖ. В результате мы отказались от дальнейшего испытания прототипа с тремя крючками желудочковой фиксации в качестве протеза нативного митрального клапана. После модификации конструкции был создан опытный образец протеза с двумя фиксирующими крючками. Данный эксперимент продемонстрировал эффективность нового прототипа транскатетерного биологического протеза при имплантации в позицию нативного митрального клапана. Выявлены адекватная ориентация предсердных и желудочковых элементов каркаса, на- дежный круговой охват и прилегание аннулярной части каркаса, обеспечивающие стабильное крепление всей конструкции в целом без обструкции выходного отдела ЛЖ, полноценное функционирование створок биопротеза, отсутствие парапротезной регургитации.
Результаты данного исследования позволяют перейти к следующему этапу доклинических испытаний транскатетерного митрального протеза — эксперименту in vivo на крупных животных.
Заключение
Опытный образец первого отечественного транскатетерного митрального биопротеза на самораскрываю-щемся нитиноловом каркасе продемонстрировал удовлетворительные характеристики в испытании in vitro на модели изолированного свиного сердца. Для оценки возможности его использования в качестве медицинского изделия необходимы дальнейшие доклинические испытания, в частности стендовые, а также ортотопическая имплантация крупным лабораторным животным.
Финансирование
Работа выполнена при поддержке гранта Российского научного фонда (16-15-10315).
Список литературы Имплантация in vitro первого отечественного транскатетерного протеза в нативный митральный клапан
- Бокерия Л.А., Гудкова Р.Г. Сердечно-сосудистая хирургия -2015. Болезни и врожденные аномалии системы кровообращения. М.: НЦССХ им. А.Н. Бакулева, 2016. 208 с.
- Железнев С.И., Богачев-Прокофьев A.B., Афанасьев A.B., Назаров В.М., Демин И.И., Караськов А.М. Среднеотдаленные результаты реконструктивных операций на митральном клапане при дисплазии соединительной ткани с помощью опорных колец D. ring и C. flex. Патология кровообращения и кардиохирургия. 2015; 19(3): 36-49. http://dx.doi.оrg/ DOI: 10.21688/1681-3472-2015-3-36-49
- Журавлева И.Ю., Богачев-Прокофьев A.B., Демидов Д.П., Караськов А.М. Транскатетерное протезирование митрального клапана: современное состояние проблемы. Кардиология. 2017; 57(8): 51 -59. http://dx.doi.оrg/ DOI: 10.18087/cardio.2017.8.10018
- Baumgartner H., Falk V., Bax J.J., De Bonis M., Hamm C., Holm P.J., lung B., Lancellotti P., Lansac E., Munoz D.R., Rosenhek R.,Sjögren J., Tornos Mas P., Vahanian A., Walther T., Wendler O., Windecker S., Zamorano J.L. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart ]. 2017; 38(36): 2739-2791. PMID: 28886619. http://dx.doi.оrg/ DOI: 10.1093/eurheartj/ehx391
- Nishimura R.A., Vahanian A., Eleid M.F., Mack M.J. Mitral valve disease-current management and future challenges. Lancet. 2016; 387(10025): 1324-34. PMID: 27025438. DOI: 10.1016/S0140-6736(16)00558-4


