In silico и in vivo изучение противовоспалительной активности азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида и 2-замещённых 5,6,7,8-тетрагидробензо[4,5]тиено[2,3-d]пиримидин-4(3h)-она
Автор: Чиряпкин А.С., Кодониди И.П., Абисалова И.Л., Дьякова И.Н.
Журнал: Juvenis scientia @jscientia
Рубрика: Оригинальные исследования
Статья в выпуске: 1 т.11, 2025 года.
Бесплатный доступ
Введение. Поиск эффективных и малотоксичных веществ с противовоспалительным действием является актуальной задачей фармации, так как патологический процесс воспаления развивается при различных заболеваниях. Целью исследования являлся поиск новых соединений с выраженным противовоспалительным действием среди азометиновых и пиримидиновых производных. Объектами исследования являются азометиновые производные 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида (3a-3s) и соответствующие им 2-замещённые 5,6,7,8-тетрагидробензо[4,5]тиено[2,3-d]пиримидин-4(3H)-она (4a-4s).
Прогноз, молекулярный докинг, противовоспалительная активность, цог-2, азометины, тетрагидротиенопиримидины
Короткий адрес: https://sciup.org/14133129
IDR: 14133129 | DOI: 10.32415/jscientia_2025_11_1_16-24
In silico and in vivo study of the anti-inflammatory activity of azomethine derivatives of 2-amino-4,5,6,7-tetrahydro-1-benzothiophene-3-carboxamide and 2-substituted 5,6,7,8-tetrahydrobenzo[4,5]thieno[2,3-d]pyrimidine-4(3h)-one
Introduction. Azomethines and pyrimidines constitute an extensive class of organic compounds that can exhibit various types of biological activity, particularly anti-inflammatory effects. The search for effective and low-toxicity substances with anti-inflammatory properties is an urgent goal in pharmaceutical research, as the pathological process of inflammation is involved in numerous diseases. The aim of this work was to search for new compounds with pronounced anti-inflammatory effects among azomethine and pyrimidine derivatives. The objects of the study were azomethine derivatives of 2-amino-4,5,6,7-tetrahydro-1-benzothiophene-3-carboxamide (3a-3s) and their corresponding 2-substituted 5,6,7,8-tetrahydrobenzo[4,5]thieno[2,3-d]pyrimidine-4(3H)-one (4a-4s).
Текст научной статьи In silico и in vivo изучение противовоспалительной активности азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида и 2-замещённых 5,6,7,8-тетрагидробензо[4,5]тиено[2,3-d]пиримидин-4(3h)-она
Основания Шиффа (азометины) представляют собой обширный класс органических соединений, которые проявляют различные виды биологической активности. Например, у них выявлены противогрибковые, антибактериальные, противомалярийные, антипролиферативные, противовоспалительные, противовирусные и жаропонижающие свойства [1]. В частности, имеются источники литературы, указывающие на наличие противовоспалительных свойств у данного класса веществ. Например, осуществлялось изучение противовоспалительной активности новых оснований Шиффа c тиадиазолом на трёх моделях: ингибирование денатурации белка и гемолиза эритроцитов, стабилизация мембраны эритроцитов и анализ ингибирования протеиназ. В результате установлено, что тестируемые соединения могут замедлять процесс денатурации белка. Все вещества эффективно уменьшали гемолиз, вызванный нагреванием, а также оказывали значительную антипротеазную активность, что может свидетельствовать о наличии у них противовоспалительных свойств [2]. Установлено, что основания Шиффа на основе 2-амино-5-хлорбензойной кислоты могут проявлять противовоспалительную активность, сопоставимую с ацеклофенаком [3]. Результаты фармакологических исследований синтезированных оснований Шиффа из 2-[(1,3-бензо-тиазол-2-ил)сульфанил]-N-[4-(гидразинкарбонил) фенил]ацетамида вывялили у них наличие противовоспалительной активности [4]. Для азометинов 7-гидрокси-4-формилкумарина и 7-метокси-4-фор-милкумарина in vitro установлено противовоспалительное действие на модели денатурации белка посредством ингибирования циклооксигеназы-2 (ЦОГ-2) [5]. Также осуществлялась оценка противовоспалительной активности на модели in vivo, основанной на имитации воспалительного отёка путём инъекции свежего альбумина куриного яйца в лапу мыши, оснований Шиффа с фрагментами коричного альдегида и аминокислотами триптофаном или гистидином. Наибольшую противовоспалительную активность, сопоставимую по силе с аспирином, оказала структура, содержащая остаток триптофана [6]. Основания Шиффа на основе хиназолинона показали высокую противовоспалительную активность путём ингибирования фермента — микросомальной простагландин-синтазы (mPGES-1), снижение активности которой приводит к избирательному снижению биосинтеза простагландина Е2 [7]. По результатам молекулярного докинга были выбраны и затем целенаправленно синтезированы наиболее перспективные соединения с ядром 1,3,4-оксадиазола, которые могут оказать противовоспалительную активность. Дальнейшая in vivo оценка противовоспалительной активности полученных соединений показала, что некоторые из них проявляют активность, но уступают в силе фармакологического эффекта препарату сравнения индометацину [8]. Таким образом, рассматриваемый класс органических соединений является перспективным для разработки на его основе новых лекарственных средств с противовоспалительным действием.
МАТЕРИАЛЫ И МЕТОДЫ
В качестве объектов исследования выступают азометиновые производные 2-амино-4,5,6,7-тетра-гидро-1-бензотиофен-3-карбоксамида (3a-3s) и соответствующие им 2-замещённые 5,6,7,8-тетра-гидробензо[4,5]тиено[2,3-d]пиримидин-4(3H)-она (4a-4s). Азометиновые производные образовывались в ходе взаимодействия 2-амино-4,5,6,7-тетра-гидро-1-бензотиофен-3-карбоксамида ( 1 ) с ароматическими альдегидами ( 2 ) в среде этанола при слабом кипячении исходных соединений [9, 10]. Затем полученный продукт реакции ( 3 ) подвергли гетероциклизации до 2-замещённых 5,6,7,8-тетра-гидробензо[4,5]тиено[2,3-d]пиримидин-4(3H)-она ( 4 ). Реакцию проводили в среде ледяной уксусной кислоты при добавлении каталитических количеств диметилсульфоксида (ДМСО) [11, 12]. Схема синтеза исследуемых соединений представлена на рисунке 1.
Молекулярный докинг проводился в свободно распространяемой программе Autodock 4.0 [13]. Молекулярное моделирование осуществлялось с учётом конформационной подвижности лигандов, торсионные углы которых были установлены и заданы в данной программе. Заряды всех атомов моделируемой системы рассчитаны алгоритмом
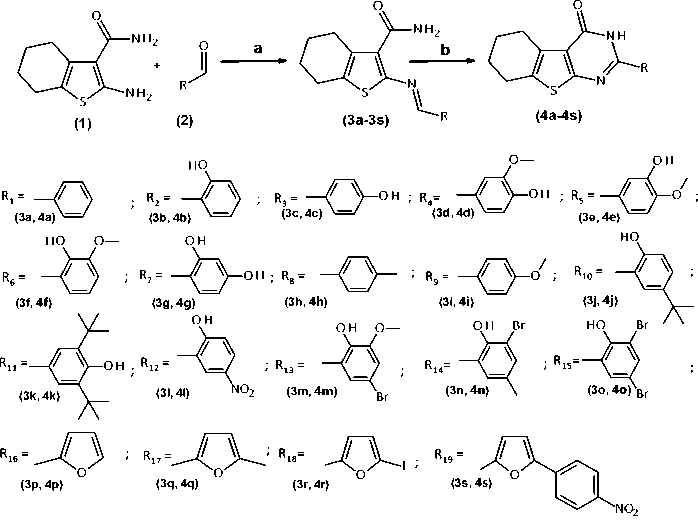
Рисунок 1 / Figure 1. Схема синтеза исследуемых соединений. Реагенты и условия: а — этанол, нагревание; b — ледяная уксусная кислота, ДМСО, нагревание / Synthesis scheme of the studied compounds. Reagents and conditions: a — ethanol, heating; b — glacial acetic acid, DMSO, heating.
Гастейгера (Gasteiger algorithm), и у них присутствуют только полярные атомы водорода. В программе был задан поиск 200 энергетически выгодных конформаций образования молекулярного комплекса изучаемых соединений с белковой мишенью с использованием ламарковской скоринговой функции подсчёта энергии взаимодействия (Lamarckian GA 4.2). Расстояние между точками сетки составляло 0,375 Å. Прогноз противовоспалительной активности проводился с использованием человеческой ЦОГ-2 с идентификационным номером 5IKT [14] из базы данных виртуальных структур RCSB Protein Data Bank (. В этом комплексе находится ингибитор данного фермента — толфе-намовая кислота. Областью вычислительного эксперимента является куб, центр которого находится по следующим координатам: x = 165,42, y = 185,74, z = 192,38. Количество точек в измерениях по осям x, y и z равно 46. Среднеквадратическое отклонение между местоположением толфенамовой кислоты в комплексе 5IKT (рентгеноструктурный анализ) и её расположением в лиганд-рецепторном комплексе по данным молекулярной стыковки составляет 0,86 Å (должно быть не выше 3 Å), что позволяет получить низкое различие между истинной и прогнозируемой конформацией моделируемой молекулы в активном сайте ЦОГ-2 согласно применяемому алгоритму молекулярного докинга [15].
Виртуальные структуры моделируемых соединений были построены в программе HyperChem 8.0.4, а затем геометрически оптимизированы методом молекулярной механики с использованием метода MM+, который позволяет получить приближённую равновесную геометрию молекулы без длительных вычислительных расчётов. Окончательная оптимизация геометрии виртуальных структур рассчитывалась в программе ORCA 4.1 с использованием теории функционала плотности (UB3LYP) и базового набора 6–311G** [16].
Изучение противовоспалительной активности синтезированных соединений проводили на модели острого экссудативного воспаления, вызван- ного субплантарным введением 2% раствора формалина в правую переднюю лапку мышей-самцов линии Balb/C весом 32,0–36,0 г (на момент начала эксперимента) в объёме 0,05 мл [17]. Исследуемые вещества вводили в дозе 50 мг/кг однократно перорально в виде водной суспензии за один час до введения формалина и при курсовом введении один раз в течение пяти суток. В качестве референтного средства использовали диклофенак (таблетки 50 мг), который вводили в дозе 50 мг/кг. Животные содержались в стандартных условиях вивария при естественном освещении: температура окружаю- щего воздуха 22 ± 2 °C, относительная влажность 65 ± 5%. Оценку прироста массы правой передней лапки проводили на пике воспаления через 3 часа после введения формалина путём взвешивания ампутированных передних лап мышей. Сравнение массы проводили между интактной (левой передней лапкой) и контрольной (правой передней лапкой).
Полученные результаты обрабатывали методом вариационной статистики и проверяли на нормальность распределения с помощью критерия Колмогорова-Смирнова. Рассчитывали среднее значение (М) и стандартные ошибки среднего (m).
Таблица 1 / Table 1
Значения минимальной энергии лиганд-ферментного взаимодействия моделируемых соединений с активным сайтом ЦОГ-2 / Values of the minimum energy of ligand-enzyme interaction of the modeled compounds with the active site of COX-2
|
Соединение / Compound |
Энергия, ккал/моль / Energy, kcal/mol |
Соединение / Compound |
Энергия, ккал/моль / Energy, kcal/mol |
|
3a |
-8,72 |
4a |
-8,70 |
|
3b |
-9,36 |
4b |
-9,61 |
|
3c |
-8,39 |
4c |
-8,07 |
|
3d |
-8,60 |
4d |
-8,01 |
|
3e |
-8,70 |
4e |
-7,94 |
|
3f |
-9,27 |
4f |
-9,22 |
|
3g |
-8,87 |
4g |
-8,36 |
|
3h |
-8,80 |
4h |
-8,38 |
|
3i |
-8,43 |
4i |
-8,05 |
|
3j |
-9,07 |
4j |
-9,01 |
|
3k |
-4,17 |
4k |
-4,11 |
|
3l |
-9,12 |
4l |
-9,30 |
|
3m |
-9,54 |
4m |
-9,79 |
|
3n |
-9,37 |
4n |
-9,35 |
|
3o |
-9,46 |
4o |
-9,56 |
|
3p |
-8,53 |
4p |
-8,03 |
|
3q |
-8,61 |
4q |
-8,52 |
|
3r |
-8,36 |
4r |
-8,22 |
|
3s |
-7,98 |
4s |
-7,96 |
|
Толфенамовая кислота / Tolfenamic acid |
-8,52 |
Диклофенак / Diclofenac |
-8,21 |
|
Целекоксиб / Celecoxib |
-8,35 |
Рофекоксиб / Rofecoxib |
-8,30 |
Для нормального распределения в качестве параметрического критерия использовали критерий Стьюдента, а в случаях отличного от нормального распределения в качестве непараметрического критерия — U-критерий Манна — Уитни.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Согласно данным молекулярного докинга наиболее перспективными соединениями среди азо-метиновых производных 2-амино-4,5,6,7-тетрагид-ро-1-бензотиофен-3-карбоксамида с точки зрения ингибирования ЦОГ-2 могут являться следующие структуры: 3b, 3l, 3m, 3n, 3o и получаемые из них пиримидиновые производные — 4b, 4l, 4m, 4n, 4o, энергия образования молекулярного комплекса которых превосходит виртуальные референты. При этом особый интерес представляют вещества 3m, 3n, 3o, 4m, 4n и 4o, так как в своей структуре содержат атом галогена, который, например, присутствует в структуре таких нестероидных противовоспалительных средств, как диклофенак, индометацин, эторикоксиб и целекоксиб.
Для дальнейшего изучения in vivo противовоспалительной активности было выбрано 10 наиболее перспективных соединений, исходя из данных предшествующего вычислительного эксперимента: 3b, 3l, 3m, 3n, 3o, 4b, 4l, 4m, 4n, 4o (таблица 1).
Исследование проводили на модели острого экссудативного воспаления, вызванного субплан- тарным введением 2% раствора формалина в правую переднюю лапку в объёме 0,05 мл. Первая серия опытов была скрининговой и выполнялась на ограниченном количестве животных (n=3). Результаты представлены в таблице 2.
Таблица 2 / Table 2 Влияние исследуемых соединений в дозе 50 мг/ кг на экссудативную фазу острого воспаления (n=3) / The effect of the studied compounds at a dose of 50 mg/kg on the exudative phase of acute inflammation (n=3)
|
Соединение / Compound |
Прирост массы лапы в % / Paw weight gain in % |
|
3b |
35,93 ± 3,05 |
|
3l |
47,84 ± 3,59 |
|
3m |
39,87 ± 6,65 |
|
3n |
33,67 ± 2,63 |
|
3o |
42,69 ± 2,08 |
|
4b |
43,52 ± 1,87 |
|
4l |
49,32 ± 4,58 |
|
4m |
53,86 ± 5,51 |
|
4n |
43,60 ± 6,32 |
|
4o |
58,39 ± 7,01 |
|
Контроль / Control |
67,06 ± 3,17 |
Таблица 3 / Table 3
Влияние исследуемых соединений и препарата сравнения на экссудативную фазу острого воспаления в дозе 50 мг/кг (n=8) при однократном профилактическом применении / The effect of the studied compounds and the reference drug on the exudative phase of acute inflammation at a dose of 50 mg/kg
(n=8) with a single prophylactic application
|
Соединение / Compound |
Показатели / Indicators |
Значение Р, отличия от контрольной группы в % / P-value, % of difference with the control group |
|
|
Прирост массы лапы в % / Paw weight gain in % М ± m |
Прирост массы лапы, г / Paw weight gain, g М ± m |
||
|
Контроль / Control |
53,84 ± 8,56 |
0,090 ± 0,020 |
– |
|
Диклофенак / Diclofenac |
32,14 ± 5,47 |
0,054 ± 0,010 |
0,05 (– 40%) |
|
3b |
37,49 ± 5,42 |
0,062 ± 0,008 |
0,21 (– 31%) |
|
3n |
32,57 ± 7,46 |
0,055 ± 0,013 |
0,16 (– 39%) |
Таблица 4 / Table 4
Изучение противовоспалительной активности соединений-лидеров при курсовом терапевтическом применении в дозе 50 мг/кг на модели формалинового отёка (n=8) / Study of the anti-inflammatory activity of leading compounds in the course of therapeutic use at a dose of 50 mg/kg on a model of formalin edema (n=8)
|
Соединение / Compound |
Прирост массы лапы, г / Paw weight gain, g М ± m |
Значение Р, отличия от контрольной группы в % / P-value, % of difference with the control group |
|
Контроль / Control |
0,090 ± 0,006 |
— |
|
Диклофенак / Diclofenac |
0,051 ± 0,006* |
0,0005 (- 43%) |
|
3b |
0,074 ± 0,006 |
0,08 (-18%) |
|
3n |
0,054 ± 0,008* |
0,003 (-40%) |
*статистически значимые различия по сравнению с контрольной группой / *statistical significance in comparison with the control group
По результатам скрининговых исследований были выбраны соединения 3b и 3n. Для этих соединений проводились исследования на 4 группах животных, состоящих из 8 особей в каждой. В первой серии исследуемые вещества вводили разово за час до инъекции формалина (профилактическое введение). Результаты представлены в таблице 3. Во второй серии исследуемые вещества вводили ежедневно в течение 5 суток (терапевтическое введение). Результаты представлены в таблице 4. В качестве референтного средства использовали диклофенак.
Изучение соединений на модели формалин-индуцированного острого экссудативного воспаления показало, что соединение 3b при профилактическом введении снижает развитие отёка на 31%, а соединение 3n — на 39% по сравнению с контрольной группой. Полученный эффект сопоставим с действием диклофенака, снижающего прирост повреждённой лапки на 40%.
При курсовом применении исследуемых субстанций на пятые сутки эксперимента прирост массы лапки в группе животных, получавших соединение 3b, снизился на 18%, в группе, получавшей
3n, — на 40%, в группе, получавшей диклофенак, — на 43% относительно контроля.
ЗАКЛЮЧЕНИЕ
Соединения под лабораторным шифром 3b и 3n демонстрируют наличие противовоспалительной активности на модели формалинового отёка. Соединение 3n является наиболее перспективным для дальнейшего исследования, так как его действие сопоставимо с препаратом сравнения диклофенаком.
Финансирование: Авторы заявляют об отсутствии финансирования.

![In silico и in vivo изучение противовоспалительной активности азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида и 2-замещённых 5,6,7,8-тетрагидробензо[4,5]тиено[2,3-d]пиримидин-4(3h)-она In silico и in vivo изучение противовоспалительной активности азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида и 2-замещённых 5,6,7,8-тетрагидробензо[4,5]тиено[2,3-d]пиримидин-4(3h)-она](/file/cover/14133129/in-silico-i-in-vivo-izuchenie-protivovospalitelnoj-aktivnosti-azometinovyh.png)
