Использование полимерных имплантов в реконструктивной хирургии околоносовых пазух (экспериментальное исследование)
Автор: Покровская Елена Михайловна
Рубрика: Хирургия, анестезиология и реанимация, гематология
Статья в выпуске: 5-4 т.16, 2014 года.
Бесплатный доступ
Экспериментально-морфологические исследования на 24 кроликах свидетельствуют о выраженных остеоиндуктивных свойствах полимерного импланта «Рекост». Результаты проведенных гистологических исследований подтверждают целесообразность и перспективность применения полимерных материалов.
Полимерный имплантат, микрогайморотомия, пластика передних стенок
Короткий адрес: https://sciup.org/148101959
IDR: 148101959 | УДК: 616.216-089
Using the polymeric implants in reconstructive surgery of paranasal sinuses (experimental research)
Experimental and morphological researches on 24 rabbits testify to the expressed osteoinductive properties of polymeric implant "Recost". Results of the conducted histological researches confirm expediency and prospects of using the polymeric materials.
Текст научной статьи Использование полимерных имплантов в реконструктивной хирургии околоносовых пазух (экспериментальное исследование)
Проблема возмещения посттравматических и послеоперационных костных дефектов ЛОР-органов остается актуальной на протяжении многих лет. В течение нескольких десятилетий оториноларингологи ищут способы закрытия дефектов стенок пазух. Наиболее рациональным решением проблемы является пластическое восстановление стенок околоносовых пазух различными материалами. Сегодня на мировом рынке существует огромное количество каркасных материалов, используются как синтетические, так и биологические материалы. К синтетическим имплантируемым материалам относятся эксплантаты (металлы, полимеры, пористоуглеродные соединения и др.), к биологическим – аутотрансплантаты (костные лоскуты, измельченная и консервированная аутокость); аллотрансплантаты (эмбриональная закладка или кость, свежая аллогенная кость, измельченная аллогенная кость, консервированная кость и деминерализованный костный матрикс). Наиболее интересными работами последних лет являются работы с применением деминерализованных костных трансплантатов [1-3] и титановых имплантов в ринологии [4-8].
Используемые в практике импланты не всегда отвечают необходимым требованиям: оптимальной биосовместимости, инертности, прочности. В нашей работе мы использовали костный цемент «Рекост» – полимерный материал для закрытия костных дефектов. Основа материала «Рекост» – форполимер, полиол в качестве отвердителя, а также ортофосфат кальция. Готовый «Рекост» имеет пористую микроструктуру, которая способствует остеокондукции и остеоиндукции.
Цель работы: изучение биосовместимости костного цемента «Рекост» для пластики передней стенки верхнечелюстной пазухи в эксперименте.
Материал и методы. Апробацию материала проводили в экспериментах по возмещению дефектов костей у лабораторных животных. Всего прооперировано 24 кролика, изучено 48 микро
препаратов. Моделирована пластика передней стенки верхнечелюстной пазухи. Каждому кролику произведена двухсторонняя микрогайморотомия. Из «Рекоста» формировали фрагмент, адекватный костному дефекту, который устанавливался под-надкостнично. Животных выводили из эксперимента по 6 кроликов в сроки: через 7 и 14 дней, 6 недель и 12 недель. Фрагмент передней стенки верхнечелюстной пазухи иссекали вместе с имплантом с помощью циркулярного стоматологического бора. Изготовление гистологических препаратов проводили по методике декальцинации, разработанной для костных тканей [9-10]. На приведенных рисунках нет включений импланта, так как он удалялся во время процесса декальцинации. Гистологические срезы использовались для иммуногистохимического исследования (табл. 1).
Результаты и обсуждение.
-
7 сутки. Во всех наблюдениях дефект кости в краевых участках был выполнен грануляционной тканью с большим количеством кровеносных сосудов (прежде всего капилляров). Иммуногистохимический анализ (рис. 1) при этом показывал высокую экспрессию моноклональных антител (МКАТ) к CD 31-антигену в эндотелии крупных сосудов, капилляров, а также в отдельных клетках. Базальные мембраны микроциркуляторного русла четко контурировались МКАТ против коллагена-IV. Между сосудистыми петлями располагались мезенхимальные элементы, в основном, фибробластического типа, экспрессирующие виментин. Редко сохранялись остаточные явления реактивных процессов, прежде всего экссудативного воспаления, вызванных повреждением. В подавляющем числе наблюдений травматический отек либо отсутствовал, либо был выражен незначительно. Иногда по краю перфоративного отверстия имели место некротические изменения с наличием запустевших полостей остеоцитов. Здесь обнаруживалась инфильтрация полиморфно-ядерными лейкоцитами и, в меньшей степени, макрофагами. Иммуногистохимически это выражалось в высокой экспрессии МКАТ к миелопероксидазе и антигену CD 68.
Таблица 1. Характеристика моноклональных антител
|
Антитело |
Клон |
Специфичность |
Рабочее разведение |
Фирма-производитель |
|
CD 68 |
PGM1 |
макрофаги |
1:200 |
BioGenex |
|
миело-перокси-даза (МРО) |
поликлональные |
Нейтрофильные лейкоциты |
1:800 |
Dako |
|
CD 31 |
9611 |
эндотелий сосудов |
1:20 |
BioGenex |
|
виментин |
V9 |
фибробласты, соединительная ткань |
1:300 |
Lab Vision |
|
коллаген IV |
PHM-12 + CIV22 |
базальные мембраны |
1:150 |
Lab Vision |

Рис. 1. Экспрессия МКАТ к CD 31-антигену в эндотелии крупных сосудов, капилляров, а также в отдельных клетках грануляционной ткани. 7 сутки эксперимента. LSAB-метод с докраской гематоксилином. х 400
-
14 сутки. Во всех наблюдениях происходило развитие соединительнотканных структур с разрастанием коллагеновых волокон и началом остеогенеза (рис. 2). На фоне гомогенизации коллагена образовывались костные балки, пространство между которыми заполняла рыхлая волокнистая соединительная ткань. Между отдельными костными балками появлялись поперечные перемычки. Обнаруживались пролиферирующие остеобласты. Иммуногистохимически в зоне трансформации соединительной ткани в костную определялась выраженная экспрессия виментина. Некротические массы, в том числе и в костной ткани, практически полностью рассасывались с накоплением в данных участках остеокластов. Проявления воспалительной реакции в отдельных наблюдениях сохранялись, но были весьма незначительными на фоне репаративных процессов. При этом нейтрофильная инфильтрация замещалась макрофагальной, на что указывала низкая экспрессия МКАТ к миелопероксидазе и высокая к CD 68-антигену. В гаверсовы каналы по краям дефекта проникали мезенхимальные клеточные элементы и врастали кровеносные сосуды, что подтверждалось иммуногистохимической реакцией МКАТ против виментина и CD 31-антигена. Ни в одном из случаев не наблюдалось костеобразования через формирование хрящевой ткани.
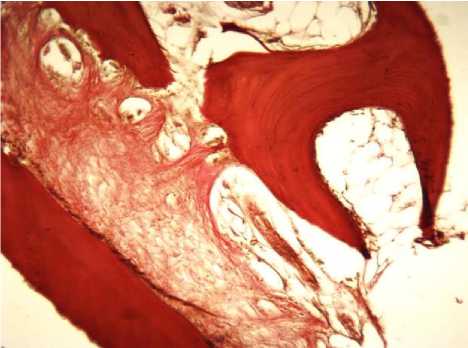
Рис. 2. Зона трансформации соединительной ткани в костную ткань балочного строения. 14 сутки эксперимента. Окраска по ван Гизону. х 200
-
6 недель. В большинстве наблюдений на этом сроке эксперимента костный дефект был полностью или частично закрыт сформированной грубоволокнистой костью (рис. 3). По краям бывшего перфоративного отверстия костные трабекулы частично резорбировались и наблюдались начальные признаки перестройки данной ткани в пластинчатую. Параллельно с этим, по сравнению с предыдущим сроком, уменьшалась экспрессия вименти-на. Признаков воспалительной реакции при этом не наблюдалось. Экспрессия МКАТ к миелопероксидазе (маркера нейтрофильных лейкоцитов) имела место в отдельных клеточных элементах. Несколько чаще обнаруживались CD 68(+) макрофаги, в основном по краям бывшего перфоративного отверстия.
-
12 недель. Во всех наблюдениях перфоративное отверстие было замещено грубоволокнистой костью, которая на многих участках трансформировалась в пластинчатую с развитой системой гаверсовых каналов. Практически во всех из них находились кровеносные сосуды, что выявлялось иммуногистохимически реакцией МКАТ против CD 31-антигена. Нейтрофильные лейкоциты и макрофаги при этом не обнаруживались – окраска на миелопероксидазу и CD 68-антиген была негативной. Экспрессия МКАТ к виментину, по сравнению с предыдущими сроками эксперимента, была выражена значительно меньше и наблюдалась только в отдельных клеточных и структурных элементах вокруг балок грубоволокнистой кости.
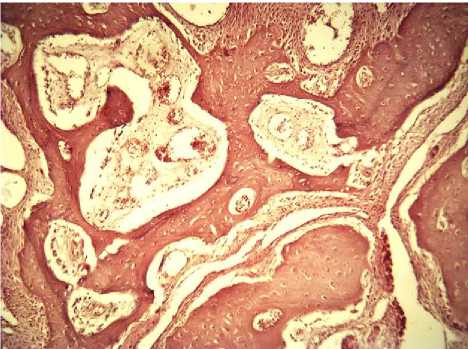
Рис. 3. Сформированная грубоволокнистая кость балочного строения на месте перфоративного отверстия. 6 недель эксперимента. Окраска гематоксилином и эозином. х 200.
Выводы: применение костного цемента «Рекост» способствует восстановлению костной ткани путем постепенного замещения «Рекоста» грануляционной, а затем соединительной тканью уже на ранних сроках (7-14 дней). При этом практически отсутствует воспалительная реакция с наличием обширных лейкоцитарно-некротических масс и травматического отека. Процесс репаративной регенерации ускоряется, о чем свидетельствует трансформация соединительной ткани непосредственно в костную (через 6 недель) без формирования хряща, что зачастую имеет место при заживлении повреждений кости. К 12 неделям во всех наблюдениях имеется сформированная грубоволокнистая костная ткань с участками пластинчатой кости, полностью восполняющая экспериментальный дефект. Таким образом, костный цемент «Рекост» является биоэнертным и биодеградируемым восстановительным материалом, пригодным для реконструктивно-пластических операций на околоносовых пазухах.
Список литературы Использование полимерных имплантов в реконструктивной хирургии околоносовых пазух (экспериментальное исследование)
- Волков, А.Г. Особенности выявления деминерализованных костных трансплантатов при пластике стенок околоносовых пазух / А.Г. Волков, А.Р. Боджоков // Материалы 7 Всероссийской научно-практической конференции оториноларингологов // Вестник оторинолар. 2008. №5 (приложение). С. 143-144.
- Боджоков, А.Р. Антибактериальные возможности трансплантата после пластики стенок лобных пазух // Материалы 7 Всероссийской научно-практической конференции оториноларингологов // Вестник оторинолар. 2008. №5 (приложение). С. 139-140.
- Боджоков, А.Р. Пластика костных дефектов стенок околоносовых пазух деминерализованными костными трансплантатами: Автореф. дис. … д-ра мед.наук. -Ростов-на-Дону. 2011. 41 с.
- Староха, А.В. Новые технологии хирургического лечения риносинуситов с применением сверхэластичных имплантатов с памятью формы: Автореф.дис. … д-ра мед. наук. -СПб., 1998. 40 с.
- Михайленко, Н.Ю. Титановые имплантаты с покрытием биоситаллом в реконструктивно-пластической хирургии околоносовых пазух и носовой перегородки/Н.Ю. Михайленко, Е.Е. Строганова, И.Г. Батрак и др.//Рос. оторинолар. 2005. №3(16). С. 53-57.
- Крюков, А.И. Оптимизация реконструктивных операций на лобной пазухе/А.И. Крюков, А.А. Агафонов// Вестник оторинолар. 2010. № 3. С. 71-72.
- Абдулкеримов, Х.Т. Применение металлоконструкций в восстановлении дефектов кранио-фасциально-орбитальной зоны/Х.Т. Абдулкеримов, Р.С. Давыдов//Рос. ринол. 2010. №3. С. 35.
- Абдулкеримов, Х.Т. Металлоконструкции из титана в реконструктивной хирургии костных дефектов основания черепа и лицевой зоны/Х.Т. Абдулкеримов, Р.С. Давыдов, К.И. Карташова и др.//Материалы 2 Петербургского форума оториноларингологов России. -СПб., 2013. С. 229.
- Коржевский, Д.Э. Краткое изложение основ гистологической техники для врачей и лаборантов-гистологов. -СПб: Кроф, 2005. 48 с.
- Пахт, А.В. Особенности обработки костной ткани/А.В. Пахт, Н.М. Манизер//Библиотека патологоанатома (научно-практический журнал). -СПб., 2008. С. 6-11.


