Исследование биологически активных веществ сухого экстракта из листьев облепихи Hippophae rhamnoniedes
Автор: Сынгеева Э.В., Ламажапова Г.П., Хантургаев А.Г., Котова Т.И.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Пищевые технологии
Статья в выпуске: 6, 2025 года.
Бесплатный доступ
Цель исследования – определение содержания биологически активных веществ в сухом экстракте, полученном из листьев облепихи крушиновидной Hippophae rhamnoides и исследование противовоспалительного эффекта полученного экстракта. Задачи: произвести анализ биологической и токсикологический чистоты листьев облепихи крушиновидной; установить концентрацию водорастворимых витаминов, дубильных веществ, флавоноидов и общий уровень антиоксидантов в исходном растительном материале, сухом экстракте и препарате «Гипорамин»; провести микробиологический анализ чистоты полученного сухого экстракта из листьев облепихи крушиновидной; изучить противовоспалительное действие экстракта, полученного из указанного растительного материала, при моделировании отека, вызванного формалином, у экспериментальных животных. Результаты показали, что листья облепихи соответствуют критериям безопасности: содержание тяжелых металлов не превышает допустимых норм, а патогенные микроорганизмы отсутствуют. В исходном сырье содержание дубильных веществ составило 14,46 %, флавоноидов – 3,16 %, суммарное содержание антиоксидантов – 0,352 мг/г, витамина С – 0,08 мг/100 г. В полученном сухом экстракте концентрация дубильных веществ достигла 45,9 %, флавоноидов – 9,61 %, суммарного содержания антиоксидантов – 1,453 мг/г, витамина С – 0,34 мг/100 г. Микробиологический анализ подтвердил соответствие экстракта нормативным требованиям. Исследование противовоспалительной активности на модели формалинового отека у крыс продемонстрировало выраженный противовоспалительный эффект экстракта. Применение экстракта листьев облепихи может быть успешным не только в медицине, но и в пищевой индустрии, например для обогащения функциональных пищевых продуктов. Это также указывает на значимость дополнительных исследований для усовершенствования методов обработки сырья и расширения областей его использования.
Облепиха крушиновидная, биологически активные вещества, сухой экстракт, фенольные соединения, дубильные вещества, флавоноиды, витамины
Короткий адрес: https://sciup.org/140310254
IDR: 140310254 | УДК: 663.051.2;66.974.434;636.085.16 | DOI: 10.36718/1819-4036-2025-6-319-328
Investigation of biologically active substances of dry extract from sea buckthorn leaves Hippophae rhamnoniedes
The aim of the study is to determine the content of biologically active substances in the dry extract ob-tained from the leaves of sea buckthorn Hippophae rhamnoides and to study the anti-inflammatory effect of the obtained extract. Objectives: to analyze the biological and toxicological purity of sea buckthorn leaves; to determine the concentration of water-soluble vitamins, tannins, flavonoids and the total level of antioxidants in the original plant material, dry extract and the drug Giporamin; to conduct a microbiological analysis of the purity of the obtained dry extract from the leaves of sea buckthorn; to study the anti-inflammatory effect of the extract obtained from the specified plant material when modeling formalin-induced edema in experimental animals. The results showed that sea buckthorn leaves meet the safety criteria: the content of heavy metals does not exceed the permissible limits, and there are no pathogenic microorganisms. The initial raw material contained 14.46 % tannins, 3.16 % flavonoids, 0.352 mg/g total antioxidants, and 0.08 mg/100 g vitamin C. The obtained dry extract contained 45.9 % tannins, 9.61 % flavonoids, 1.453 mg/g total antioxidants, and 0.34 mg/100 g vitamin C. Microbiological analysis confirmed that the extract complied with regulatory requirements. A study of anti-inflammatory activity using a forma-lin edema model in rats demonstrated a pronounced anti-inflammatory effect of the extract. The use of sea buckthorn leaf extract can be successful not only in medicine, but also in the food industry, for example, for enriching functional foods. This also indicates the importance of additional research to improve raw mate-rial processing methods and expand the areas of its use.
Текст научной статьи Исследование биологически активных веществ сухого экстракта из листьев облепихи Hippophae rhamnoniedes
Acknowledgments : the work was carried out within the framework of the grant "Young Scientists of VSGUTU-2024" and within the framework of the program "Priority 2036 No. 075-15-2025-049".
Введение. В результате многочисленных исследований в области биотехнологии биологически активных веществ (БАВ) на данный момент имеется достаточный объем данных того, что БАВ полифенольной природы, содержащиеся в растительных объектах, обладают им-мунорегуляторными, антиангиогенными, анти-воспалительными, антидиабетическими, антиканцерогенными, антиоксидантыми и другими фармакологическими свойствами [1]. Согласно нормативным требованиям к энергетической и пищевой ценности для различных групп населения России, ежедневно взрослому человеку необходимо до 30 мг флавонов, 30 мг флавонолов, до 200 мг флаван-3-олов, а также 200 мг конденсированных и 200 мг гидролизуемых танинов [2].
В обзоре В.А. Тутельяна с соавт. (2013) представлена достаточно обширная информация о содержании флавонов и флавонолов в различных продуктах (овощах, фруктах, ягодах, бобовых, чаях, вине), также приведены данные об их потреблении в различных странах (Нидерланды, Хорватия, Сербия, Греция, Италия, Германия, Дания, США, Китай, Япония, Австралия, Великобритания). Анализ литературы показал, что пока отсутствуют данные о количественном потреблении флавоноидов населением РФ, и на отечественном рынке нет упоминаний о функциональных продуктах, которые могли бы полностью обеспечить суточную потребность организма в этих полифенольных соединениях. При этом существует большое количество исследований об их содержании в различных растительных объектах, в частности накоплено достаточно информации о химическом составе в таком уникальном растении, как облепиха крушиновидная [3].
Плоды и шрот ягод облепихи уже давно находят широкое применение в различных отраслях промышленности. В отличие от них, листья облепихи изучены гораздо меньше, хотя в последние годы активно проводятся исследования, направленные на изучение их химического состава и фармакологических свойств. Установлено, что листья содержат практически тот же набор БАВ, что и плоды. Танины, выделенные из видов рода Hippophae , преимущественно представлены такими соединениями, как гидролизуемые танины: страститнин (strictinin), 1,2,6-тригаллоилглюкоза (1,2,6-trigalloylglucose), изостриктинин (isostricti-nin), касталагин (castalagin), вескалагин (vescala-gin) и другие флавоноиды [4].
Используя метаболомику нецелевого ядерно-го резонанса (ЯМР), ученые кафедры биохимии университета Хельсинки исследовали листья двух сортов облепихи, выращенных на юге и севере Финляндии в течение двух сезонов роста. R. Pariyani et al. обнаружили, что наибольшая вариация метаболического профиля связана со стадией роста: листья в первые 7 недель сбора урожая содержат много полифенолов, в то время как углеводы и сахара становятся более распространенными в последующие недели роста. Место роста также оказывает значительное влияние на метаболический профиль, причем сравнение севера и юга показало различия в жирных кислотах и сахарах. Также была обнаружена потенциальная связь метаболома с естественными абиотическими стрессорами, обратная корреляция между содержанием углеводов/сахаров и жирных кислот с более длинными цепями углерода и была установлена связь с температурными переменными. Хемометрические модели с высокой чувствительностью и специфичностью позволили классифицировать и предсказать образцы на основе стадии роста, местоположения и сорта. Метаболомика нецелевого ЯМР позволила выявить метаболический профиль и его вариации, связанные с различными биотическими и абиотическими факторами [5].
Новосибирские исследователи изучили химический состав листьев сибирской облепихи
(Hippophae rhamnoides L. ssp. mongolica Rousi), которая растет в Западной Сибири. Г.М. Скури-дин и его команда обнаружили, что листья этого растения являются ценным источником необходимых микроэлементов, таких как хром (Cr) и марганец (Mn), которые находятся в биодоступ-ной форме. Также ученые выяснили, что ягоды облепихи не накапливают вредные вещества, например свинец (Pb) и мышьяк (As), что подтверждает их безопасность для употребления [6].
В результате исследований, проведенных N. Оllingen et al. из Австрийского центра компетенций по качеству кормов и продуктов питания безопасности и инновациям, было изучено воздействие облепихового масла, экстрактов плодов, листьев и жмыха на метаболизм глюкозы после приема пищи. Было установлено, что облепиха не имела значительного воздействия на всасывание глюкозы в кишечнике in vitro и не изменяла секрецию инсулина, однако она стимулировала перемещение GLUT4 в плазматическую мембрану, что повышает клиренс глюкозы в крови. Во всех исследованных образцах облепихи был обнаружен изорамнетин, который обладал биологической активностью, способствуя локализации GLUT4 на поверхности клеток. Продукты из облепихи снижали уровень глюкозы в крови примерно на 10 % у куриных эмбрионов. Более того, эти продукты полностью устраняли гипергликемию у нематоды Caenorhabditis elegans , в то время как у Drosophila mela их эффективность была ниже [7]. В Научно-исследовательском институте лекарственных и ароматических растений (ГНУ ВИЛАР Россельхозака-демии) разработан препарат «Гипорамин», созданный на основе листьев облепихи крушиновидной [8].
В Селенгинском районе Республики Бурятии (РБ) два года назад начал свою деятельность завод, занимающийся промышленной переработкой облепихового сырья. Предприятие выпускает облепиховое масло высокого качества, при этом производство товаров из других, не менее ценных частей растения, довольно ограниченно [9].
Цель исследования – определение содержания биологически активных веществ в сухом экстракте, полученном из листьев облепихи крушиновидной Hippophae rhamnoides , и исследование противовоспалительного эффекта полученного экстракта.
Задачи: произвести анализ биологической и токсикологической чистоты в листьях облепихи крушиновидной; установить концентрацию водорастворимых витаминов (ВВ), дубильных веществ (ДВ), флавоноидов (ФЛ) и общий уровень антиоксидантов в исходном растительном материале, сухом экстракте (СЭ) из листьев облепихи и препарате «Гипорамин»; провести микробиологический анализ чистоты полученного СЭ; изучить противовоспалительное действие экстракта, полученного из исследуемого растительного сырья, на основе отека, вызванного формалином, у экспериментальных животных.
Объекты и методы. Листья облепихи были собраны в период массового созревания и плодоношения ягод (2021–2023 гг.) после сбора основного урожая и высушены при комнатной температуре в тени до остаточной влажности (4,75 ± 0,25) %. Заготовка растительного материала для этого исследования проводилась в селе Ацула (51°08′33″ с. ш., 106°38′33″ в. д.) Селенгинского района Республики Бурятия [1].
Сотрудники инновационного центра под руководством А.Г. Хантургаева (2024) разработали методику получения СЭ с применением вакуумно-импульсных технологий [9]. Для сравнительного анализа применялся препарат «Гипорамин» (производитель – Российский фарм-центр «Вилар»). Он представляет собой очищенный СЭ из листьев облепихи крушиновидной ( Hippophae rhamnoides L.) [8].
Определение содержания токсичных элементов в листьях проводилось в соответствии с санитарными нормами [10]. Определение содержания ВВ проводили в соответствии с ГОСТ Р 53193-2008 в ЦКП «Прогресс» ВСГУТУ. Содержание суммы антиоксидантов (ССА) было установлено на приборе ЦветЯуза-01-АА (НПО «Хи-мавтоматика», г. Москва) согласно ГОСТ Р 54037-2010. Содержание ДВ в пересчете на танин было определено согласно ОФС.1.5.3. 0008.15. Для определения содержания ФЛ в исследуемом растительном сырье и полученных экстрактах была использована методика, основанная на получение соединения с хлоридом алюминия [11].
Отбор и подготовку листьев облепихи и полученного экстракта для микробиологических анализов проводили в соответствии с ОФС.1.2.4.1. 0001.15 «Микробиологическая чистота».
В ходе исследования противовоспалительной активности сухого экстракта из листьев облепихи было проведено испытание на 24 кры- сах линии Wistar массой (146,0 ± 5,8) г. До начала проведения эксперимента все животные получали стандартный рацион вивария и имели неограниченный доступ к воде. Использование животных в исследованиях соответствовало законодательству РФ, включая СанПиН 2.2.1.3218-14 и СанПиН 1.2.3685-21.
Экспериментальные животные были разделены на три экспериментальные группы по восемь особей мужского пола в каждой: контрольная группа (животные без лечения), группа сравнения (животные, получавшие ромашковый отвар) и группа, которая получала водный раствор сухого экстракта из листьев облепихи (концентрация 0,1 г/кг массы животного). У всех животных был вызван отек лап с использованием 3 % водного раствора формалина, который вводили субплантарно в правую заднюю лапу в объеме 0,1 мл. Выраженность отека измеряли штангенциркулем в три временных момента: до введения формалина (нулевой момент), через два часа и через двадцать четыре часа после введения флогогена [12].
Выраженность отека лап (%) рассчитывали по формуле
О= ∙100 %, где О – отек лапы экспериментальных животных, %; Vn – объем лапы через n ч (n = 2 или 24 ч), см3; V0 – исходный объем лапы, см3.
Опытные животные получали изучаемые экспериментальные препараты ежедневно в течение 7 дней один раз в сутки утром натощак внутрижелудочно через зонд. Объем вводимых жидкостей составлял 1 мл на 100 г массы тела животного (10 мл/кг).
Экспериментальные исследования и опыты были проведены с соблюдением принципов достоверности и воспроизводимости: каждый эксперимент выполнялся в 3-кратной повторности для обеспечения статистической значимости результатов. Полученные данные подвергались обработке и анализу с использованием современных программных инструментов, таких как Statistica и MS Excel, что позволило провести корректную статистическую оценку и визуализацию результатов.
Результаты и их обсуждение. На первоначальном этапе изучался исходный материал – проводилось исследование листьев облепихи на предмет токсикологической и биологической безопасности и оценки микробиологических показателей. Данные представлены в таблице 1.
Таблица 1
Содержание токсичных веществ и микробиологических показателей листьев облепихи крушиновидной
The content of toxic elements and microbiological indicators of buckthorn leaves
|
Показатель |
Допустимые уровни*** |
Результаты испытаний ± погрешность, P = 0,95 |
|
Токсичные вещества*, мг/кг |
||
|
Свинец |
6,0 |
0,10 |
|
Мышьяк |
0,5 |
< 0,0025 |
|
Кадмий |
1,0 |
0,40 |
|
Ртуть |
0,1 |
< 0,0025 |
|
ГХЦГ (α-, β-, γ-изомеры) |
0,1 |
< 0,005 |
|
ДДТ и его метаболиты |
0,1 |
< 0,005 |
|
Гептахлор |
Не допускается (<0,002) |
< 0,002 |
|
Алдрин |
Не допускается (<0,002) |
< 0,002 |
|
Микробиологические показатели** |
||
|
КМАФАнМ, КОЕ/г, не более |
5 · 105 |
95 · 102 |
|
БГКП в 0,01 г |
Не допускаются |
Не обнаружено |
|
E. coli в 0,1 г |
Не допускаются |
Не обнаружено |
|
Патогенные, в т. ч. сальмонеллы , в 10 г |
Не допускаются |
Не обнаружено |
|
Дрожжи, КОЕ/г, не более |
100 |
62 |
|
Плесени, КОЕ/г, не более |
103 |
102 |
Примечание : (*) – сухие чаи; (**) – смеси высушенных лекарственных растений; (***) – ТР ТС
021/2011 «О безопасности пищевой продукции».
В ходе исследования было установлено, что содержание тяжелых металлов, пестицидов, общее микробное число, количество дрожжей и плесневых грибов в облепиховых листьях не превышают норм, определенных Едиными санитарно-эпидемиологическими и гигиеническими требованиями [10].
Из данного растительного материала на базе малого инновационного предприятия был получен CЭ из листьев облепихи, фильтрацию и водили в концентраторе, оснащенном мешалкой, в течение часа, влажность полученного экстракта составила (8,75 ± 0,05) % [9].
Данные по содержанию в листьях облепихи и исследуемом сухом экстракте водорастворимых витаминов представлены в таблице 2. В качестве сравнения использовался фармакопейный препарат «Гипорамин» [8]. Влажность фармакопейного препарата «Гипорамин» составлила (0,92 ± 0,04) %.
концентрирование полученного экстракта про
Таблица 2
Содержание ВВ в листьях облепихи и экстрактах из листьев облепихи, мг/г The content of WV in sea buckthorn leaves and extracts from sea buckthorn leaves, mg/g
|
Водорастворимый витамин |
Листья облепихи |
Сухой экстракт |
Сухой экстракт «Гипорамин» |
|
С |
0,08 |
0,34 |
0,03 |
|
В 2 |
0,02 |
0,07 |
0,002 |
|
В 3 |
0,28 |
0,04 |
0,04 |
|
В 5 |
0,006 |
0,009 |
0,006 |
|
В с |
0,01 |
0,02 |
0,007 |
Содержание аскорбиновой кислоты в полученном СЭ из листьев облепихи увеличилось в 4,25 раза, витамина В 2 в 3,5 раза, витамина В 5 в
1,5, витамина Вс в 2 раза по сравнению с исходным растительным сырьем. Содержание витамина В3 уменьшилось в 7 раз, возможно, это связано с тем, что пантотеновая кислота плохо растворяется в спиртах и при кипячении может быть потеряно до 50 % (вследствие выщелачивания) [13]. В сравнение с фармакопейным препаратом «Гипорамин» содержание витамина С в полученном экстракте превышает в 11 раз, витамина В2 – в 35 раз, витамина Вс – в 2,9 раза.
В таблице 3 представлены данные, отражающие ССА (в пересчете на кверцетин), ДВ (в пересчете на танин) и ФЛ (в пересчете на рутин) в исследуемых образцах. Полученные значения свидетельствуют о высокой биологической активности образцов, что может быть связано с их потенциальными антиоксидантными и противовоспалительными свойствами.
Таблица 3
|
БАВ |
Листья облепихи |
Сухой экстракт |
Сухой экстракт «Гипорамин» |
|
Дубильные вещества (танин), % |
14,46±1,63 |
45,9±1,22* |
6,99±0,38** |
|
Флавоноиды, (рутин), % |
3,16 ±0,22 |
9,61±0,43* |
5,29±0,09** |
|
ССА (кверцетин), мг/г |
0,352±0,08 |
1,453±0,35* |
0,559±0,07** |
Примечание: (*) - достоверное отклонение значения СЭ по сравнению со значением в листьях облепихи (p ≤ 0,05), (**) – достоверное отклонение значения СЭ «Гипорамин» по сравнению со значениями в листьях облепихи (p ≤ 0,05).
БАВ в листьях облепихи и экстрактах из листьев облепихи
BAS in sea buckthorn leaves and extracts from sea buckthorn leaves
При определении содержания ДВ в листьях и полученном экстракте наблюдалось достоверное увеличение в 3,14 раза по сравнению с исходным сырьем, тогда как в сухом экстракте «Гипорамин» содержание было меньше в 2,06 раза. Максимальное содержание ФЛ наблюдалось в полученном СЭ из листьев облепихи, которое было выше в 3,04 раза по сравнению с исходным сырьем и на 81 % больше, чем в «Гипорамине». При анализе ССА в листьях и полученном экстракте было обнаружено увеличение в 4,21 раза по сравнению с исходным материалом, тогда как этот показатель у «Гипорамина» был ненамного выше, чем у исходного растительного сырья.
В таблице 4 представлены данные по микробиологическим исследованиям СЭ из листьев облепихи.
Таблица 4
|
Показатель |
Допустимые уровни, мг/кг, не более* |
Результаты исследования |
|
КМАФАнМ, КОЕ/г, не более |
5 · 104 |
2 · 103 |
|
БГКП (колиформы) в 0,01 г |
Не допускаются |
Не обнаружено |
|
E. coli в 0,1 г |
Не допускаются |
Не обнаружено |
|
Патогенные, в т. ч. сальмонеллы, в 10 г |
Не допускаются |
Не обнаружено |
|
Дрожжи и плесени, КОЕ/г, не более |
100 |
Не обнаружено |
Примечание: (*) – ТР ТС 021/2011 «О безопасности пищевой продукции».
Микробиологической анализ чистоты экстракта из листьев облепихи Microbiological аnalysis of the purity extract of sea buckthorn leaf extract
Исследования микробиологической чистоты экстракта, полученного из листьев облепихи, подтвердили его соответствие установленным нормативным требованиям [10]. После процесса экстрагирования было зафиксировано значительное снижение общего количества микроорганизмов в экстракте – их количество уменьшилось в 4 раза. При этом дрожжи и плесневые грибы в готовом экстракте обнаружены не были.
СЭ из листьев облепихи обладает высокой степенью чистоты и безопасности, что позволяет рекомендовать его для использования в пищевой промышленности в качестве биологически активной добавки (БАД). Его применение не только безопасно для человека, но и может способствовать обогащению продуктов питания полезными БАВ, характерными для облепихи.
Далее было проведено исследование противовоспалительного эффекта СЭ из листьев облепихи на модели отека лапы крыс [12].
В ходе исследования было обнаружено, что у животных в контрольной группе после введения флогогена объем задней лапы значительно увеличился (на 61 %) через 2 ч и снизился до 36 % через 24 ч (рис.), что указывает на развитие отека лап у подопытных животных. У крыс из опытной группы II, которые получали отвар ромашки в течение 7 дней, отек лапы составил 43 % через 2 ч и 18 % через 24 ч (эффективность по сравнению с контрольной группой составила 18 %). В группе III было обнаружено достоверное уменьшение отека лап через 2 ч -до 18 % (эффективность - 43 %), через 24 ч эффективность в данной группе составила 62 %. Установлена достоверная разница в эффективности приема экстракта из листьев облепихи по сравнению с отваром ромашки.
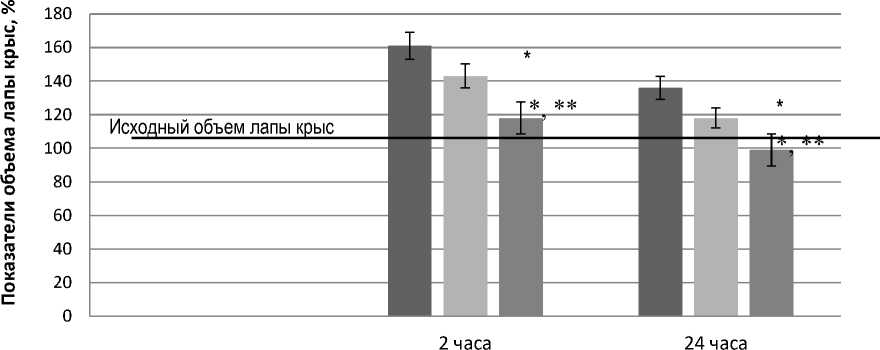
Контроль
Отвар ромашки
Экстракт из листьев облепихи
Примечание : * - достоверное отклонение значения в группе относительно контрольной группы, ** - достоверное отклонение значения в группе экстракта из листьев облепихи относительно значений во II группе Р < 0,05.
Показатели объема лапы крыс на фоне формалинового отека Indicators of rat paw volume against the background of formalin-induced edema
В ходе проведенного исследования было выявлено, что в листьях облепихи, собранных на территории Республики Бурятия, отсутствуют токсичные элементы. Это также подтверждают выводы новосибирских ученых о том, что данный растительный вид не накапливает токсичные вещества, как было установлено в исследовании Г.М. Скуридина (2014) [6].
Полученные показатели количественного определения БАВ в листьях облепихи, собранных в Республике Бурятия (2023) в частности по содержанию ФЛ (которое составило 3,16 % в пересчете на рутин), коррелируют с результатами исследований Э.Н. Новрузова (2018) с коллегами из Института ботаники Азербайджана, которые изучали флавоноидный состав листьев мужских растений облепихи с помощью спектрофотометрического метода (содержание фла- воноидов в их образцах варьировало от 2,81 до 3,20 %) [11].
В ходе изучения биофармакологической активности экстракта облепихи, как и в работе Н.А. Ковалевой с соавт. (2023), был доказан его противовоспалительный эффект на модели отека лап крыс, где в качестве препарата сравнения использовался настой цветков ромашки [12].
Заключение. Проведенные исследования подтвердили, что исходное растительное сырье (листья облепихи крушиновидной) полностью соответствует установленным нормативным требованиям. В частности, были соблюдены допустимые уровни по следующим параметрам: общее микробное число, количество дрожжей и плесневых грибов, а также содержание токсичных элементов, таких как тяжелые металлы и другие потенциально вредные вещества. Это свидетельствует о высоком качестве сырья и его безопасности для дальнейшего использования.
Проведенный дальнейший анализ сырья, произрастающего на территории Республики Бурятия, также подтвердил его высокий антиоксидантный (АО) потенциал, что делает его перспективным для разработки функциональных премиксов различного назначения. Кроме того, СЭ из листьев облепихи крушиновидной продемонстрировал выраженную противоотечную активность в экспериментах на лабораторных животных, что связано с высоким содержанием АО.
Эти данные открывают возможности для создания новых БАД и лекарственных средств на основе данного сырья, направленных на поддержание здоровья и профилактику заболеваний, связанных с окислительным стрессом и воспалительными процессами. Дополнительно можно отметить, что использование экстракта листьев облепихи может быть перспективным не только в фармакологии, но и в пищевой промышленности, например для обогащения продуктов функционального питания. Это также подчеркивает важность дальнейших исследований для оптимизации технологий переработки сырья и расширения спектра его применения.


