Исследование известково-карбонатной системы сахарного производства
Автор: Кульнева Надежда Григорьевна, Шматова Анастасия Ивановна
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Биотехнология, бионанотехнология и технология сахаристых продуктов
Статья в выпуске: 3 (53), 2012 года.
Бесплатный доступ
Изучено влияние рН среды и температуры на активность известково-карбонатной суспензии в условиях сахарного производства. Установлена возможность снижения расхода реагентов на процесс очистки производственных сахарных растворов.
Гидроксид кальция, карбонат кальция, известково-карбонатно-сахарозные растворы, суммарная растворимость
Короткий адрес: https://sciup.org/14039873
IDR: 14039873 | УДК: 664.1.03
Research of limy and carbonate system of sugar production
Influence of рН and temperature on activity of suspension of lime and carbonate in sugar production is investigated. Possibility of decrease in a consumption of reagents on purification of production sugar solutions is established.
Текст научной статьи Исследование известково-карбонатной системы сахарного производства
Основной задачей, стоящей на современном этапе развития свеклосахарного производства, является разработка ресурсосберегающей технологии известково-углекис-лотной очистки (ИУО), обеспечивающей высокий эффект удаления несахаров из диффузионного сока при минимальных затратах реагентов на ее реализацию.
Для теоретического обоснования процессов ИУО важное значение имеют физикохимические свойства основных реагентов – гидроксида кальция и карбоната кальция, в частности, их растворимость, определяющая эффективность протекания химических и адсорбционных процессов очистки сахарсодержащих растворов.
Наиболее важное место в очистке диффузионного сока занимает предварительная дефекация, на которой удаляется более половины несахаров за счет химических реакций и адсорбции на поверхности кристаллического карбоната кальция. На преддефекацию можно возвращать сгущенную сусп ензию или нефильтрованный сок I сатурации, сгущенную суспензию сока II сатурации, активированную различными методами.
Основное удаление несахаров из раствора осуществляется адсорбцией на осадке карбоната кальция, образующемся в процессе карбонизации гидроксида кальция. Совместное присутствие гидроксида и карбоната кальция наблюдается на всех этапах известково-углекислотной очистки диффузионного сока.
Карбонат кальция в кристаллическом виде присутствует уже на начальной стадии очистки, куда он вводится с суспензией сатурированных соков для формирования устойчивой структуры преддефекованного осадка и более полной коагуляции коллоидных веществ [2]. В условиях сахарного производства карбонат кальция подвергается воздействию температуры от 40 0С на преддефекации до 95 0С на II сатурации и рН среды от 7,2 на предварительной дефекации до 12,5 на основной дефекации. Зная влияние рН, температуры и состава среды, других факторов на состояние известково-карбонатно-сахарозной системы можно опти -мизировать режимы ИУО диффузионного сока.
Содержание ионов кальция в растворе определяет интенсивность химических реакций осаждения и коагуляции, имеет большое значение при выборе оптимального режима II сатурации, влияет на процессы сгущения и уваривания утфелей. Зная суммарную растворимость гидроксида и карбоната кальция в зависимости от условий процесса и присутствующих несахаров, можно выбрать оптимальные условия для введения или формирования кристаллического карбоната кальция в процессе ИУО.
Изучено влияние различных факторов на суммарную растворимость гидроксида и карбоната кальция, характеризующую полноту протекания химических и физико-химических процессов, а также дисперсность образующихся осадков. Критерием для оценки влияния различных факторов на растворимость приняли массовую долю солей кальция в известко-
ВестникВГУИТ, № 3, 201 2 во-карбонатных и известково-карбонатно-сахарозных растворах.
Для определения суммарной растворимости гидроксида и карбоната кальция термостатированную ячейку заполняли бидистил-лированной водой либо раствором химически чистой сахарозы с различной массовой долей сахарозы, приготовленным на бидистиллиро-ванной воде. Значение рН регулировали введением раствора гидроксида кальция. Вводили химически чистый карбонат кальция при массовой долей 0,6 %. Ячейку герметично закрывали и выдерживали суспензию при постоянном перемешивании до достижения состояния насыщения (время выбиралось эмпирически). Надосадочную жидкость фильтровали через обеззоленный фильтр, в фильтрате определяли массовую долю кальция комплексометрическим или фотоколориметрическим методами [1]. Результаты эксперимента по влиянию рН на растворимость приведены в табл. 1.
Таблица 1
Равновесная концентрация Са2+ в водном растворе
|
рН раствора |
Моляльная концентрация, 10-3 моль/кг Н 2 О при температуре, оС |
|||||
|
20 |
30 |
40 |
50 |
60 |
80 |
|
|
8,0 |
0,28 6 |
0,51 8 |
0,69 6 |
0,69 6 |
1,03 6 |
0,64 2 |
|
9,0 |
0,14 3 |
0,35 7 |
0,56 4 |
0,51 8 |
0,62 5 |
0,57 2 |
|
10,0 |
0,21 4 |
1,00 0 |
0,64 2 |
1,08 9 |
0,64 2 |
0,60 7 |
|
11,0 |
0,35 7 |
1,68 9 |
1,44 7 |
1,66 1 |
1,35 7 |
0,60 7 |
В гетерогенных системах, к которым относят производственные сахарные растворы, протекают два противоположных процесса: растворение и формирование нерастворимых комплексов из гидроксида и карбоната кальция. Величина рН, требуемая для достижения практически полного осаждения какой-либо малорастворимой соли слабой кислоты, зависит от произведения растворимости этой соли. Кроме произведения растворимости, большое значение имеет также константа ионизации слабой кислоты, входящей в состав соли.
Данные эксперимента подверждают, что растворимость карбоната кальция в водных растворах минимальна при рН 9. При снижении рН до 8 растворимость повышается, т.к. в растворе увеличивается концентрация ионов Н+, которые связывают анионы СО32- в неионизированные молекулы Н2СО3 и анионы НСО3--, что вызывает растворение осадка:
NaNI 3 □ Na 2 +NI 2
ÑÎ 32-+2H+=H2ÑÎ 3
ÑÎ 32-+H+=HÑÎ 3- .
Следовательно, концентрация в растворе анионов СО 3 2- зависит от концентрации ионов Н+, убывая с их увеличением, т.е. при понижении рН.
В насыщенном растворе карбоната кальция существует равновесие
NaNI 3(оа) □ Na2 +NI 2 (1), характеризующееся величиной произведения растворимости
ПР = [Ca2 ]·[CO 3 2-] = ΠA/γ2 (2)
где ПА=3,7 · 10-9 – произведение активности; γ – средний ионный коэффициент активности, рассчитываемый по уравнению Дэвиса:
lgY=—0,509[z+z—] VJ /(1 + VJ) + 0,1 [z+z—]J, где Z+, z- – заряд ионов; J – ионная сила раствора.
Анионы СО 3 2- в нейтральной и кислой средах взаимодействуют с молекулами воды, образуя гидрокарбонат-ионы:
NI 2 +1 2I □ I NI 3+I I (3)
Равновесие реакции (3) характеризуется константой
Г ~ A - A f -
[Í ÑÎ - ][Î Í - ]
Ê1= 3 , (4)
[ÑÎ3 2- ]
связанной с константой диссоциации Н 2 СО 3 по второй ступени
K ii =[H+H СО2" ]/[ НСО- ]
соотношением
K 1 =K II /K W , где К W =10-14 – константа ионизации воды. Так как K II =4,7 · 10-11, отсюда К 1 =4,7 · 103. С уменьшением рН равновесие реакции (3) смещается в сторону связывания карбонат-иона, что вызывает увеличение растворимости СаСО 3 .
В щелочной среде ионы Са2+ могут частично связываться с ОН--ионами по уравнению
Na2 +I I □ NaI I (5)
Значение константы диссоциации
Са(ОН) 2 по второй ступени составляет 4 · 10-2.
К = [Ca2+]-[OH-]/[CaOH+] (6)
С увеличением концентрации ОН--ионов равновесие (5) смещается в сторону связывания ионов Са2+, что приводит к увеличению растворимости СаСО3.
Количественную оценку влияния рН на растворимость проводили на модельной системе [2], в которой протекают равновесные процессы (1), (3), (5), характеризуемые константами (2), (4), (6). Поскольку концентрации компонентов системы [Са2+], [СаОН+], [ОН-], [СО32-], [НСО3-] связаны между собой тремя константами, однозначное решение невозможно. Систему моделировали численно с использованием математического аппарата. Задавали начальные значения [ОН-], [Са2+]=[СО32-] = V ПА , [СаОН+]=0, [НСО3-] = 0. Из уравнений (3), (4), (5), (6) находили равновесные концентрации первого приближения.
Поскольку произведение концентраций [Са2+]-р[СО32-] становилось меньше ПР, до равновесных значений их доводили с помощью уравнений (1)-(2). После этого расчетный цикл повторялся.
Через несколько итерационных шагов в системе достигалось равновесие, концентрации всех ионов стабилизировались. В табл. 2 приведены результаты расчетов равновесных концентраций ОН-, Са2+, СаОН+ , а также суммы [Са2+]+[СаОН+] в зависимости от начального рН.
Таблица2 Зависимость равновесных концентраций Са2+, СаОН + и их суммы от рН водного раствора (расчетные данные)
|
Начальное р Н20 |
Равновесные рН и концентрации ионов, 10-3 моль/дм3 |
|||
|
р Н20 |
[Са2+] |
[СаОН + ] |
Ʃ |
|
|
8,0 |
7,97 |
12,05 |
0,03 |
12,0 8 |
|
9,0 |
9,20 |
10,24 |
0,04 |
10,28 |
|
10,0 |
10,00 |
7,77 |
0,20 |
7,97 |
|
11,0 |
11,00 |
8,40 |
2,10 |
10,50 |
В водно-сахарных растворах равновесие в системе карбонат кальция - гидроксид кальция отличается от равновесия в воде, что обусловлено образованием сахаратов (рис. 1-2).
После обработки экспериментальных данных получено уравнение для равновесной концентрации ионов Са2+ при совместном присутствии Са(ОН)2 и СаСО3 в сахарном растворе массовойдолей 15 %:
-18,0109 • [ H + ] 10700/ RT 9,25106 • [ H + ] - 24080/ RT С=0,087 e • e + 130 e • e
Анализ зависимостей показывает, что процесс растворения в полученном диапазоне параметров состоит из двух накладывающихся друг на друга процессов. Первый процесс усиливается с понижением кислотности, т. е. с повышением рН раствора и, как показывает знак показателя второй экспоненты, экзотер-мичен. Экзотермический процесс, вероятнее всего, является результатом образования комплексов с участием сахарозы. Напротив, конкурирующий процесс ослабевает с повышением рН и эндотермичен.
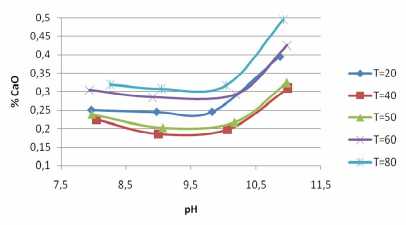
Рис. 1. Влияние рН на равновесную концентрацию ионов Са2+ в водно-сахарном растворе
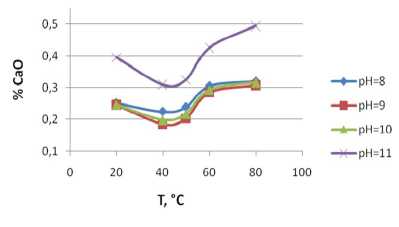
Рис. 2. Зависимость равновесной концентрации ионов Са2+ в водно-сахарном растворе от температуры
Как видно из табл. 2, суммарное содержание растворимых форм кальция в виде Са2+ и СаОН+ достигает минимума в интервале рН 9-10, что согласуется с опытными данными, приведенными выше. Некоторое расхождение может быть объяснено влиянием неучтенных побочных реакций.
Из экспериментальных данных видно, что в водно-сахарных растворах суммарная растворимость гидроксида и карбоната кальция зависит от рН и температуры. Растворимость кальция в сахарных растворах выше, чем в водных. Сахароза в щелочной среде проявляет себя как многоосновная кислота, по- этому повышенная растворимость в сахарном растворе обусловлена образованием соединений сахарозы с кальцием:
NaNI 3(qa) □ Na2 +NI 2 ,
Na 2 +IN 12 I 21 I 11 □ Na(N12I 21I п) +1 ,
N a (N12 l 211 11 ) + N12 ^ 21I 11 □
-
□ Na(N 12 l 21 I 11 ) 2 +1 +
Na2 +I I □ NaI I ,
[NaI I ] +1 N12I 21I 11 □ Na(N12I 21I 11 ) +1 2I .
В сахарном растворе, содержащем карбонат кальция, сахароза связывается с ионом кальция в моносахарат или дисахарат кальция с соответствующим повышением концентрации ионов водорода.
Связывание и снижение в связи с этим концентрации ионов кальция ведет к дополнительному растворению карбоната кальция до достижения равновесия. Растворимость карбоната кальция определяется концентрацией ионов водорода, т.е. рН раствора. В насыщенных известью растворах сохраняется постоянство значений рН даже при варьировании концентрации сахарозы.
По данным Даишевой Н.М. [4], при растворении извести в сахарном растворе сахароза связывается с ионом гидроксикальция в моносахарат или дисахарат гидроксокальция с соответствующим снижением концентрации ионов гидроксила, препятствуя тем самым диссоциации гидроксида кальция по второй ступени:
_ ~ - ^ ' ^ Г _ Г ~ Г /V
[Nai I ] +I I +1 N12I 21i 11 □
-
□ [NaI I ]N 12 l 21 I 11 +1 2 I ,
2[NaI 1 ]++211 -+i 2n12i 20I 11 □
-
□ [NaI 1 ]2N1 2 i 2o I 11 +21 2I .
Снижение концентрации ионов гидроксикал ция и гидроксила ведет к дополнительном растворению гидроксида кальция.
Для равновесия (5) константа диссоциации Са(ОН)2 по второй ступени при температуре 25 оС составляет 4,0 - 1 О-2. Для расчета константы при других температурах запишем уравнение диссоциации СаОН+:
NaI I □ Na2 +I I . (7)
Рассчитаем стандартное изменение энергии Гиббса:
A G ° 2 98 = [(-553,04) + (-157,2)] - [(-718,4)]=
= 8,2 кДж/моль.
Уравнение изотермы химической реакции: К Т = exp(- A G ° 298/RT).
При температуре 298 К К298 =
= exp (-8200/8,314 - 298) = 3,65 - 1О-2.
Аналогично рассчитаем значения для других температур:
|
Температура, оС |
К Т |
К 1 =1/КТ |
|
20 |
3,45 - 1О-2 |
29,О |
|
30 |
3,86 - 1О-2 |
25,9 |
|
40 |
4,28 - 1О-2 |
23,4 |
|
50 |
4,72 - 1О-2 |
21,2 |
|
60 |
5,17 - 1О-2 |
19,3 |
|
80 |
6,12 - 1О-2 |
16,3 |
Константа диссоциации для (7) имеет [Ca 2+ ][OH - ] вид: Е =-------т— ,
[CaOH ]
отсюда [ Na 2+ ][ I I - ] =Е 1 [ NaI I + ] .
Это отношение в исследуемом диапазоне значений температуры и рН лежит в интервале от 1,63 - 1О-6 (температура 80 оС, рН 7) до 2,9О - 1О-2 (температура 20 оС, рН 11). Таким образом, равновесие (7) практически полностью смещено вправо, и его можно не принимать во внимание при последующем анализе.
Для оц енки реакционной способности сахарозы построены диаграммы равновесия различных ионных форм сахарозы в зависимости от рН среды при условии, что константы диссоциации сахарозы как слабой кислоты при температуре 25 оС составляют: по первой ступени К 1 =4,15 - 1О " 13, рК 1 = 12,38; по второй ступени К 1 =9,6 - 1О " 14, рК2 = 13,О2 (рис. 3).
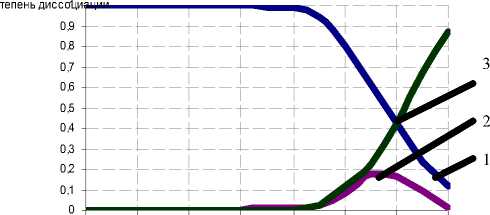
7 8 9 10 11 12 13 14 рН
Рис. 3. Ионные формы сахарозы при массовой доле сахарозы в растворе 15 % : 1 - С12Н22ОП 2 -С 12 Н 21 О 11 3 - С 12 Н 20 О 11 2
Представленные результаты свидетельствуют, что образование сахаратов возможно только при рН среды 11 и более. При массовой доле сахарозы 15 % , соответствующей концентрации диффузионного сока, в насыщенных известью сахарных растворах образуются преимущественно двухкальциевый сахарат с константой нестойкости 1,79 - 10 " 3 и комплекс [Са(ОН)2]СаСах2 c константой нестойкости 2,4 - 10-5.
Уравнение для равновесной концентрации ионов Са2+ при совместном присутствии Са(ОН)2 и СаСО3 в сахарозном растворе массовой долей 50 %:
-1,5 - 109 - [ H + ] 6160/ RT 18,3 - 106 - [ H + ] - 9440/ RT C-0,005 e • e + 1,72 e • e
Анализ зависимости показывает, что молярный тепловой эффект при концентрации сахарозы 15 % значительно ниже, чем при 50 %. Можно полагать, что в концентрированном растворе сахарозы образуется устойчивая форма комплексов кальция с сахарозой с более прочной координационной связью (рис. 4-5).
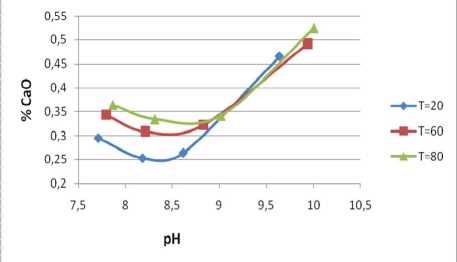
Рис. 4. Влияние рН на равновесную концентрацию иона кальция при массовой доле сахарозы 50 %
Температура, оС рН11 рН10
рН9
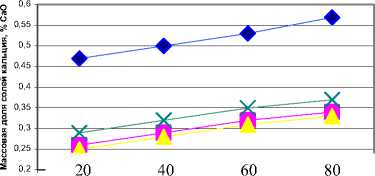
рН8
Рис. 5. Зависимость равновесной концентрации иона Са2+ от температуры при массовой доле сахарозы 50 %
Анализ результатов подтверждает, что в рассматриваемых условиях при рН более 10 и массовой доле сахарозы 50 % сахароза проявляет свойства одноосновной кислоты, что способствует образованию преимущественно монокальциевых сахаратов.
Мищуком Р.Ц. [3] доказан состав комплексов сахарозы и кальция, образующихся за счет координационной связи и записывающихся в виде [Ca m Cx m ]1 ± , что подтверждает существование в системе сахароза - известь - вода строгого соответствия между количеством сахарозы и кальция. Образование комплексных соединений приводит к изменению рН извест-ково-сахарного раствора.
В соответствии с исследованиями Даи-шевой Н.М. ионный состав известково-карбонатно-сахарозных суспензий определяет концентрация ионов гидроксила, т.е. рН, в зависимости от которого концентрация двухзарядного иона кальция может меняться от максимума при низких значениях рН (ниже оптимального для II сатурации) до почти полного исчезновения в насыщенных гидроксидом кальция растворах (рН выше 12,5). Соответственно с повышением рН возрастает доля однозарядного комплексного иона гидроксикальция.
Анализ явлений, происходящих при ИУО производственных растворов, показывает, что из двух видов ионов кальция осаждающим в виде малорастворимых кальциевых соединений является двухзарядный ион. Однозарядный ион гидроксикальция, подобно ионам щелочных металлов, образует лишь растворимые соли.
В соответствии с исследованиями Подгорновой Н.М. [5] в насыщенных известково-карбонатных растворах степ ень диссоциации комплексного иона [СаОН+] в зависимости от температуры и рН составляет от 90,7 % при температуре 40 оС до 96,1 % при температуре 80 оС и от 98,6 % при рН 11,2 до 99,4 % при рН 9,8. Таким образом, в рассматриваемой модельной известково-карбонатно-сахарозной системе преобладающим является ион Са2+.
При проведении ИУО диффузионного сока на преддефекацию вводятся 0,2-0,3 % СаО в виде известкового молока и щелочные возвраты суспензии сока I или II сатурации, содержащие кристаллический карбонат каль- ция. Из присутствующего карбоната кальция в раствор в зависимости от рН и температуры переходит 0,2-0,5 % СаО, что полностью обеспечивает необходимое содержание ионов кальция для протекания реакций осаждения и коагуляции несахаров.
Добавление гидроксида кальция необходимо лишь для нейтрализации кислот диффузионного сока и создания значения рН среды, при котором эффективно осаждаются отдельные группы несахаров. Это количество составляет от 0,15 до 0,25 % СаО и должно вводиться в диффузионный сок постепенно в процессе прогрессивной предварительной дефекации.
Таким образом, установлена возможность снижения расхода гидроксида кальция на ИУО при введении суспензии карбоната кальция на стадии предварительной дефекации.


