Изучение ассоционных взаимодействий каротиноидных пигментов с полигидроксиоксосоединениями
Автор: Болотов Владимир Михайлович, Комарова Елена Владимировна, Саввин Павел Николаевич, Перикова Людмила Ивановна
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Фундаментальная и прикладная химия, химическая технология
Статья в выпуске: 3 (53), 2012 года.
Бесплатный доступ
На примере экстракционного выделения β -каротина из модельной смеси основных химических соединений корнеплодов красной моркови, а также продуктов гидролиза природных веществ в присутствии молочной кислоты подтвержден эффект процесса комплексообразования.
Каротиноиды, пектиновые соединения, олигомеры сахаров, комплексообразование, экстракция, сarotinoids
Короткий адрес: https://sciup.org/14039866
IDR: 14039866 | УДК: 664:547.979.8
Studying association interactions of carotinoid pigments with polygidroksiand oksocompounds
On an example of extraction allocation β - carotin from a modelling mix of the basic chemical combinations of red carrots root crops, and also hydrolysates of connatural materials in the presence of milk acid the effect of complex process formation is confirmed.
Текст научной статьи Изучение ассоционных взаимодействий каротиноидных пигментов с полигидроксиоксосоединениями
Современные технологии позволяют получать натуральные пищевые красители из различного пищевого сырья. Известно, что натуральные пищевые колоранты содержат в своем составе, кроме красящих пигментов, другие биологически активные компоненты, которые полезны для человека . Поэтому использование естественных пигментов для окрашивания продуктов питания позволяет не только улучшить внешний вид, но и повысить пищевую ц енность продуктов. Природные каротиноидные красители широко используются в пищевой промышленности для окраски жиросодержащих продуктов питания. Основными пигментами красителей являются гидрофобные углеводородные каротиноиды типа каротина.
Проводимые нами исследования по изучению закономерностей экстрагирования каротиноидов из корнеплодов моркови красной посевной (Daucus sativus Roehl) показывают, что эффективность процесса зависит не только от химического строения молекулы растворителя и его полярности, но и от присутствия в сырье ряда природных органических соединений, способных в определенных условиях вместе с каротиноидами переходить в состав экстракта.
При экстрагировании основного компонента полиеновых пигментов корнеплодов моркови β -каротина неполярным органическим растворителем CCl 4 или малополярным
Перикова Л.И., 2012
этилацетатом получается прозрачный экстракт красно-оранжевого цвета с характерными для β -каротина поглощениями в этилацетате при 428, 450 и 474 нм (рис. 1):
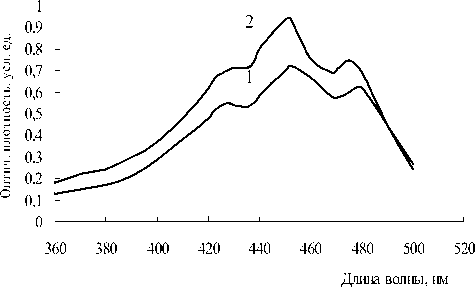
Рис. 1. Электронные спектры поглощения экстрактов каротиноидных соединений свежеизмельчен-ной моркови в этилацетате после предварительной экстракции пигментов этиловым спиртом с объемной долей этанола 96 % (кривая 1) и без обработки этанолом (кривая 2) (толщина кюветы 5 мм, разбавление экстракта – в 40 раз)
Обработка свежеизмельченных выжимок корнеплодов моркови полярным водно-этанольным раствором с объемной долей этанола 96 % приводит к образованию прозрачного спиртового экстракта желтого цвета без максимума поглощения в области 360-500 нм (рис. 2).
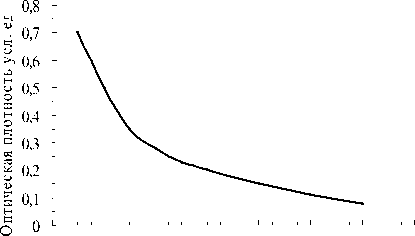
360 380 400 420 440 460 480 500
Длина волны, нм
Рис. 2. Электронный спектр поглощения водно-этанольного экстракта свежеизмельченных выжимок моркови (с объемной долей этанола 96 %)
Смещение максимума поглощения в более коротковолновую область свидетель -ствует о необходимости облучения молекулы β -каротина квантами света с большей энергией для перевода электронов π-связей β -каротина с основной на разрыхляющую орбиталь из-за образования ассоциата (комплекса) β -каротина с полярными гидроксилсодержащими гидрофильными органическими молекулами (например, пектином), также перешедших в состав водно-спиртового экстракта.
Ассоциация между молекулами β -каротина и олигомерными формами макромолекул пектина, по-видимому, происходит за счет образования межмолекулярных связей донорно-акцепторного типа. При этом β -каротин с системой сопряженных π-связей выступает в качестве электронодонора, а пектин с большим количеством гидроксильных и карбоксильных групп – электроноакцептором.
Следует отметить, что при разбавлении прозрачного фильтрата спиртом с объемным содержанием этанола 96 % в 2 раза наблюдается опалесценция и помутнение окрашенного в желтый цвет раствора. Мы считаем, что разбавление спиртоводорастворимого комплекса пигментов приводит к диссоциации ассоциата на исходные компон енты и плохо растворимые в этаноле β -каротин и пектин, что вызывает наблюдаемый эффект.
Для подтверждения участия в экстрагировании β -каротина олигомерных форм пектина и гемицеллюлоз при обработке корнеплодов моркови полярным водно-этанольным раствором нами изучено влияние молочной кислоты на эффективность процесса.
Из литературы известно, что скорость гидролиза полисахаров увеличивается в присутствии кислотного катализатора.
В связи с этим мы исследовали влияние молочной кислоты на эффективность экстракционного извлечения каротиноидов из корнеплодов посевной красной моркови (Daucus sanivus Roehl) 96 %-ным водно-этанольным раствором после их термообработки в температурном интервале 40-80 °С с градиентно-ступ енчатым режимом.
Исследования проводились с использованием спектрофотометрического метода анализа состава спиртовых экстрактов.
К одинаковым навескам измельченных корнеплодов моркови добавляли различные количества молочной кислоты и далее сырье термообрабатывали по разработанному нами способу (патент РФ № 2221829).
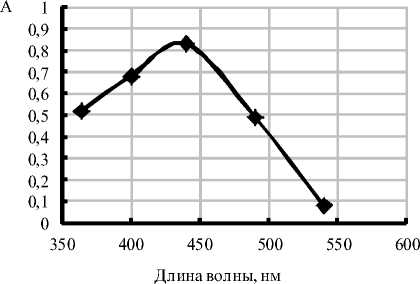
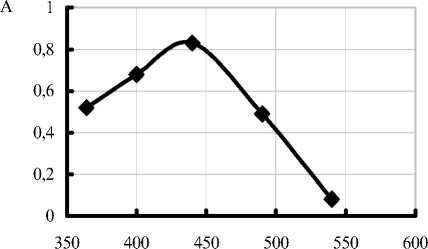
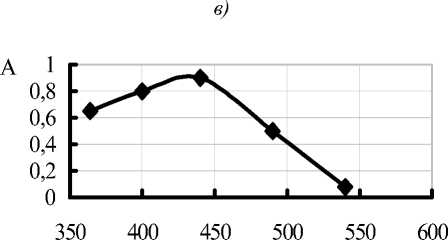
Экстракция красящих веществ проводилась в аппарате Сокслета в течение 2 ч (рис. 3).
Из представленных данных видно, что добавление к сырью небольшого количества молочной кислоты (0,5 мл на 24 г сырья) и последующая термообработка способствуют наибольшему содержанию пигментов в составе экстракта (рис. 4).
Увеличение количества кислоты снижает выход красящих веществ.
Наблюдаемый эффект влияния молочной кислоты может быть связан с уменьшением концентрации олигомерных форм углеводов определенной молекулярной массы, способных образовывать ассоциаты с каротиноидами из-за более интенсивного гидролиза полисахаров в присутствии большого количества молочной кислоты.
С целью изучения влияния основных химических соединений корнеплодов моркови красной посевной (Daucus sanivus Roehl) приготовлена модельная смесь компонентов моркови в природных пропорциях: β -каротин – 0,01 г; глюкоза – 2,5 г; сахароза – 3,5 г; пектин – 0,6 г; яблочная кислота – 0,2 г; аспарагиновая кислота – 0,14 г; глутаминовая кислота – 0,24 г.
А
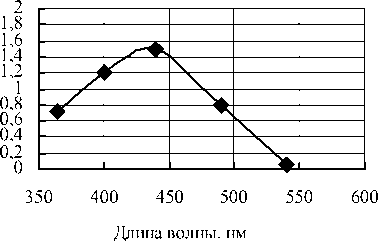
а)
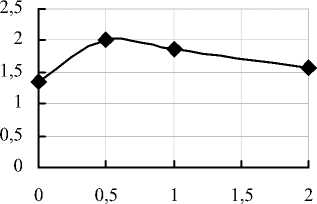
Количество молочной кислоты, мл
Рис. 4. Влияние количества молочной кислоты в составе термообработанных корнеплодов моркови на выход красящих веществ в водно-этанольном экстракте
б)
Длина волны, нм
Длина волны, нм
г)
Рис. 3. Спектральные характеристики водно-этанольных экстрактов красящих веществ из моркови после градиентной термообработки в присутствии различных количеств молочной кислоты: а - 0,5 мл мол. кисл. и 9,5 мл воды; б - 1,0 мл мол. кисл. и 9,0 мл воды; в - 2,0 мл мол. кисл.и 8,0 мл воды; г - 10 мл воды.
Спектрофотометрический анализ водно-этанольных экстрактов каротиноидных пигментов из полученной смеси с различным объемным содержанием спирта показывает, что в -каротина (определяемому по поглощению при X = 440 нм - А440) и сопутствующих соединений (определяемых по поглащению при X = 364 и 400 нм - А364, А 4 00) больше в растворе 96 %-го этанола по сравнению с 48 %.
Например, для 96 %-го этанола А 440 /А 400 = 0,58/0,31 = 0,61, а для 48 % этанола А440 А400 = 0,16/0,31 = 0,52, А 440 /А 36 4 = 0,16/0,95 = 0,17, что объясняется меньшей полярностью и большей растворяющей способностью ассоциатов в -каротина с гидрофильными компонентами модельной смеси моркови.
Интересно отметить, что содержание в -каротина в насыщенном этанольном растворе с объемной долей этанола 96 % меньше по сравнению с содержанием в -каротина в модельной смеси компонентов моркови, что подтверждает факт влияния сопутствующих полярных веществ моркови на растворимость каротиноидов.
При добавлении к насыщенному раствору в -каротина (имеющего осадок в -каротина) в 96 %-ном этаноле соответствующего раствора пектина (в отношении 1 объем раствора каротина и 1 объем раствора пектина) содержание в -каротина в получаемой смеси увеличивается.
Например, при добавлении к спиртовому с объемной долей этанола 96 % насыщенному раствору в -каротина (с осадком в -каротина) спиртового насыщенного раствора пектина со степенью этерификации 70 % содержание каротина увеличилось в 1,36 раза (А440 смеси каротин и пектин 0,34; А440 смеси каротин и растворитель 0,25).
После ступенчатой термооработки модельной смеси основных компонентов корнеплодов моркови в присутствии 10 % воды на воздухе последовательно при t = 40 °C ( т 1 = 2 ч), t = 60 °C ( т 2 = 2 ч), t = 80 °C ( т з = 2 ч) сожержание каротиноидов в составе этанольного экстракта с объемной долей этанола 96 % практически не изменилось, а содержание каротиноидов в составе этанольного экстракта с объемной долей этанола 48 % увеличилось в среднем от 1,15 до 1,35 раз (А440/А400 = = 0,15/0,25 = 0,60; А 440 /А 364 = 0,15/0,66 = 0,23 для 48 % этанольного экстракта из модельного состава моркови после термообработки; А440/А364 = 0,16/0,95 = 0,17 этанольного экстракта из модельного состава моркови без термообработки).
Наблюдаемый эффект, по-видимому, связан не только с увеличением концентрации более окисленных форм каротиноидов, но и большей концентрацией ассоциатов каротиноидов с термообработанным пектином.
Анализ спектральных характеристик этанольных экстрактов с объемным содержанием этанола 96 % из пектинов со степенями этерификации 40 - 70 % до и после термообработки указывает на увеличение концентрации низкомолекулярных пектиновых соединений особенно для термообработанного пектина со степенью этерификации 40 %.
Хроматографические исследования с использованием ВЭЖХ подтверждают данные спектрофотометрии о повышении содержания каротиноидов в водно-этанольных растворах в присутствии пектина, причем термообработка в -каротина с пектином способствует увеличению содержания каротиноидов в спиртовых растворах.
Таким образом, проведенные исследования подтверждают, что повышение гидрофильных свойств природных каротиноидов растительного сырья после термообработки связано с образованием ассоциата пектин- в -каротин-фитоксантины.


