Экстракорпоральная гемокоррекция в комплексной терапии деструктивного панкреатита
Автор: Добрякова Э.А., Казарян С.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 3 (49), 2016 года.
Бесплатный доступ
Проанализировано 386 больных с панкреонекрозом (APACH 11-15 балов Renson >3 балов. При-менялся плазмаферез в 0,5 объема ОЦП за сеанс в сочетании с ВВГФ или ВВГДФ с УФ по показаниям в непрерывном режиме. Подбор программы эфферентной терапии проводился индивидуально, учитывая патогенетическую направленность процесса. Дифференциальный подход и патогенетически подобранная программа экстракорпоральной гемокоррекции позволили снизить частоту гнойно-септических осложнений, сократить пребывание в ОРИТ и летальность.
Панкреонекроз, деструктивный панкреатит, панкреатогенный шок, полиорганная недостаточность, гемофильтрация, экстракорпоральная терапия, плазмаферез, продленная веновенозная гемофильтрация, ультрафильтрация, режимы экстракорпоральной гемокоррекции
Короткий адрес: https://sciup.org/142211264
IDR: 142211264 | УДК: 616-035.1
Extracorporeal hemocorrection in the treatment of destructive pancreatitis
Analyzed 386 patients with necrotizing pancreatitis (APACH 11-15 score RENSON >3 score.) Plasmapheresis was applied in 0.5 volume of plasma circulatsion combined with CVVH or CVVHD end UF on readings in continuous mode. Recruitment program of efferent therapy was conducted individually taking into account pathogenetic orientation process. Differential approach and pathogenetic chosen programme of extracorporeal hemocorrection possible to reduce the frequency of purulent -septic complications, shorten the stay in the intensive care unit and mortality.
Текст научной статьи Экстракорпоральная гемокоррекция в комплексной терапии деструктивного панкреатита
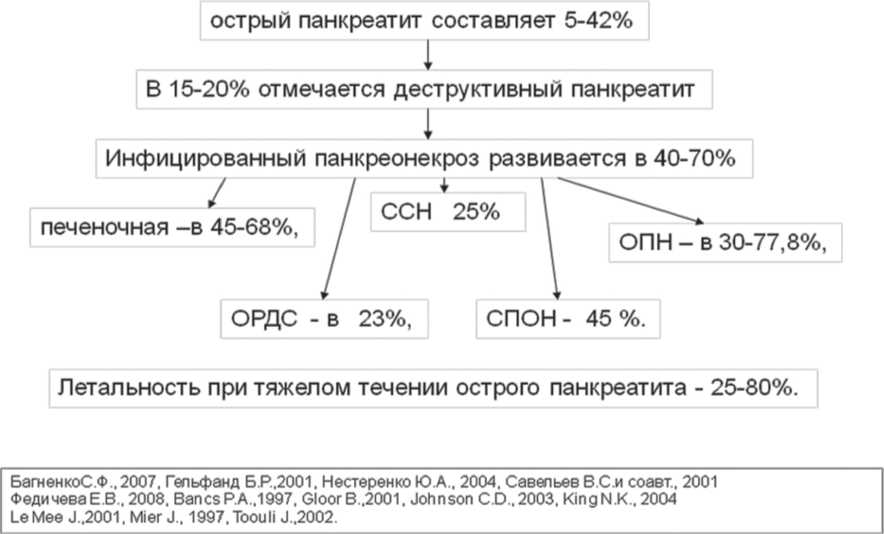
Высокий процент неблагоприятных исходов (от 25 до 80%) [2] при деструктивном панкреатите обусловлен не только тяжестью эндогенной интоксикации, но и стремительным развитием патологического процесса, панкреатогенного шока, полиорганной недостаточностью и тяжестью септических осложнений.
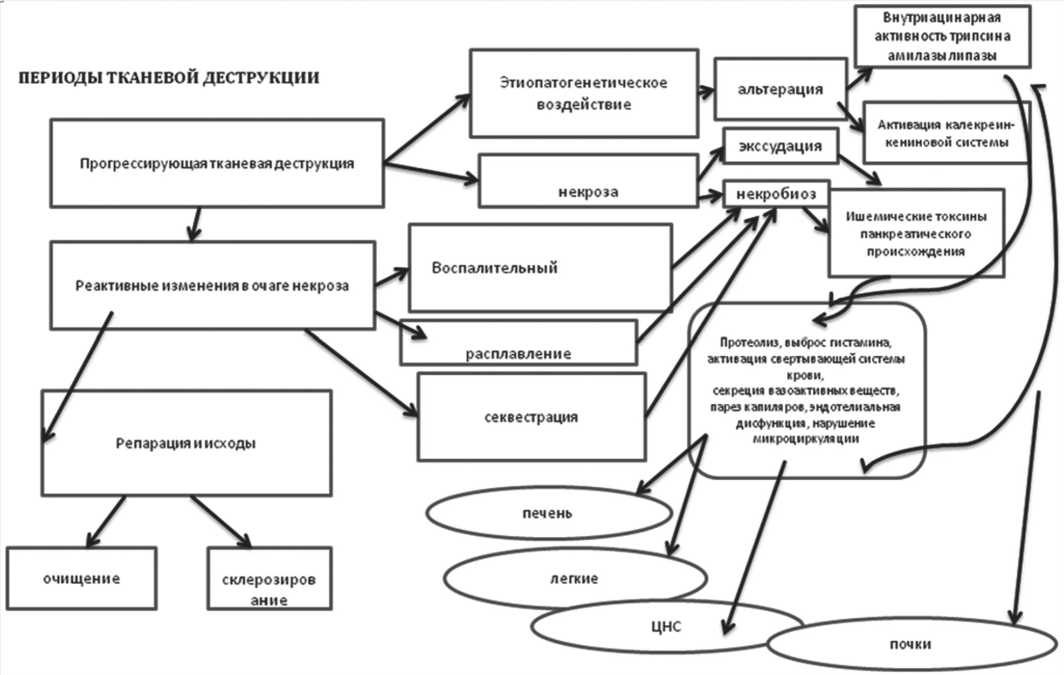
Патофизиологическая суть заболевания состоит в том, что в результате воздействия различных факторов возрастает давление в протоках поджелудочной железы (ПЖ), возникает ее отек, нарушается микроциркуляция, оксигенация и иннервация. Панкреатический секрет выходит за пределы протоков, попадает в ткань железы и повреждает е е. При этом активируются цитокиназы, которые активируют трипсиноген, переводя его в активный трипсин. Запускается каскад реакций с формированием генерализованной воспалительной реакции. В течение первых 2 недель от начала заболевания аутолиз и некробиоз ПЖ, забрюшинной клетчатки с развитием ферментативного асцит-перитонита носит абактериальный характер.
Тяжесть состояния больных обусловлена выраженной панкреатогенной токсинемией. У части больных в этих условиях в течение 72 ч от начала заболевания развивается панкреатогенный шок и "ранняя" полиорганная недостаточность, которая служит основной причиной смерти у 30-40% больных в эти сроки. [5]
Токсемия проходит две фазы. Первая фаза характеризуется воздействием вышедшего из канальцев трипсина на паренхиму железы и превращением трипсиногена в трипсин, химотрипсиногена в химотрипсин и калликреиногена в калликреин с развитием от ека железы и появления множественных кровоизлияний. Активированные ферменты поступают в кровоток. Освобожд енная липаза при активации трипсином и желчными кислотами эмульгирует жиры и вызывает жировые некрозы. На фоне гипоксии, повышенной проницаемости сосудов развивается «химический перитонит» с диапедезом форменных элементов крови и гибелью их [6].
Вторая фаза – острый панкреонекроз – развивается в результате комплексного воздействия эластазы, фосфолипазы и трипсина. Протеолиз сопровождается накоплением гистидина в поджелудочной железе и превращением его в гистамин. Гистамин усугубляет нарушение кровообраще- ния, вызывая паралич капилляров. Освободившиеся из разрушенной ткани железы калликреин вместе с трипсином расщепляет белки крови, освобождая из альфа-глобулиновой фракции брадикинин и каллидин. Брадикинин, каллидин и гистамин являются теми биологическими агентами, под влиянием которых происходят изменения периферической и центральной гемодинамики на фоне нарушения обмена веществ. Нарушение гемодинамики вначале может носить гипердинамический характер, когда отмечается некоторое увеличение минутного объ ема сердца (МОС), центрального венозного давления (ЦВД) и артериального давления на фоне учащения пульса и повышения периферического сосудистого сопротивления. Уже в этот период начинает уменьшаться объ ем циркулирующей крови (ОЦК) преимущественно за сч ет плазмы в результате от ека межуточной ткани, развития перитонита, динамической кишечной непроходимости, экссудации в забрюшинную клетчатку и плевральную полость и интерстициальную ткань легких. При геморрагическом панкреонекрозе уменьшается и объ ем циркулирующих эритроцитов (ОЦЭ)[2].
Нарушение гемодинамики, как правило, сочетается с болевым синдромом. Боль возникает при от еке и пере-растяжении капсулы поджелудочной железы, раздражении нервно-рецепторных окончаний при повышении давления в е е протоках. Болевым синдромом сопровождается также вовлечение в процесс брыжейки поперечной ободочной кишки и малого сальника. Боль провоцирует выброс катехоламинов, которые также вызывают расстройство микроциркуляции что усугубляет централизацию кровообращения. Гиповолемия сопровождает это заболевание с первых часов и приводит к уменьшению ОЦК на 30-50% при продолжающемся увеличении периферического сосудистого сопротивления.
Снижение АД может стать причиной развития коронарной недостаточности с характерным изменениями на ЭКГ: снижением интервала S-T, появлением отрицательного или двухфазного зубца Т. При токсическом поражении сердечной мышцы могут появиться стойкие нарушения сердечного ритма и снижение сердечного выброса. Кроме того, в условиях ишемии и снижения кровотока поджелудочная железа продуцирует кардиодепрессивный фактор, угнетающий сократительную способность миокарда.
Нарушение гемодинамики тесно связано с расстройством водно-солевого обмена. Причиной водно-электролитных
нарушений могут быть протеолиз, рвота, нарушение функций почек. Протеолиз вед ет к кратковременной гиперкалиемии вследствие выхода калия из клеток наряду с потерей метаболического азота и клеточной массы. После гиперка-лийурии наступает плазменная и клеточная гипокалиемия, которая клинически проявляется снижением сократительной способности миокарда, гладкой мускулатуры кишечника и бронхов, развитием респираторного дистресс синдрома и острой дыхательной недостаточности.
При остром панкреатите имеет место метаболический ацидоз вследствие нарушения тканевого кровообращения и накопления избытка лактата. Олигоурия первоначально носит преренальный характер и является ответом на гиповолемию и гипотонию, затем в стадии токсической дистрофии паренхиматозных органов на фоне грубых структурных изменений в почках в виде нефрозонефрита и некроза канальцев переходит в ренальную олигоурию.
Нарушения белкового обмена при панкреонекрозе выражается в появлении гипопротеинемии и диспротеинемии за сч ет уменьшения содержания альбуминов и некоторого увеличения количества α1-, α2- и γ-глобулинов. Эти изменения вызваны действием протеолитических ферментов и иммунологическими нарушениями в организме.
При остром панкреатите и панкреонекрозе происходят нарушения и в системе гемостаза, которые находятся в прямой зависимости от тяжести основного патологического процесса. Так, при от ечной форме панкреатита наблюдается гиперкоагуляция, которая носить обратимый характер, не проявляться клинически, в этот период эффективна консервативная терапия. При стеатонекрозе и геморрагическом панкреонекрозе имеет место массивное поступление в кровь тканевого тромбопластина и ферментов ПЖ с
появлением клинических и лабораторных признаков ДВС - синдрома. Диагностика и лечение ДВС-синдрома при панкреонекрозе крайне затруднительна, так как его развитие обусловлено сложными нарушениями в гемостазе и калликреин-кининовой системе [8].
Вторая фаза острого панкреатита связана с развитием "поздних" постнекротических инфекционных осложнений. В этот период основу патогенеза составляет качественно новый этап формирования системной воспалительной реакции в виде септического (инфекционно-токсического) шока и септической полиорганной недостаточности. Наибольшая летальность зарегистрирована после первой недели от начала заболевания, преимущественно за счет развития инфицированного панкреонекроза, при котором летальность варьирует от 40 до 70% [7]. Средняя частота инфицирования при панкреонекрозе составляет 40-70 %. Инфицированные формы некроза выявляют у 24 % больных на 1-й неделе заболевания, у 36 % - на 2-й, у 71 % - на 3-й и у 47% больных - на 4-й неделе заболевания [2]. Удаленные на операции некротические ткани в 75% инфицированы грамотрицательными бактериями. что обусловлено транслокацией условно-патогенной микрофлоры эндогенного (внутрикишечного) происхождения [1, 3].
Материалы и методы исследования
Нами проведен анализ лечения 386 больных с панкрео-некрозом в возрасте от 19 до 86 лет. Острый стерильный панкреонекроз в фазе токсемии был у 63% пациентов, не-инфицированный инфильтрат – у 37%, инфицированный панкреонекроз - у 22% (84 больных). У 211 больных выполнены операции по поводу ферментативного панкреатогенного перитонита и гнойных осложнений. Операции носили преимущественно малоинвазивный характер
Алгоритм обследования включал: оценку тяжести эндотоксикоза (лейкоцитарный индекс интоксикации, индекс сдвига нейтрофилов, уровня мочевины, амилазы крови, миоглобина, альбуминсвязывающей способности плазмы, прокальцитонина, IgG, IgM, IL 6 и 10, С-реактивного белка, эластазы трипсиноген-активирующего белка фагоцитарная активность), оценку нарушения функций печени, почек и повреждения поджелудочной железы (печеночные трансферазы, билирубин, щелочная фосфатаза, лактатдегидрогеназа, мочевина, альбумин, фибриноген, тромбоциты, креатинин, уровни натрия и калия, почасовой диурез, ультразвуковое исследование, допплерография, компьютерная томография), динамический илеус характеризовал моторно-эвакуаторную и всасывательную активность кишечника в динамике заболевания.

о отечный панкреатит
■ стерильный панкреонекроз
а инф ицированный панкреонекроз
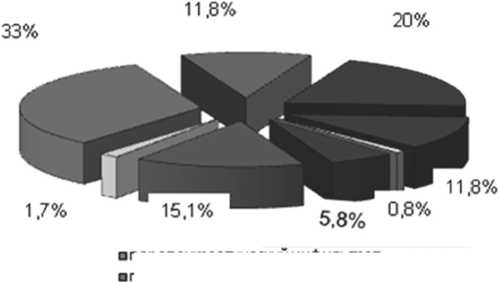
парапаньреатическии инфильтрат п ан кр еатогенный аб сцесс афер мен тативный перитонит
■флегмона забрюшинной клетчатки
□арро зивное кровотечение а мех ан и ческа я же лтуха
■псевдо киста
□ ди гестивные свищи
Проведен анализ лечения 386 больных с острым панкреатитом в возрасте от 19 до 86лет (мужчин-67%, женщин-33% МГМСУ>20, APACHE 15211, RansonaS).
Тяжесть общего состояния пациентов при этом дополнительно уточняли по шкалам SAPS II, APACHE II, тяжесть органных расстройств – по шкале SOFA, прогноз при поступлении – по шкале Ranson. Контрольная группа (n=100) набрана ретроспективно, адекватная по полу, возрасту и нозологии.
Результаты
По шкале Ranson до 5 баллов при поступлении было у 43% больных, 5-6 баллов – у 48%, 7 баллов и более – у 9%. Нарушения функций печени и почек различной степени тяжести до и после операций выявлены у 243 (63%) больных. У 68% с тяжелым эндотоксикозом (2-3степень) выявлено нарушение функций и других жизненно важных органов. Наиболее тяжелая печеночно-почечная дисфункция выявлена у лиц пожилого и старческого возраста, с предсу-ществующей печеночно-почечной патологией, у больных сахарным диабетом и у лиц с эндотоксикозом 2-3 степени. При поступлении выполняли установку назоэнтерального зонда для энтерального лаважа, стимуляции кишечника и энтеральной нутритивной коррекции. В качестве стартовой терапии в зависимости от тяжести состояния назначались карбапенемы, фторхинолоны II и III поколений, антиоксиданты, низкомолекулярные гепарины (клексан, фраксипа-рин, фрагмин), профилактика синдрома интраабдоминаль-ной гипертензии, защита слизистых оболочек, гепато- и нефропротекция, коррекция центральной гемодинамики и микроциркуляторных расстройств. Перевод на ИВЛ осуществляли при ИО ниже 260% и клинических проявлениях дыхательной недостаточности и психомоторного возбуждения.. Эфферентную терапию выполняли на аппаратах Prisma и PrismaFlex(Gambro), Multifiltrat, Acvarius для субституции применяли растворы Prismasol 4.
Результаты исследования
У пациентов группы наблюдения эфферентная терапия проводилась в упреждающем режиме при средней и тяжелой степени тяжести(APACHE II≥15). Плазмаферез и(или) плазмообмен проводили вначале 1-2 сеанса при выведении из токсической фазы (в среднем 0,5 объема циркулирующей
Динамика параметров крови при раннем применении ЭКД у групп риска
|
Основная группа |
||
|
Параметры |
До ЭКД (М± σ , р < 0,05) |
После ПФ (М± σ , р < 0,05) |
|
Клнический анализ |
||
|
Лейкоциты |
19,50 ±3,82 |
8,28 ±2,11 |
|
Нейтрофилы |
81,38 ±7,46 |
69,87 ±7,21 |
|
Контроль 1 |
||
|
Параметры |
До ЭКД (М± σ , р < 0,05) |
После ГФ и ГДФ (М± σ , р < 0,05) |
|
Клнический анализ |
||
|
Лейкоциты |
15,90 ±3,82 |
8,28 ±2,11 |
|
Нейтрофилы |
79,26 ±7,46 |
70,33 ±7,21 |
|
Контроль 2 без ЭКД |
||
|
Параметры |
Исходно (М± σ , р < 0,05) |
На третьи сутки (М± σ , р < 0,05) |
|
Клнический анализ |
||
|
Лейкоциты |
14,80 ±3,82 |
23,28 ±2,11 |
|
Нейтрофилы |
67,16 ±7,46 |
87,15 ±7,21 |
Динамика параметров крови при раннем применении ЭКД у групп риска
|
Основная группа |
||
|
Параметры |
До ЭКД (М± σ , р < 0,05) |
После ПФ (М± σ , р < 0,05) |
|
Биохимический анализ |
||
|
О. белок |
54,32±6,81 |
63,25±5,42 |
|
Альбумин |
30,03±5,43 |
40,05±3,25 |
|
АЛТ |
195,33±9,67 |
47,5±5,86 |
|
АСТ |
128,86±21,54 |
31,43±431 |
|
ЛДГ |
497,02±29,83 |
195,62±9,68 |
|
КФК |
401,24±45,22 |
76,54±12,35 |
|
Амилаза |
899,25±122,89 |
52,42±5,78 |
|
О. билирубин |
47,63±5,68 |
11,69±2,43 |
|
Контроль 1 |
||
|
Параметры |
До ЭКД (М± σ , р < 0,05) |
После ГФ и ГДФ (М± σ , р < 0,05) |
|
Биохимический анализ |
||
|
О. белок |
57,32±6,81 |
6,25±5,42 |
|
Альбумин |
32,03±5,43 |
35,05±3,25 |
|
АЛТ |
95,33±9,67 |
78,5±5,86 |
|
АСТ |
188,86±21,54 |
90,43±4,31 |
|
ЛДГ |
397,02±29,83 |
295,62±9,68 |
|
КФК |
381,24±45,22 |
116,54±12,35 |
|
Амилаза |
799,25±122,89 |
236,42±5,78 |
|
О. билирубин |
27,63±5,68 |
18,69±2,43 |
|
Контроль 2 без ЭКД |
||
|
Параметры |
Исходно (М± σ , р < 0,05) |
На третьи сутки (М± σ , р < 0,05) |
|
Биохимический анализ |
||
|
О. белок |
59,32±6,81 |
53,25±5,42 |
|
Альбумин |
32,03±5,43 |
29,05±3,25 |
|
АЛТ |
115,33±9,67 |
147,5±5,86 |
|
АСТ |
140,86±21,54 |
231,43±4,31 |
|
ЛДГ |
397,02±29,83 |
495,62±9,68 |
|
КФК |
301,24±45,22 |
476,54±12,35 |
|
Амилаза |
756,25±22,89 |
822,42±5,78 |
|
О. билирубин |
29,63±5,68 |
41,69±2,43 |
|
Показатель |
Основная группа (n=58). Лечение с соблюдением выше приведенной схемы и ранняя ЭКД |
Контроль 1 (n=123) |
Контроль 2 n=205) без ЭКД |
|
Среднее количество суток, проведенных в стационаре |
27,5±9,6 |
32,1 ±8,4 |
48,9 ±10,8 |
|
Среднее количество суток, проведенное в ОРИТ |
5,2 ±2,6 |
5,8 ±1,7 |
7,1 ±3,1 |
|
Переход к ИВЛ (%) |
8,2 |
9,2 |
24,5 |
|
Летальность (%) |
7,4 |
8,457 |
26,5 |
|
Присоединение полиорганной недостаточности (%) |
12,9 |
14,0 |
29,4 |
|
Переход в фазу гнойных осложнений (%) |
20,7 |
35 |
78 |
|
Потребность в ГФ(%) |
41,4 |
100 |
– |

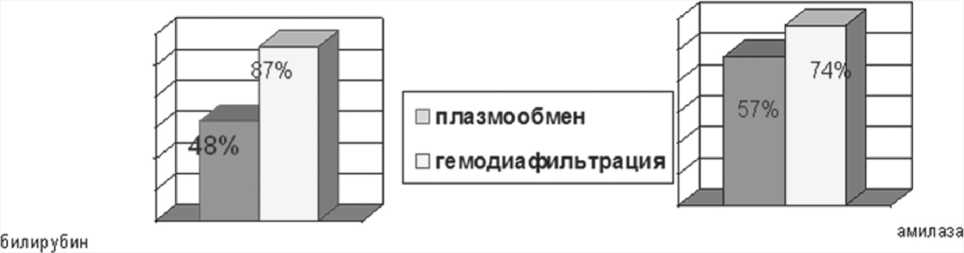
плазмы со 100% замещением свежезамороженной плазмой), далее переходили к продленной гемофильтрации или гемодиафильтрации (свыше 24 часов в дозе от 35 до 60 мл/кг до стабилизации показателей гомеостаза, выхода из токсического шока и коррекции полиорганной недостаточности). Гемодиафильтрацию выполняли при выявлении острой почечной недостаточности. Выбор метода эфферентной терапии и его объем зависел от тяжести гомеостатических нарушений – выраженности эндотоксикоза, уровня амилазы, тяжести коагулопатии, а также превалирования печеночной или почечной дисфункции.
У 56 больных методы экстракорпоральной детоксикации применяли с первых суток после поступления при APACHE II≥15. В контрольной группе эфферентные методы применяли при наличии почечных показаний по общепринятой методике, преимущественно в интермитирующем режиме. Результаты клинических и биохимических исследований у больных с острым панкреатитом при проведении пато-гениетически подобранных методов экстракорпоральной гемокоррекции свидетельствуют о эффективном снижении активности ферментных систем протеолиза, улучшении иммунного статуса, протеиназно – ингибиторного баланса, в регрессе отека стенок кишечника, ткани пожделудочной железы, почечной паренхимы, забрюшинной клетчатки, уменьшения выпота в брюшной полости (документировано исследованиями КТ и УЗИ в динамике). Клинически это проявлялось в регрессе полиорганной недостаточности; отказе от вазопрессорной поддержки в среднем через 6-8 часов от начала экстракорпоральной гемокоррекции, улучшении оксигенирующей функции легких (увеличение респираторного индекса на 30% к концу первых суток), в исчезновении признаков почечной дисфункции у 70% пациентов к концу вторых суток проведения экстракорпоральной гемокоррекции, в восстановлении пассажа илеуса и функции кишечника к концу четвертых суток. Изменения в системе гемостаза носили разнонаправленный характер, были статистически не достоверны и не отражали истинных изменений в системе гемостаза поэтому в основном ориентировались на клинические проявления нарушений в системе гемостаза, а в последний год на изменения ТЭГ.
Средний койко-день в реанимационном отделении составил 5,2±2,6суток, в контрольной группе(2) -7,1±3,1. Общая летальность в основной группе составила 7,4%, послеоперационная летальность - 15,6%; в контрольной группе(2) общая летальность -10%, послеоперационная - 26%.
Выводы
Применение патогенетически направленной терапии в сочетании с ранней патогенетически подобранной комбинацией методов экстракорпоральной детоксикации , а так же дифференцированный подход к ее применению позволяет улучшить результаты лечения панкреатогенного эндотоксикоза и снизить прогрессирование органной недостаточности и летальность. Анализ коагулограммы не отражает реальное состояние системы гемостаза при данной патологии. Применение плазмафереза в объеме 0,5 ОЦП позволяет эффективно провести коррекцию гемостаза и добиться клинически значимого эффекта.
Мы планируем продолжить наши исследования у данной категории пациентов с использованием новых технологий высокопроницаемых мембран и сорбентов.
Список литературы Экстракорпоральная гемокоррекция в комплексной терапии деструктивного панкреатита
- Гельфанд. Е.Б. Гологорский В.А. Гельфанд Б.Р. Клиническая характеристика абдоминального сепсиса у хирургических больных//Consilium medicum. 2000. № 1. С. 231-237.
- Савельев В.С. Филимонов М.И. Гельфанд Б.Р. Бурне-вич С.З. Деструктивный панкреатит: алгоритм диагностики и лечения (проект)//Consilium medicum 2001. Том 3. N 6. С. 273-279.
- Петрищев Н.Н. Беркович О.А. власов Т.д. Диагностическая ценность определения десквамированных эндотелиальных клеток в крови//Клин. лаб. диагностика. 2001. № 1. С. 50-52.
- Савельев В.С. Гельфанд Б.Р. Гологорский В.А. Системная воспалительная реакция и сепсис при панкреонекрозе//Анест. и реанимат. 1999. № 6. С. 28-33.
- Гельфанд Е.Б. Гологорский В.А. Гельфанд Б.Р. Абдоминальный сепсис: интегральная оценка тяжести состояния больных и полиорганной дисфункции//Анестезиология и реаниматология 2000;№3;с 29-34.
- Neoptolemos J.P. Raraty M. Finch M. Sutton R. Acute pancreatitis: the substantial human and financial costs//Gut. 1998. Vol. 42. P. 886-891.
- Tenner S. Banks P. Acute pancreatitis: nonsurgical management.//World J Surg 1997; 21: 143-8.
- Rau B. Uhl W. Buchler M.W. Beger H.J. Surgical treatment of infected necrosis.//world j Surg 1997; 21: 155-61.
- Beger H.G. Bittner R. Buchler M. Bacterial contamination of pancreatic necrosis//Gastroenterology 1986; 91(2): 433-8.
- Bradley E.L.III. A clinically based classification system for acute pancreatitis. Summary of the international symposium on acute pancreatitis. Atlanta. Ga. september 11-13. 1992; 586-590.
- John R Prowle. Antoine Schneider and Rinaldo Bellomo. Clinical review: Optimal dose of continuous renal replacement therapy in acute kidney injury Prowle et al. Critical Care 2011. 15:207 http://ccforum.com/content/15/2/207.
- Berger Hans G. Rau Bettina M. Severe acute pancreatitis: Clinical course and management. world j Gastroenterol 2007. October 14; 13(38): 5043-5051.


