Электрофорез белков биоконсервированной крови
Автор: Бубеев А.Т., Данилова Т.Е., Цыренов В.Ж.
Журнал: Вестник Восточно-Сибирского государственного университета технологий и управления @vestnik-esstu
Статья в выпуске: 1 (32), 2011 года.
Бесплатный доступ
Методом электрофореза исследовано состояние белков крови убойных животных при обработке ее высококислотной молочной сывороткой. Показано, что в результате автолитических процессов и воздействия молочной кислоты наблюдается денатурация белков крови.
Биоконсервированная кровь убойных животных, молочная сыворотка, белки плазмы, lactobacillus acidophilus 20т
Короткий адрес: https://sciup.org/142142282
IDR: 142142282 | УДК: 637.661:66.099.4:543.545
Electrophoresis of bioconserved blood proteins
The article describes electrophoresis method processing of blood proteins of slaughtered animals which is processed by highly acidic whey. It is shown that as a result of autolytic processes and effects of lactic acid the denaturation of blood proteins is observed.
Текст научной статьи Электрофорез белков биоконсервированной крови
Одним из интенсивных путей расходования компонентов аминокислотного пула организма является синтез белков плазмы крови, принимающих участие в поддержании рН, вязкости, коллоидноосмотического давления, уровня катионов крови, транспорте гормонов, липидов, жирных кислот, пигментов, жирорастворимых витаминов, свертывании крови, иммунных и других процессах.
Плазма крови содержит свыше 300 белков. Большинство белков плазмы - гликопротеины, количество углеводных компонентов в их составе варьирует от 1%, например, в альбуминах до 40% - а 1 -глобулинах. Белки плазмы содержат дисульфидные связи и небольшое количество свободных тиоловых (-SH) групп: предполагают, что это имеет большое значение для предотвращения денатурации белков в плазме, которая возможна вследствие высокого парциального давления кислорода.
Исследования белков плазмы организма, кроме специфической нозологической информации, дают определенное представление о состоянии белкового обмена в целом. Исследованию подлежат количественные и качественные характеристики белкового состава плазмы.
Концентрация белков плазмы определяется тремя основными факторами: скоростью синтеза, скоростью метаболизма и объемом жидкости, в котором распределены белки.
В настоящее время различными методами можно получить от 5 до 100 фракций белков плазмы [1].
С помощью электрофореза выделяют 6 стандартных фракций: альбумины и четыре фракции глобулинов (α 1 -, α 2 -, β 1 -, β 2 -, и γ- ). Соотношение этих основных белковых фракций в сыворотке крови следующее (%): альбумин – 56-60, α 1 -глобулин – 4-5, α 2 -глобулины - 8, β-глобулины – 12, фибриноген – 4, γ- глобулины – 16 [2].
Каждая фракция содержит многочисленные индивидуальные белки, среди которых имеются белки как свертывающей, так и противосвертывающей систем.
Цель работы: исследование влияния компонентов молочной сыворотки на белковую систему биоконсервированной крови.
Задачи эксперимента:
-
1. Провести электрофоретические исследования динамики состояния биоконсервированной крови в динамике хранения.
-
2. Установить наличие изменений в белковой системе биоконсервированной крови.
-
3. Сделать сравнительный анализ протеинограмм молочной сыворотки, биоконсервированной и стабилизированной крови.
Объекты исследования: Кровь, стабилизированная фосфатами (КСФ), биоконсервированная кровь (БК), высококислотная молочная сыворотка (МС), полученная в результате ферментирования обезжиренного молока культурой Lactobacillus acidophilus.
Методы исследования: электрофоретические исследования проводили на автоматическом анализаторе крови и ее компонентов фирмы Cormay [3].
Результаты эксперимента . БК получали путем смешивания изъятой из кровеносных сосудов крови убойных животных с ферментированной сывороткой. Стабилизированную таким образом кровь хранили в течение 20 суток при температуре плюс 4 – плюс 60С. Результаты электрофоретических исследований белковой системы биоконсервированной крови представлены в таблице 1 и на рисунках 1-6.
Из таблицы 1 и рисунков 1,2,3,4,5 видно, что фракции альбуминов, α 1 -, α 2 -, β 2 -, γ- глобулинов имеют тенденцию к уменьшению. В данном случае возможен протеолиз белков собственными ферментами. Вероятно, и молочная кислота оказывает определенное влияние на распределение белковых фракций.
В норме альбумин синтезируется в печени и его период полураспада составляет около 20 суток. Следовательно, постепенное уменьшение фракции альбуминов в изучаемой системе связано с отсутствием процессов пополнения их пула (процессов синтеза) и воздействием молочной кислоты, что существенно влияет на скорость их естественного распада.
Таблица 1
Изучение белковых фракций БК в процессе хранения при 4 - 6ºС
|
Наименование фракции |
Содержание белковых фракций, г/л |
||||||
|
МС |
КСФ |
БК, сроки хранения, сут |
|||||
|
0 |
6 |
13 |
17 |
20 |
|||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
альбумины |
1,25±0,21 |
5,6±0,55 |
12,36± 0,91 |
11,40± 1,10 |
3,51± 0,59* |
2,78± 0,55* |
0,02± 0,01* |
|
α1-глобулины |
0,52±0,020 |
0,08±0,01 |
5,61± 0,78 |
1,11± 0,18* |
0,10± 0,02* |
0,13± 0,02* |
0,66± 0,07* |
|
α2-глобулины |
0,25±0,050 |
0,44±0,06 |
6,67± 0,32 |
1,79± 0,06* |
11,7± 0,64* |
0,65± 0,07* |
0,29± 0,075* |
|
β1-глобулины |
0,38± 0,040 |
15,97±2,72 |
5,3± 1,05 |
2,02± 0,016* |
14,2± 0,38* |
29,2± 5,40* |
38,13± 0,88* |
|
β2-глобулины |
1,07± 0,025 |
68,90±8,90 |
21,9± 3,89 |
2,36± 0,36* |
1,27± 0,09* |
1,56± 0,16* |
1,10± 0,13* |
|
γ- глобулины |
1,86±0,56 |
6,35±2,30 |
10,6± 10,36 |
9,66± 1,62 |
1,70± 0,25* |
2,70± 0,09* |
2,77± 0,29* |
|
белок |
5,3±0,18 |
97,40±11,12 |
62,1± 11,9 |
28,40± 1,50* |
32,5± 2,90* |
37,0± 1,17* |
46,20± 1,80* |
Обозначение: * - достоверно при р ≤ 0,05
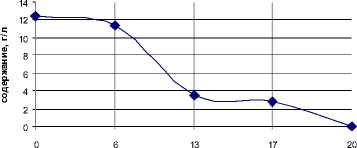
время, сут ал ьбумины
Рис. 1. Изменения содержания альбуминов в БК в процессе хранения при t =4 - 6˚С
Анализируя данные таблицы 1, можно обнаружить наличие в процессе хранения белковой системы БК локального увеличения α 1 -глобулинов (рис. 3) и стабильного возрастания - β 1 -глобулинов (рис. 4). Вместе с тем параллельно наблюдается общая тенденция изменения фракций α 1 -, α 2 -глобулинов в сторону уменьшения.
Учитывая тот факт, что кровь в присутствии молочной сыворотки не свертывается, можно предположить образование комплексов между белками фракций α 1 -, α 2 -глобулинов, а именно α 1 -антитрипсином и α 2 -макроглобулином, с плазминогеном.
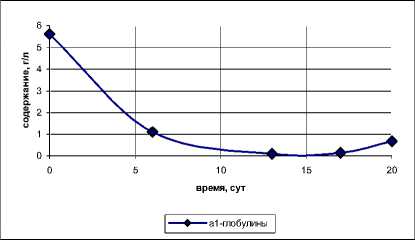
Рис. 2. Изменения содержания α 1 -глобулинов в БК в процессе хранения при t =4 - 6˚С
Кроме того, известно, что в состав а 1 -глобулинов входят гаптоглобины, которые составляют 25% от всего их содержания. Эта группа белков плазмы крови связывает свободный гемоглобин с образованием комплексов. В живых организмах данный комплекс метаболизируется в ретикуло-эндотелиальной системе, что необходимо для предотвращения потерь железа и повреждения почек гемоглобином [1]. Следовательно, низкие уровни α 1 -глобулинов могут быть обусловлены также снижением в их составе гаптоглобинов, которые при гемолизе связывают гемоглобин. Наличие гемолиза в изучаемой системе обнаружено на 4-е сутки.
Резкое увеличение α 2 -глобулинов (рис. 3) на 13-е сутки хранения, возможно, связано и с автолизом клеток Lactobacillus acidophilus. Снижение клеток Lactobacillus acidophilus установлено на 5-е сутки.
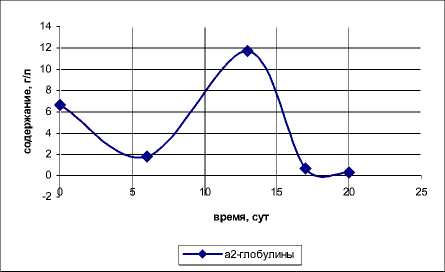
Рис. 3. Изменения содержания α 2 -глобулинов в БК в процессе хранения при t =4-6˚С
Как уже указывалось выше, в процессе хранения имеет место стабильное увеличение содержания только фракции β 1 - глобулинов (рис. 4).
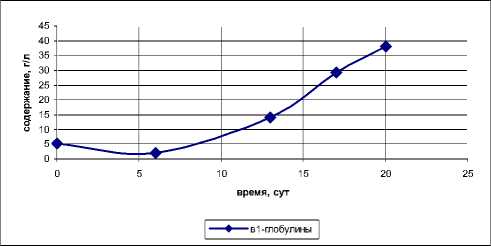
Рис.4. Изменения содержания β 1 -глобулинов в БК в процессе хранения при t =4 - 6˚С
К фракциям β 1 -глобулинов относятся трансферрин, гемопексин [4], которые характеризуют интенсивность процессов распада гемоглобина. Так, in vivo гемопексин (β-глобулин) связывает гем и предотвращает его выделение почками. Сродство гемопексина к гему значительно выше, чем у альбумина. Комплекс гем-гемопексин поступает из крови в печень, где освобождается Fe3+ для образования гемоглобина [1]. Трансферрин, связывая свободный гем, также поступает на деструкцию или ресинтез гемоглобина. То есть накопление и устойчивость гем- β-глобулиновых комплексов также способствует высокому уровню данной фракции (β 1 -глобулинов) к 20 суткам хранения БК.
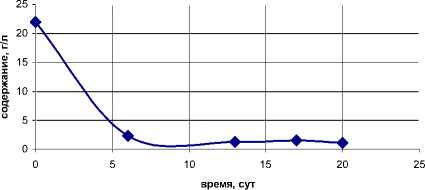
Снижение фракции β 2 - глобулинов (рис. 5) согласуется с результатами проведенных исследований коагуляционной и фибринолитической систем БК [5], которые показали достоверное уменьшение содержания основного белка свертывания крови - фибриногена. Данный белок имеет заряд и молекулярную массу, позволяющие отнести его к фракциям β 2 - глобулинов.
в2-глобулины
Рис. 5. Изменения содержания β 2 -глобулинов в БК в процессе хранения при t=4-6˚С
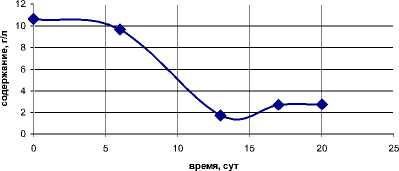
Наиболее значительная в количественном отношении фракция белков молочной сыворотки – это фракция иммуноглобулинов. Снижение исходного содержания γ- глобулинов молочной сыворотки и БК в процессе хранения свидетельствует, вероятно, об их связывании с антигенными детерминантами клеток крови и последующей биодеградации комплексов (рис. 6).
y-глобулины
Рис. 6. Изменения содержания γ -глобулинов в БК в процессе хранения при t =4 - 6˚С
Таким образом, исследования электрофоретической подвижности белков БК показали следующие изменения белкового профиля: уменьшение альбуминов и большинства глобулиновых фракций, за исключением фракции β 1 -глобулинов, которая претерпевает резкое избирательное увеличение.
Выводы
-
1. Определена динамика распределения общего белка биоконсервированной крови по отдельным белковым фракциям.
-
2. Установлено изменение профиля электрофореграмм биоконсервированной крови под действием компонентов высококислотной сыворотки.
-
3. Показано наличие процессов комплексообразования и денатурации белков биоконсервирован-ной крови.


