Кинетика высвобождения сульфаниламида из полимерного композита на основе акрилового гидрогеля и детонационных наноалмазов
Автор: Григорьев Д.В., Гудкин А.В., Хоманец Е.В., Успенская М.В., Олехнович Р.О., Сивцов Е.В.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 4 (102) т.86, 2024 года.
Бесплатный доступ
Методом радикальной полимеризации получен полимерный композиционный материал на основе акриловых гидрогелей и детонационных наноалмазов медицинского назначения, содержащий лекарственное вещество сульфаниламид, способный стать заменой традиционным перевязочным средствам. Изучена кинетика набухания синтезированного гидрогеля. Предложены математические модели, которые наилучшим образом описывают процесс десорбции сульфаниламида и кинетику набухания материала. На основе результатов исследований для описания процесса набухания была выбрана модель псевдовторого порядка. Методом УФ-спектроскопии изучена кинетика высвобождения сульфаниламида на основании анализа зависимости концентрации выделяемого лекарственного вещества от времени. Сделано предположение о механизме процесса десорбции лекарственного вещества из гидрогелевой матрицы. В ходе эксперимента была рассчитана максимальная доля высвободившегося из полимерной матрицы сульфаниламида (она составила 91%). Время выхода зависимости доли выделившегося лекарства от времени на плато составило 24 часа. На основе полученных данных сделано предположение о возможности создания пролонгированной формы сульфаниламида на основе синтезируемого композиционного материала. Для описания процесса релиза была выбрана модель Корсмаера-Пеппаса на основе наибольшего коэффициента детерменирования. Подобраны значения pH соответствующие разным стадиям течения раневого процесса (7,9, 7,2, 5,8). Изучено влияние pH на кинетику релиза сульфаниламида и на параметры процесса набухания гидрогелевого материала. Методами осцилляционной реометрии исследованы механические свойства синтезированных гидрогелей. Получены зависимости динамических модулей от амплитуды и частоты. Показано влияние наполнителя (детонационных наноалмазов) и лекарственного вещества на значения динамических модулей.
Полимерные композиционные материалы, акриловые гидрогели, детонационные наноалмазы, перевязочные материалы, сульфаниламид, кинетика высвобождения
Короткий адрес: https://sciup.org/140309688
IDR: 140309688 | УДК: 678.744.32+678.745.842 | DOI: 10.20914/2310-1202-2024-4-230-238
Kinetics of sulphanilamide release from polymer composite material for medical purpose based on acrylic hydrogels and detonating nanodiamonds
A polymer composite material for medical use was obtained, using the method of radical polymerization, based on acrylic hydrogels and detonation nanodiamonds, containing the drug sulfanilamide, which can become a replacement for traditional dressings. The swelling kinetics of the synthesized hydrogel was studied. Mathematical models that best describe the process of sulfonamide desorption and swelling kinetics have been proposed. Based on the research results, a pseudo-second order model was chosen to describe the swelling process. The kinetics of sulfonamide release was studied using UV spectroscopy based on an analysis of the dependence of the concentration of the released drug on time. An assumption has been made about the mechanism of the process of desorption of a medicinal substance from a hydrogel matrix. During the experiment, the maximum proportion of sulfonamide released from the polymer matrix was calculated (it amounted to 91%). The time for the dependence of the proportion of released drug on time to reach a plateau was 24 hours. Based on the data obtained, an assumption about the possibility of creating a prolonged form of sulfonamide based on the synthesized composite material was made. The Korsmaier-Peppas model was chosen to describe the release process based on the highest coefficient of determination. pH values were selected corresponding to different stages of the wound process (7.9, 7.2, 5.8). The effect of pH on the kinetics of sulfonamide release and on the swelling of the hydrogel was studied. The mechanical properties of hydrogels were studied using oscillatory rheometry methods. The dependences of the dynamic modules on amplitude were obtained. The influence of the filler (detonation nanodiamonds) and the drug substance on the values of dynamic moduli is shown.
Текст научной статьи Кинетика высвобождения сульфаниламида из полимерного композита на основе акрилового гидрогеля и детонационных наноалмазов
На сегодняшний день известно большое количество заболеваний, которые вызывают повреждения кожи (микозы, пиодермии, псориаз) [1–2]. Для их местного лечения используются традиционные лекарственные формы (мази, порошки, кремы), применение которых, в сочетании с классическими бинтовыми повязками, имеет ряд существенных недостатков. Перевязка ран доставляет боль и дискомфорт из-за присыхания бинтовой повязки к ране. Кроме того, чаще всего, наблюдается взрывной характер высвобождения лекарственного вещества (ЛВ): препарат достигает своей пиковой концентрации в течение 2 часов и далее снижается.
В связи с этим в настоящее время создание перевязочных материалов, не обладающих перечисленными недостатками, является актуальной задачей [3–4]. Кроме того, особое внимание в медицине уделяется материалам с контролируемыми физико-механическими и сорбционными характеристиками [5–6]. Один из вариантов таких систем – это акриловые гидрогели (АГ). АГ широко изучены и могут быть использованы как нетоксичные, относительно дешевые, обладающие высокой сорбционной емкостью полимерные матрицы [7–8]. Материалы на их основе находят применение в медицине в качестве раневых повязок, изолирующих рану от внешней среды и создающих барьер для микроорганизмов, оставаясь проницаемыми для кислорода. При этом АГ характеризуются низкими физикомеханическими свойствами и не обладают собственной биологической активностью. Для улучшения эксплуатационных характеристик гидрогелевого материала можно использовать активный наполнитель, способный взаимодействовать с полимерной матрицей гидрогеля.
В представленной работе в качестве такого наполнителя был выбран дисперсный неорганический филлер – детонационные наноалмазы (ДНА), которые характеризиру-ются химической стойкостью алмазного ядра, активностью периферической оболочки и сверхтвердостью [9]. В зависимости от вида обработки на поверхности ДНА могут присутствовать различные функциональные группы, в частности, -NH2, -OH, -COOH, -NO2 и др. [10]. Наличие такого разнообразия функциональных групп на поверхности наполнителя открывает возможность конъюгации ДНА с полимерами и ЛВ. Известно, что ДНА могут быть использованы в качестве носителя ЛВ [11]. Кроме того, ДНА проявляют антимикробную и антимикотическую активность, поскольку усиливают генерацию активных форм кислорода, подавляя проникновение вирусов и бактерий в клетки, а также нарушают жизненный цикл вирусов и рост микромицетов [12].
В то же время ДНА могут значительно улучшить механические характеристики гидрогелей, именно поэтому использование ДНА в качестве наполнителя может стать ключом к одновременному повышению физико-механических свойств гидрогелевого материала и приданию ему биологической активности, необходимой для медицинского применения.
Для придания целевой терапевтической активности в структуру гидрогеля необходимо включить ЛВ. Нами был выбран сульфаниламид (СФА), обладающий бактериостатическим эффектом [13]. СФА активен в отношении грамположительных и грамотрицательных кокков и уже долгое время успешно применяется в составе комплексной терапии при воспалительных процессах на коже и инфицированных ожогах в виде порошка [14].
Цель работы – получение и исследование свойств полимерного композиционного материала медицинского назначения на основе акрилового гидрогеля и ДНА, содержащего сульфаниламид.
Материалы и методы
Синтез гидрогелевого композита. Акриловую кислоту (АК) марки ч. производства ЗАО «Вектон», перегоняли и хранили в холодильнике. Акриламид (АА) марки ч., тетраэтил-метилендиамин (ТМЕД) марки ч. и персульфат аммония (ПСА) марки ч. производства Sigma
Aldrich использовали без дополнительной подготовки. N,N-метиленбисакриламид (МБА) производства ЗАО «Вектон» марки ч. хранили в холодильнике. СФА использовали в виде порошка.
Акриловый композит, содержащий ДНА и СФА, получен методом радикальной полимеризации в водной среде. Для этого, в заранее нейтрализованную гидроксидом натрия (степень нейтрализации 0,8) АК добавляли АА в эквимолярном соотношении. В качестве инициатора полимеризации использовалась окислительновосстановительная система: ТМЕД и ПСА в виде 2 масс. % водных растворов при соотношении ТМЕД:ПСА = 2:1. В качестве сшивающего агента выступал МБА концентрацией 0,2 масс %. ДНА предварительно дробили в ультразвуковой ванне в воде. К суспензии ДНА концентрацией 0,5 масс. % от массы мономеров добавляли 0,27 масс % СФА. Полимеризация проводилась при 45 ℃ в течение 2 часов.
Изучение набухания акриловых композитных гидрогелей. Набухание гидрогелей и релиз СФА проводили в растворах фосфатных буферов с pH 7,9, 7,2, 5,8. Это связано с тем, что на разных стадиях течения раневого процесса раны обладают различным pH [15]. На стадии начала воспалительного процесса pH смещен в кислую область; на стадии регенерации и в случае хронических ран – в слабощелочную [16].
Набухание гидрогелевых материалов проводили в течение 48 часов. Степень набухания полимерного материала рассчитывали по формуле:
m - tm
Q t =------ 0 , (1)
m 0
где m – масса набухшего образца за определенный промежуток времени, г; m – масса высушенного образца.
Кинетика набухания гидрогеля описывалась следующими математическими моделями.
-
а) Модель Фика [17] характеризует процесс набухания на начальной стадии ( Qt /Q^ < 0,6 ) :
Q = kt" , (2)
Q .
где Q , Q – текущая и равновесная степени набухания, представляющие собой количество растворителя, диффундировавшего в гидрогель к текущему моменту времени t и к моменту времени, соответствующему равновесной степени набухания, отнесенное к 1 грамму сухого вещества; k – эмпирическая константа (мин -n ); n – показатель степени, определяющий тип диффузии растворителя.
-
б) Кинетическая модель псевдопервого порядка (P1P) [18]
dQ- = M Q . - Q t ) . (3)
где Q, Q – сорбционная емкость в момент времени t и предельная сорбционная емкость; k – константа скорости сорбции, (мин-1)
-
в) Кинетическая модель псевдовторого порядка (P2P) [19]
Q = ,
t 1/ k 2 Q . + t/Q .
где k – константа скорости сорбции,
(г/ммоль⋅мин).
-
г) Модель Пелега [20]
Q t = Q o +
t
, k + kit
где Q – степень набухания в момент времени t = 0; k - кинетическая константа, (мин-г/г); k – характеристическая константа, (г/г).
Высвобождение сульфаниламида . Высвобождение СФА изучали методом УФ-спектроскопии с помощью спектрометра Shimadzu UV-1800i. Спектры записывали в диапазоне 190–500 см -1 при средней скорости сканирования. Предварительно строили калибровочную прямую зависимости оптической плотности от концентрации ЛВ при длине волны 260 нм.
Кинетику релиза СФА описывали следующими математическими моделями:
Модель Хигучи, которая описывает высвобождение ЛВ из матриц как процесс диффузии, основанный на законе Фика [21].
Qt = Kh^ , (6)
где Q – количество высвобожденного лекарства; K – константа (мг/с -2 ).
-
1) Модель Бейкера–Лонсдейла, разработанная на основе модели Хигучи, позволяет привести кривую высвобождения к линейному виду [22]. K bl - = 1,5 ( 1 - ( 1 - M t /M 0 ) 0,66 ) - M t IM o , (7)
где M , M – масса вещества, выделившегося в раствор в момент времени t и в начальный момент времени; K – константа, (мин -1 ).
-
2) Модель Корсмаера–Пеппаса описывает релиз ЛВ из нерастворимой и набухающей матрицы [23].
ln Q L = " *in t + In к , (8)
p ii-oo где Q-Q, – доля препарата, высвобождаемая в момент времени t; K – константа; n – показатель степени из уравнения (2).
-
3) Модель Хопфенберга описывает релиз, учитывая геометрию молекулы ЛВ [24].
b
M t_ , k 0 * t}
— 1 — 1
M 0 I c 0 * a )
где k – эмпирическая константа, (мин -1 ) c – начальная концентрация ЛВ; b – коэффициент, учитывающий геометрию ЛВ ( b = 1, 2 или 3 для плоских, цилиндрических или сферических соответственно); a – радиус для сферы или цилиндра или половина толщины плиты для плоских ЛВ, мм.
Реологические исследования. Реологические исследования проводились с использованием реометра MCR302 Anton-Paar (Австрия, Грац). Геометрия измерительного устройства представляла собой две пластины диаметром 25 мм. Высота измерительного зазора составляла 500 мкм. Все эксперименты проводили при 25 °С. Для обеспечения одинаковой степени набухания все образцы предварительно высушивали до постоянной массы, а затем добавляли дистиллированную воду в соотношении 3 мл воды на 1 г сухого геля.
Результаты и обсуждение
Кинетика набухания гидрогелей, содержащих наноалмазы и ЛВ. Зависимости степени набухания синтезированного гелелевого материала, содержащего ДНА и ЛВ, от времени в растворах фосфатных буферов с заданным значением pH представлена на рисунке 1.
Их анализ позволил определить параметры, присутствующие в математических моделях кинетики набухания в формулах (2), (3), (4), (5) (таблица 1).
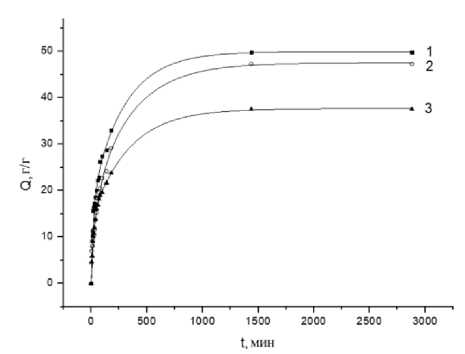
Рисунок 1. Зависимость степени набухания (Q) от времени (t) гидрогелевого композита с детонационными наноалмазами и сульфаниламидом при различных pH: 1 – pH = 7,9; 2 – pH = 7,2; 3 – pH = 5,8 Figure 1. Dependence of the degree of swelling (Q) on time (t) of a hydrogel composite with detonation nanodiamonds and sulfanilamide at different pH: 1 – pH = 7.9; 2 – pH = 7.2; 3 – pH = 5.8
Исходя из коэффициента детерминации (R 2 = 0,995) процесс набухания гидрогеля в фосфатных буферах наилучшим образом описывает модель псевдовторого порядка (Р2Р). Показатель степени n синтезированных образцов не превышает 0,5, что свидетельствует о диффузии Фика, которая описывает те случаи, когда скорость проникновения жидкости намного ниже скорости релаксации полимерной цепи. Наибольшая степень набухания 49 г/г достигается при наибольшем рН (рН равном 7,9), что объясняется взаимным отталкиванием де-протонированных карбоксильных групп полимерной цепи, которое приводит к растяжению пространственной структуры полимерной сетки.
Таблица 1.
Параметры математических моделей кинетики набухания гидрогелевого композита Table 1.
Parameters of mathematical models of swelling kinetics of hydrogel composite
|
Модель Фика Fik’s model |
Модель Пелега Peleg model |
Модель P1P P1P model |
Модель P2P P2P model |
|||||||
|
pH |
n |
k |
R 2 |
k 1 , мин ⋅ г/г |
k 2 , г/г |
R 2 |
k 1 , 1/мин |
R 2 |
k 2 , г/ммоль ⋅мин |
R 2 |
|
7,9 |
0,361 |
-0,994 |
0,957 |
0,148 |
0,081 |
0,912 |
0,0009 |
0,986 |
0,017 |
0,994 |
|
7,2 |
0,332 |
-1,168 |
0,953 |
0,153 |
0,112 |
0,936 |
0,0013 |
0,911 |
0,018 |
0,995 |
|
5,8 |
0,306 |
-1,124 |
0,929 |
0,985 |
0,042 |
0,937 |
0,0051 |
0,910 |
0,022 |
0,990 |
Примечание: n – коэффициент Фика; k, k 1 , k 2 – кинетические константы; R 2 – коэффициент детерминации
Note: n - Fick's coefficient; k, k1, k2 - kinetic constants; R2 - coefficient of determination
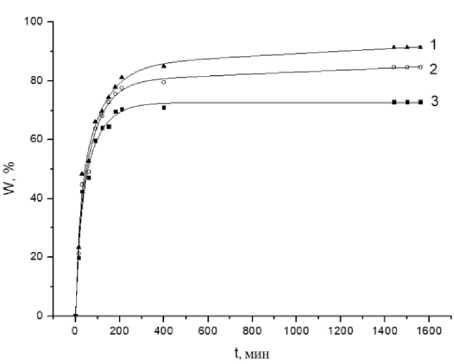
Кинетика релиза сульфаниламида из гидрогеля, наполненного наноалмазами. Зависимость доли высвободившегося СФА из гелевого композита, наполненных ДНА, от времени в фосфатно-буферных растворах представлена на рисунке 2.
t, min
Рисунок 2. Зависимость доли выделившегося сульфаниламида (W) из акриловых гидрогелевых композитов, наполненных детонационными наноалмазами, от времени (t) в различных pH: 1 – pH = 5,8; 2 – pH = 7,2; 3 – pH = 7,9
-
Figure 2. Dependence of the proportion of released sulfonamide (W) from acrylic hydrogel composites filled with detonation nanodiamonds on time (t) at different pH: 1 – pH = 5.8; 2 – pH = 7.2; 3 – pH = 7.9
Во всех изученных случаях высвобождение лекарственного средства из полученного композиционного материала можно описать экспоненциальной зависимостью. Максимальная доля выделившегося ЛВ 91% наблюдалась в кислой среде для композита, содержащего ДНА и СФА. Хорошо известно, что высвобождение сульфаниламида происходит в две стадии: первая – быстрая десорбция около 65 % ЛВ в течение 180 минут, вторая – высвобождение оставшегося ЛВ в течение 24 часов. Выход на плато предельного значения высвобождения сульфаниламида происходил через 24 часа. Стоит отметить, что наиболее полное выделение СФА происходит при pH = 5,8, см. рисунок 2, то раневые повязки, полученные на основе предлагаемых компонентов, наиболее эффективны при лечении ран на начальных стадиях воспаления.
Изучение кинетики высвобождения лекарственного средства с помощью математических моделей Хигучи, Бейкера–Лонсдейла, Корсмаера– Пеппаса, Хопфенберга (таблица2) показало, что, основываясь на значении коэффициента детерминации, процесс релиза СФА наилучшим образом описывается моделью Корсмаера–Пеппаса.
Таблица 2.
Параметры математических моделей кинетики десорбции СФА из синтезированного ПКМ в фосфатно-буферном растворе
Table 2.
Parameters of mathematical models of the kinetics of desorption of SFA from synthesized PCM in a phosphate buffer solution
|
Модель Хигучи Higuchi model |
Модель Бейкера–Лонсдейла Baker-Lonsdale model |
Модель Корсмаера–Пеппаса Korsmayer-Peppas model |
Модель Хопфенберга Hopfenberg model |
|||||
|
pH |
K h , мг/см2 |
R2 |
K bl , 1/ч |
R2 |
K p |
R2 |
k 0 , 1/ч |
R2 |
|
7,9 |
0,85×10-5 |
0,922 |
5,40×10-4 |
0,936 |
0,919 |
0,949 |
2,916 |
0,942 |
|
7,2 |
0,80×10-5 |
0,949 |
7,88×10-4 |
0,958 |
0,862 |
0,962 |
1,965 |
0,915 |
|
5,8 |
0,77×10-6 |
0,954 |
8,44×10-4 |
0,965 |
0,807 |
0,981 |
1,769 |
0,941 |
Примечание: K H , К BL , K p , k 0 – кинетические константы; R2 – коэффициент детерминации
Note: KH, KBL, Kp, k0 - kinetic constants; R2 - coefficient of determination
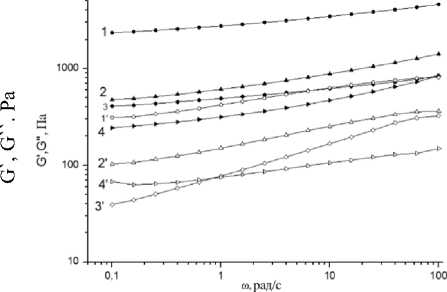
Реологические исследования. Физикомеханические характеристики полученных полимерных гидрогелевых образцов исследовали с помощью реометра в режиме осцилляции. В предварительном исследовании с амплитудной разверткой был определен диапазон линейности вязкоупругих свойств, в котором структура исследуемого полимерного образца сохраняется. Было показано, что во всех случаях линейность вязкоупругих свойств нарушалась при амплитудах выше 10% (100% соответствует углу поворота в 2,3 градуса), поэтому в осцилляционном эксперименте использовали амплитуду 1%. На рисунке 3 представлены результаты осцил-ляционного эксперимента, в ходе которого были получены зависимости динамических модулей G’ и G’’ от частоты. Значения модуля упругости акрилового гидрогелевого материала, наполненного ДНА (1, 1’), в 2 раза больше значения модуля гидрогеля без наполнителей (2, 2’). Такая разница в значениях, вероятнее всего, связана с тем, что функциональные группы на поверхности ДНА обеспечивают более сильное взаимодействие между полимерными цепями за счет образования сетки водородных связей. Значения модулей упругости полученных акриловых гидрогелей, не содержащих наполнители (2, 2’), и гидрогелей, содержащих как ДНА, так и ЛВ (3, 3’) практически одинаковы. Это может быть связано с тем, что ЛВ взаимодействует с функциональными группами на поверхности ДНА в процессе синтеза гидрогеля, что препятствует образованию дополнительных водородных связей между частицами ДНА и полимерными цепями. Таким образом, не происходит увеличения значений механических характеристик гидрогеля при введении ДНА совместно с СФА.
ω, rad/s
Рисунок 3. Зависимость динамических модулей от частоты при амплитуде 1%. Модули накопления G’ (1, 2, 3, 4), модули потерь G’’ (1’, 2’, 3’, 4’) для геля, не содержащего ДНА и сульфаниламид (2, 2’) и гелей, содержащих: только ДНА (1, 1’), и ДНА, и сульфаниламид (3, 3’), только сульфаниламид (4, 4’)
Figure 3. Dependence of dynamic modules on frequency ω at an amplitude of 1%. Accumulation modules G' (1, 2, 3, 4), loss modules G'' (1', 2', 3', 4') for a gel that does not contain DND and sulfonamide (2, 2') and gels containing: DNA only (1, 1'), and DNA and sulfonamide (3, 3'), sulfonamide only (4, 4')
В ходе реологического исследования были изучены зависимости тангенса механических потерь от частоты. Отношение модуля потерь и модуля упругости представляет собой тангенс угла механических потерь, который является мерой баланса упругих и пластичных свойств исследуемого материала. Полученные в ходе настоящего эксперимента значения тангенса механических потерь для всех гидрогелевых образцов были меньше единицы, что свидетельствует о том, что образцы больше проявляют свойства, характерные для твердого тела.
Заключение
В работе методом радикальной полимеризации в водной среде был получен полимерный композиционный материал на основе сополимера акриловой кислоты, акрилата натрия и акридамида, ковалентно сшитого N,N-метилен-бисакриламидом, наполненный детонационными наноалмазами и содержащий лекарственное вещество – сульфаниламид. Степень набухания гидрогеля ожидаемо увеличивалась при повышении значения pH. Показано, что доля высвободившегося сульфаниламида увеличивается при уменьшении pH, что позволяет рекомендовать такие полимерные материалы при лечении ран на начальных стадиях воспаления. Максимальная доля выделившегося сульфаниламида из полимерной матрицы достигает 91%. Продемонстрировано, что кинетика набухания акриловых композитов наилучшим образом описывается моделью псевдовторого порядка, а релиз сульфаниламида – моделью Корсмаера-Пеппаса. Введение ДНА и сульфаниламида оказывает существенное влияние на физико-механические свойства акриловых гидрогелевых материалов. Изучение реологических характеристик полученного гидрогелевого материала показало, что увеличение модуля упругости гидрогеля происходит в зависимости от содержания наполнителей и модификаторов в ряду: ЛВ < ДНА + ЛВ < нена-полненный гидрогель < ДНА. Основываясь на времени полного высвобождения из гидрогеля сульфаниламида, которое составляет 24 часа, можно говорить о возможности пролонгированного терапевтического эффекта при использовании полученной полимерной гидрогелевой композиции в качестве основы раневой повязки.


