Клинический случай лечения пациента с локальным поздним рецидивом фолликулярной лимфомы – узловым поражением мягких тканей левой щеки
Автор: Петровский В.Ю., Ивашин А.В., Дыкина А.В., Соловьева С.В., Гурбатова М.Д., Измайлов Т.Р.
Журнал: Вестник Российского научного центра рентгенорадиологии Минздрава России @vestnik-rncrr
Рубрика: Клинические наблюдения
Статья в выпуске: 1 т.21, 2021 года.
Бесплатный доступ
Приведен клинический случай пациента с локальным поздним рецидивом фолликулярной лимфомы IV стадии с поражением мягких тканей левой щеки. Рецидив зарегистрирован после радиологического лечения по радикальной программе с хорошими непосредственными результатами. Вопрос лечения пациентов с данной патологией имеет большое значение, так как на сегодняшний день не существует единых стандартов лечения при рецидивах заболевания.
Фолликулярная лимфома, рецидив, конформная лучевая терапия
Короткий адрес: https://sciup.org/149132164
IDR: 149132164
Clinical case of treatment of a patient with a local late recurrence of follicular lymphoma – nodular lesion of the soft tissues of the left cheek
We present a clinical case of a patient with a local late recurrence of stage IV follicular lymphoma with soft tissue damage to the left cheek. Relapse was registered after radiological treatment according to a radical program with good immediate results. The problem of treatment of patients with this pathology is of great importance, since today there are no uniform standards of treatment for relapses of the disease.
Текст научной статьи Клинический случай лечения пациента с локальным поздним рецидивом фолликулярной лимфомы – узловым поражением мягких тканей левой щеки
Наиболее распространенным вариантом индолентных лимфом является фолликулярная лимфома (ФЛ), которая занимает второе место в мире по частоте встречаемости после диффузной В-клеточной крупноклеточной лимфомы (ДВККЛ) и составляет в среднем 20–30% всех лимфопролиферативных заболеваний. Этот показатель значительно варьирует в различных географических регионах, а также зависит от этнической и расовой принадлежности пациентов, например, в азиатских странах доля ФЛ в структуре лимфопролиферативных заболеваний существенно ниже, чем в Европе и составляет 9–10%. По данным литературы в западных странах заболеваемость ФЛ равна 5–7 случаев на 100 тыс.
населения. В США ежегодно этот диагноз устанавливается у 14 тыс. человек. Заболеваемость ФЛ увеличивается с возрастом. Средний возраст заболевших составляет 60 лет, при этом заболеваемость среди лиц моложе 30 лет низкая, а возникновение ФЛ у детей является редкостью. Женщины заболевают несколько чаще и соотношение заболеваемости ФЛ мужчины/женщины равно 1:1,7 [1–3]. Морфологически выделяют три типа фолликулярной НХЛ: I тип – опухоль состоит преимущественно из мелких клеток (количество центробластов менее 5 в поле зрения); II тип – смешанное представительство мелких и крупных клеток (6–15 центробластов в поле зрения), III тип – преобладание в опухолевой ткани крупных клеток (>15 центробластов в поле зрения). В настоящее время ВОЗ не рекомендует различать тип I и II (наиболее часто встречаемые типы, содержащие до 15 центробластов на поле). Кроме того, ФЛ III типа с диффузным ростом, содержащим > 15 центробластов на поле с большим увеличением, следует классифицировать как ДВККЛ в соответствии с системой ВОЗ [1]. При установлении диагноза следует учитывать наличие четырех вариантов ФЛ (ВОЗ 2016):
-
1. Фолликулярная неоплазия in situ
-
2. Дуоденальный тип ФЛ
-
3. ФЛ яичек
-
4. Диффузный вариант ФЛ
Стадирование ФЛ проводится в соответствии с критериями классификации Аnn Arbor, модификация Лугано от 2014 г. (Таблица 1).
Таблица 1. Стадирование лимфом по Ann Arbor, модификация Лугано (2014 год)
|
Стадии |
Поражения лимфатических узлов |
Экстранодальное поражение |
|
I |
вовлечение одного или одной группы лимфатических узлов |
локализованное поражение одного экстралимфатического органа или ткани без поражения лимфатических узлов |
|
II |
вовлечение двух и более лимфатических узлов по одну сторону диафрагмы. Стадия II bulky-стадия II с массивным поражением лимфатических узлов |
локализованное поражеиие экстралимфатического органа или ткани + поражение регионарных лимфатических узлов по одну сторону диафрагмы |
|
III |
вовлечение лимфатических узлов по обе стороны диафрагмы или вовлечение лимфатических узлов выше диафрагмы с поражением селезенки |
|
|
IV |
диффузное или диссеминированное поражение экстралимфатического органа или ткани с/без вовлеченных лимфатических узлов либо поражение экстранодального органа или ткани + поражение не регионарных лимфатических узлов |
|
Примечание: миндалины, кольцо Вальдейера, селезенка относятся к нодальным образованиям.
Правильному стадированию в последние годы помогает позитронно-эмиссионная томография/компьютерная томография (ПЭТ/КТ). Использованию ПЭТ/КТ при первоначальном диагнозе и рецидиве ФЛ посвящено много литературы. Несмотря на погрешности, применение ПЭТ/КТ в клинической практике сохраняет высокую прогностическую ценность при ФЛ [5, 6]. Ведущим методом лечения ФЛ является химиотерапия. Новая эра лечения ФЛ наступила с введением ритуксимаба вхимиотерапевтический протокол, 5-летняя выживаемость пациентов увеличилась с 70% до 88,4%. Пациенты с рецидивом ФЛ имеют широкий спектр вариантов лечения, включая несколько режимов химиоиммунотерапии с использованием ингибиторов фосфоинозитид-3-киназы и леналидомида в сочетании с ритуксимабом. Несмотря на терапевтические достижения, все чаще признается неоднородность клинического течения ФЛ. Для анализа индивидуального риска раннего прогрессирования используются два варианта
Международного прогностического индекса ФЛ FLIPI и FLIPI-2 (Follicular Lymphoma International Prognostic Index) (Таблица 2). К группе низкого риска относятся пациенты с 0 – 1 фактором, промежуточного риска – с двумя факторами, высокого риска – 3 – 5 факторами риска [1, 4].
Таблица 2. Прогностические индексы FLIPI и FLIPI-2
|
Параметры |
Факторы риска FLIPI |
Факторы риска FLIPI-2 |
|
зона поражения |
более 4 зон |
максимальный размер более 6 см |
|
возраст |
старше 60 лет |
старше 60 лет |
|
биохимические маркеры |
повышение ЛДГ |
повышение B 2 - микроглобулина |
|
стадия |
III–IV |
поражение костного мозга |
|
уровень гемоглобина |
ниже 12 г/дл |
ниже 12 г/дл |
Рецидивы при ФЛ неизбежны, причем каждая последующая ремиссия бывает короче предыдущей. При рецидиве желательно выполнение повторной биопсии, поскольку известно, чем длительнее наблюдение за больным, тем выше риск трансформации ФЛ в диффузную В-крупноклеточную лимфому: 15% при 10-летнем и 26% при 14-летнем наблюдении. Как при первичном обращении, так и при рецидиве больной может не нуждаться в немедленном лечении, если на это нет оснований [4]. Выбор тактики лечения рецидива зависит от множества факторов, однако решающими все же являются длительность предшествующей ремиссии и метод ее достижения. Прогноз на длительную выживаемость больных, у которых было прогрессирование или рецидив ФЛ в течение 24 месяцев от начала лечения крайне неблагоприятный – пятилетняя общая выживаемость (OS) в этой подгруппе не превышает 50%. Одним из ведущих методов лечения ФС при рецидиве является лучевая терапия. Лучевая терапия – высокоэффективный метод лечения больных с небольшой опухолевой нагрузкой и при локальных стадиях ФЛ. Для определения объема опухоли (опухолевой нагрузки) и показаний к началу лечения наиболее полезными представляются критерии французской группы по изучению ФЛ (Groupe d’Etudedes Lymphomes Folliculaire – GELF) и Британской национальной группы по исследованию лимфом (British National Lymphoma Investigators – BNLI). Опухолевая нагрузка считается низкой при отсутствии следующих 4 групп признаков: 1) признаки, связанные с опухолью – лимфатические узлы или узлы опухолевой массы > 3 см в 3 различных зонах, симптомы сдавления органов, плеврит, асцит, спленомегалия, поражение печени, почек, костей; 2) признаки биологические – повышение уровня сывороточного ЛДГ и/или 2-микроглобулина, цитопении, связанные с выраженной инфильтрацией костного мозга (лейкоциты < 100 х 109 /л и/или тромбоциты < 100 х 109 /л); 3) признаки, характеризующие состояние больного - симптомы интоксикации (лихорадка, потливость, потеря веса), соматический статус по ECOG > 2; 4) признаки, отражающие течение болезни – генерализованное прогрессирование заболевания за последние 3 месяца [1, 3, 7]. Выбор оптимальной лечебной тактики у пациентов с рецидивом/прогрессированием ФЛ зависит от сроков развития рецидива/прогрессирования по отношению к ранее проведенному лечению, варианта ранее проведенного лечения, клинической манифестации рецидива/прогрессирования, возраста и соматического состояния пациента, наличия или отсутствия признаков рефрактерности к ритуксимабу [8]. Пациентам с химиорезистентным локальным рецидивом ФЛ рекомендовано применение лучевой терапии в низких суммарных дозах с использованием крупных фракций – РОД 4 Гр однократно или РОД 2 Гр х 2 фракции с паллиативной целью [9, 10]. Как и при первичном обращении, в период рецидива пациенту может быть предложена выжидательная тактика, и начало лечения может быть отложено c учетом прогностических факторов, которые были перечислены выше. Тактика лечения рецидивов зависит от многих факторов, однако решающими все же являются: длительность предшествующей ремиссии и метод ее достижения. Например, прогноз на повторную длительную выживаемость пациентов с прогрессированием ФЛ на фоне наблюдения без противоопухолевой терапии или пациентов с рецидивами менее чем 6 месяцев после завершения иммунохимиотерапии принципиально различаются. OS напрямую зависит от периода наступления прогрессирования заболевания. Планирование дистанционной лучевой терапии осуществляется с помощью методов визуализации, позволяющих получать трехмерные изображения. Лечение целесообразно осуществлять на линейном ускорителе электронов с использованием стандартного фракционирования дозы (одна фракция в день, 5 раз в неделю), разовая очаговая доза (РОД) 1,8–2,0 Гр, суммарная очаговая доза (СОД) составляет 24–30 Гр на зоны поражения. При отсутствии полной регрессии опухоли может быть использовано дополнительно локальное облучение (“буст”) в СОД 6–10 Гр [1]. Локализованная ФЛ традиционно считалась «излечимой» с применением локальной лучевой терапии. Одним из первых исследований, в которых упоминается "излечимость", стала серия работ Mac Manus M.P. и Hoppe R.T. из Стэнфорда, опубликованная еще в 1996 году [11]. Seymour J. с соавторами обобщили результаты эффективности лучевой терапии 6568 больных с I–II стадией ФЛ. Целью исследования была оценка эффективности лучевой терапии в первой линии. Оказалось, что 10- и 20-летняя ОS при I и II стадиях составила 62% и 35%, соответственно, для получавших лучевую терапию, против 48% и 23% в группе без облучения (p < 0,0001). Однако, если обобщить мировой опыт, только 20–30 % больных с локальными стадиями получают лучевую терапию. Было предпринято несколько попыток комбинировать лучевую терапию с другими методами. Оказалось, что добавление химиотерапии к облучению не улучшает показателей выживаемости больных за счет высокой частоты поздних осложнений [12]. Более того, согласно материалам Стэнфордского университета [13], отдаленные результаты комбинированного лечения вполне сопоставимы не только с данными больных, получавших лучевую терапию, но и с группой пациентов, которые только наблюдались.
Oliver J. Ott с соавторами провели ретроспективный анализ пролеченных 58 пациентов (средний период наблюдения 8,75 г.), из них 48 пациентов (83%) с ФЛ (I стадия – 23 пациента, II стадия– 15 пациентов и III стадия – 10 пациентов). Средний возраст составил 51 год. Облучение было применено со средней общей дозой 40 Гр, 13 пациентов (22%) дополнительно получили химиотерапию. Через 6 недель после лечения у 91% пациентов имелся полный ответ, у 7% – частичный ответ. Прогрессирование заболевания отмечено у одного пациента. Пяти- и 10-летняя OS составили 86% и 69%, соответственно. Что касается OS, то многовариантный анализ определил возраст (р=0,001) как независимый прогностический фактор. В подгруппе пациентов с ФЛ у 92% была зарегистрирована полная ремиссия, у 6% – частичная ремиссия, и у одного пациента (2%) наблюдалось прогрессирование заболевания. 5- и 10-летняя OS составили 87% и 70%, соответственно. Частота рецидивов вне поля облучения для всех 58 пациентов составила 34%. Представленные результаты, по мнению авторов, свидетельствуют в пользу лучевой терапии при лечении ФЛ ранних стадий, особенно у молодых пациентов [14].
-
K. Fakhrian с соавторами сообщили о лечении лучевой терапией 50 пациентов I–III стадиями ФЛ. Общая доза лучевой терапии колебалась от 26 до 56 Гр (медиана 40 Гр) с ежедневными фракциями 1,2–2,5 Гр, полная и частичная регрессия наблюдалась у 76% и 20% пациентов, соответственно, медиана ОS и бессобытийная выживаемость (EFS) составили 18 лет (95% доверительный интервал (ДИ) 10–26 лет) и 7 лет (6–8 лет), соответственно. Двух-, 5- и 10-летняя ОS были 96 ± 3%, 90 ± 5% и 70 ± 9%, соответственно; 2-, 5-, и 10-летняя EFS – 90 ± 5%, 70 ± 7%, и 38 ± 9%, соответственно. Лечение с размером очага ФЛ < 5 см (р = 0,039) и полная ремиссия после лучевой терапии (р = 0,021) были статистически достоверно связаны с лучшей OS [15].
Laila König с соавторами провели анализ лечения 47 пациентов (средний возраст 64 г.) с 50 поражениями, которым проводилась лучевая терапия и при рецидивирующем заболевании, в т.ч. включались ФЛ (57%). Средний срок наблюдения составил 21 месяц. 84% поражений были экстранодальными (32% орбиты, 14% слюнных желез, 30% кожи и 8%
– другие локализации). Большинство поражений были ≤ 5 см (90%). 26% пациентов получали одновременно ритуксимаб с лучевой терапией. Общие ответы (ORR) составили 90% (все поражения), 93,3% (первичное лечение) и 85% (лечение рецидивов) при р=0,341. Двухлетняя OS составила 91,1% при р=0,522. Прогностическим фактором для выживаемости отмечен размер опухоли ≤ 5 см (р=0,003) [16].
В исследовании J.L. Brady проанализировано лечение 512 пациентов, средний возраст составил 58 лет (диапазон, 20 – 90 лет), у 410 пациентов (80,1%) была болезнь I стадии, средняя доза лучевой терапии составила 30 Гр (24 – 52Гр), медиана наблюдения – 52 месяца (3,2–174,6), 5-летняя OS – 95,7% [17].
Michael Oertel с соавторами ретроспективно проанализировали лечение 26 пациентов с 44 очагами, из них семь пациентов (16%) лечились низкими дозами (LDRT) (4Гр) и 37 (84%) с обычной дозой лучевой терапии ≥24 Гр, средняя доза составила 40 Гр. Средняя продолжительность наблюдений была 76 месяцев. Были получены следующие показатели лечения: ORR – 91% , полная ремиссия (CRR) – 75%, 5-летний локальный контроль (LCR) – 88%, 10-летний LCR – 84%. Показатели ответов были значительно выше после обычной лучевой терапии (ORR: 92% против 86%; CRR: 84% против 29%; р= 0,007). С точки зрения дозы облучения, частота рецидивов в области полей облучения (14% против 11%, P= 0,4) и 5 лет LCR (86% против 90%, P=0,4) были сопоставимы в группах при LDRT и обычной лучевой терапии. Во время проведения лучевой терапии около двух третей пациентов испытывали легкую токсичность, с I и II степенями острой токсичности были 61% и 9% пациентов, соответственно. После LDRT показатели токсичности I и II степени были ниже (р=0,004). Таким образом, долгосрочный анализ подтверждает высокую эффективность лучевой терапии при лимфомах. Концепция LDRT с 4 Гр была связана с сопоставимым LCR и снижением выраженности острой токсичности. Тем не менее, показатели ответов на лечение были значительно ниже для этой группы, и поэтому LDRT не может быть рекомендована в качестве стандартного лечения [18].
В одном из последних исследований G. Pedro Mauro c соавторми (2021 г.) были проанализированы результаты лечения 34 больных с ФЛ, получавших лучевую терапию (у более 2/3 пациентов СОД составила 30–36 Гр). Острые реакции 0 – 1 степени отмечались у 76,4%, OS и выживаемость без прогрессии были 48,7 и 33,6 месяца, соответственно, 2- и 3-летная OS составили 94,1% и 91,2% соответственно. Авторы отмечают, что ФЛ является индолентным заболеванием, при этом наблюдаются хорошие результаты для пациентов, пролеченных лучевой терапией с низким уровнем трансформации и низкой частотой рецидивов, и делается заключение, что лучевая терапия является важной частью лечения этих пациентов [19].
Таким образом можно отметить, что на текущий момент по данным отечественной и мировой литературы при рецидиве ФЛ возможно применение химиотерапии и (или) лучевой терапии, но нет единых критериев использования данных методов лечения. По нашему мнению, использование лучевой терапии в качестве самостоятельного радикального курса лечения у данной группы больных с низкой опухолевой нагрузкой возможно с учетом низкой токсичности данного метода и высокой эффективности по данным литературы. Клиническое наблюдение
Пациент А., 1961 г. р. У пациента установлена в 2011 году фолликулярная лимфома IV стадии с множественным поражением легких, периферической и висцеральной лимфаденопатией в средостении и брюшной полости, поражением костного мозга. Проведено 6 курсов химиотерапии по схеме R-CHOP, далее 3 курса монотерапии ритуксимабом. Достигнута полная ремиссия. При дальнейших контрольных обследованиях данных за прогрессирования заболевания не было. По данным контрольной ПЭТ-КТ от 12.04.2020 г. – данных о наличии активной специфической ткани получено не было. По поводу появившегося образования в области левой щеки в начале августа 2020 г. пациент был направлен к челюстно-лицевому хирургу. Выполнена биопсия данного образования.
При гистологическом исследовании и ИГХ – фолликулярная лимфома, G I–II. По данным
ПЭТ-КТ от 08.09.2020 г. – узловое образование мягких тканей щеки слева 25 × 20 × 22 мм
(SUVmax-8.34) (Рис. 1–3).
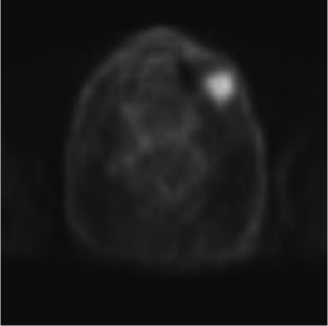
Рис 1. Накопление РФП при ПЭТ-КТ
На рисунках 2 и 3 показаны объемы поражения на сканах компьютерной томографии больного А. в двух плоскостях.
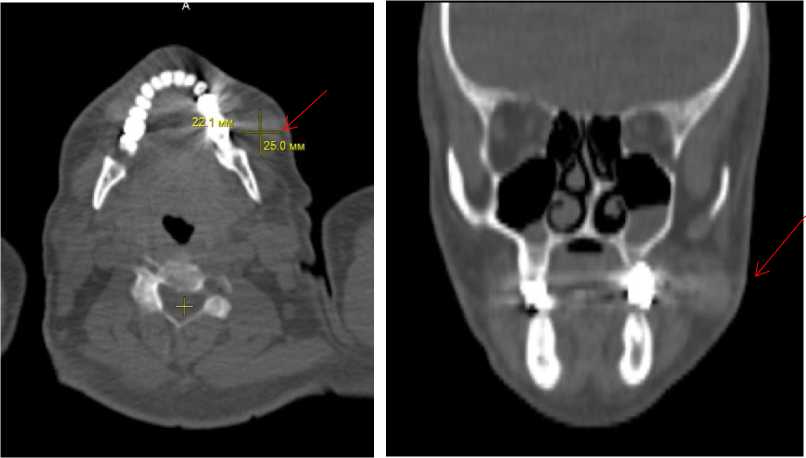
Рис 2. Компьютерная томография
Рис 3. Компьютерная томография
(сагиттальная плоскость)
(фронтальная плоскость)
По данным УЗИ-исследования – в мягких тканях левой щеки на глубине примерно 5,5 мм определяется гипоэхогенное образование с умеренно неровными, несколько нечеткими контурами, размерами 26×14 мм, однородной структуры (Рис. 4). Других очагов поражения не выявлено.
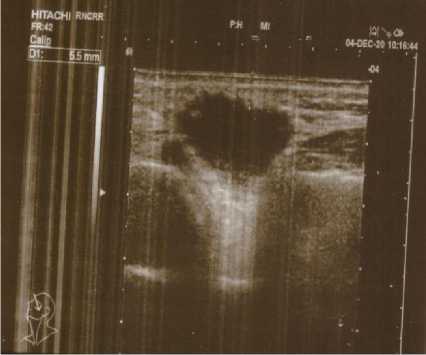
Рис 4. УЗИ мягких тканей левой щеки (до лечения)
Пациент проконсультирован гематологом – с учетом локального рецидива лимфомы проведение химиотерапии не целесообразно. Больной также проконсультирован врачом-радиотерапевтом. Рекомендовано провести курс конформной дистанционной лучевой терапии в режиме классического фракционирования с РОД 2 Гр 5 раз в неделю на аппарате ЛУЭ на зону локального рецидива – мягкие ткани щеки слева до СОД 36–40 Гр с учетом рецидивного характера болезни. С 23.11.2020 г. после предлучевой подготовки (МСКТ-топометрии в положении лечения, в фиксирующем устройстве, оконтуривания клинического объема облучения/органов риска, 3D-дозиметрического планирования, верификации дозиметрического плана с портальной визуализацией) начат курс в рамках 3D адаптивной конформной дистанционной лучевой терапии на аппарате ЛУЭ в режиме классического фракционирования в термофиксирующей маске на зону рецидива (щечная область слева) с РОД 2 Гр, с учетом методики, принятой в РНЦРР [20, 21]. Позиционирование пациента проводилась в соответствии с методикой, описанной Смысловым А.Ю. с соавторами [22]. По данным контрольного УЗИ-исследования (Рис. 5) после подведения СОД 20 Гр в мягких тканях левой щеки определялось гипоэхогенное образование с несколько неровными, нечеткими контурами, размерами 19 × 10 мм, однородной структуры. По сравнению с предыдущими данными отмечается уменьшение объема образования на 52% (с 19.05 см3 до 9.9 см3).
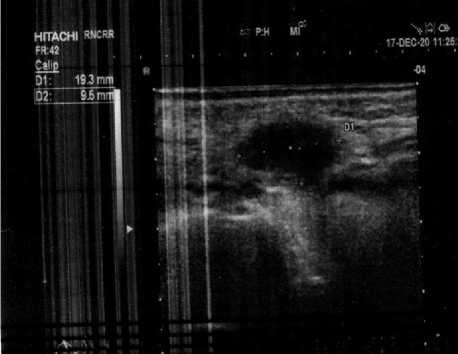
Рис 5. УЗИ мягких тканей левой щеки ( после СОД 20 Гр)
После контрольного УЗИ исследования мягких тканей щеки слева проведена ре- топометрия с ремоделированием фиксирующей термомаски с новым объемом и продолжена лучевая терапия в режиме классического фракционирования 5 раз в неделю на линейном ускорителе электронов (ЛУЭ) на зону рецидива с РОД 2 Гр до СОД 40 Гр. На Рис. 6 и 7
представлены изодозные кривые при планирования лучевой терапии с изначальным PTV1 и
PTV2 (рассчитанный после подведенной дозы 20 Гр и контрольного УЗИ с ре- планированием лучевой терапии) и гистограмма доза-объем (обобщенной для PTV1/PTV2).
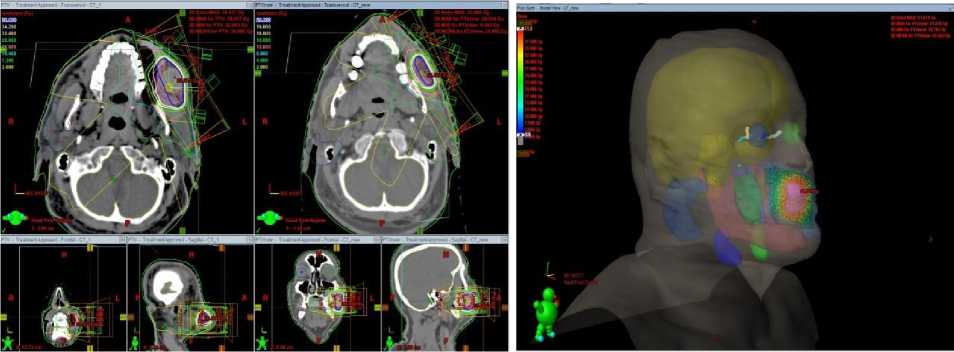
Рис.6. Дозиметрический план лучевого лечения
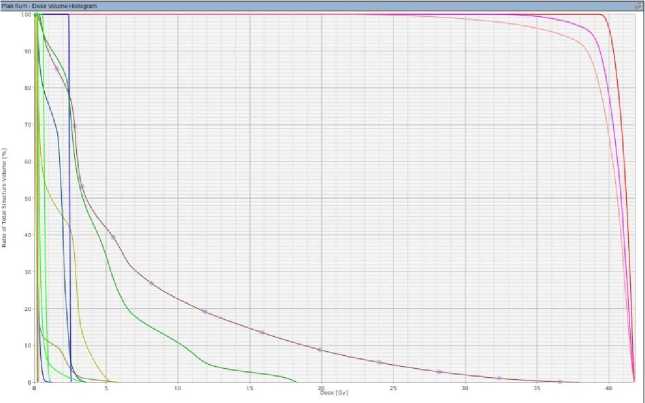
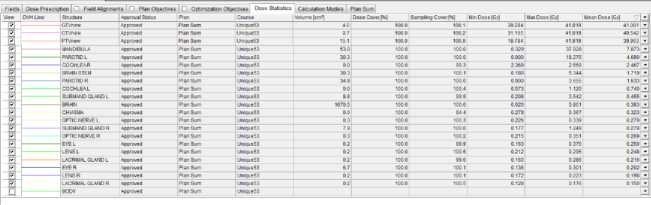
Рис.7. Гистограмма доза-объем для суммированного PTV
К концу лучевой терапии у пациента развились ранние лучевые реакции в виде лучевого мукозита в зоне облучения минимальной выраженности 1 степени по классификации RTOG. Лечение перенес относительно удовлетворительно, при выписке минимальные явления мукозита без отрицательной динамики, общий статус пациента 1 ст. по ECOG. По данным контрольного УЗИ щеки через 8 недель (Рис. 8) после завершения лучевой терапии – в мягких тканях левой щеки дополнительных образований не выявлено.
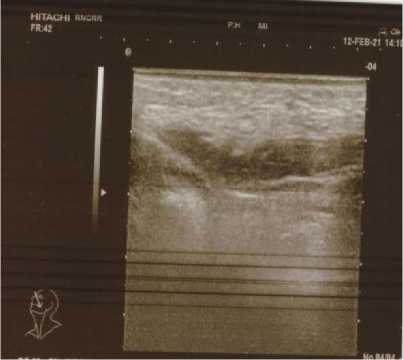
Рис. 8. Контрольное УЗИ мягких тканей щеки слева
Заключение
Рассмотренный клинический случай показывает, что возможно проведение лучевого лечения по радикальной программе у больных с локальным поздним рецидивом фолликулярной лимфомы G I–II после ранее проведенной полихимиотерапии по поводу первичного заболевания. Выбранный алгоритм лечения с применением современного радиологического режима облучения позволил получить хорошие непосредственные результаты лечения при минимальной лучевой токсичности и без ухудшения качества жизни пациента.
Список литературы Клинический случай лечения пациента с локальным поздним рецидивом фолликулярной лимфомы – узловым поражением мягких тканей левой щеки
- Бабичева Л.Г., Тумян Г.С., Кравченко С.К. и др. Фолликулярная лимфома. Российские клинические рекомендации по диагностике и лечению злокачественных лимфопролиферативных заболеваний. Под ред. И.В. Поддубной, В.Г. Савченко. 2018. С.43-52.
- Демина Е.А. Тумян Г.С., Моисеева Т.Н. и др. Общие принципы диагностики лимфом. Российские клинические рекомендации по диагностике и лечению злокачественных лимфопролиферативных заболеваний. Под редакцией Поддубной И.В., Савченко В.Г. 2018. С. 9-27.
- Armitage J.O. A clinical evaluation of the International Lymphoma Study Group classification of non-Hodgkin’s lymphoma. Blood. 1997. V. 89. No. 11. P. 3909- 3918.
- Matasar M.J., Luminari S., Barr P.M. et al. Follicular Lymphoma: Recent and Emerging Therapies, Treatment Strategies, and Remaining Unmet Needs. Oncologist. 2019. V. 24. No. 11. P. e1236-e1250. doi: 10.1634/theoncologist.2019-0138.
- Бабичева Л. Г., Поддубная И. В. Роль ПЭТ в лечении В-клеточных лимфопролиферативных заболеваний в рутинной клинической практике в России. Злокачественные опухоли. 2020. Т. 10. № 2. С.53-58. doi: 10.18027 / 2224-5057-2020-10-2-5.
- Barrington S. F., Trotman J. The role of PET in the first-line treatment of the most common subtypes of non-Hodgkin lymphoma. Lancet Haematology. 2021. V. 8. No 1. P.80-93. doi.org/10.1016/S2352-3026(20)30365-3.
- Ghielmini M., Rule S., Salles G., et al. Newly diagnosed and relapsed follicular lymphoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2016. V. 27 (Suppl 5). P. v83-v90.
- Поддубная И.В. Рецидивы фолликулярной лимфомы: проблемы и пути решения. Современная онкология. 2011. Т. 1. С. 10-15.
- Zelenetz A.D., Gordon L.I., Abramson J.S., et al. NCCN Guidelines Insights: B-Cell Lymphomas, Version 3.2019. J Natl Compr Canc Netw. 2019. V. 17. No. 6. P. 650-661. doi: 10.6004/jnccn.2019.0029.
- GrignanoE., Deau-Fischer B., Loganadane G., et al. Radiotherapy of relapse-refractory follicular lymphoma. Сancer Radiother. 2018. V. 22. No. 2. P.126-130.
- Mac Manus M.P., Hoppe R.T. Is radiotherapy curative for stage I and II low-grade follicular lymphoma? Results of a long-term follow-up study of patients treated at Stanford University. J Clin Oncol. 1996. V. 14. No. 4. P.1282-1290.
- Seymour J.F., Pro B., Fuller L.M., et al. Long-Term Follow-Up of a Prospective Study of Combined Modality Therapy for Stage I-II Indolent Non-Hodgkin’s Lymphoma. J. Clin. Oncol. 2003. V. 21. No. 11. P. 2115-2122.
- Petersen P.M., Gospodarowicz M., Tsang R., et al. Long-term outcome in stage I and II follicular lymphoma following treatment with involved field radiation therapy alone. J Clin Oncol. 2004. V. 22. Suppl. 14. Poster 6521.
- Ott O.J., Rödel C., Gramatzki M., et al. Radiotherapy for stage I-III nodal low-grade non-Hodgkin's lymphoma. Strahlenther Onkol. 2003. V. 179. No. 10. P. 694-701. doi: 10.1007/s00066-003-1062-8.
- Fakhrian K., Klemm S., Keller U., et al. Radiotherapy in stage I-III follicular non-Hodgkin lymphoma. Retrospective analysis of a series of 50 patients. Strahlenther Onkol. 2012. V. 188. No. 6. P. 464-470. doi: 10.1007/s00066-011-0057-0.
- König L., Hörner-Rieber J., Bernhardt D.et al. Response rates and recurrence patterns after low-dose radiotherapy with 4 Gy in patients with low-grade lymphomas. Strahlenther Onkol. 2018. V. 194. No. 5. P. 454-461. doi: 10.1007/s00066-018-1277-3.
- Brady J.L., Binkley M.S., Hajj C., et al. Definitive radiotherapy for localized follicular lymphoma staged by 18 F-FDG PET-CT: a collaborative study by ILROG. Blood. 2019. V. 133. No. 3. P. 237-245. doi: 10.1182/blood-2018-04-843540.
- Oertel M., Elsayad K., Weishaupt C. et al. De-escalated radiotherapy for indolent primary cutaneous B-cell lymphoma. Strahlenther Onkol. 2020. V. 196. No. 2. P. 126-131.doi: 10.1007/s00066-019-01541-7.
- Mauro G.P., Medici C.T.M., Casimiro L.C., Weltman E. Radiotherapy for early and advanced stages Follicular Lymphoma. Clinics (Sao Paulo). 2021. V.76. P. e2059. doi: 10.6061/clinics/2021/e2059.
- Измайлов Т.Р., Смыслов А.Ю., Амелина Н.С. Подготовка и реализация планов облучения пациента, проходившего лечение в ФГБУ «РНЦРР» с использованием метода стереотаксиса. Вестник "Российского научного центра рентгенорадиологии". 2017. № 3. http://vestnik.rncrr.ru/vestnik/v17/docs/izmailov.pdf.
- Петровский В.Ю., Цаллагова З.С., Амелина Н.С. и др. Клинический случай лечения пациента с местно-распространенным раком ротоглотки с регионарными метастазами и тяжелой сопутствующей соматической патологией. Вестник РНЦРР. 2018. T.18. № 3.
- Смыслов А.Ю., Васильев В.Н., Дыкина А.В., Коконцев А.А. Оценка точности позиционирования мишени при лучевой терапии с использованием термопластиковых масок Q-Fix. Медицинская физика. 2018. Т. 2. № 78. С. 53-61.


